Capitolo C 4 Pillole di Chimica La legge









- Slides: 10

Capitolo C 4 Pillole di Chimica: La legge di Proust Giovanni Casavecchia

3 Le leggi ponderali della chimica Le leggi ponderali sono tre leggi fondamentali della chimica che riguardano le masse delle sostanze coinvolte nelle reazioni Legge di conservazione della massa La legge di conservazione della massa afferma che, in una reazione chimica, la somma delle masse delle sostanze che reagiscono è uguale alla somma delle masse delle sostanze che si formano Questa legge è nota anche come legge di Lavoisier Capitolo 4 Le trasformazioni chimiche 2

3 Le leggi ponderali della chimica Legge delle proporzioni definite e costanti La legge delle proporzioni definite e costanti afferma che, quando due o più elementi reagiscono per formare un determinato composto, le loro masse stanno fra loro in un rapporto definito e costante Il rapporto fra le masse è detto rapporto di combinazione La legge delle proporzioni definite e costanti è nota anche come legge di Proust Capitolo 4 Le trasformazioni chimiche 3

3 Le leggi ponderali della chimica Capitolo 4 Le trasformazioni chimiche 4

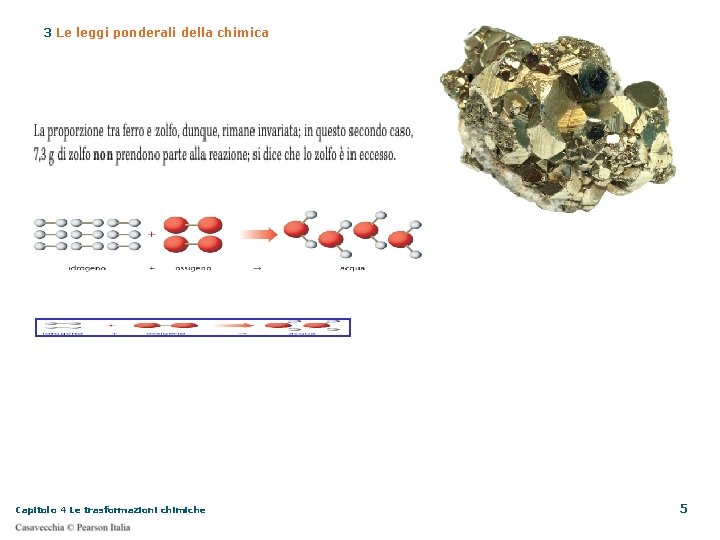
3 Le leggi ponderali della chimica Capitolo 4 Le trasformazioni chimiche 5

3 Le leggi ponderali della chimica Capitolo 4 Le trasformazioni chimiche 6

3 Le leggi ponderali della chimica Capitolo 4 Le trasformazioni chimiche 7

3 Le leggi ponderali della chimica La teoria atomica di Dalton La prima teoria scientifica sulla natura atomica della materia fu formulata da John Dalton nel 1808 Secondo la teoria atomica di Dalton la materia è formata da atomi indivisibili e indistruttibili gli atomi di uno stesso elemento sono tutti uguali e hanno la stessa massa nelle reazioni, gli atomi di un elemento si combinano con atomi interi dello stesso elemento o di altri elementi gli atomi di un elemento non possono essere creati o distrutti e neppure trasformati in atomi di altri elementi Capitolo 4 Le trasformazioni chimiche 8

3 Le leggi ponderali della chimica La spiegazione della legge di Proust Quando l’idrogeno reagisce con l’ossigeno per dare l’acqua, ogni particella di ossigeno si lega a due d’idrogeno Se mettessimo a reagire dell’idrogeno in eccesso, la reazione non sarebbe completa Capitolo 4 Le trasformazioni chimiche 9

3 Le leggi ponderali della chimica Ripassare/studiare legge Proust C 73, C 74, C 75 Pag C 83 N° 19, 20, 21, 22. Capitolo 4 Le trasformazioni chimiche 10