Capitolo 18 Le applicazioni degli equilibri in soluzione

Capitolo 18 Le applicazioni degli equilibri in soluzione acquosa Copyright © 2008 Zanichelli editore 18. 1 Le soluzioni dei sali non sono neutre se i loro ioni sono acidi o basi deboli 18. 2 I tamponi consentono di controllare il p. H 18. 3 Gli acidi poliprotici sono coinvolti in equilibri multipli 18. 4 Le titolazioni acido-base mostrano brusche variazioni di p. H al punto di equivalenza 18. 5 Alcune titolazioni utilizzano reazioni di ossidoriduzione come indicatori 18. 6 Un sale indisciolto è in equilibrio con la soluzione che lo circonda

18. 1 LE SOLUZIONI DEI SALI NON SONO NEUTRE SE I LORO IONI SONO ACIDI O BASI DEBOLI Gli equilibri chimici ci permettono di analizzare adesso e comprendere i fenomeni riguardanti altri tipi di equilibri in soluzione acquosa, alcuni dei quali vengono ampiamente utilizzati nelle tecniche di laboratorio e sono pertanto di fondamentale importanza pratica. Per prima cosa studieremo la natura delle soluzioni saline. Non ci siamo ancora chiesti se la soluzione di un sale sia sempre neutra oppure possa essere anche acida o basica. Dobbiamo ricordare che in un sale sono presenti due ioni, un catione e un anione. Copyright © 2008 Zanichelli editore

18. 1 LE SOLUZIONI DEI SALI NON SONO NEUTRE SE I LORO IONI SONO ACIDI O BASI DEBOLI Possiamo immaginare sempre i due ioni come se fossero l’acido e la base coniugata di due sostanze che hanno reagito attraverso una reazione di neutralizzazione. Per prevedere il comportamento di un sale in soluzione, quindi, occorre studiare come si comportano i suoi cationi e i suoi anioni nei confronti dell’acqua, cioè se reagiscono con essa. Una volta dissociato il sale, dobbiamo poi considerare se il catione si comporta da acido e l’anione da base nei confronti dell’acqua. Copyright © 2008 Zanichelli editore Se un sale reagisce con l’acqua, determinando la comparsa in soluzione di ioni H+ o ioni OH-, si parla di idrolisi salina.

18. 1 LE SOLUZIONI DEI SALI NON SONO NEUTRE SE I LORO IONI SONO ACIDI O BASI DEBOLI ► COME PREVEDERE LE PROPRIETÀ ACIDO-BASE DI UN SALE Per comprendere se un sale è in grado di influenzare il p. H di una soluzione acquosa, dobbiamo esaminare ciascuno dei suoi ioni e il rispettivo comportamento acido-base. Esistono quattro possibilità. 1. Né il catione né l’anione possono modificare il p. H: la soluzione è neutra. Tutti i sali derivanti dalla neutralizzazione di un acido forte con una base forte si comportano così. Prendiamo per esempio Na. Cl, che si dissocia secondo la seguente equazione già nota: Copyright © 2008 Zanichelli editore

18. 1 LE SOLUZIONI DEI SALI NON SONO NEUTRE SE I LORO IONI SONO ACIDI O BASI DEBOLI ► COME PREVEDERE LE PROPRIETÀ ACIDO-BASE DI UN SALE Na+ deriva dalla dissociazione della base forte Na. OH, mentre Cl - è la base coniugata dell’acido forte HCl. I due ioni sono quindi debolissimi, non reagiscono con l’acqua (non idrolizzano) e il p. H della soluzione è neutro. Copyright © 2008 Zanichelli editore

18. 1 LE SOLUZIONI DEI SALI NON SONO NEUTRE SE I LORO IONI SONO ACIDI O BASI DEBOLI ► COME PREVEDERE LE PROPRIETÀ ACIDO-BASE DI UN SALE 2. Il catione del sale è acido: la soluzione è acida. Questo è il caso di un sale derivante dalla neutralizzazione di un acido forte con una base debole. Prendiamo come esempio NH 4 Cl, che si dissocia in soluzione secondo la seguente equazione: Cl- non idrolizza, ma NH 4+ è un acido di una certa forza, coniugato della base debole NH 3: esso quindi reagisce con l’acqua producendo H 3 O + secondo l’equazione: Copyright © 2008 Zanichelli editore Il p. H pertanto sarà acido.

18. 1 LE SOLUZIONI DEI SALI NON SONO NEUTRE SE I LORO IONI SONO ACIDI O BASI DEBOLI ► COME PREVEDERE LE PROPRIETÀ ACIDO-BASE DI UN SALE 3. L’anione del sale è basico: la soluzione è basica. In questo caso il sale deriva dalla neutralizzazione di una base forte con un acido debole. Come esempio riferiamoci al caso del cianuro di potassio, KCN. Lo ione K+ deriva da una base forte e quindi non idrolizza, mentre CN - deriva dall’acido debole HCN, quindi possiede una certa forza e reagisce con l’acqua secondo la reazione: Copyright © 2008 Zanichelli editore Gli ioni ossidrile che si liberano dall’idrolisi aumentano il p. H e la soluzione è basica.

18. 1 LE SOLUZIONI DEI SALI NON SONO NEUTRE SE I LORO IONI SONO ACIDI O BASI DEBOLI ► COME PREVEDERE LE PROPRIETÀ ACIDO-BASE DI UN SALE 4. Il sale è formato da un catione acido e da un anione basico: il p. H della soluzione dipende dalla forza relativa dell’acido e della base. Prendiamo come esempio il bicarbonato di ammonio, (NH 4)HCO 3. NH 4+ idrolizza e così lo ione bicarbonato, che è la base coniugata dell’acido carbonico (acido debole). Le rispettive costanti di ionizzazione sono: Copyright © 2008 Zanichelli editore Le due costanti indicano che lo ione con maggiore forza è il bicarbonato, che determina un’idrolisi basica e per la soluzione un p. H > 7.

18. 1 LE SOLUZIONI DEI SALI NON SONO NEUTRE SE I LORO IONI SONO ACIDI O BASI DEBOLI ► COME PREVEDERE LE PROPRIETÀ ACIDO-BASE DI UN SALE La seguente tabella riporta l’esempio di alcuni cationi acidi. Copyright © 2008 Zanichelli editore

18. 1 LE SOLUZIONI DEI SALI NON SONO NEUTRE SE I LORO IONI SONO ACIDI O BASI DEBOLI SI PUÒ CALCOLARE IL p. H DI UNA SOLUZIONE DI UN SALE A PARTIRE DA Ka (O Kb) E DALLA CONCENTRAZIONE INIZIALE ► Se si idrolizza solo l’anione del sale, procediamo come se si trattasse di una soluzione di una base di Brönsted: dobbiamo conoscere la sua Kb e la concentrazione molare. Se, invece, si idrolizza il catione del sale, dobbiamo conoscere la sua Ka, oltre alla concentrazione molare. Per il calcolo del p. H di soluzioni saline è possibile arrivare a formulare delle espressioni riassuntive: se la specie attiva del soluto è una base debole: Copyright © 2008 Zanichelli editore se la specie attiva del soluto è un acido debole: dove cs è la concentrazione molare iniziale del soluto.

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H Le variazioni di p. H possono promuovere reazioni chimiche spesso indesiderate. Gli acidi accelerano la corrosione degli oggetti metallici; con poche gocce di limone il latte si rapprende, come sanno bene i cuochi; una variazione di p. H del sangue dai valori normali di 7, 35 -7, 42 a 7, 00 o 8, 00 è letale per il nostro organismo. Per fortuna, esistono modi per proteggere efficacemente i sistemi dalle variazioni di p. H. Copyright © 2008 Zanichelli editore Scegliendo opportunamente i soluti, è possibile preparare soluzioni che non vanno incontro a variazioni apprezzabili di p. H, anche quando vi si aggiungono piccole quantità di acidi o basi forti. Queste soluzioni vengono chiamate tamponi proprio perché sono in grado di tamponare il sistema rispetto a una variazione di p. H. La soluzione stessa viene definita tamponata oppure è descritta con il termine soluzione tampone.

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H Un tampone è generalmente costituito da due soluti, uno che si comporta come acido debole di Brönsted, l’altro come base debole di Brönsted. L’acido e la base rappresentano, di norma, una coppia coniugata; se l’acido è molecolare, la base coniugata è fornita da un sale solubile dell’acido. È possibile preparare tamponi che funzionino a un dato valore di p. H scegliendo un acido debole e un suo sale, negli opportuni rapporti molari. Copyright © 2008 Zanichelli editore

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H Per semplicità, limiteremo inizialmente la nostra discussione ai sistemi tampone del tipo HA/A-. Per poter agire, un tampone deve essere in grado di neutralizzare l’aggiunta sia di un acido forte sia di una base forte «riassorbendo» gli ioni H+ o OH- che vengono aggiunti al sistema. Copyright © 2008 Zanichelli editore

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H Vediamo come questo sia possibile, studiando prima il caso dell’aggiunta di un acido. 1. Quando aggiungiamo H+ (da un acido forte) al tampone, la base debole coniugata reagisce come nella figura. L’aggiunta dell’acido determina la trasformazione di parte della base di Brönsted del tampone, A -, nel suo acido coniugato (debole), HA, spostando l’equilibrio a destra. Questa reazione impedisce l’aumento della concentrazione di H + che altrimenti si avrebbe a causa dell’aggiunta dell’acido forte. Copyright © 2008 Zanichelli editore

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H 2. Analogamente, gli ioni OH- provenienti da una base forte reagiscono con l’acido debole HA del tampone. In questo caso, gli ioni OH- trasformano parte dell’acido di Brönsted del tampone, HA, nella sua base coniugata, A-. La reazione limita l’aumento di concentrazione degli ioni OH-, che altrimenti determinerebbe una notevole variazione del p. H. Copyright © 2008 Zanichelli editore Riassumendo, una sostanza del tampone neutralizza gli ioni H+ eventualmente aggiunti alla soluzione, mentre l’altra neutralizza gli ioni OH-

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H Il tampone acido acetico/ione acetato è del tipo HA/A- e contiene acido acetico e acetato di sodio, sale che fornisce lo ione acetato in soluzione. L’acido acetico presente nel tampone neutralizza OH- nel seguente modo: mentre lo ione acetato neutralizza H+ come segue: Copyright © 2008 Zanichelli editore

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H Anche in una soluzione acquosa di cloruro di ammonio e ammoniaca sono presenti un acido debole, NH 4+, e la sua base coniugata, NH 3. Si tratta quindi di un tampone che può neutralizzare l’aggiunta di ioni OH -: E di ioni H+ : Copyright © 2008 Zanichelli editore

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H COME CALCOLARE IL p. H DI UNA SOLUZIONE TAMPONE DEL TIPO HA/A► Quando si svolgono calcoli sui tamponi, dobbiamo considerare che HA è un acido debole, per cui solo una sua piccolissima quantità è ionizzata all’equilibrio; inoltre, la soluzione contiene anche A-, proveniente dal sale disciolto, che limita la già scarsa ionizzazione di HA. Possiamo quindi fare due semplificazioni: Copyright © 2008 Zanichelli editore Per risolvere i problemi sulle soluzioni tampone, possiamo usare indifferentemente i valori di Ka o Kb e il risultato finale è lo stesso. Nel caso si decida di usare Ka, deve essere scritta l’equazione chimica relativa alla ionizzazione acida. L’uso di Kb implica l’impiego dell’equazione per la ionizzazione basica.

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H DI UNA SOLUZIONE TAMPONE PUÒ ESSERE RICAVATO DA UN’EQUAZIONE GENERALE ► Riprendiamo l’equazione di ionizzazione di un acido debole e risolviamola cercando il valore di [H+], primo passo necessario per calcolare poi il p. H. Da cui: Copyright © 2008 Zanichelli editore

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H DI UNA SOLUZIONE TAMPONE PUÒ ESSERE RICAVATO DA UN’EQUAZIONE GENERALE ► Il primo fattore che influenza [H+] (e quindi il p. H) è la Ka dell’acido debole; il secondo è il rapporto fra le concentrazioni molari dei due membri della coppia coniugata acido-base. Quando prepariamo un tampone in modo che le concentrazioni dei due componenti siano uguali, il sistema ha la massima efficienza. In questa situazione, il rapporto [HA]iniziale/[A-] iniziale dell’equazione risulta uguale a 1, quindi [H+] = Ka ovvero p. H = p. Ka. Copyright © 2008 Zanichelli editore Di conseguenza, il fattore principale che determina il p. H al quale la soluzione tampone agisce più efficacemente è il valore p. Ka dell’acido debole.

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H DI UNA SOLUZIONE TAMPONE PUÒ ESSERE RICAVATO DA UN’EQUAZIONE GENERALE ► Considerando il logaritmo negativo di entrambi i membri dell’equazione e invertendo il termine delle concentrazioni, otteniamo: Copyright © 2008 Zanichelli editore Questa espressione, conosciuta come equazione di Henderson. Hasselbalch, si incontra molto spesso nella letteratura chimica e in biochimica. Essa permette di ricavare direttamente il p. H di soluzioni costituite da un acido debole con la sua base coniugata. Questa equazione è più comunemente formulata in questo modo:

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H DI UNA SOLUZIONE TAMPONE PUÒ ESSERE RICAVATO DA UN’EQUAZIONE GENERALE ► In maniera analoga, per una soluzione costituita da una base debole e da un suo sale, otteniamo: Copyright © 2008 Zanichelli editore

18. 2 I TAMPONI CONSENTONO DI CONTROLLARE IL p. H DI UNA SOLUZIONE TAMPONE PUÒ ESSERE RICAVATO DA UN’EQUAZIONE GENERALE ► Il p. H di un tampone non cambia se l’intero sistema viene diluito (o concentrato). La diluizione determina una variazione di volume della soluzione ma non altera il numero di moli dei soluti: il rapporto in moli rimane pertanto costante, così come [H+]. Per questo, solo per le soluzioni tampone, nell’espressione di K a (o Kb) possiamo usare indifferentemente le concentrazioni molari o le moli per rappresentare le quantità delle due sostanze che costituiscono la coppia coniugata acido-base. Copyright © 2008 Zanichelli editore La diluizione determina invece una variazione del potere tampone, cioè della quantità di acido o base forte che il sistema è in grado di assorbire prima che il suo effetto sia esaurito.

18. 3 GLI ACIDI POLIPROTICI SONO COINVOLTI IN EQUILIBRI MULTIPLI In natura esistono molti acidi che rilasciano più di un H+ per molecola, i cosiddetti acidi poliprotici. Per esempio, l’acido carbonico, H 2 CO 3, è un acido diprotico, la cui ionizzazione avviene in due stadi successivi. Vi sono perciò due valori di Ka, uno per ciascuno dei due atomi di idrogeno ionizzabili. La costante di prima ionizzazione, Ka 1, si riferisce al seguente equilibrio: Copyright © 2008 Zanichelli editore

18. 3 GLI ACIDI POLIPROTICI SONO COINVOLTI IN EQUILIBRI MULTIPLI Mentre la costante di seconda ionizzazione Ka 2, si riferisce all’equilibrio: Copyright © 2008 Zanichelli editore
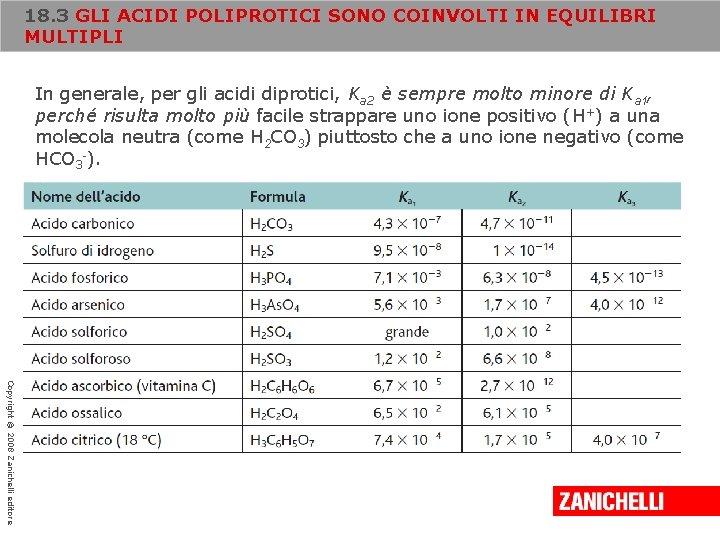
18. 3 GLI ACIDI POLIPROTICI SONO COINVOLTI IN EQUILIBRI MULTIPLI In generale, per gli acidi diprotici, Ka 2 è sempre molto minore di Ka 1, perché risulta molto più facile strappare uno ione positivo (H+) a una molecola neutra (come H 2 CO 3) piuttosto che a uno ione negativo (come HCO 3 -). Copyright © 2008 Zanichelli editore

18. 3 GLI ACIDI POLIPROTICI SONO COINVOLTI IN EQUILIBRI MULTIPLI Dato che Ka 1 supera Ka 2 di diversi ordini di grandezza, quasi tutti gli H+ presenti nella soluzione dell’acido provengono dalla prima ionizzazione. In altri termini, possiamo adottare la seguente approssimazione: Copyright © 2008 Zanichelli editore Di conseguenza, quando è necessario calcolare la concentrazione di H+, possiamo considerare l’acido come se fosse monoprotico e trascurare le successive.

18. 3 GLI ACIDI POLIPROTICI SONO COINVOLTI IN EQUILIBRI MULTIPLI LE SOLUZIONI DEI SALI DEGLI ACIDI POLIPROTICI SONO BASICHE ► Il carbonato di sodio, Na 2 CO 3 (contenuto in molti detersivi), è esempio di sale derivato da un acido poliprotico. Si tratta di un sale dell’acido carbonico, H 2 CO 3, in cui lo ione carbonato si comporta da base di Brönsted e genera due equilibri che producono ioni OH-, influenzando così il p. H della soluzione. Copyright © 2008 Zanichelli editore

18. 3 GLI ACIDI POLIPROTICI SONO COINVOLTI IN EQUILIBRI MULTIPLI LE SOLUZIONI DEI SALI DEGLI ACIDI POLIPROTICI SONO BASICHE ► Confrontiamo adesso i due valori di Kb. Per CO 32 -, Kb 1 = 2, 1 x 10 -4, mentre per la base HCO 3 - (molto più debole), Kb 2 = 2, 3 x 10 -8. La Kb di CO 32 - è circa 10 000 volte più grande di quella di HCO 3 -. Per questo motivo, la reazione di CO 32 - con l’acqua genera una quantità di OHnettamente maggiore della reazione di HCO 3 -. Copyright © 2008 Zanichelli editore Il contributo di quest’ultima reazione alla quantità totale di ioni OH - è talmente piccolo da poter essere trascurato. La semplificazione è molto simile a quella vista per la ionizzazione degli acidi poliprotici e consente di ignorare le altre reazioni se desideriamo calcolare il p. H di una soluzione dell’anione basico di un acido poliprotico, utilizzando la sola Kb 1.
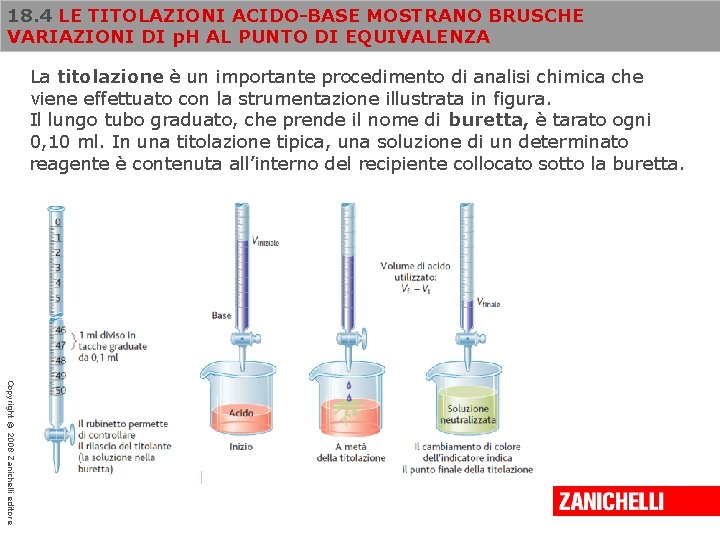
18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA La titolazione è un importante procedimento di analisi chimica che viene effettuato con la strumentazione illustrata in figura. Il lungo tubo graduato, che prende il nome di buretta, è tarato ogni 0, 10 ml. In una titolazione tipica, una soluzione di un determinato reagente è contenuta all’interno del recipiente collocato sotto la buretta. Copyright © 2008 Zanichelli editore

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA Volumi accuratamente misurati di un’altra soluzione, che contiene il secondo reagente, vengono fatti gocciolare dalla buretta nel recipiente sottostante il cui contenuto viene continuamente agitato. Una delle due soluzioni ha concentrazione nota ed è definita soluzione standard. L’aggiunta prosegue fino a quando nel recipiente si evidenzia (di norma, grazie a un effetto visivo, per esempio un cambiamento di colore) l’avvenuto completamento della reazione, dovuto alla combinazione dei due reagenti nelle esatte proporzioni. Copyright © 2008 Zanichelli editore Il rubinetto posto sul fondo della buretta consente all’analista di fermare l’aggiunta del titolante una volta che la reazione sia giunta a completamento, e di misurare poi con esattezza la quantità di titolante (la soluzione contenuta nella buretta) che è stata fatta gocciolare nel recipiente.

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA Le titolazioni vengono spesso impiegate nelle reazioni acido-base. Prima di iniziare una titolazione acido-base, una goccia o due di indicatore vengono aggiunte alla soluzione contenuta nel recipiente posto sotto la buretta. Copyright © 2008 Zanichelli editore Nel corso di una titolazione acido-base, l’analista aggiunge la sostanza titolante lentamente, aspettando il cambiamento di colore della soluzione nel recipiente che segnala il passaggio dall’ambiente acido a quello basico (o viceversa, a seconda della natura dei reagenti contenuti nella buretta e nel recipiente). Il cambiamento di colore (viraggio) è generalmente brusco e avviene dopo l’aggiunta di una sola goccia di titolante, proprio quando la reazione è giunta a completamento.

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA Il viraggio evidenzia il raggiungimento del punto finale della titolazione, a cui dobbiamo chiudere il rubinetto e annotare la quantità esatta di titolante aggiunta alla soluzione. L’ideale sarebbe che il punto finale coincidesse con il punto di equivalenza, al quale si sono combinate quantità equivalenti di acido e di base. Per ottenere questo risultato è importante scegliere con attenzione l’indicatore adatto. Questo concetto può essere compreso più facilmente studiando come varia il p. H della soluzione titolata durante l’aggiunta del titolante. Copyright © 2008 Zanichelli editore
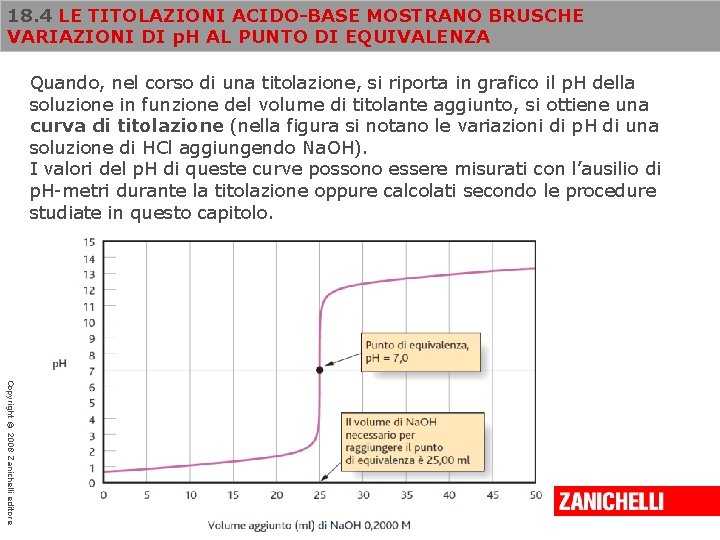
18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA Quando, nel corso di una titolazione, si riporta in grafico il p. H della soluzione in funzione del volume di titolante aggiunto, si ottiene una curva di titolazione (nella figura si notano le variazioni di p. H di una soluzione di HCl aggiungendo Na. OH). I valori del p. H di queste curve possono essere misurati con l’ausilio di p. H-metri durante la titolazione oppure calcolati secondo le procedure studiate in questo capitolo. Copyright © 2008 Zanichelli editore

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA LA TITOLAZIONE ACIDO FORTE-BASE FORTE HA UN PUNTO DI EQUIVALENZA A p. H = 7 ► La titolazione di HCl(aq) con una soluzione standard di Na. OH è un esempio di titolazione di un acido forte con una base forte. Le equazioni molecolare e ionica netta sono: Copyright © 2008 Zanichelli editore
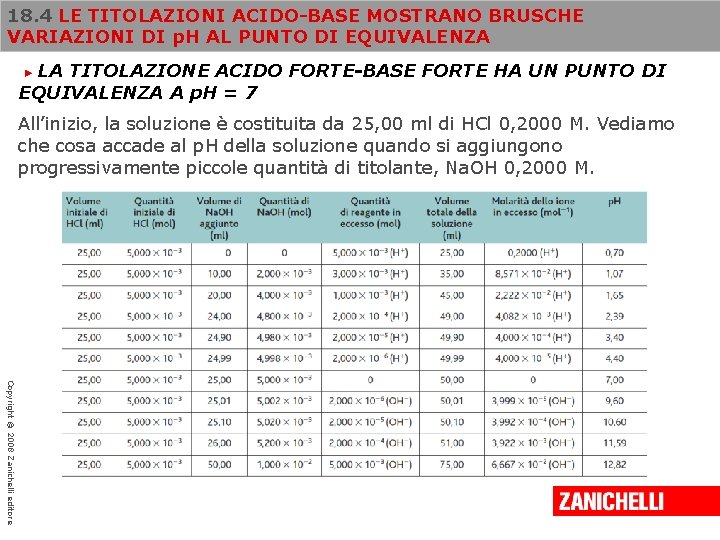
18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA LA TITOLAZIONE ACIDO FORTE-BASE FORTE HA UN PUNTO DI EQUIVALENZA A p. H = 7 ► All’inizio, la soluzione è costituita da 25, 00 ml di HCl 0, 2000 M. Vediamo che cosa accade al p. H della soluzione quando si aggiungono progressivamente piccole quantità di titolante, Na. OH 0, 2000 M. Copyright © 2008 Zanichelli editore
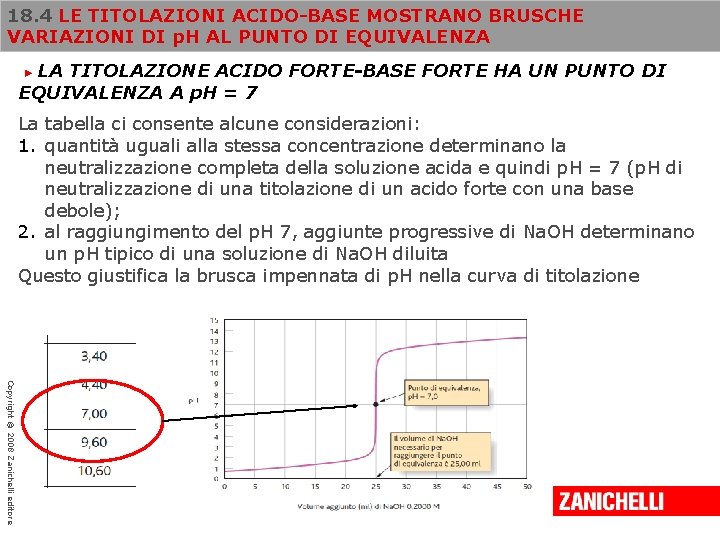
18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA LA TITOLAZIONE ACIDO FORTE-BASE FORTE HA UN PUNTO DI EQUIVALENZA A p. H = 7 ► La tabella ci consente alcune considerazioni: 1. quantità uguali alla stessa concentrazione determinano la neutralizzazione completa della soluzione acida e quindi p. H = 7 (p. H di neutralizzazione di una titolazione di un acido forte con una base debole); 2. al raggiungimento del p. H 7, aggiunte progressive di Na. OH determinano un p. H tipico di una soluzione di Na. OH diluita Questo giustifica la brusca impennata di p. H nella curva di titolazione Copyright © 2008 Zanichelli editore
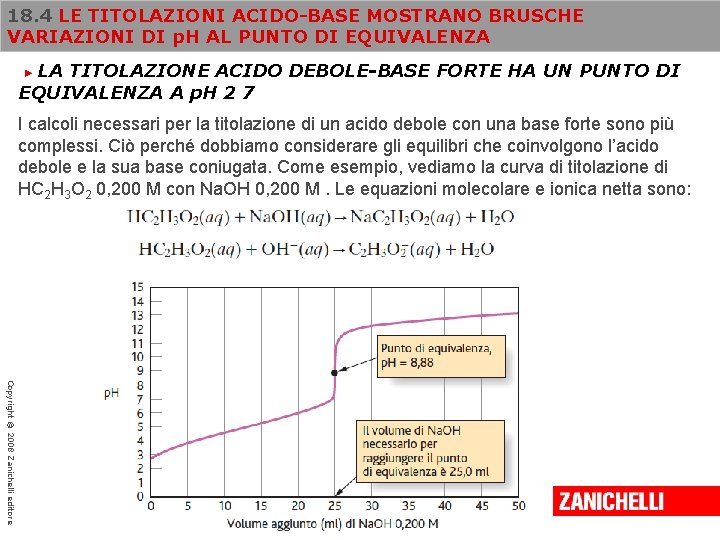
18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA LA TITOLAZIONE ACIDO DEBOLE-BASE FORTE HA UN PUNTO DI EQUIVALENZA A p. H 2 7 ► I calcoli necessari per la titolazione di un acido debole con una base forte sono più complessi. Ciò perché dobbiamo considerare gli equilibri che coinvolgono l’acido debole e la sua base coniugata. Come esempio, vediamo la curva di titolazione di HC 2 H 3 O 2 0, 200 M con Na. OH 0, 200 M. Le equazioni molecolare e ionica netta sono: Copyright © 2008 Zanichelli editore

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA LA TITOLAZIONE ACIDO DEBOLE-BASE FORTE HA UN PUNTO DI EQUIVALENZA A p. H > 7 ► 1. Prima che la titolazione inizi. La soluzione contiene solo l’acido debole, HC 2 H 3 O 2, edobbiamo usare Ka per calcolarne il p. H. 2. Durante la titolazione, prima del punto di equivalenza. A mano a mano che si aggiunge Na. OH a HC 2 H 3 O 2, la reazione chimica produce C 2 H 3 O 2 - , quindi la soluzione contiene sia HC 2 H 3 O 2 sia C 2 H 3 O 2 - (è una soluzione tampone). Anche in questo caso possiamo usare Ka per trovare il p. H. Copyright © 2008 Zanichelli editore

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA LA TITOLAZIONE ACIDO DEBOLE-BASE FORTE HA UN PUNTO DI EQUIVALENZA A p. H > 7 ► 3. Al punto di equivalenza. Tutto HC 2 H 3 O 2 ha reagito e la soluzione contiene il sale. Na. C 2 H 3 O 2 (abbiamo quindi una miscela di ioni Na+ e C 2 H 3 O 2 - ). Il catione Na+ non si idrolizza e non influenza il p. H. L’anione è invece una base debole, si idrolizza, e la soluzione risulta leggermente basica. Dobbiamo usare la Kb corrispondente per calcolare il p. OH e il p. H della soluzione. Copyright © 2008 Zanichelli editore 4. Dopo il punto di equivalenza. Gli ioni OH- introdotti per ulteriore aggiunta di Na. OH non reagiscono con alcuna specie e rendono la soluzione sempre più basica. La concentrazione di OH-, prodotta dalla base che non ha reagito, serve per calcolare il p. OH e il p. H della soluzione.
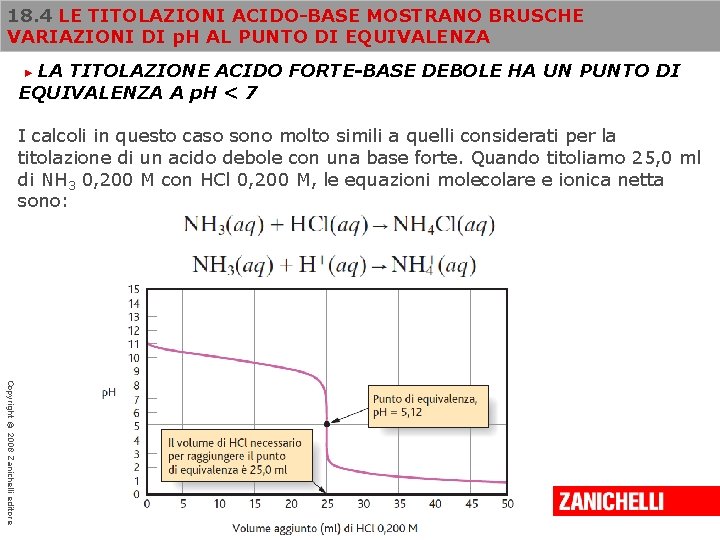
18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA LA TITOLAZIONE ACIDO FORTE-BASE DEBOLE HA UN PUNTO DI EQUIVALENZA A p. H < 7 ► I calcoli in questo caso sono molto simili a quelli considerati per la titolazione di un acido debole con una base forte. Quando titoliamo 25, 0 ml di NH 3 0, 200 M con HCl 0, 200 M, le equazioni molecolare e ionica netta sono: Copyright © 2008 Zanichelli editore

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA LA TITOLAZIONE ACIDO FORTE-BASE DEBOLE HA UN PUNTO DI EQUIVALENZA A p. H < 7 ► 1. Prima che la titolazione inizi. La soluzione contiene solo la base debole, NH 3, per cui dobbiamo usare Kb per calcolarne il p. OH e il p. H. 2. Durante la titolazione, prima del punto di equivalenza. A mano a mano che si aggiunge HCl a NH 3, la reazione chimica produce NH 4+, quindi la soluzione contiene sia NH 3 sia NH 4+ (è una soluzione tampone). Anche in questo caso possiamo usare Kb per trovare il p. OH e il p. H. Copyright © 2008 Zanichelli editore

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA LA TITOLAZIONE ACIDO FORTE-BASE DEBOLE HA UN PUNTO DI EQUIVALENZA A p. H < 7 ► 3. Al punto di equivalenza. NH 3 ha completamente reagito e la soluzione contiene il sale NH 4 Cl. L’anione Cl- deriva dall’acido forte HCl ed è una base talmente debole da non influenzare il p. H. Il catione NH 4+, al contrario, si idrolizza e forma una soluzione leggermente acida. Dobbiamo perciò usare la sua Ka per calcolare il p. H della soluzione. Copyright © 2008 Zanichelli editore 4. Dopo il punto di equivalenza. Gli ioni H+ introdotti per ulteriore aggiunta di HCl non reagiscono con alcuna specie e rendono la soluzione sempre più acida. La concentrazione di H+, prodotta dall’acido HCl che non ha reagito, serve per calcolare direttamente il p. H della soluzione.

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA ► COME FUNZIONANO GLI INDICATORI ACIDO-BASE Molti indicatori acido-base sono acidi organici deboli che possiamo rappresentare con la formula generale HIn (In sta per «indicatore» ). La forma acida (HIn) ha un colore, mentre la sua base coniugata (In-) ne ha un altro. In soluzione, l’indicatore partecipa all’equilibrio acido-base: . Copyright © 2008 Zanichelli editore In ambiente acido, l’equilibrio è spostato a sinistra e la maggior parte dell’indicatore esiste nella forma acida; in soluzione basica, l’equilibrio è spostato a destra e la maggior parte dell’indicatore esiste nella forma basica.

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA ► COME FUNZIONANO GLI INDICATORI ACIDO-BASE In una tipica titolazione acido-base, una volta raggiunto il punto di equivalenza, si ha una brusca e ampia variazione di p. H. Questa determina uno spostamento improvviso della posizione dell’equilibrio per l’indicatore, che passa da una condizione in cui la maggior parte è nella forma acida (o basica) a un’altra in cui la maggior parte è in forma basica (o acida). Ciò è evidenziato dal cambiamento di colore dell’indicatore. La spiegazione data in precedenza si basa sull’assunzione che il punto centrale di viraggio dell’indicatore corrisponda al valore del p. H al punto di equivalenza. In queste condizioni, sono presenti quantità uguali di entrambe le forme dell’indicatore, cioè [HIn] = [In-], e quindi: Copyright © 2008 Zanichelli editore

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA ► COME FUNZIONANO GLI INDICATORI ACIDO-BASE In una tipica titolazione acido-base, una volta raggiunto il punto di equivalenza, si ha una brusca e ampia variazione di p. H. Questa determina uno spostamento improvviso della posizione dell’equilibrio per l’indicatore, che passa da una condizione in cui la maggior parte è nella forma acida (o basica) a un’altra in cui la maggior parte è in forma basica (o acida). Ciò è evidenziato dal cambiamento di colore dell’indicatore. La spiegazione data in precedenza si basa sull’assunzione che il punto centrale di viraggio dell’indicatore corrisponda al valore del p. H al punto di equivalenza. In queste condizioni, sono presenti quantità uguali di entrambe le forme dell’indicatore, cioè [HIn] = [In-], e quindi: Copyright © 2008 Zanichelli editore

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA ► COME FUNZIONANO GLI INDICATORI ACIDO-BASE Prendendo il logaritmo negativo di entrambi i membri otteniamo: Questo importante risultato ci indica che in una titolazione la scelta deve cadere su un indicatore che abbia p. KIn uguale o più vicino possibile al p. H del punto di equivalenza. La fenolftaleina, per esempio, vira da incolore a fucsia in un intervallo di p. H compreso fra 8, 2 e 10, 0 Copyright © 2008 Zanichelli editore

18. 4 LE TITOLAZIONI ACIDO-BASE MOSTRANO BRUSCHE VARIAZIONI DI p. H AL PUNTO DI EQUIVALENZA ► COME FUNZIONANO GLI INDICATORI ACIDO-BASE La fenolftaleina è quindi l’indicatore più adatto per le titolazioni di un acido debole con una base forte, in cui il p. H del punto di equivalenza è basico. La fenolftaleina è indicata anche per le titolazioni di un acido forte con una base forte , dove l’aggiunta di una sola goccia di titolante può spostare il p. H da valori acidi a circa 10. Nelle titolazioni di una base debole con un acido forte, in cui il p. H di equivalenza è acido, è preferibile il metilarancio (intervallo tra 3, 2 e 4, 4) anche se la sua variazione di colore (dal rosso al giallo) non è facile da osservare nelle soluzioni molto diluite. Copyright © 2008 Zanichelli editore

18. 5 ALCUNE TITOLAZIONI UTILIZZANO REAZIONI DI OSSIDORIDUZIONE COME INDICATORI Poiché molte reazioni implicano processi di ossidazione e riduzione, non sorprende che queste abbiano importanti applicazioni in laboratorio. Alcune reazioni redox sono particolarmente utili in analisi chimica, soprattutto nelle titolazioni. Diversamente da quanto accade per una titolazione acido-base, tuttavia, non vi sono semplici indicatori che possano segnalare il punto finale di una titolazione redox e dobbiamo quindi basarci sui cambiamenti di colore dei reagenti stessi. Copyright © 2008 Zanichelli editore

18. 5 ALCUNE TITOLAZIONI UTILIZZANO REAZIONI DI OSSIDORIDUZIONE COME INDICATORI Uno dei reagenti maggiormente impiegati nelle titolazioni redox è il permanganato di potassio, KMn. O 4, in particolare quando la reazione avviene in soluzione acida. Lo ione permanganato è un ossidante molto energico in grado di ossidare la maggior parte delle sostanze ossidabili. Ancora più importante, tuttavia, è l’intenso colore viola delle soluzioni di Mn. O 4 -, mentre il suo prodotto di riduzione in ambiente acido, lo ione Mn 2+, dà soluzioni incolori. Pertanto, quando una soluzione di KMn. O 4 viene aggiunta con una buretta a una soluzione di riducente, la reazione chimica che avviene porta alla produzione di una sostanza incolore. Copyright © 2008 Zanichelli editore

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA Quando i sali si sciolgono, in genere si dissociano completamente; si stabilisce così un equilibrio fra il solido e gli ioni presenti in soluzione. Esistono molti sali che possiamo considerare insolubili, tanto che quando si formano attraverso una reazione di metatesi giungono subito a saturazione e precipitano. A questo punto possiamo affrontare il problema della solubilità in termini di equilibrio chimico. Per prima cosa dobbiamo subito tenere presente che nessun sale è totalmente insolubile: in acqua pura, una certa quantità è sempre solubile, anche se in minima parte. Copyright © 2008 Zanichelli editore

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA Consideriamo, per esempio, il cloruro di argento, Ag. Cl, sale definito «insolubile» in base alle regole di solubilità. Se viene posto in acqua, se ne discioglie una piccolissima quantità e, una volta che si è formata la soluzione satura, abbiamo il seguente equilibrio: Si tratta di un equilibrio eterogeneo perché implica la presenza di un reagente solido (Ag. Cl) in equilibrio con i suoi ioni in soluzione acquosa. Visto che la quantità di sale non cambia molto prima e dopo la reazione, scriviamo la seguente legge dell’equilibrio senza riportare il solido stesso nell’espressione dell’azione di massa: Copyright © 2008 Zanichelli editore
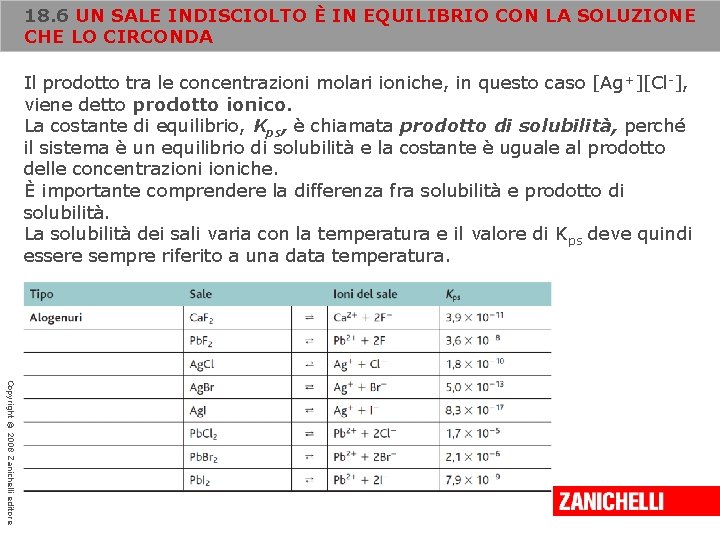
18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA Il prodotto tra le concentrazioni molari ioniche, in questo caso [Ag +][Cl-], viene detto prodotto ionico. La costante di equilibrio, Kps, è chiamata prodotto di solubilità, perché il sistema è un equilibrio di solubilità e la costante è uguale al prodotto delle concentrazioniche. È importante comprendere la differenza fra solubilità e prodotto di solubilità. La solubilità dei sali varia con la temperatura e il valore di K ps deve quindi essere sempre riferito a una data temperatura. Copyright © 2008 Zanichelli editore

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA IL VALORE DEL PRODOTTO IONICO CI DÀ INDICAZIONI SULLA SOLUBILITÀ DI UN SALE ► Nelle soluzioni insature, le concentrazioniche e quindi il prodotto ionico variano in base alla concentrazione del sale. Al contrario, nelle soluzioni sature il prodotto ionico assume un valore costante, Kps; solo in questo caso il prodotto ionico è uguale al prodotto di solubilità. Quando una soluzione di Ag. Cl non è satura, il valore del prodotto ionico è minore di Kps. Il confronto fra il valore numerico del prodotto ionico di una soluzione e Kps ci consente dunque di valutare se la soluzione è satura. Molti sali, quando si dissociano, generano più di una particella di un dato ione. Per esempio, con il cromato d’argento, Ag 2 Cr. O 4 , si stabilisce il seguente equilibrio: Copyright © 2008 Zanichelli editore

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA IL VALORE DEL PRODOTTO IONICO CI DÀ INDICAZIONI SULLA SOLUBILITÀ DI UN SALE ► Dissociandosi, ciascuna unità formula di Ag 2 Cr. O 4 dà origine a due ioni Ag+ e a uno ione Cr. O 42 -. Nel prodotto ionico di un sale come questo, ciascun termine di concentrazione è elevato a un esponente che è pari al numero di ioni liberati per unità formula. Così, il prodotto ionico del cromato d’argento è [Ag+]2[Cr. O 42 -]. Per ottenere l’espressione corretta del prodotto ionico dobbiamo, quindi, conoscere la formula del composto che si scioglie in acqua. Copyright © 2008 Zanichelli editore

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA IL VALORE DEL PRODOTTO IONICO CI DÀ INDICAZIONI SULLA SOLUBILITÀ DI UN SALE ► Uno dei modi per ottenere il valore di Kps di un sale consiste nel misurare la sua solubilità, cioè la quantità di sale necessaria per produrre una data quantità di soluzione satura. La concentrazione molare del sale nella sua soluzione satura viene chiamata solubilità molare ed è pari al numero di moli di sale disciolte in un litro di soluzione satura. La solubilità molare può essere utilizzata per calcolare K ps, assumendo che tutto il sale disciolto sia dissociato al 100% negli ioni che compaiono nella sua unità formula. Copyright © 2008 Zanichelli editore

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA UN SALE È MENO SOLUBILE SE IL SOLVENTE CONTIENE GIÀ UN SUO IONE ► Supponiamo di mescolare un po’ di cloruro di piombo (un sale a bassa solubilità) in acqua fino a che si stabilisce il seguente equilibrio: Copyright © 2008 Zanichelli editore Se adesso aggiungiamo una soluzione concentrata di un composto solubile del piombo, come Pb(NO 3)2, l’aumento di concentrazione di Pb 2+ determina uno spostamento dell’equilibrio verso sinistra, causando la precipitazione di una certa quantità di Pb. Cl 2. Questo fenomeno è una conseguenza del principio di Le Châtelier; il risultato è una minor solubilità di Pb. Cl 2 in una soluzione che già contiene Pb 2+ rispetto all’acqua pura.

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA UN SALE È MENO SOLUBILE SE IL SOLVENTE CONTIENE GIÀ UN SUO IONE ► Quando la miscela di Pb. Cl 2 e Pb(NO 3)2 giunge all’equilibrio, vi sono due fonti di Pb 2+ in soluzione. Uno ione liberato in soluzione da due o più sali viene definito ione comune. L’aggiunta dello ione comune abbassa la solubilità di Pb. Cl 2; il sale diviene meno solubile in presenza di Pb(NO 3)2 (o di qualsiasi altro sale di piombo solubile) di quanto lo sia in acqua pura. Copyright © 2008 Zanichelli editore Lo stesso effetto si produce se una soluzione di un cloruro solubile viene versata nella soluzione satura di Pb. Cl 2. L’aggiunta dello ione Cl- spinge l’equilibrio verso sinistra riducendo la quantità di Pb. Cl 2 disciolto. Lo ione comune in questo caso è Cl-.

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA UN SALE È MENO SOLUBILE SE IL SOLVENTE CONTIENE GIÀ UN SUO IONE ► Copyright © 2008 Zanichelli editore L’abbassamento della solubilità di un composto ionico in presenza dello ione comune è noto come effetto dello ione comune. Nella figura un sale solubile, come Na. Cl, esce dalla sua soluzione satura se si aggiunge acido cloridrico concentrato, una fonte di ioni Cl-. Come si vedrà nel prossimo esempio, l’effetto dello ione comune può ridurre in modo notevole la solubilità di un sale.

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA ► Kps INDICA SE SI FORMA UN PRECIPITATO IN SOLUZIONE Alcuni esperimenti prevedono la preparazione di soluzioni che contengono molti ioni. Può accadere che in queste condizioni si formi un precipitato e si debba quindi variare la composizione della soluzione. Un precipitato si forma solo se la soluzione è sovrasatura. Possiamo valutare se una soluzione di un dato sale è insatura, satura o sovrasatura, utilizzando le concentrazioni degli ioni per calcolare il prodotto ionico e quindi confrontando quest’ultimo con K ps. Copyright © 2008 Zanichelli editore

18. 6 UN SALE INDISCIOLTO È IN EQUILIBRIO CON LA SOLUZIONE CHE LO CIRCONDA ► Kps INDICA SE SI FORMA UN PRECIPITATO IN SOLUZIONE Se la soluzione è satura, il prodotto ionico è uguale a K ps; se è insatura, le concentrazioniche sono minori rispetto alla soluzione satura e il prodotto ionico risulta inferiore a Kps. Se, però, la soluzione è sovrasatura, contiene una quantità di soluto maggiore di quella necessaria per la saturazione e le concentrazioniche sono maggiori rispetto a una soluzione satura; il prodotto ionico risulta quindi più alto del valore di Kps. Ciò può essere riassunto come segue: si forma precipitato prodotto ionico > Kps (soluzione sovrasatura) Copyright © 2008 Zanichelli editore non si forma precipitato prodotto ionico = Kps (soluzione satura) prodotto ionico < Kps (soluzione insatura)
- Slides: 61