Cantidades en Qumica Uma unidad de masa atmica










- Slides: 13

Cantidades en Química Uma (unidad de masa atómica; unidad relativa) masa 12 C = 12 uma (antes fueron el hidrógeno y el oxígeno) 1 uma = 1, 66054 x 10 -24 g 1 g = 6, 02214 x 1023 uma

Masa atómica relativa promedio: abundancia isotópica l l En la naturaleza C: 98, 892 % 12 C + 1, 108 % 13 C. Masa promedio del carbono= (0, 98892)(12 uma) + (0, 0108)(13, 00335 uma) = 12, 011 uma. ¿Cuál es la masa de un átomo de carbono?

Las masas (o pesos) atómicos (de la Tabla Periódica) para muchos elementos corresponden a las masas o pesos atómicos promedio (notar excepciones). ¿Por qué los valores de masas atómicas no son números enteros? ¿ Todos los elementos tienen más de un isotopo?

Fórmulas Químicas l l Fórmula molecular Fórmula mínima Masa molecular, masa fórmula Absoluta (en gramos) Relativa (en uma)

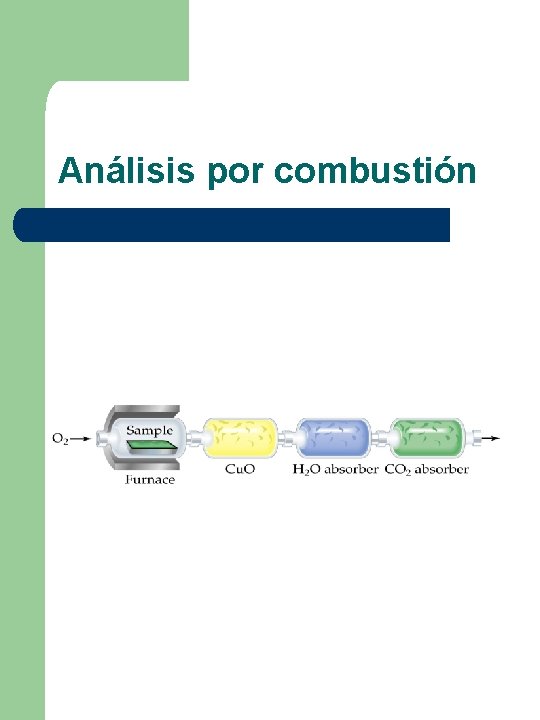
Composición centesimal (porcentual) l l l Expresa los gramos de cada uno de los elementos presentes en 100 gramos de ese compuesto. Se determina experimentalmente (análisis por combustión) También puede calcularse a partir de la fórmula del compuesto (molecular o mínima)

Análisis por combustión

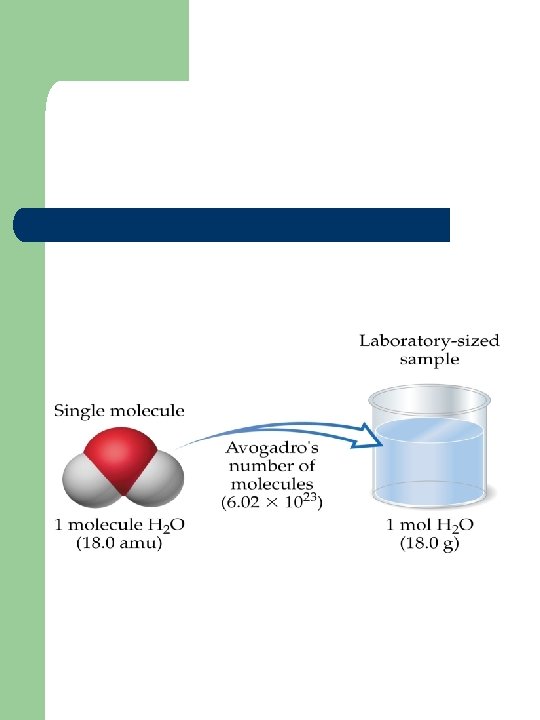
MOL 1 mol de X contiene 6, 023 1023 X l l l 1 mol de moléculas contiene 6, 023 1023 moléculas 1 mol de átomos contiene 6, 023 1023 átomos 1 mol de iones contiene 6, 023 1023 iones

Experimentalmente: 1 mol de 12 C tiene una masa of 12 g. Otra definición: Cantidad de sustancia en una muestra que contiene tantas unidades (átomos, moléculas o iones) como átomos de 12 C hay en 12 gramos de C.

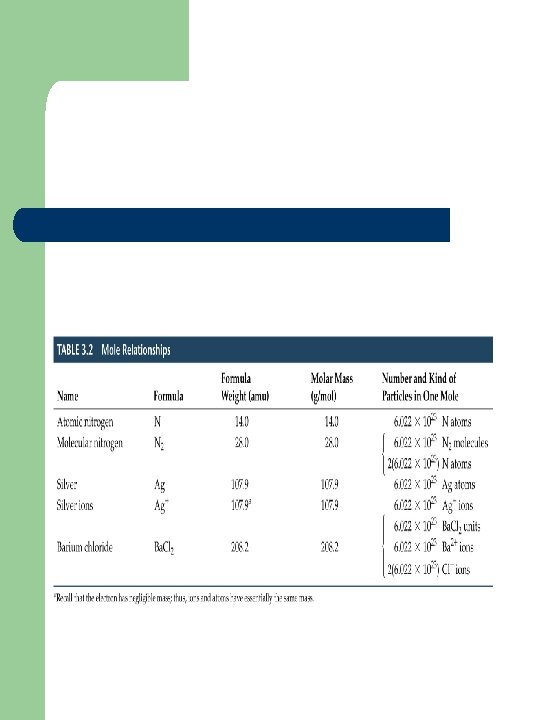
l Masa molar (la masa de un mol de un elemento o compuesto) La masa de un mol de elemento monoatómico en gramos es numéricamente igual a la masa atómica (dato de la tabla). Masa de un mol de moléculas. Masa de un mol de fórmulas mínimas. l l l Masa de 1 mol de 12 C = 12 g. Masa de 1 mol de C Masa de 1 mol de O 2 Masa de 1 mol de Na. Cl Masa de 1 mol de H 2 O



Un mol de agua, un mol de cloruro de sodio y un mol de N 2

Obtención de la fórmula mínima de un compuesto A partir de la composición centesimal