CANCER DU REIN THERAPIES CIBLEES HISTORIQUE Chimiothrapie inefficace

CANCER DU REIN THERAPIES CIBLEES

HISTORIQUE • Chimiothérapie inefficace • Immunothérapie : IL 2 et/ou INFα • Gain en survie modeste : 3 à 7 mois • Toxicité non négligeable (IL 2 IV) • Facteurs pronostiques de réponse à • • l’immunothérapie : Etat général, délai depuis néphrectomie, un seul site métastatique Impact favorable de la néphrectomie première 5 à 10% de long répondeurs en rémission complète à plus de 5 ans
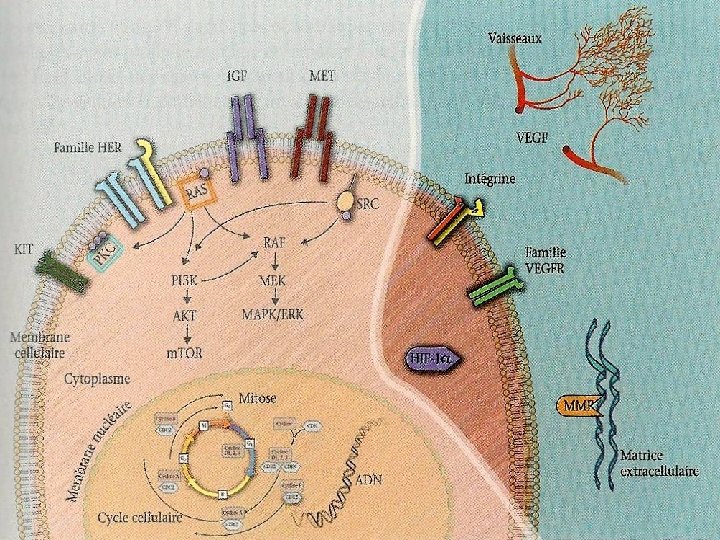

ANGIOGENESE ET CANCER DU REIN • Carcinome à Cellules claires : hypervascularisation • 60 % d’inactivation du gène VHL • Protéine VHL = suppresseur de tumeur • Protéine VHL régule la sécrétion des protéines de l’angiogénèse (VEGF), de la prolifération cellulaire (PDGF), du métabolisme glucidique et de l’EPO

ANTIANGIOGENIQUES • Avastin : anti VEGF circulant intraveineux • Sutent, nexavar (per os) : inhibiteur multicible VEGFR-R + PDGFR + CKIT … Profil de tolérance différent entre ces deux groupes

AVASTIN (Bevacizumab) • Premier antangiogénique utilisé en clinique • AC humanisé anti VEGF circulant (ligand) • • • monocible Forme : IV Développement : colorectal, sein, poumon, rein, glioblastome…ovaire… AMM K rein métastatique : première ligne

Phase III IFα +/- Avastin (Escudier, lancet 2007) • 659 patients néphrectomisés, métastatiques, non • • prétraités IFα 9 M UI SC x 3/s +/- Avastin 10 mg/kg/2 s TTP doublé (10. 2 vs 5. 4 mois) Réponse : 31% vs 13 % (1% CR) OS non significatif (p= 0. 067)
Phase III IFα +/- Avastin (CALGB JCO 2008) • 732 patients néphrectomisés, métastatiques non prétraités • IFα 9 M UI SC x 3/s +/- Avastin 10 mg/kg/2 s • TTP : 8. 5 mois vs 5. 2 mois • ORR : 25, 5% vs 13% • Survie globale : non signifiatif

AVASTIN : PRECAUTIONS D’EMPLOI • Risque hémorragique : patient sous anticoagulant, • • tumeur hémorragique Risque perforatif (tumeur digestive en place) Risque thromboembolique : phlébite ou embolie récente, AVC récent, patient vasculaire Risque hypertensif : HTA non équilibrée Risque néphrologique : surveillance protéinurie Ce ne sont pas des contre indications absolues : le rapport bénéfice/risque est apprécié au cas par cas

Sunitinib (SUTENT) • Inhibiteur multicible à activité antithyrosine • • kinase de VEGFR-1, VEGFR-2, VEGFR-3, PDGFR et KIT Forme orale AMM : cancer du rein première ligne métastatique – Tumeur stromale digestive
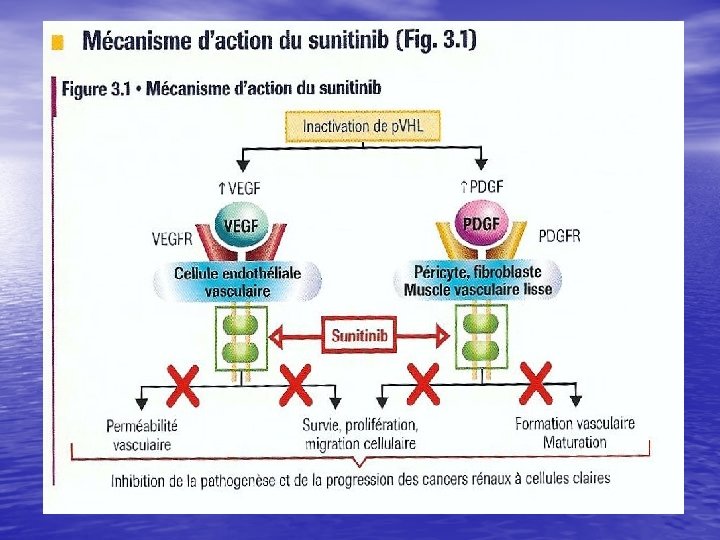

Sunitinib phase III (Mozer, N Engl J Med, 2007 et JCO 2009) • 750 patients CCR métastatique en première ligne • 90% néphrectomie première • 101 centres • Métas cérébrales, HTA non contrôlée exclues • Sutent 50 mg/j 4 s/6 vs IFα (3 à 9 MUI SC x 3/s) • Pronostic MSKCC bon ou intermédiaire
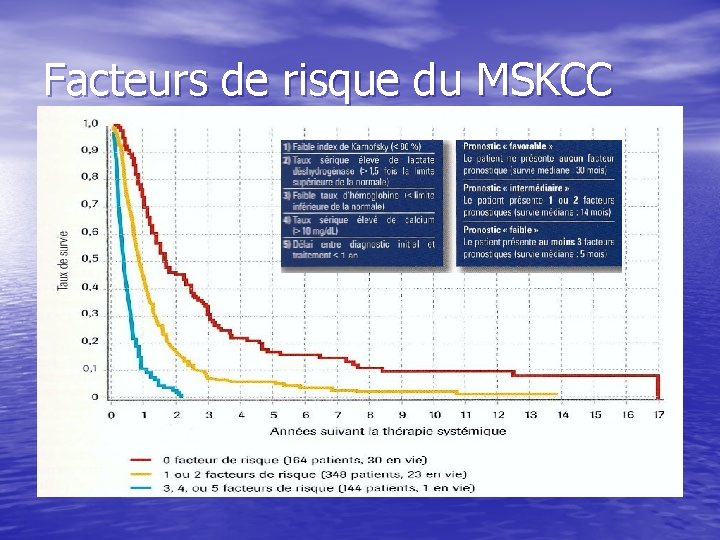
Facteurs de risque du MSKCC

Sunitinib phase III (Mozer, N Engl J Med, 2007 et JCO 2009) • RO (RECIST): 47 % vs 6% (p< 0. 001) • RC : 3% • SSP : 11 vs 5 mois (p< 0. 001) • SG : 26. 4 vs 21. 8 mois (p=0. 51) • Devient significatif si exclusion du cross over • Médiane de survie non atteinte chez les patients • de bon pronostique Amélioration de la qualité de vie ds le bras SUTENT

SUTENT : principaux effets secondaires • • • • Fréquents Fatigue Troubles digestifs : diarrhée, nausées, gastrite, reflux gastro oesophagien Inflammation de la bouche, aphtes Perte d’appétit, modification du goût Modification de la couleur de la peau et des cheveux Hypertension artérielle Syndrome main pieds, sécheresse cutanée Risque hémorragique : arrêt si intervention chirurgicale ou soins dentaires hémorragiques Peu fréquents troubles cardiovasculaires : diminution de la FEVG Embolie pulmonaire (1%) Risque hémorragique intratumoral (1% G 3 -4) Cytopénie (<1% G 3 -4) Hypothyroïdie Insuffisance hépatique (<1%) Pancréatite leucoencéphalopathie

Sunitinib phase III (Mozer, N Engl J Med, 2007 et JCO 2009) • Plus d’effets secondaires de tous grades dans le • • bras sutent Asthénie G 3 -4 IFα 12% vs 7 % Neutropénie : sutent 12% vs 7% Thrombopénie : sutent 8% vs 0 Diarrhée : sutent 5% vs 0 Vomissements : sutent 4% vs 0 HTA : sutent 8% vs 1% Syndrome mains pieds : 5% vs 0

SORAFENIB (nexavar) • Inhibiteur multicible à activité antithyrosine kinase de VEGFR-2, VEGFR 3, PDGFα, FLT-3 et c-KIT • Forme orale

Phase III TARGET (Escudier N Eng J Med, 2007) • Deuxième ligne après échec de cytokine • 903 patients : sorafenib 400 mg/j vs placebo • Néphrectomie première : 94% • Pronostic favorable ou intermediaire (MSKCC) • Métastases cérébrales exclues • Objectif principal : survie globale

Phase III TARGET (Escudier N Eng J Med, 2007) • Analyse intermédiaire : SSP 5. 5 mois vs 2. 8 en faveur du sorafenib (p< 0. 01) : cross over autorisé • Contrôle de la maladie : 75 % vs 55% • Réponse objective : 10% (RC 1%) • Pas de différence statistique significative en SG (19. 3 vs 15. 9 mois)

Nexavar : principaux effets secondaires • • • • • Syndrome main pieds, rash cutané (6% G 3 -4) Diarrhée (2% G 3 -4) Fatigue (5% G 3 -4) Troubles digestifs : diarrhée, nausées, anorexie, perte de poids mucite, aphtes Modification du goût Arthralgies, myalgie Alopécie , modification couleur de peau et cheveux, rash Hypertension artérielle et troubles cardiovasculaires (4%) Risque hémorragique : arrêt si intervention chirurgicale ou soins dentaires hémorragiques Cytopénie : anémie Hypothyroïdie Hyperamylasémie Insuffisance hépatique Dépression Leucoencéphalopathie enrouement

Sorafenib vs IFα en première ligne métastatique (Escudier, JCO 2009) • Phase II randomisée • 189 patients • SSP 5. 7 mois vs 5. 6 mois • Sorafenib n’est pas la molécule de référence en première ligne

INHIBITEURS DE m. TOR
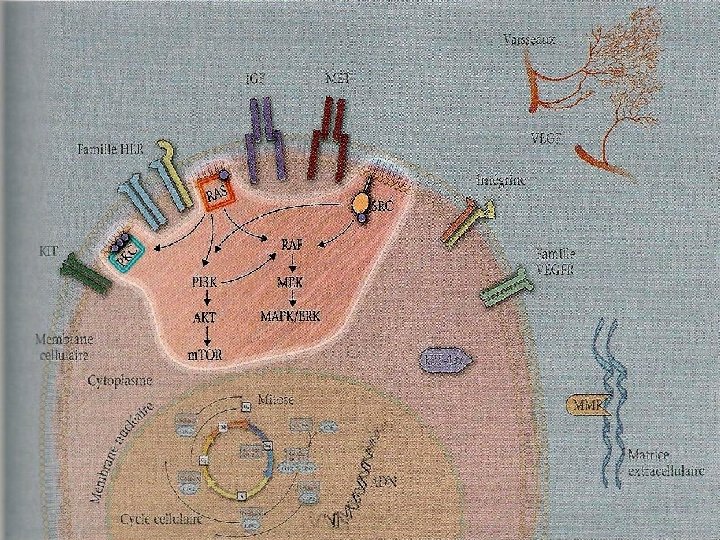


TEMSILORIMUS (Torisel) • Inhibiteur spécifique de m-TOR • Voie IV • AMM en première ligne métastatique chez les patients présentant au mois 3 des 6 facteurs de risque pronostique (MSKCC)
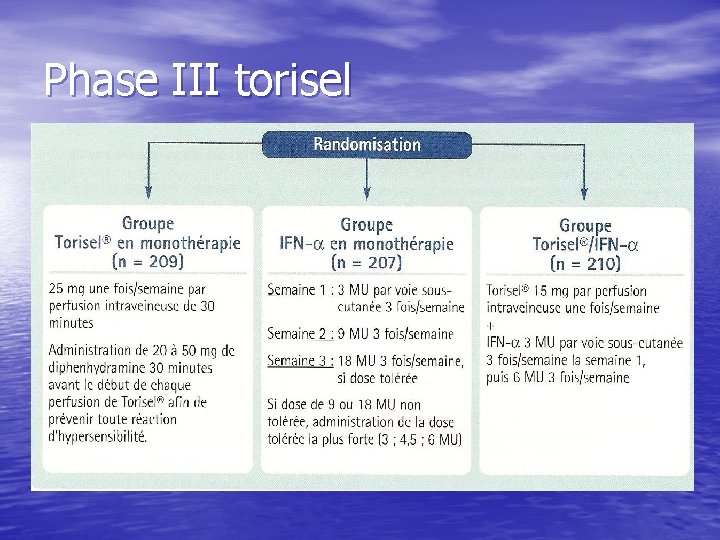
Phase III torisel
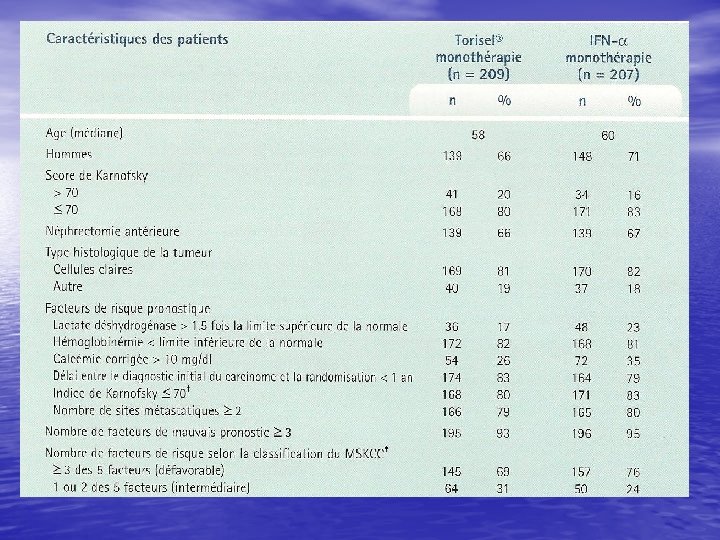
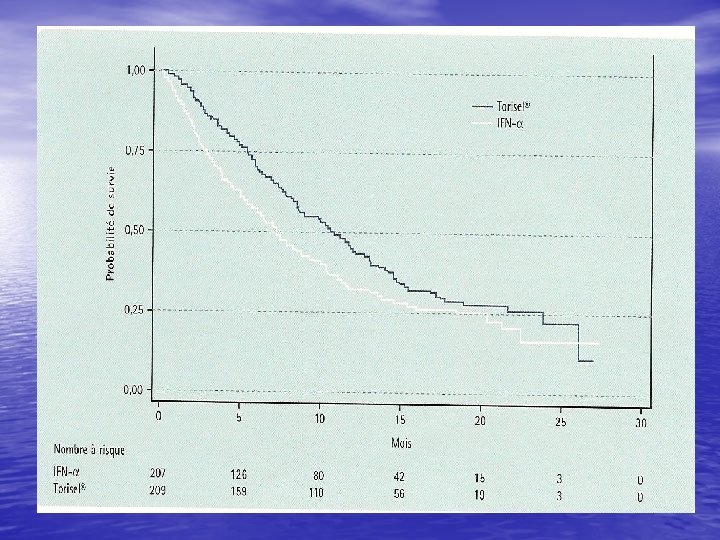


Résultats de tolérance • Toxicité G 3 -4 inférieure ds bras torisel (6 vs • • • 78%) Rash cutané (47%), œdèmes périphériques (27%) et stomatite (20%) Hyperglycémie 26%), hyperlipidémie (27%) hypersensibilité

AFINITOR • Inhibiteur m-TOR • Voie orale: 1 cpé 10 mg tous les jours • AMM : après échec d’une première ligne avec anti. VEGF
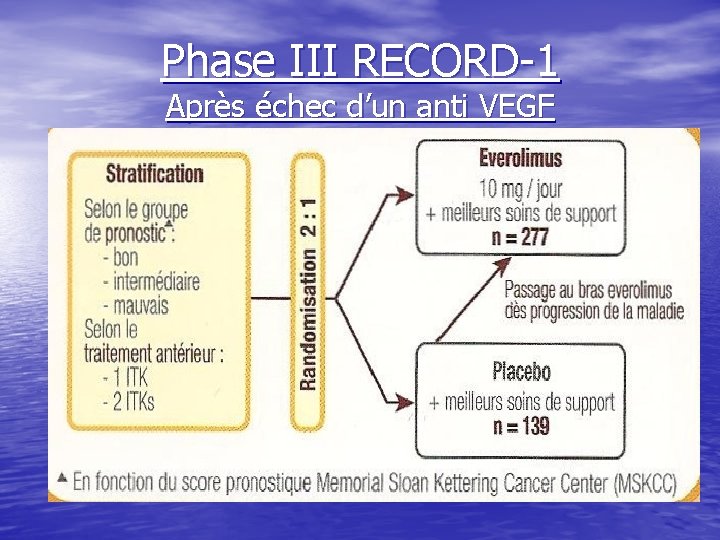
Phase III RECORD-1 Après échec d’un anti VEGF
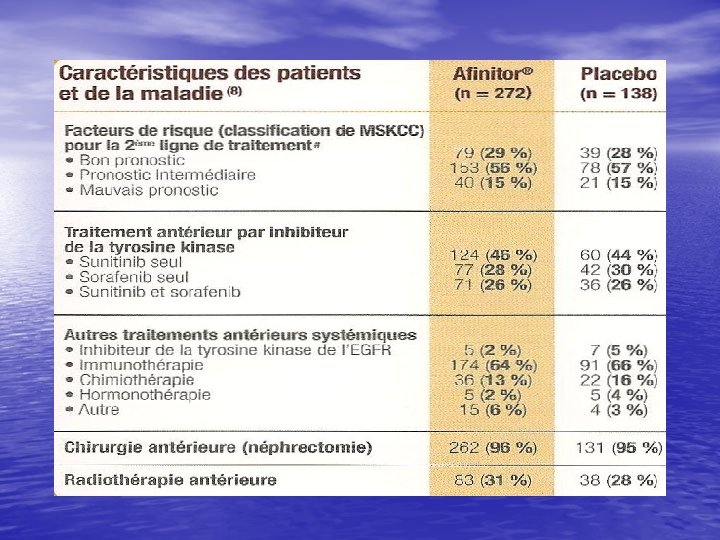
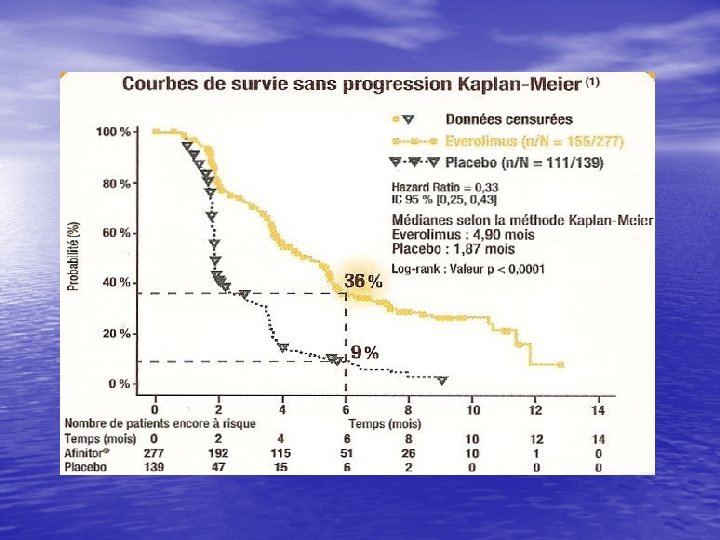
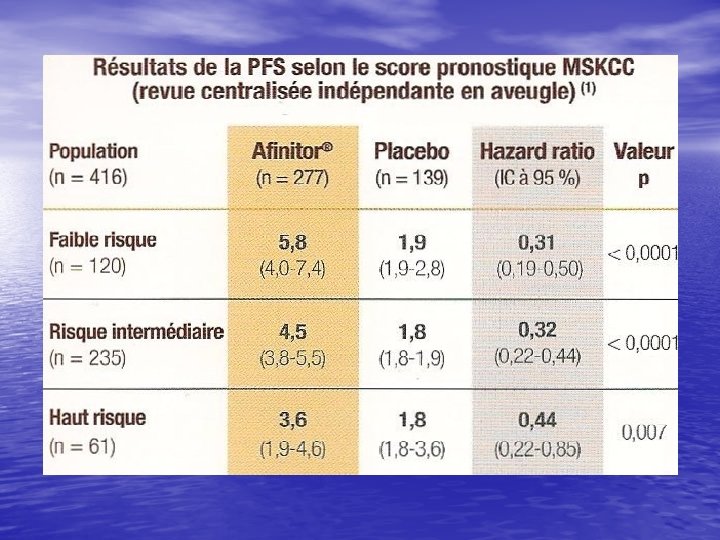

Tolérance afinitor Grade 3 -4 > 2% • Lymphopénie • Hyperglycémie • Anémie • hypercholesterolémie • stomatite • Asthénie • Pneumopathie interstitielle
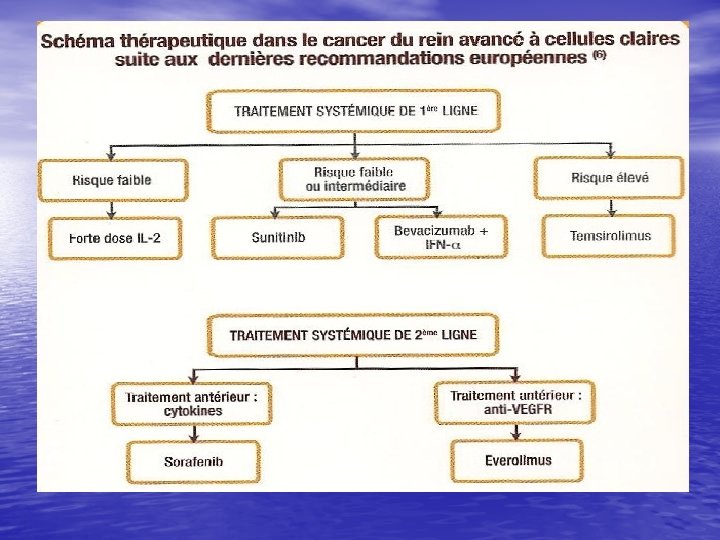

Impact économique (NICE) • Etude de coût non prospective ds 4 pays européens • Analyse le coût du médicament et la sévérité des effets indésirables G 3 -4 et leur coût de gestion • Bevacizumab 171300 Livre/an • Sutent 71462 Livre/an

QUESTIONS D’AVENIR • Place de la néphrectomie première ? • Possibilités d’association de thérapies ciblées ? • Meilleure stratégie ? • Traitement des cancers du rein non à cellules claires ?
- Slides: 40