Cancer du col utrin prcoce Protocole SFOG DR























- Slides: 46


Cancer du col utérin précoce Protocole SFOG DR Malik Boukerrou ; Pr Denis Vinatier ; D Pr Gilles Body Pr Jean Levêque Chirurgie Gynécologique Hôpital Jeanne de Flandre CHRU Lille

Bilan d’extension détermine le stade FIGO N’intègre pas le statut ganglionnaire Importance du volume tumoral Stades précoces: <4 cm pas d’atteinte paramétriale pas d’atteinte à distance

early stage disease : FIGO IA IB 1 II A 1

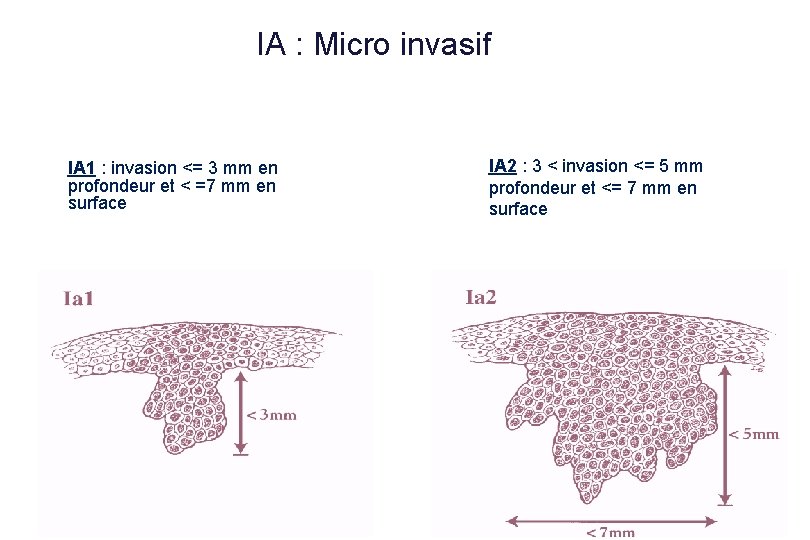
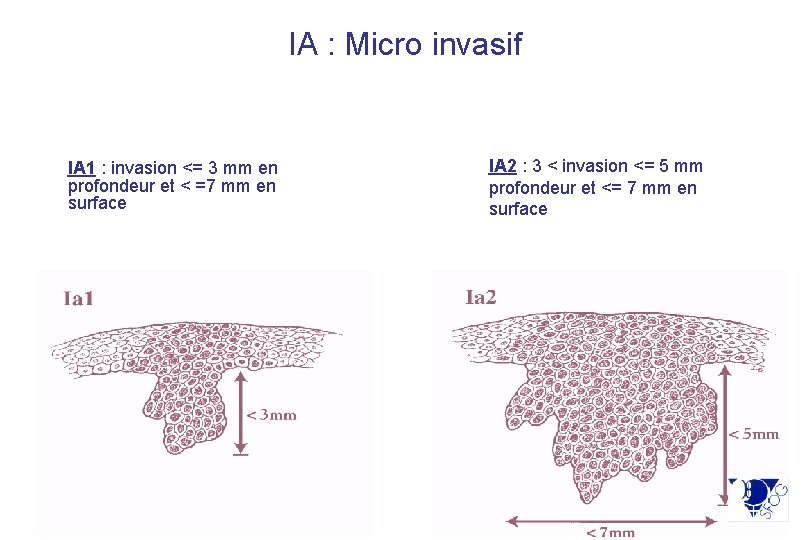
IA : Micro invasif IA 1 : invasion <= 3 mm en profondeur et < =7 mm en surface IA 2 : 3 < invasion <= 5 mm profondeur et <= 7 mm en surface

Bilan d’extension pré thérapeutique Histologie est indispensable Examen clinique IRM pelvienne Exploration abdominale: IRM ou scanner TEP TDM recommandée > stades IB 1 Evaluation radiologique thoracique >IB 1 Dosage du SCC Dans les formes infracliniques: Conisation

Les options thérapeutiques 1 - Hystérectomie élargie +- lymphadénectomie +- RT +- chimiothérapie 2 – Radiochimiothérapie concomittante adaptée 3 – Trachélectomie élargie 4 – Conisation simle

Prise en charge thérapeutique Le protocole choisi dépend de deux facteurs 1 – La taille Les cancers micro invasifs 2 cm 2 -4 cm 2 – Le statut ganglionnaire pelvien et para aortique

Lésion micro-invasive : faire préciser sa taille en mm (en surface et profondeur) et si présence d’emboles vasculaires sur pièce de conisation le plus souvent

Conisation à l’anse électrique

Conisation au bistouri froid

Conisation au laser

Saignement

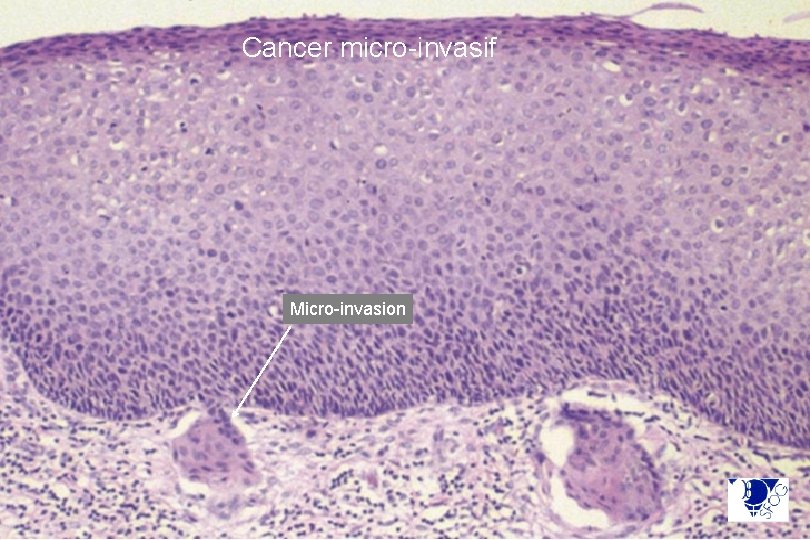
Cancer micro-invasif Micro-invasion

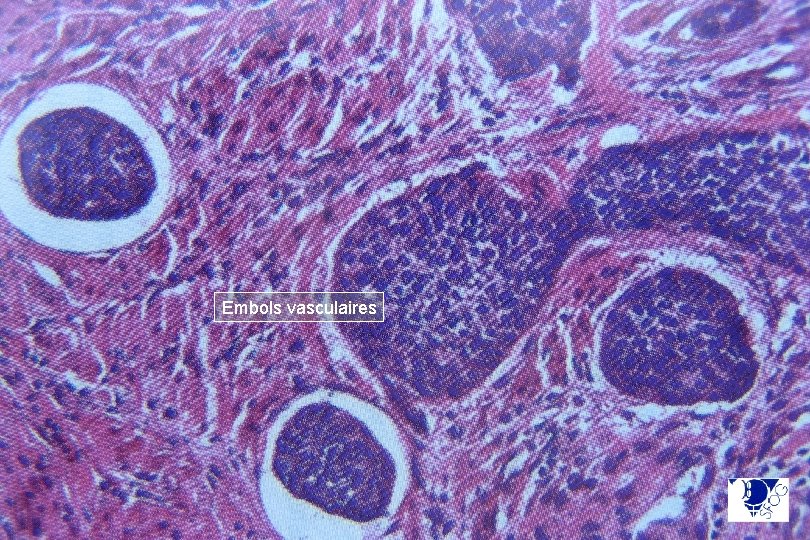
Cancer micro-invasif Embols vasculaires

IA : Micro invasif IA 1 : invasion <= 3 mm en profondeur et < =7 mm en surface IA 2 : 3 < invasion <= 5 mm profondeur et <= 7 mm en surface

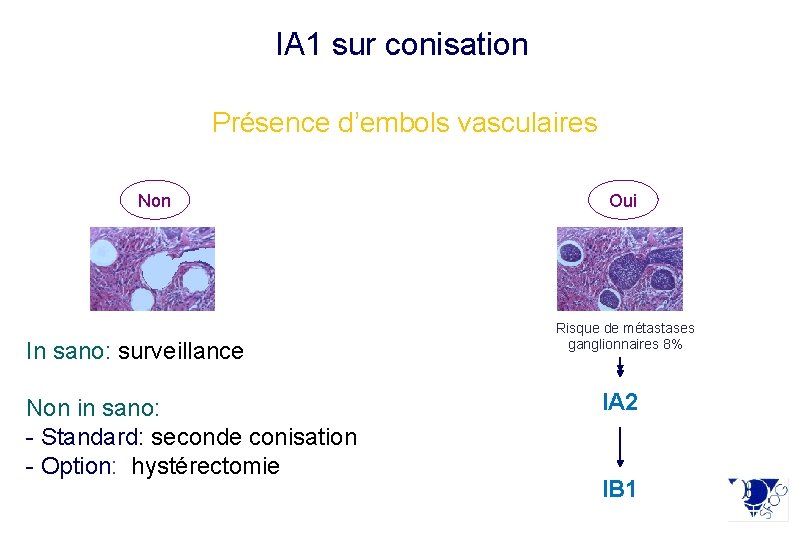
IA 1 sur conisation Présence d’embols vasculaires Non In sano: surveillance Non in sano: - Standard: seconde conisation - Option: hystérectomie Oui Risque de métastases ganglionnaires 8% IA 2 IB 1

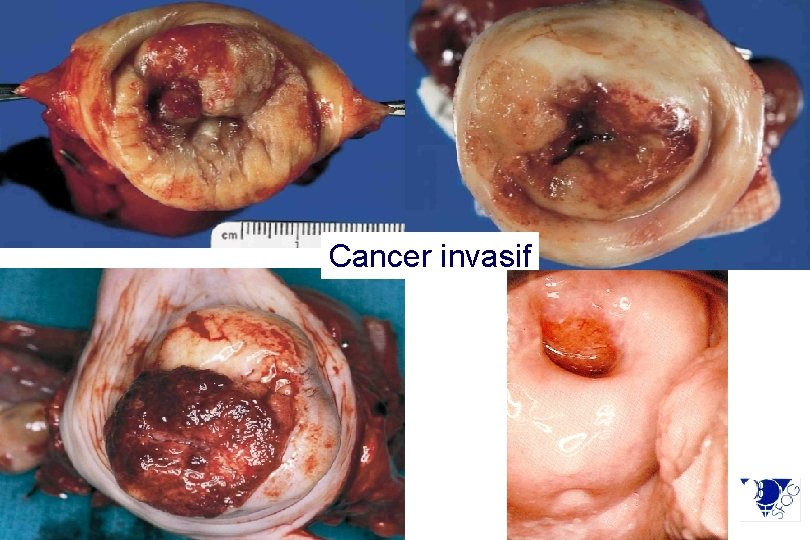
Cancer invasif retour

Stade IA 2, IB 1, IIA, IIB <= 4 cm Stade IB 2, IIA–IIB, III, IV > 4 cm

Stade IA 2, IB 1, IIA, IIB <= 4 cm Stade IB 2, IIA–IIB, III, IV > 4 cm

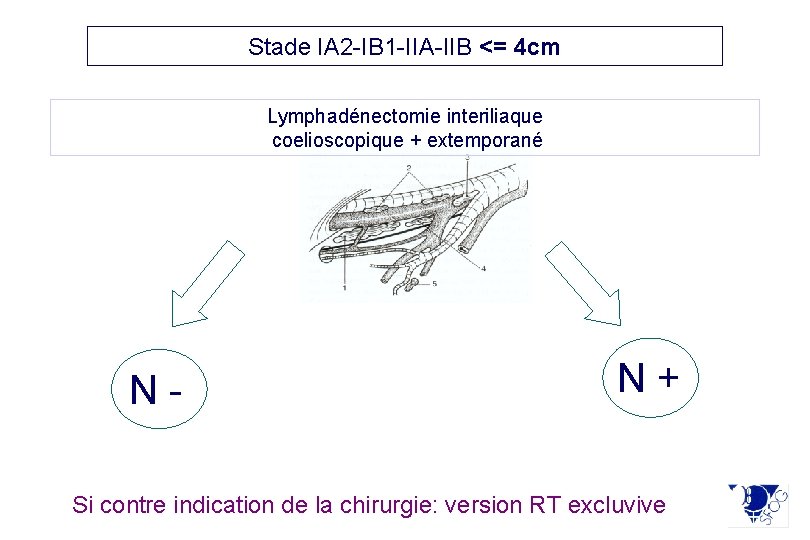
Stade IA 2 -IB 1 -IIA-IIB <= 4 cm Lymphadénectomie interiliaque coelioscopique + extemporané N- N+ Si contre indication de la chirurgie: version RT excluvive

Absence de métastases ganglionnaires pelviennes (N 0) T<=2 cm Standard: Colpo-hystérectomie type wertheim - soit Wertheim par laparotomie - soit Wertheim par coelioscopie - soit Coelio Shauta Options: Traitement conservateur de l’utérus Traitement conservateur des ovaires

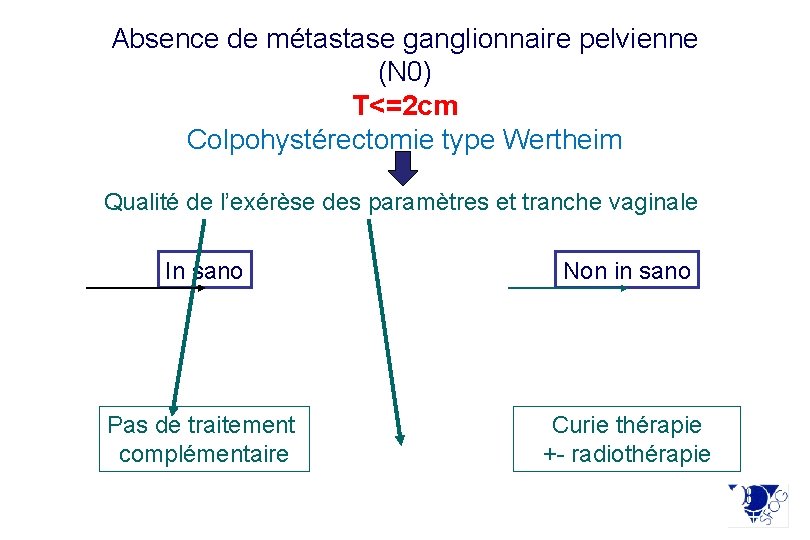
Absence de métastase ganglionnaire pelvienne (N 0) T<=2 cm Colpohystérectomie type Wertheim Qualité de l’exérèse des paramètres et tranche vaginale In sano Non in sano Pas de traitement complémentaire Curie thérapie +- radiothérapie

Absence de métastases ganglionnaires pelviennes (N 0) T<=2 cm les options Traitement conservateur de l’utérus Conisation pré thérapeutique ge compatible avec une grossesse Désir de grossesse Taille <=2 cm Absence d’embole vasculaire p. N (0) Marge endocervicale >= 8 mm Trachélectomie élargie Traitement conservateur des ovaires Cancer épidermoïde <2 cm et p. N(0) ge inférieur à 40 ans

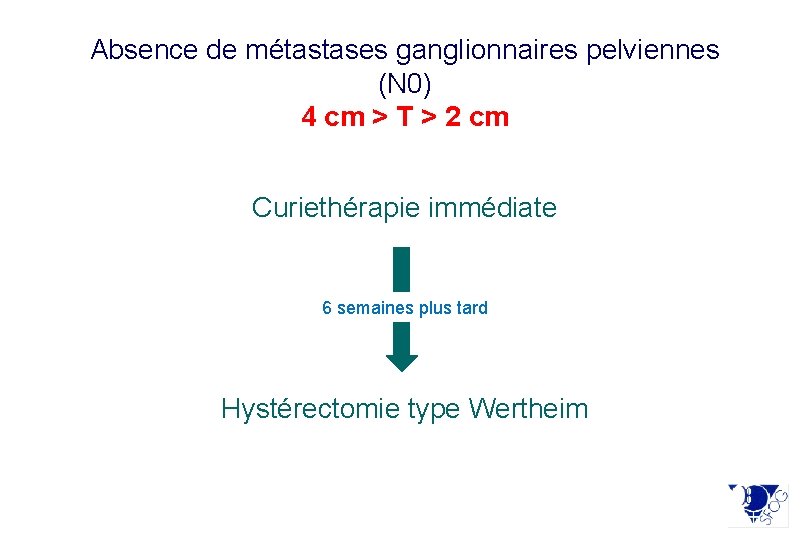
Absence de métastases ganglionnaires pelviennes (N 0) 4 cm > T > 2 cm Curiethérapie immédiate 6 semaines plus tard Hystérectomie type Wertheim

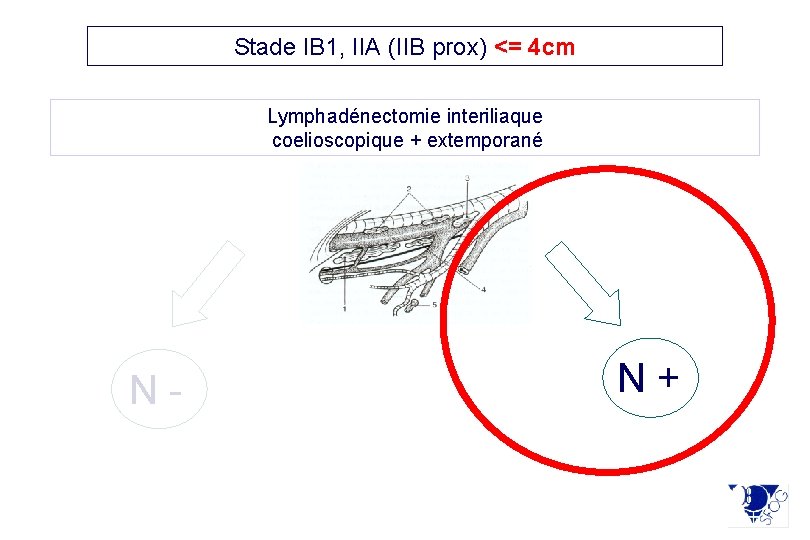
Stade IB 1, IIA (IIB prox) <= 4 cm Lymphadénectomie interiliaque coelioscopique + extemporané N- N+

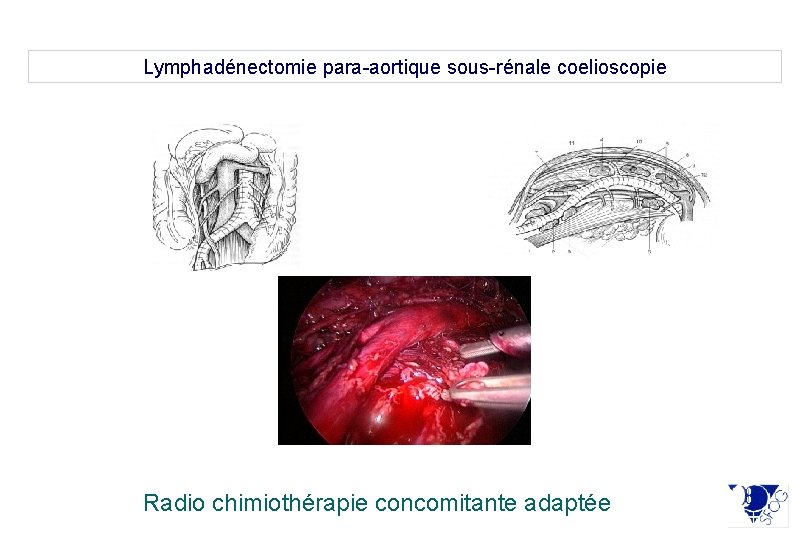
Lymphadénectomie para-aortique sous-rénale coelioscopie Radio chimiothérapie concomitante adaptée

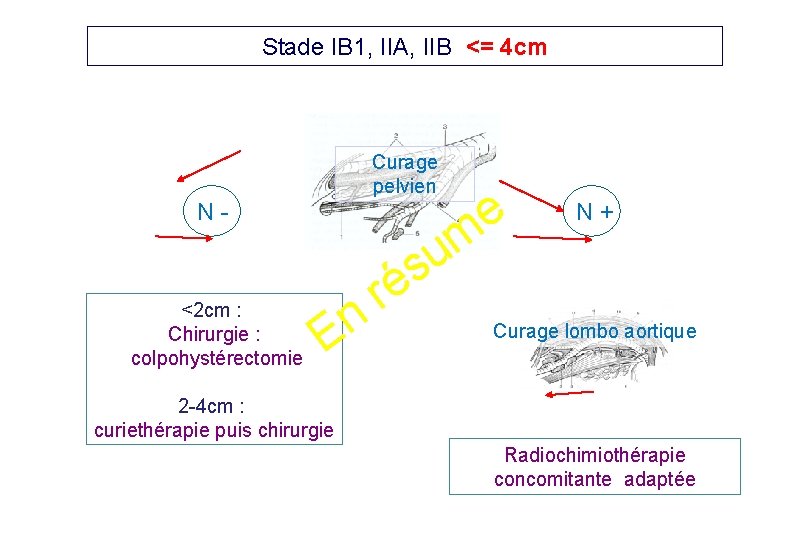
Stade IB 1, IIA, IIB <= 4 cm Curage pelvien N- <2 cm : Chirurgie : colpohystérectomie n E r m u s é e N+ Curage lombo aortique 2 -4 cm : curiethérapie puis chirurgie Radiochimiothérapie concomitante adaptée

Stade IB 1, IIA, IIB <= 4 cm OPTION RADIOTHERAPIE EXCLUSIVE Radiothérapie pelvienne et curiethérapie

Stade IA 2, IB 1 <= 4 cm Stade IB 2, IIA–IIB, III, IV > 4 cm

Stade IB 2, IIA, IIB, Stade IIB, III, IV > 4 cm Standard: Radio-chimiothérapie concomitante Curiethérapie utéro vaginale.

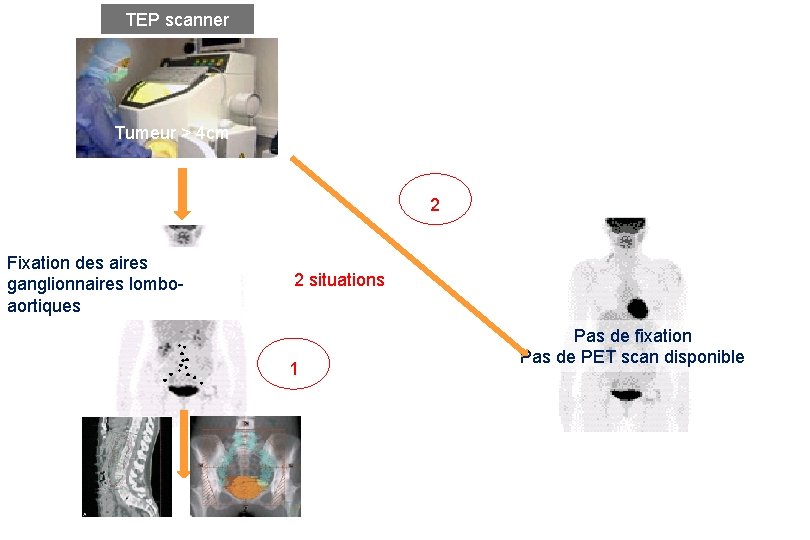
TEP scanner Tumeur > 4 cm 2 Fixation des aires ganglionnaires lomboaortiques 2 situations 1 Pas de fixation Pas de PET scan disponible

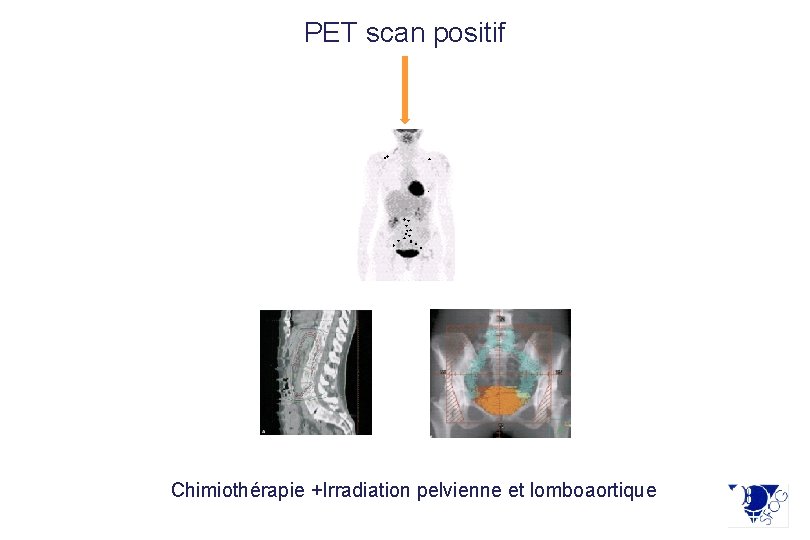
PET scan positif Tumeur > 4 cm Chimiothérapie +Irradiation pelvienne et lomboaortique

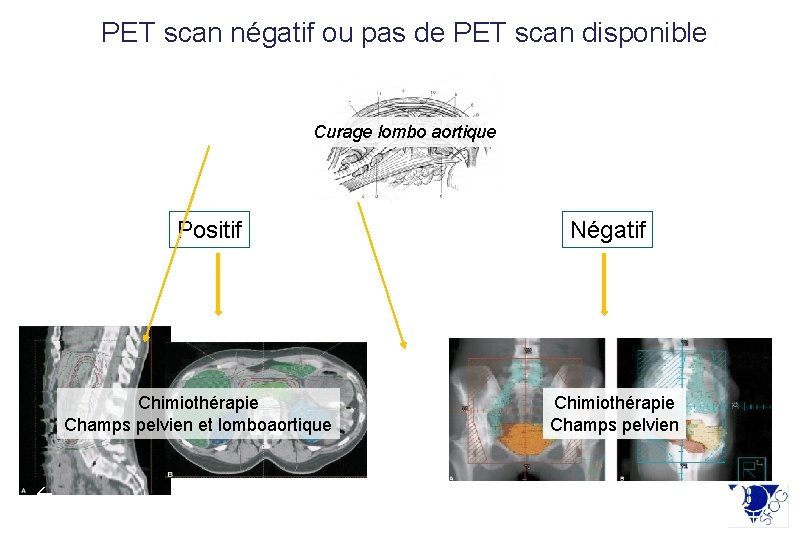
PET scan négatif ou pas de PET scan disponible Curage lombo aortique Positif Chimiothérapie Champs pelvien et lomboaortique Négatif Chimiothérapie Champs pelvien

La radiochimiothérapie concomitante Radiothérapie externe (RTE) : 45 Gy en moyenne en 5 -6 semaines par fraction de 1. 8 Gy par séance Chimiothérapie base de Cis-platine : 40 mg/m², 1 fois/semaine pendant les 5 -6 semaines de la RTE. Atteindre le seuil de 200 mg/m 2 Curiethérapie après radiothérapie externe : 20 Gy

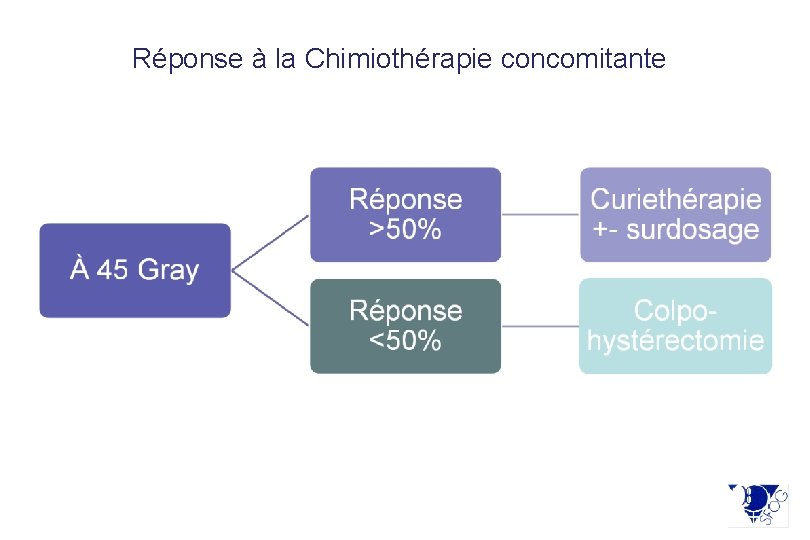
Réponse à la Chimiothérapie concomitante

La survie à 5 ans: 100 % : cancers in situ 80 % : stade I et IIa 55 % : stade IIb 35 % : stade III 10 % : stade IV

Surveillance 90 % des récidives surviennent dans les deux premières années Modalités de surveillance Examen clinique seul sans frottis en cas d’hystérectomie Pas d’examen radiologique systématique Examens complémentaires uniquement en cas de symptômes En cas de trachélectomie Frottis annuel Option: IRM Rythme Tous les 4 mois pendant 2 ans puis tous les 6 mois pendant 3 ans Puis annuel

Déséscalade chirurgicale Quel intérêt à réséquer les paramètres dans les stades précoces ? Hystérectomie radicale Trachélectomie élargie Conisation simple – hystérectomie simple

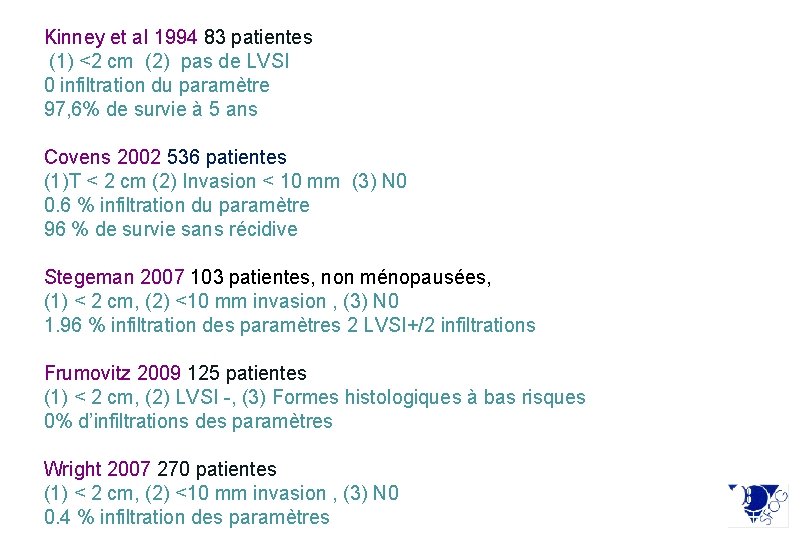
Kinney et al 1994 83 patientes (1) <2 cm (2) pas de LVSI 0 infiltration du paramètre 97, 6% de survie à 5 ans Covens 2002 536 patientes (1)T < 2 cm (2) Invasion < 10 mm (3) N 0 0. 6 % infiltration du paramètre 96 % de survie sans récidive Stegeman 2007 103 patientes, non ménopausées, (1) < 2 cm, (2) <10 mm invasion , (3) N 0 1. 96 % infiltration des paramètres 2 LVSI+/2 infiltrations Frumovitz 2009 125 patientes (1) < 2 cm, (2) LVSI -, (3) Formes histologiques à bas risques 0% d’infiltrations des paramètres Wright 2007 270 patientes (1) < 2 cm, (2) <10 mm invasion , (3) N 0 0. 4 % infiltration des paramètres

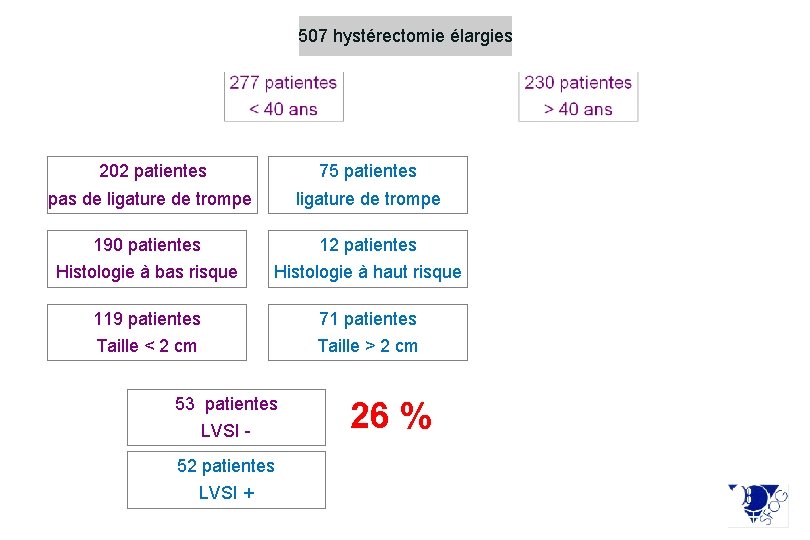
507 hystérectomie élargies 202 patientes 75 patientes pas de ligature de trompe 190 patientes 12 patientes Histologie à bas risque Histologie à haut risque 119 patientes 71 patientes Taille < 2 cm Taille > 2 cm 53 patientes LVSI 52 patientes LVSI + 26 %


34 patientes 10 patientes IA 2 -> Conisation 24 patientes IB 1 -> Trachélectomie simple 47 mois de suivie 1 récidives centrales -> Radiochimiothérapie 1 dysplasie sévère -> Hystérectomie 24 /32 tentatives de grossesse 17 /24 grossesses – 12 enfants vivants

Gynecol Oncol 2011; 123: 557 -560 36 patientes – age moyen 31 ans Taille moyenne 11. 7 mm (8 – 25) Adénocarcinome 33 % des cas LVSI 5/36 (14%) Suivie 56 mois 1 récidive glandulaire 17 patientes enceintes – 21 grossesses 14 enfants vivants ( 11 à terme – 27 et 32 sa)

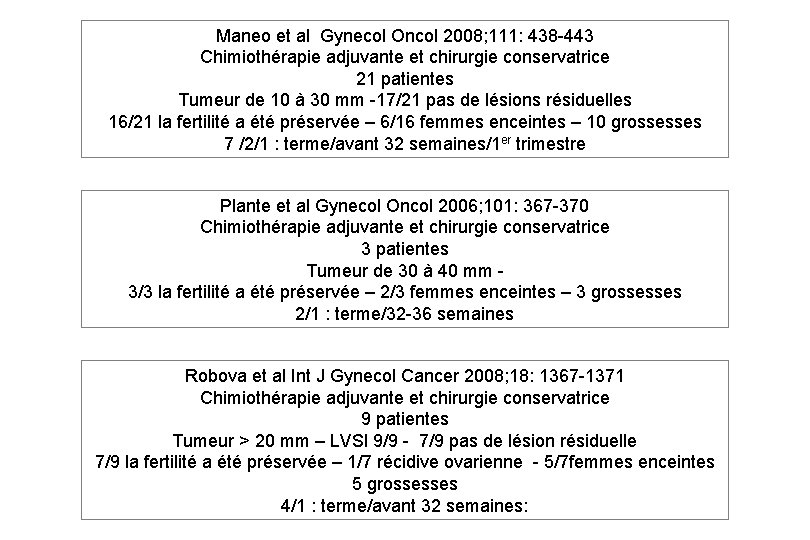
Maneo et al Gynecol Oncol 2008; 111: 438 -443 Chimiothérapie adjuvante et chirurgie conservatrice 21 patientes Tumeur de 10 à 30 mm -17/21 pas de lésions résiduelles 16/21 la fertilité a été préservée – 6/16 femmes enceintes – 10 grossesses 7 /2/1 : terme/avant 32 semaines/1 er trimestre Plante et al Gynecol Oncol 2006; 101: 367 -370 Chimiothérapie adjuvante et chirurgie conservatrice 3 patientes Tumeur de 30 à 40 mm 3/3 la fertilité a été préservée – 2/3 femmes enceintes – 3 grossesses 2/1 : terme/32 -36 semaines Robova et al Int J Gynecol Cancer 2008; 18: 1367 -1371 Chimiothérapie adjuvante et chirurgie conservatrice 9 patientes Tumeur > 20 mm – LVSI 9/9 - 7/9 pas de lésion résiduelle 7/9 la fertilité a été préservée – 1/7 récidive ovarienne - 5/7 femmes enceintes 5 grossesses 4/1 : terme/avant 32 semaines:

Marchiole et al Gynecol Oncol 2011; 122: 484 -490 Chimiothérapie adjuvante et chirurgie conservatrice 7 patientes Tumeur de 30 à 45 mm -4/7 pas de lésions résiduelles - 3/7 réponse >50% Suivie 22 mois Pas de rechute 1/7 tentative de grosesse 1/7 enfant vivant