Campaa Informativa Notificacin de sospechas de reacciones adversas








- Slides: 14

Campaña Informativa Notificación de sospechas de reacciones adversas a medicamentos por la ciudadanía ¿Le ha sentado mal algún medicamento? Si lo notifica puede contribuir a que los Medicamentos sean más seguros

Farmacovigilancia Qué es Es una actividad de salud pública destinada a la identificación, cuantificación, evaluación y prevención de los riesgos asociados al uso de los medicamentos una vez comercializados. Objetivos • Promover el uso racional y seguro de los medicamentos • Contribuir a la evaluación y comunicación de los riesgos y beneficios de los medicamentos • Fomentar la educación e información en materia de seguridad a profesionales de la salud y a la ciudadanía.

Centro de Farmacovigilancia de Navarra • Está integrado en el Servicio de Ciudadanía Sanitaria, Aseguramiento y Garantías del Departamento de Salud del Gobierno de Navarra • Forma parte del Sistema Español de Farmacovigilancia • Es la unidad responsable de ejecutar el programa de notificación espontánea de reacciones adversas a medicamentos. Reacción adversa a medicamento (RAM): Cualquier respuesta nociva y no intencionada a un medicamento

Datos año 2016 • 1. 335 notificaciones de sospechas de RAM recibidas 1. 081 en 2015 (incremento 23%) • 1. 052 Casos de sospecha de RAM evaluados y registrados 979 en 2015 (incremento 7. 4%) Ø 264 notificaciones graves Ø 788 notificaciones no graves • Tasa de notificación espontánea: 1. 601 notificaciones por millón de habitantes/año.

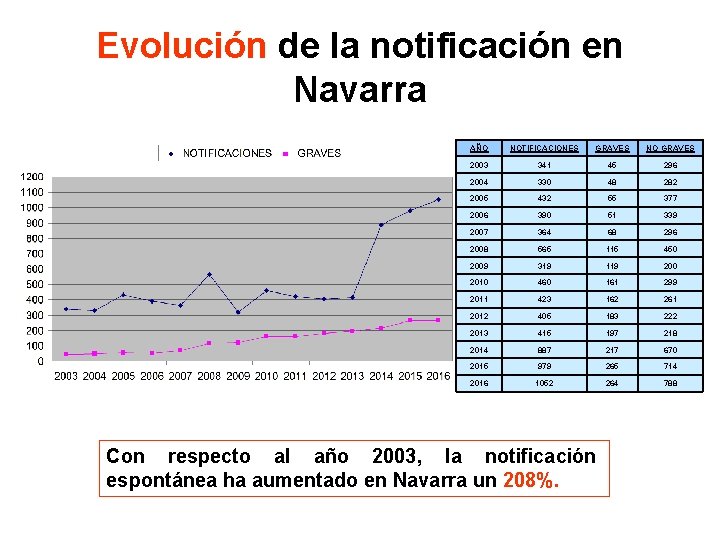
Evolución de la notificación en Navarra AÑO NOTIFICACIONES GRAVES NO GRAVES 2003 341 45 296 2004 330 48 282 2005 432 55 377 2006 390 51 339 2007 364 68 296 2008 565 115 450 2009 319 119 200 2010 460 161 299 2011 423 162 261 2012 405 183 222 2013 415 197 218 2014 887 217 670 2015 979 265 714 2016 1052 264 788 Con respecto al año 2003, la notificación espontánea ha aumentado en Navarra un 208%.

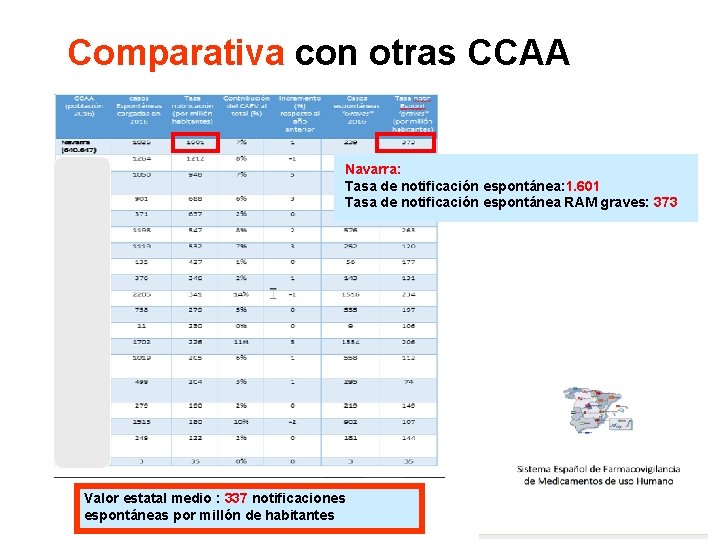
Comparativa con otras CCAA Navarra: Tasa de notificación espontánea: 1. 601 Tasa de notificación espontánea RAM graves: 373 Valor estatal medio : 337 notificaciones espontáneas por millón de habitantes

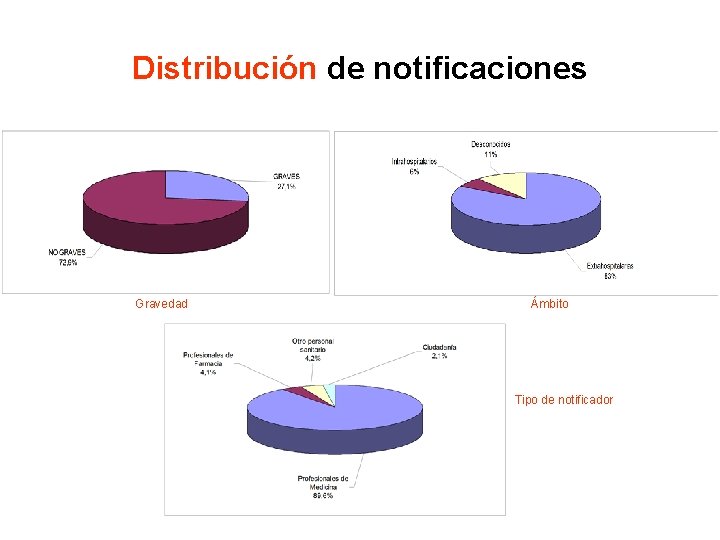
Distribución de notificaciones Gravedad Ámbito Tipo de notificador

Campaña informativa

Para qué sirve • Detectar señales: Riesgos previamente no conocidos o cambios de riesgos ya conocidos • De confirmarse, implica acciones en la práctica clínica para prevenir / minimizar un riesgo para los pacientes • Consecuencias de tipo regulador: – Inclusión de nuevas advertencias, precauciones, contraindicaciones en los prospectos de los medicamentos. – Emisión de notas informativas de seguridad. – Se puede llegar incluso a retirar un medicamento del mercado si se confirma que la relación beneficio riesgo es desfavorable.

Quién puede notificar PROFESIONALES DE SALUD PACIENTES INDUSTRIA FARMACÉUTICA

Qué es importante notificar • Medicamentos sujetos a seguimiento adicional • Vigilancia más estricta • Se dispone de menos información de seguridad • Reacciones adversas desconocidas • Reacciones adversas graves • Otras • RAM en personas ancianas y menores • RAM por interacción farmacológica • RAM por mal uso o abuso de un medicamento • RAM por uso de un medicamento en una indicación no autorizada • RAM por falta de eficacia • RAM de plantas medicinales y productos de herboristería • Errores de medicación con daño

Cómo se notifica

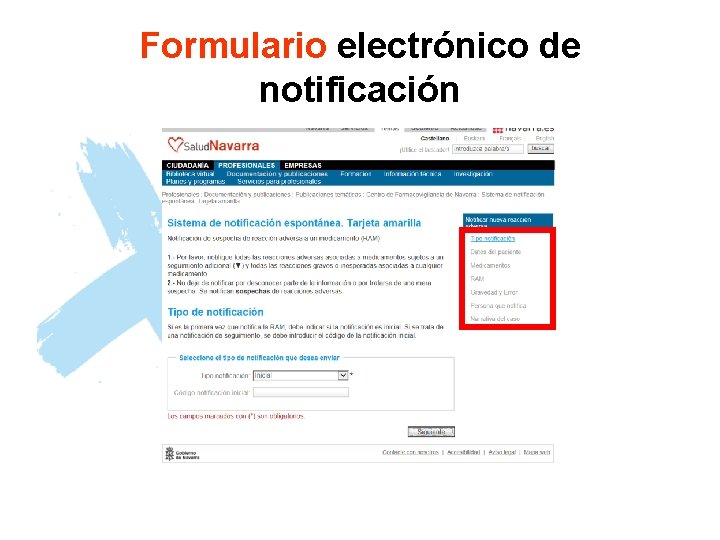
Formulario electrónico de notificación

Datos de contacto Centro de Farmacovigilancia de Navarra • C/ Amaya 2 A, tercera planta. 31002 Pamplona. • Formulario electrónico: www. RAM. navarra. es • Correo electrónico: Farmacovigilancia@navarra. es • Teléfono: 848 422584