CAMBIOS DE ENERGA DURANTE UNA REACCIN QUMICA Colegio

“CAMBIOS DE ENERGÍA DURANTE UNA REACCIÓN QUÍMICA”. Colegio Agustiniano El Bosque Un proyecto educativo único y propio Ciencias Naturales Química / I medio

Objetivos y contenidos a tratar Contenidos Objetivos v Cambios de energía en una reacción química v Sistema v Entorno v Universo v Endotérmico v Exotérmico v Conocer el de energía dentro de una reacción, analizarlo como un sistema que pierde o gana energía y la interacción de sistema y entorno.

ORIENTACIONES PARA EL ESTUDIO DE ESTE TEMA… Pon atención a los siguientes puntos para poder ayudar a poder desarrollar de mejor manera esta presentación: Ø Te recomiendo contar con un lugar para poder estudiar, no debe ser una sala de estudio, puede ser el comedor de tu casa, lo importante es que lo ordenes y acomodes para ti y tus artículos de estudio. Ø Por unos minutos desconéctate del celular, has de cuenta que estas en la sala de clases y deja el móvil en silencio. Ø Organiza tu tiempo y mantén una continuidad de principio a fin de esta presentación, lo que te permitirá no perder el hilo de el o los temas a estudiar. Ø Lee con atención y calma la información que recibirás así como las instrucciones para los desafíos o ejercitación que se encuentra al final de esta presentación. Ø Visita cada link sugerido ya sea durante la presentación o al final de ella, dado que tienen como objetivo poder explicar o reforzar de una manera distinta el contenido abordado. Ø Cuando apliques lo aprendido, trata en primera instancia de resolverlo por ti mismo, cuando ya no logres hacerlo pasa a apoyarte de las diapositivas anteriores o del texto escolar, luego al finalizar, podrás siempre encontrar el solucionario de la actividad en esta presentación. Ø No es necesario imprimir estas diapositivas, para realizar la actividad será suficiente con que la registres en tu cuaderno de asignatura, sino lo posees podrás realizarlo en una hoja anexa que luego podrás pegar en tu cuaderno. Ø Para todos los temas que se traten, en esta y en todas las presentaciones que trabajemos, podrás apoyarte del texto escolar. De no poseerlo, se adjuntará en cada ppt el link para verlo en línea. Ø Lo más importante es que confíes en tus capacidades, eres capaz de lograr lo que te propongas.
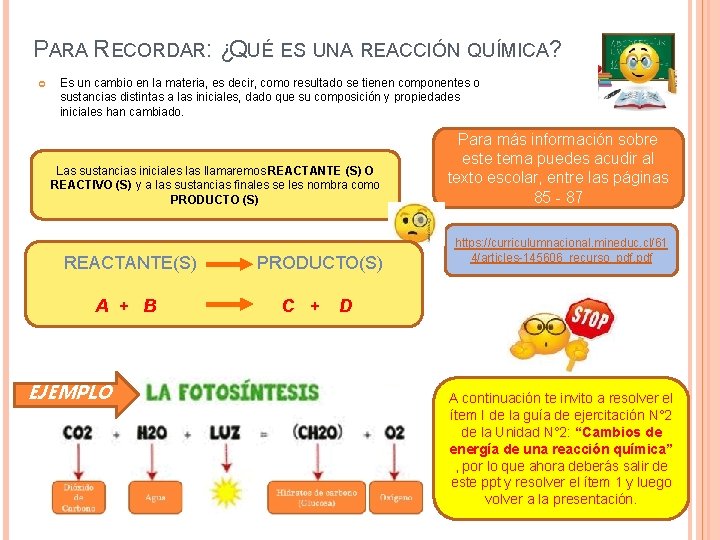
PARA RECORDAR: ¿QUÉ ES UNA REACCIÓN QUÍMICA? Es un cambio en la materia, es decir, como resultado se tienen componentes o sustancias distintas a las iniciales, dado que su composición y propiedades iniciales han cambiado. Las sustancias iniciales las llamaremos REACTANTE (S) O REACTIVO (S) y a las sustancias finales se les nombra como PRODUCTO (S) REACTANTE(S) A + B EJEMPLO PRODUCTO(S) C + Para más información sobre este tema puedes acudir al texto escolar, entre las páginas 85 - 87 https: //curriculumnacional. mineduc. cl/61 4/articles-145606_recurso_pdf. pdf D A continuación te invito a resolver el ítem I de la guía de ejercitación N° 2 de la Unidad N° 2: “Cambios de energía de una reacción química” , por lo que ahora deberás salir de este ppt y resolver el ítem 1 y luego volver a la presentación.
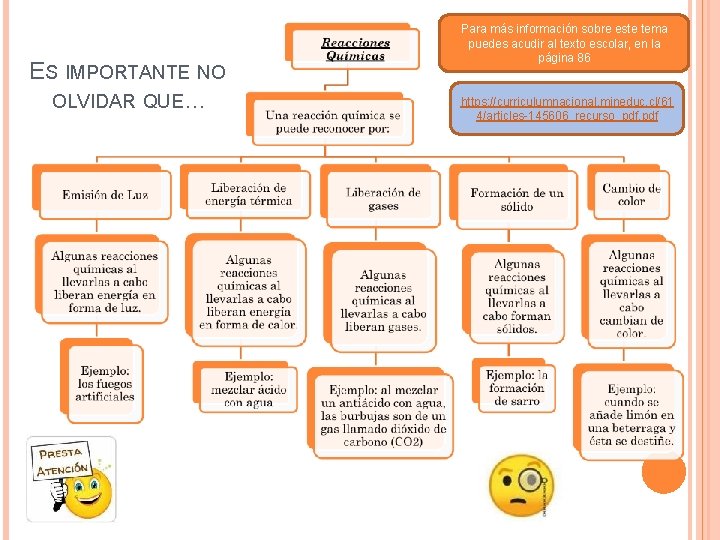
ES IMPORTANTE NO OLVIDAR QUE… Para más información sobre este tema puedes acudir al texto escolar, en la página 86 https: //curriculumnacional. mineduc. cl/61 4/articles-145606_recurso_pdf. pdf
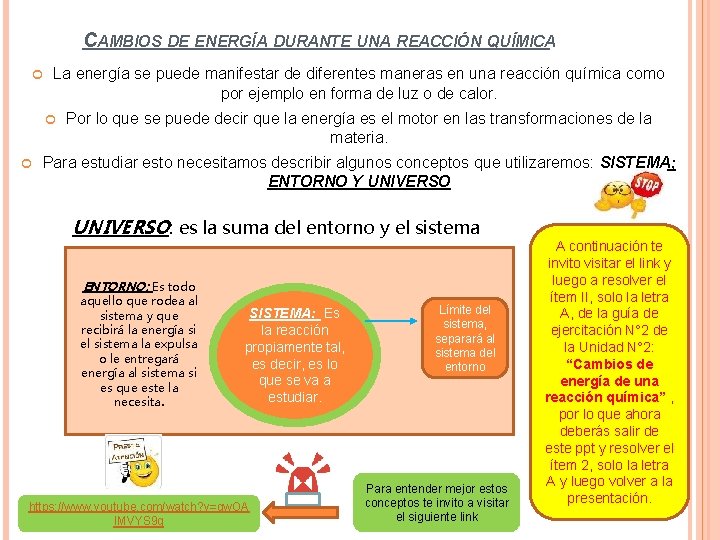
CAMBIOS DE ENERGÍA DURANTE UNA REACCIÓN QUÍMICA La energía se puede manifestar de diferentes maneras en una reacción química como por ejemplo en forma de luz o de calor. Por lo que se puede decir que la energía es el motor en las transformaciones de la materia. Para estudiar esto necesitamos describir algunos conceptos que utilizaremos: SISTEMA; ENTORNO Y UNIVERSO: es la suma del entorno y el sistema ENTORNO: Es todo aquello que rodea al sistema y que recibirá la energía si el sistema la expulsa o le entregará energía al sistema si es que este la necesita. SISTEMA: Es la reacción propiamente tal, es decir, es lo que se va a estudiar. https: //www. youtube. com/watch? v=gw. OA l. MVYS 9 g Límite del sistema, separará al sistema del entorno Para entender mejor estos conceptos te invito a visitar el siguiente link A continuación te invito visitar el link y luego a resolver el ítem II, solo la letra A, de la guía de ejercitación N° 2 de la Unidad N° 2: “Cambios de energía de una reacción química” , por lo que ahora deberás salir de este ppt y resolver el ítem 2, solo la letra A y luego volver a la presentación.
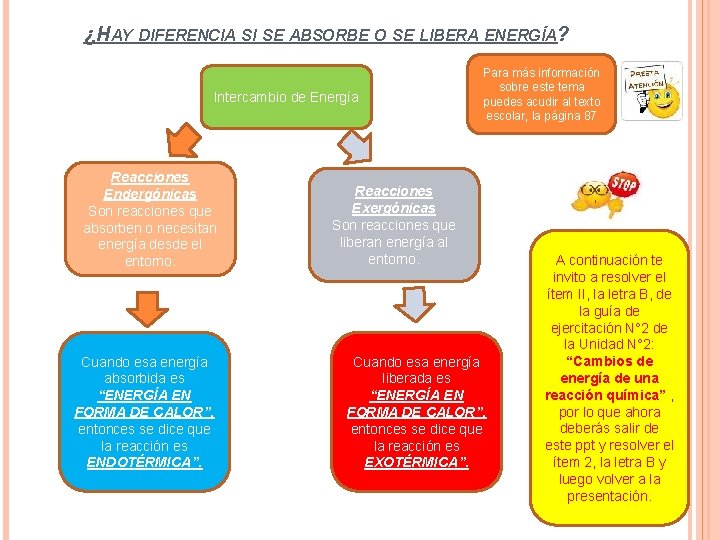
¿HAY DIFERENCIA SI SE ABSORBE O SE LIBERA ENERGÍA? Intercambio de Energía Reacciones Endergónicas Son reacciones que absorben o necesitan energía desde el entorno. Cuando esa energía absorbida es “ENERGÍA EN FORMA DE CALOR”, entonces se dice que la reacción es ENDOTÉRMICA”. Para más información sobre este tema puedes acudir al texto escolar, la página 87 Reacciones Exergónicas Son reacciones que liberan energía al entorno. Cuando esa energía liberada es “ENERGÍA EN FORMA DE CALOR”, entonces se dice que la reacción es EXOTÉRMICA”. A continuación te invito a resolver el ítem II, la letra B, de la guía de ejercitación N° 2 de la Unidad N° 2: “Cambios de energía de una reacción química” , por lo que ahora deberás salir de este ppt y resolver el ítem 2, la letra B y luego volver a la presentación.
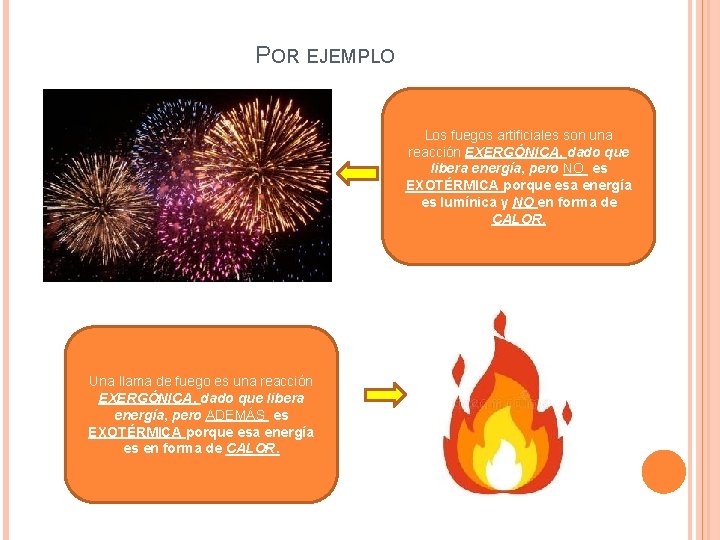
POR EJEMPLO Los fuegos artificiales son una reacción EXERGÓNICA, dado que libera energía, pero NO es EXOTÉRMICA porque esa energía es lumínica y NO en forma de CALOR. Una llama de fuego es una reacción EXERGÓNICA, dado que libera energía, pero ADEMÁS es EXOTÉRMICA porque esa energía es en forma de CALOR.
PONGAMOS A PRUEBA LO APRENDIDO… Te invito a realizar un pequeño experimento para evidenciar lo que hemos estudiado hoy. Para esto necesitamos los siguientes materiales (solo elige uno de ellos) y reactivos e idealmente trabajar con la supervisión de un adulto. 1. - Primero lee con atención el miniexperimento y luego pon Materiales Reactivos manos a la obra. 2. - En caso de no contar con los Olla – hervidor o tetera Agua materiales, tranquilo, podrás acudir a tu memoria o el apoyo de Taza o tazón Té o café los integrantes de tu hogar y cuchara Azúcar o endulzante podrás responder de todos modos las preguntas. Primero pon a hervir agua, puede ser en una olla, una tetera o un hervidor (puede ser cualquiera de los 3, lo importante que este limpio) Cuando el agua este hervida ponla en una taza o tazón y agrega el té o café (el que más te guste), por último añade azúcar o endulzante a gusto. Una vez listo tu experimento puedes disfrutar de el, puedes utilizar la imagen como apoyo y responde: 1. - ¿En este caso quién es el sistema? R: __________________________ 2. - ¿Cuál es el limite del sistema? R: ___________________________ 3. - ¿Quién es el entorno? R: ________________________________ 4. - ¿Podemos definir que el sistema es endotérmico o exotérmico? R: _______________________________

SOLUCIONARIO DE LA ACTIVIDAD Antes de revisar las respuestas, te invito a realizar por ti mismo el experimento y poner a prueba tus capacidades, recuerda que de no ser posible desarrollar el experimento puedes observar la siguiente imagen: 1. - ¿En este caso quién es el sistema? R: El sistema es el agua con café o té y el azúcar o endulzante 2. - ¿Cuál es el limite del sistema? R: El Tazón o taza 3. - ¿Quién es el entorno? R: nosotros, la mesa donde apoyamos la taza 4. - ¿Podemos definir que el sistema es endotérmico o exotérmico? R: Es exotérmico, le entrega su energía en forma de calor al entorno. Por eso se enfría.

MUCHAS GRACIAS POR SU ATENCIÓN. Recuerda que cualquier duda o consulta la puedes realizar a través del correo electrónico: quimica 1 med@agustiniano. cl A continuación te invito a realizar una AUTOEVALUACIÓN , donde se evaluará lo estudiado durante esta presentación. Para esto debes ingresar al tablón de la asignatura en trabajo de clase.
- Slides: 11