Cambio a IPr monoterapia Estudio PIVOT Estudio PIVOT

Cambio a IP/r monoterapia § Estudio PIVOT
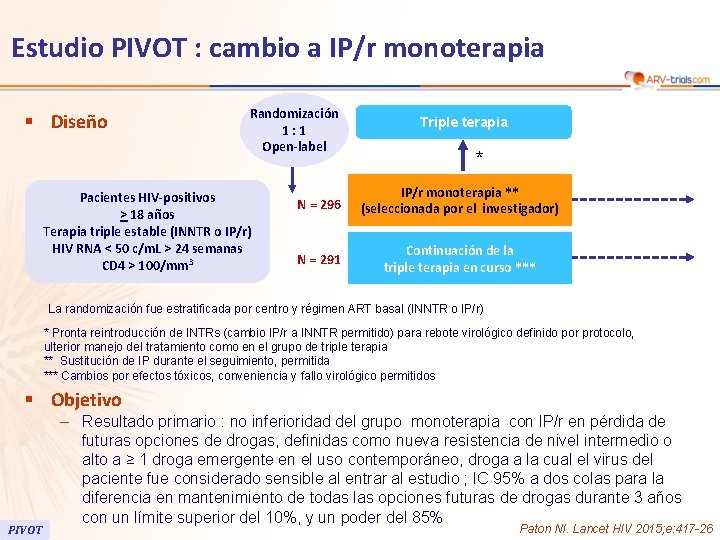
Estudio PIVOT : cambio a IP/r monoterapia § Diseño Randomización 1: 1 Open-label Pacientes HIV-positivos > 18 años Terapia triple estable (INNTR o IP/r) HIV RNA < 50 c/m. L > 24 semanas CD 4 > 100/mm 3 Triple terapia * N = 296 IP/r monoterapia ** (seleccionada por el investigador) N = 291 Continuación de la triple terapia en curso *** La randomización fue estratificada por centro y régimen ART basal (INNTR o IP/r) * Pronta reintroducción de INTRs (cambio IP/r a INNTR permitido) para rebote virológico definido por protocolo, ulterior manejo del tratamiento como en el grupo de triple terapia ** Sustitución de IP durante el seguimiento, permitida *** Cambios por efectos tóxicos, conveniencia y fallo virológico permitidos § Objetivo PIVOT – Resultado primario : no inferioridad del grupo monoterapia con IP/r en pérdida de futuras opciones de drogas, definidas como nueva resistencia de nivel intermedio o alto a ≥ 1 droga emergente en el uso contemporáneo, droga a la cual el virus del paciente fue considerado sensible al entrar al estudio ; IC 95% a dos colas para la diferencia en mantenimiento de todas las opciones futuras de drogas durante 3 años con un límite superior del 10%, y un poder del 85% Paton NI. N, Lancet 2015; e: 417 -26 Paton CROIHIV 2014, Abs. 550 LB
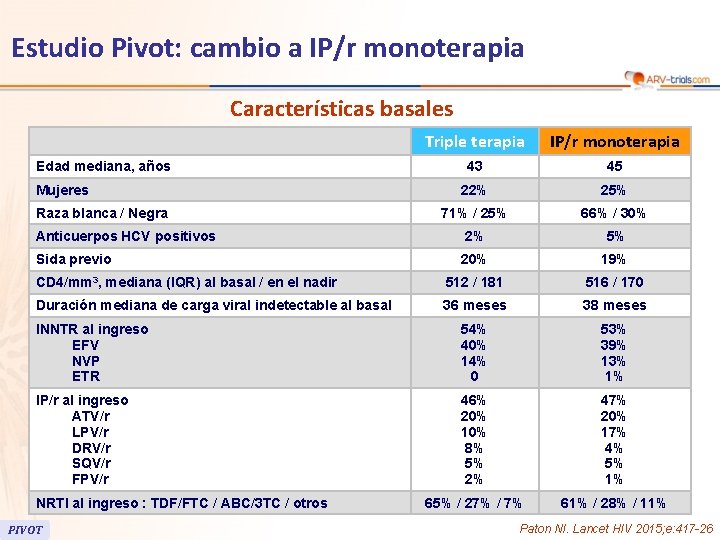
Estudio Pivot: cambio a IP/r monoterapia Características basales Triple terapia IP/r monoterapia 43 45 22% 25% 71% / 25% 66% / 30% Anticuerpos HCV positivos 2% 5% Sida previo 20% 19% CD 4/mm 3, mediana (IQR) al basal / en el nadir 512 / 181 516 / 170 Duración mediana de carga viral indetectable al basal 36 meses 38 meses INNTR al ingreso EFV NVP ETR 54% 40% 14% 0 53% 39% 13% 1% IP/r al ingreso ATV/r LPV/r DRV/r SQV/r FPV/r 46% 20% 10% 8% 5% 2% 47% 20% 17% 4% 5% 1% 65% / 27% / 7% 61% / 28% / 11% Edad mediana, años Mujeres Raza blanca / Negra NRTI al ingreso : TDF/FTC / ABC/3 TC / otros PIVOT Paton NI. Lancet HIV 2015; e: 417 -26

Estudio Pivot: cambio a IP/r monoterapia § Grupo IP/r monoterapia – – – DRV/r: 80% LPV/r: 14% ATV/r: 6% Saquinavir/r < 1% 58% aun en monoterapia IP/r al final del estudio (72% del tiempo de seguimiento en monoterapia) – Razones para reintroducción de regímenes combinados • • 23% por rebote virológico definido por el protocolo 4% por rebote virológico sin alcanzar los criterios del protocolo 5% por efectos tóxicos 7% por otras razones desconocidas § Duración mediana del seguimiento: 44 meses PIVOT Paton NI. Lancet HIV 2015; e: 417 -26
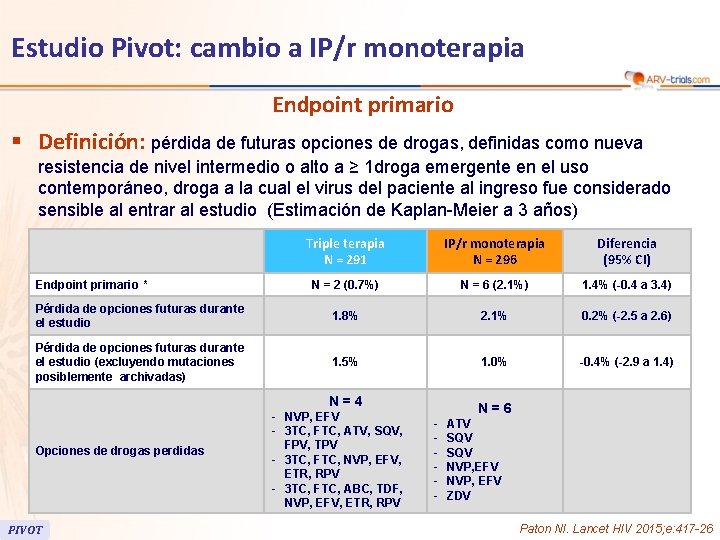
Estudio Pivot: cambio a IP/r monoterapia Endpoint primario § Definición: pérdida de futuras opciones de drogas, definidas como nueva resistencia de nivel intermedio o alto a ≥ 1 droga emergente en el uso contemporáneo, droga a la cual el virus del paciente al ingreso fue considerado sensible al entrar al estudio (Estimación de Kaplan-Meier a 3 años) Triple terapia N = 291 IP/r monoterapia N = 296 Diferencia (95% CI) N = 2 (0. 7%) N = 6 (2. 1%) 1. 4% (-0. 4 a 3. 4) Pérdida de opciones futuras durante el estudio 1. 8% 2. 1% 0. 2% (-2. 5 a 2. 6) Pérdida de opciones futuras durante el estudio (excluyendo mutaciones posiblemente archivadas) 1. 5% 1. 0% -0. 4% (-2. 9 a 1. 4) Endpoint primario * N=4 Opciones de drogas perdidas * non-inferiority met PIVOT - NVP, EFV - 3 TC, FTC, ATV, SQV, FPV, TPV - 3 TC, FTC, NVP, EFV, ETR, RPV - 3 TC, FTC, ABC, TDF, NVP, EFV, ETR, RPV N=6 - ATV SQV NVP, EFV ZDV Paton NI. Lancet HIV 2015; e: 417 -26
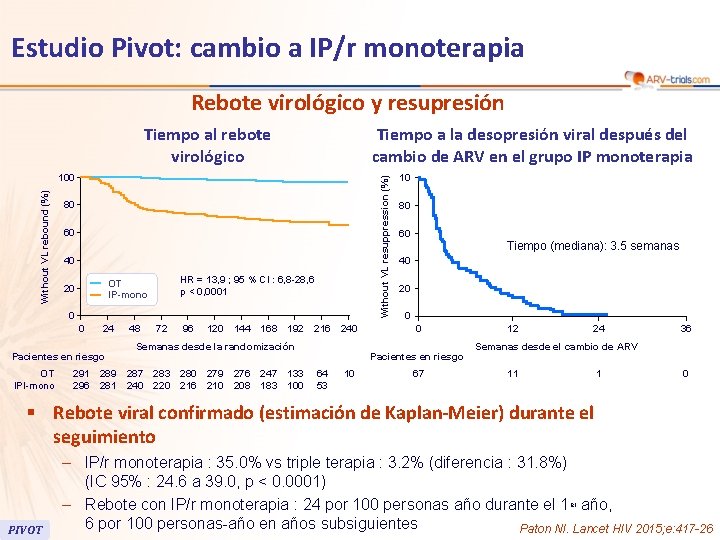
Estudio Pivot: cambio a IP/r monoterapia Rebote virológico y resupresión Tiempo al rebote virológico Tiempo a la desopresión viral después del cambio de ARV en el grupo IP monoterapia Without VL resuppression (%) Without VL rebound (%) 100 80 60 40 HR = 13, 9 ; 95 % CI : 6, 8 -28, 6 p < 0, 0001 OT IP-mono 20 0 0 24 Pacientes en riesgo OT IPI-mono 291 296 289 281 48 72 96 120 144 168 192 216 240 Semanas desde la randomización 287 240 283 220 280 216 279 210 276 208 247 183 133 100 10 80 60 Tiempo (mediana): 3. 5 semanas 40 20 0 0 Pacientes en riesgo 64 53 10 67 12 24 36 Semanas desde el cambio de ARV 11 1 0 § Rebote viral confirmado (estimación de Kaplan-Meier) durante el seguimiento PIVOT – IP/r monoterapia : 35. 0% vs triple terapia : 3. 2% (diferencia : 31. 8%) (IC 95% : 24. 6 a 39. 0, p < 0. 0001) – Rebote con IP/r monoterapia : 24 por 100 personas año durante el 1 er año, 6 por 100 personas-año en años subsiguientes Paton NI. Lancet HIV 2015; e: 417 -26
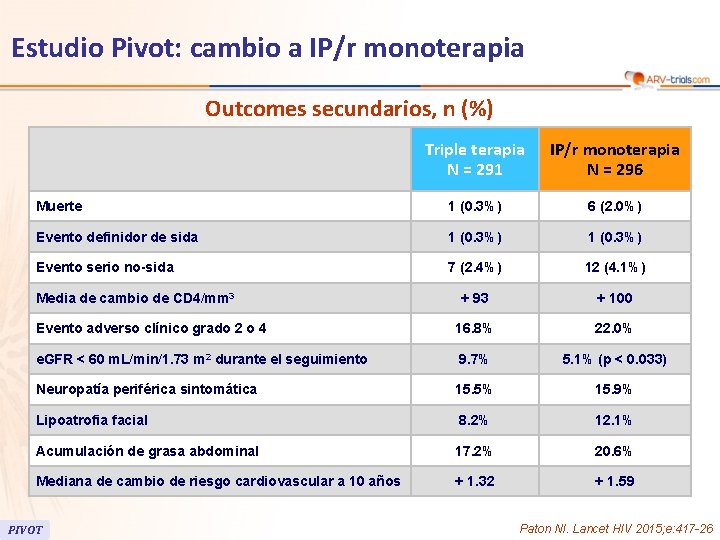
Estudio Pivot: cambio a IP/r monoterapia Outcomes secundarios, n (%) Triple terapia N = 291 IP/r monoterapia N = 296 Muerte 1 (0. 3%) 6 (2. 0%) Evento definidor de sida 1 (0. 3%) Evento serio no-sida 7 (2. 4%) 12 (4. 1%) + 93 + 100 Evento adverso clínico grado 2 o 4 16. 8% 22. 0% e. GFR < 60 m. L/min/1. 73 m 2 durante el seguimiento 9. 7% 5. 1% (p < 0. 033) Neuropatía periférica sintomática 15. 5% 15. 9% Lipoatrofia facial 8. 2% 12. 1% Acumulación de grasa abdominal 17. 2% 20. 6% Mediana de cambio de riesgo cardiovascular a 10 años + 1. 32 + 1. 59 Media de cambio de CD 4/mm 3 PIVOT Paton NI. Lancet HIV 2015; e: 417 -26

Estudio Pivot: cambio a IP/r monoterapia § Conclusiones – En pacientes que alcanzaron la supresión viral con terapia combinada, una estrategia de mantenimiento con IP/r monoterapia, con reintroducción de tratamiento combinado en caso de rebote virológico, fue no inferior al tratamiento combinado continuo para la preservación de futuras opciones de tratamiento durante 3 a 5 años • Monitoreo regular de la carga viral y pronta reintroducción del tratamiento combinado en caso de rebote es necesaria • El numero absoluto de pacientes que perdieron futuras opciones de drogas con IP/r monoterapia fue muy bajo (solo 1 paciente con resistencia a ATV) • Sin cambios en los outcomes clínicos o frecuencia de efectos tóxicos – Mayor proporción de pacientes en la rama de IP/r monoterapia con rebote viral – Rápida resupresión de la carga viral al reintroducir terapia combinada • Sin efectos negativos en el cambio de CD 4 – La monoterapia con inhibidores de proteasa es una alternativa aceptable para el manejo de largo plazo de la infección por HIV PIVOT Paton NI. Lancet HIV 2015; e: 417 -26
- Slides: 8