Cambio a INSTI NNRTI Cambio a DTG RPV

Cambio a INSTI + NNRTI § Cambio a DTG + RPV ‒ Estudio SWORD § Cambio a CAB LA + RPV LA IM ‒ Estudio LATTE-2

Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM § Diseño Inducción (oral) Naïf de ARV > 18 años CV > 1000 c/m. L CD 4 > 200/mm 3 HBs Ag negativo ALT < 5 UNL Clearance de creatinina > 50 m. L/min Randomización 2: 2: 1 Mantenimiento (si CV < 50 c/m. L a S-4 y día 1) CAB 600 mg IM + RPV 900 mg IM Q 8 S * (N = 115) CAB 30 mg QD + ABC/3 TC CAB 400 mg IM + RPV 600 mg IM Q 4 S ** (N = 115) (N = 309) CAB 30 mg QD + ABC/3 TC QD (oral) (N = 56) S-20 S-4: adición de RPV 25 mg QD oral D 1 S 32 S 48 S 96 * CAB IM, dosis de carga de 800 mg al D 1 y 600 mg a S 4 ** CAB IM, dosis de carga de 800 mg at D 1 Q 8 S: inyección cada 8 semanas ; Q 4 S: inyección cada 4 semanas Fase de inducción: CV < 50 c/m. L (ITT-E) luego de 20 semanas = 91. 3 % ; discontinuación en 18/309 pacientes, incluyendo 6 por eventos adversos y 2 por falta de eficacia § Objetivo – Primario: % CV < 50 c/m. L a S 32 de la fase de mantenimiento: selección del esquema de dosis para estudios de fase III (confirmación de dosis en S 48) ; seguridad LATTE-2 Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.
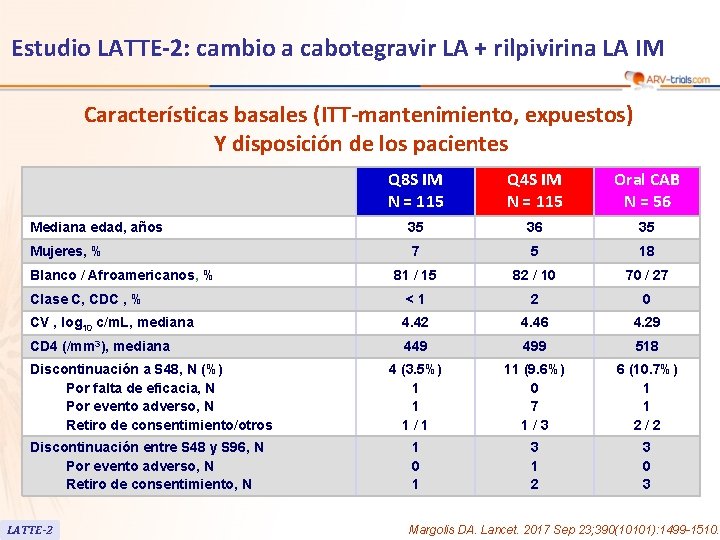
Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM Características basales (ITT-mantenimiento, expuestos) Y disposición de los pacientes Q 8 S IM N = 115 Q 4 S IM N = 115 Oral CAB N = 56 Mediana edad, años 35 36 35 Mujeres, % 7 5 18 81 / 15 82 / 10 70 / 27 Clase C, CDC , % <1 2 0 CV , log 10 c/m. L, mediana 4. 42 4. 46 4. 29 CD 4 (/mm 3), mediana 449 499 518 4 (3. 5%) 1 1 1/1 11 (9. 6%) 0 7 1/3 6 (10. 7%) 1 1 2/2 1 0 1 3 1 2 3 0 3 Blanco / Afroamericanos, % Discontinuación a S 48, N (%) Por falta de eficacia, N Por evento adverso, N Retiro de consentimiento/otros Discontinuación entre S 48 y S 96, N Por evento adverso, N Retiro de consentimiento, N LATTE-2 Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.
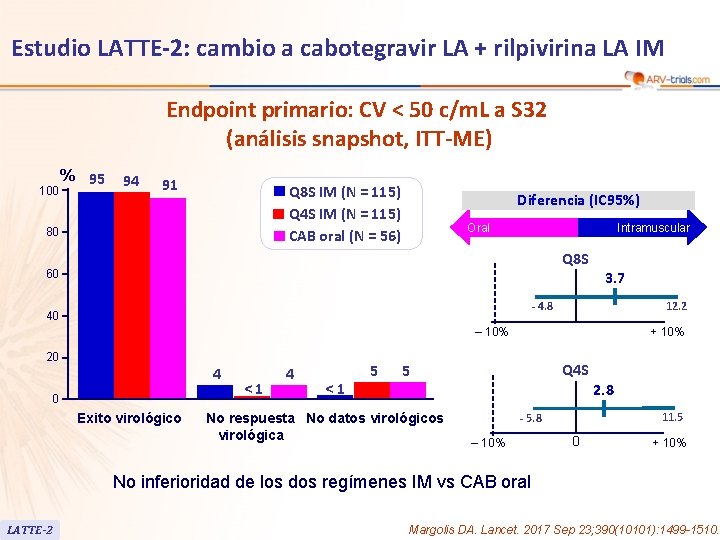
Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM Endpoint primario: CV < 50 c/m. L a S 32 (análisis snapshot, ITT-ME) 100 % 95 94 91 Q 8 S IM (N = 115) Q 4 S IM (N = 115) CAB oral (N = 56) 80 Diferencia (IC 95%) Oral Intramuscular Q 8 S 60 3. 7 - 4. 8 40 12. 2 ‒ 10% 20 4 0 Exito virológico <1 4 <1 5 + 10% Q 4 S 5 No respuesta No datos virológica 2. 8 11. 5 - 5. 8 ‒ 10% 0 + 10% No inferioridad de los dos regímenes IM vs CAB oral LATTE-2 Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.
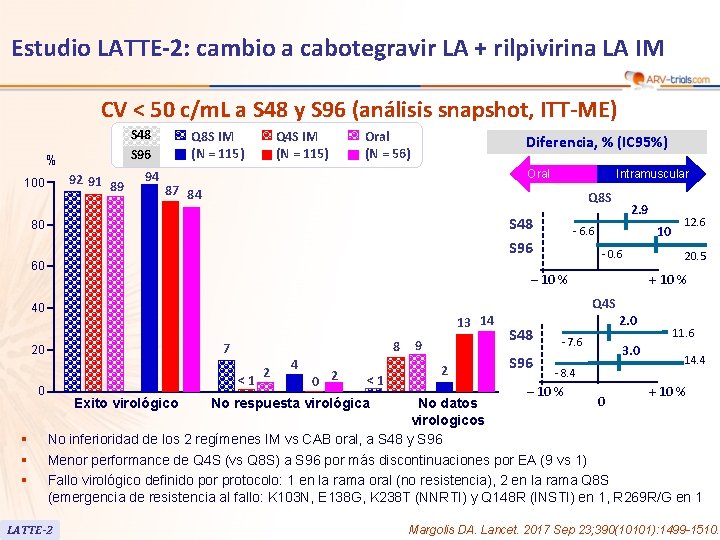
Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM CV < 50 c/m. L a S 48 y S 96 (análisis snapshot, ITT-ME) S 48 S 96 % 92 91 89 100 94 Q 8 S IM (N = 115) Q 4 S IM (N = 115) Oral (N = 56) Diferencia, % (IC 95%) Oral Intramuscular 87 84 Q 8 S S 48 80 13 14 8 7 20 § § § - 0. 6 ‒ 10 % 40 0 10 - 6. 6 S 96 60 2. 9 <1 2 4 0 2 <1 9 2 12. 6 20. 5 + 10 % Q 4 S S 48 S 96 2. 0 - 7. 6 - 8. 4 3. 0 11. 6 14. 4 ‒ 10 % + 10 % 0 No datos virologicos No inferioridad de los 2 regímenes IM vs CAB oral, a S 48 y S 96 Menor performance de Q 4 S (vs Q 8 S) a S 96 por más discontinuaciones por EA (9 vs 1) Fallo virológico definido por protocolo: 1 en la rama oral (no resistencia), 2 en la rama Q 8 S (emergencia de resistencia al fallo: K 103 N, E 138 G, K 238 T (NNRTI) y Q 148 R (INSTI) en 1, R 269 R/G en 1 LATTE-2 Exito virológico No respuesta virológica Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.
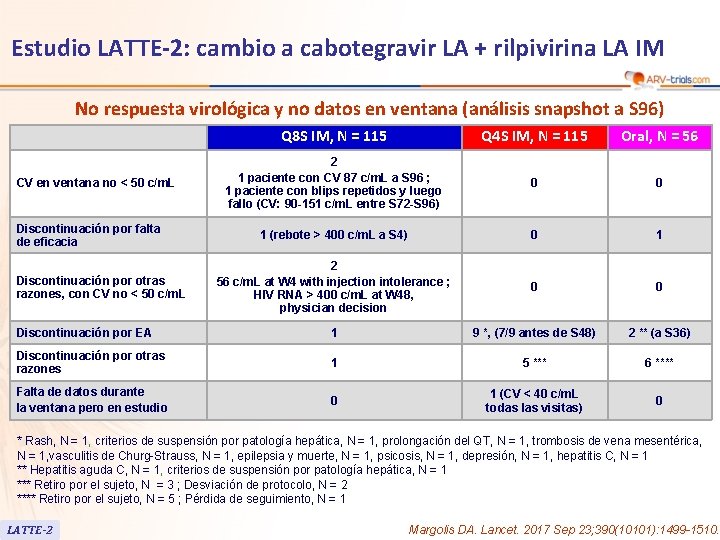
Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM No respuesta virológica y no datos en ventana (análisis snapshot a S 96) Q 8 S IM, N = 115 Q 4 S IM, N = 115 Oral, N = 56 2 1 paciente con CV 87 c/m. L a S 96 ; 1 paciente con blips repetidos y luego fallo (CV: 90 -151 c/m. L entre S 72 -S 96) 0 0 1 (rebote > 400 c/m. L a S 4) 0 1 2 56 c/m. L at W 4 with injection intolerance ; HIV RNA > 400 c/m. L at W 48, physician decision 0 0 Discontinuación por EA 1 9 *, (7/9 antes de S 48) 2 ** (a S 36) Discontinuación por otras razones 1 5 *** 6 **** Falta de datos durante la ventana pero en estudio 0 1 (CV < 40 c/m. L todas las visitas) 0 CV en ventana no < 50 c/m. L Discontinuación por falta de eficacia Discontinuación por otras razones, con CV no < 50 c/m. L * Rash, N = 1, criterios de suspensión por patología hepática, N = 1, prolongación del QT, N = 1, trombosis de vena mesentérica, N = 1, vasculitis de Churg-Strauss, N = 1, epilepsia y muerte, N = 1, psicosis, N = 1, depresión, N = 1, hepatitis C, N = 1 ** Hepatitis aguda C, N = 1, criterios de suspensión por patología hepática, N = 1 *** Retiro por el sujeto, N = 3 ; Desviación de protocolo, N = 2 **** Retiro por el sujeto, N = 5 ; Pérdida de seguimiento, N = 1 LATTE-2 Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.
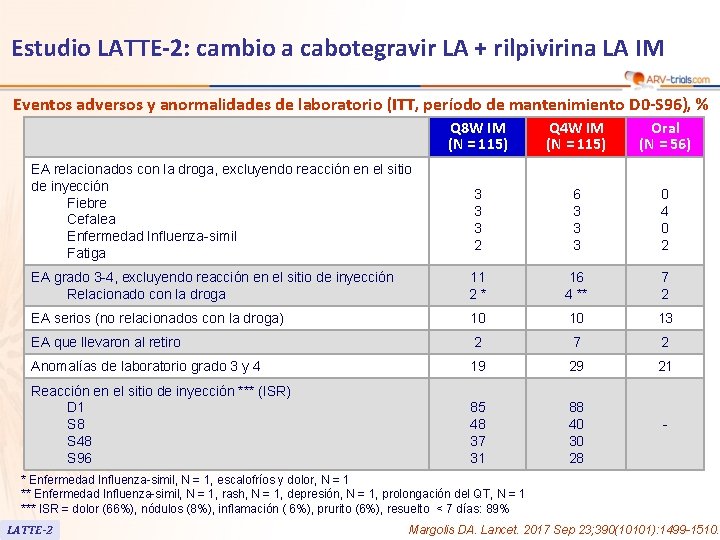
Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM Eventos adversos y anormalidades de laboratorio (ITT, período de mantenimiento D 0 -S 96), % Q 8 W IM (N = 115) Q 4 W IM (N = 115) Oral (N = 56) 3 3 3 2 6 3 3 3 0 4 0 2 EA grado 3 -4, excluyendo reacción en el sitio de inyección Relacionado con la droga 11 2* 16 4 ** 7 2 EA serios (no relacionados con la droga) 10 10 13 EA que llevaron al retiro 2 7 2 Anomalías de laboratorio grado 3 y 4 19 29 21 Reacción en el sitio de inyección *** (ISR) D 1 S 8 S 48 S 96 85 48 37 31 88 40 30 28 EA relacionados con la droga, excluyendo reacción en el sitio de inyección Fiebre Cefalea Enfermedad Influenza-simil Fatiga - * Enfermedad Influenza-simil, N = 1, escalofríos y dolor, N = 1 ** Enfermedad Influenza-simil, N = 1, rash, N = 1, depresión, N = 1, prolongación del QT, N = 1 *** ISR = dolor (66%), nódulos (8%), inflamación ( 6%), prurito (6%), resuelto < 7 días: 89% LATTE-2 Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.
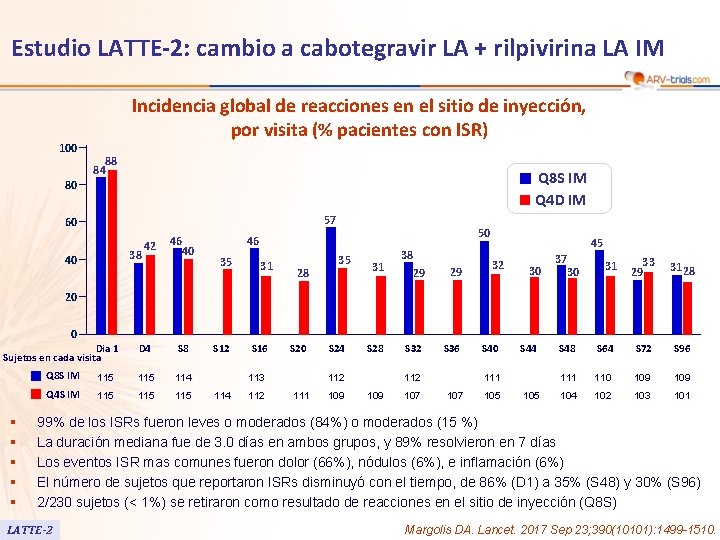
Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM 100 Incidencia global de reacciones en el sitio de inyección, por visita (% pacientes con ISR) 88 84 Q 8 S IM Q 4 D IM 80 57 60 38 40 42 46 40 50 46 35 31 28 35 31 38 29 S 28 S 32 29 45 32 30 37 31 33 29 31 28 S 48 S 64 S 72 S 96 111 110 109 104 102 103 101 30 20 0 Dia 1 Sujetos en cada visita D 4 S 8 Q 8 S IM 115 114 Q 4 S IM 115 115 § § § S 12 S 16 S 20 113 114 112 S 24 112 111 109 S 36 112 109 107 S 40 S 44 111 107 105 99% de los ISRs fueron leves o moderados (84%) o moderados (15 %) La duración mediana fue de 3. 0 días en ambos grupos, y 89% resolvieron en 7 días Los eventos ISR mas comunes fueron dolor (66%), nódulos (6%), e inflamación (6%) El número de sujetos que reportaron ISRs disminuyó con el tiempo, de 86% (D 1) a 35% (S 48) y 30% (S 96) 2/230 sujetos (< 1%) se retiraron como resultado de reacciones en el sitio de inyección (Q 8 S) LATTE-2 Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.
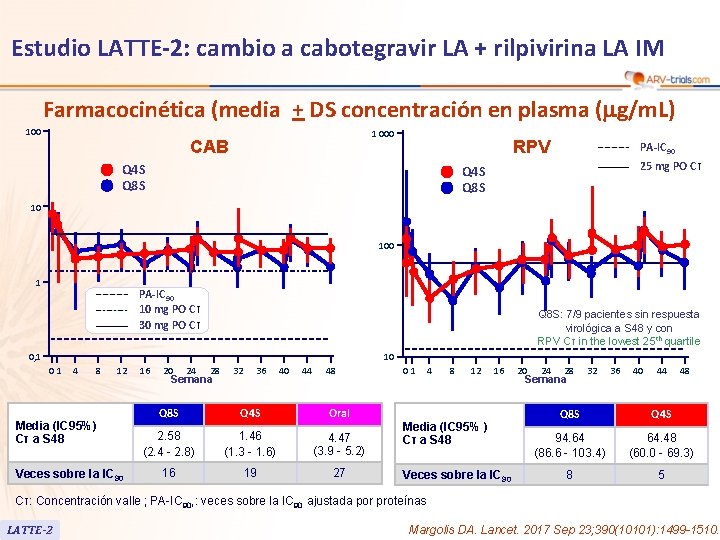
Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM Farmacocinética (media + DS concentración en plasma (mg/m. L) 100 1 000 CAB RPV Q 4 S Q 8 S PA-IC 90 25 mg PO Cτ Q 4 S Q 8 S 10 100 1 PA-IC 90 10 mg PO Cτ 30 mg PO Cτ Q 8 S: 7/9 pacientes sin respuesta virológica a S 48 y con RPV Cτ in the lowest 25 th quartile 0, 1 10 01 4 8 12 Media (IC 95%) Cτ a S 48 Veces sobre la IC 90 16 20 24 28 Semana 32 36 40 44 48 Q 8 S Q 4 S Oral 2. 58 (2. 4 - 2. 8) 1. 46 (1. 3 - 1. 6) 4. 47 (3. 9 - 5. 2) 16 19 27 01 4 8 12 16 Media (IC 95% ) Cτ a S 48 Veces sobre la IC 90 20 24 28 Semana 32 36 40 44 48 Q 8 S Q 4 S 94. 64 (86. 6 - 103. 4) 64. 48 (60. 0 - 69. 3) 8 5 Cτ: Concentración valle ; PA-IC 90, : veces sobre la IC 90 ajustada por proteínas LATTE-2 Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.

Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM Resultados reportados por el paciente (Cuestionario de satisfacción con el tratamiento) % 100 80 3 2 2 4 <1 14 100 15 21 % 1 <1 10 80 7 9 2 4 11 60 60 35 40 40 20 20 0 76 85 Q 4 W (N = 100) Q 8 W (N = 108) 76 0 CAB oral + ABC/3 TC (N = 46) CAB IM LA + RPV LA Muy satisfecho LATTE-2 88 89 Q 4 W (N = 100) Q 8 W (N = 108) 43 CAB oral + ABC/3 TC (N = 46) CAB IM LA + RPV LA 6 5 4 3 2 1 0 Muy insatisfecho Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.

Estudio LATTE-2: cambio a cabotegravir LA + rilpivirina LA IM § Conclusiones – Los resultados del estudio LATTE-2 demostraron la capacidad de CAB IM + RPV LA de mantener CV < 50 c/m. L en dosis cada 4 u 8 semanas – 3 pacientes cumplieron el criterio de fallo virológico definido por el protocolo durante el mantenimiento • Q 8 S (N = 2), CAB oral (N = 1) ; un paciente Q 8 W con emergencia de resistencia a RPV y CAB, y un sujeto Q 8 S con emergencia de una mutación menor a INSTI – Tolerancia a la inyección • La mayoría de las reacciones en el sitio de inyección (ISR) fueron dolor grado 1 -2, con una duración (mediana) de 3 días • Pocos sujetos tuvieron una ISR que lleve a la discontinuación, con mayor frecuencia en el grupo Q 4 S • Alta satisfacción global – Selección de la dosis • Dosis Q 4 S: menores tasas de falta de respuesta virológica con similar seguridad que Q 8 S • La dosis Q 4 S fue seleccionada para los estudios pivotales de fase III LATTE-2 Margolis DA. Lancet. 2017 Sep 23; 390(10101): 1499 -1510.
- Slides: 11