Cambio a DTGABC3 TC Estudio STRIIVING Estudio STRIIVING

Cambio a DTG/ABC/3 TC § Estudio STRIIVING
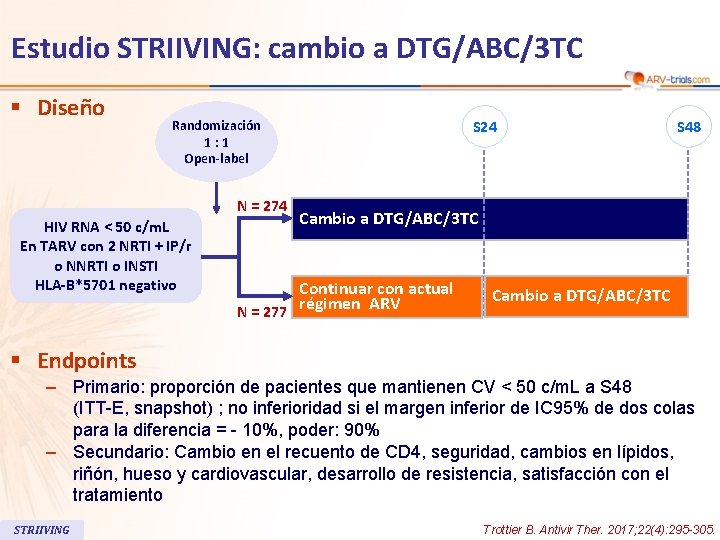
Estudio STRIIVING: cambio a DTG/ABC/3 TC § Diseño Randomización 1: 1 Open-label N = 274 HIV RNA < 50 c/m. L En TARV con 2 NRTI + IP/r o NNRTI o INSTI HLA-B*5701 negativo S 24 S 48 Cambio a DTG/ABC/3 TC Continuar con actual régimen ARV N = 277 Cambio a DTG/ABC/3 TC § Endpoints – Primario: proporción de pacientes que mantienen CV < 50 c/m. L a S 48 (ITT-E, snapshot) ; no inferioridad si el margen inferior de IC 95% de dos colas para la diferencia = - 10%, poder: 90% – Secundario: Cambio en el recuento de CD 4, seguridad, cambios en lípidos, riñón, hueso y cardiovascular, desarrollo de resistencia, satisfacción con el tratamiento STRIIVING Trottier B. Antivir Ther. 2017; 22(4): 295 -305.
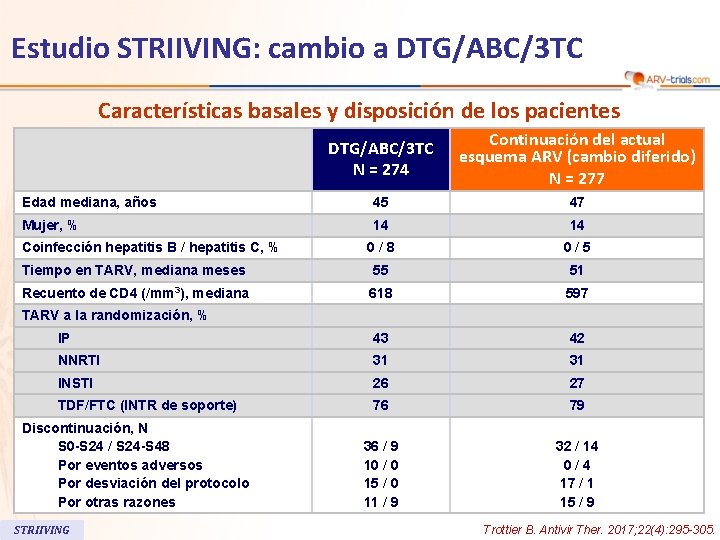
Estudio STRIIVING: cambio a DTG/ABC/3 TC Características basales y disposición de los pacientes DTG/ABC/3 TC N = 274 Continuación del actual esquema ARV (cambio diferido) N = 277 Edad mediana, años 45 47 Mujer, % 14 14 0/8 0/5 Tiempo en TARV, mediana meses 55 51 Recuento de CD 4 (/mm 3), mediana 618 597 IP 43 42 NNRTI 31 31 INSTI 26 27 TDF/FTC (INTR de soporte) 76 79 36 / 9 10 / 0 15 / 0 11 / 9 32 / 14 0/4 17 / 1 15 / 9 Coinfección hepatitis B / hepatitis C, % TARV a la randomización, % Discontinuación, N S 0 -S 24 / S 24 -S 48 Por eventos adversos Por desviación del protocolo Por otras razones STRIIVING Trottier B. Antivir Ther. 2017; 22(4): 295 -305.
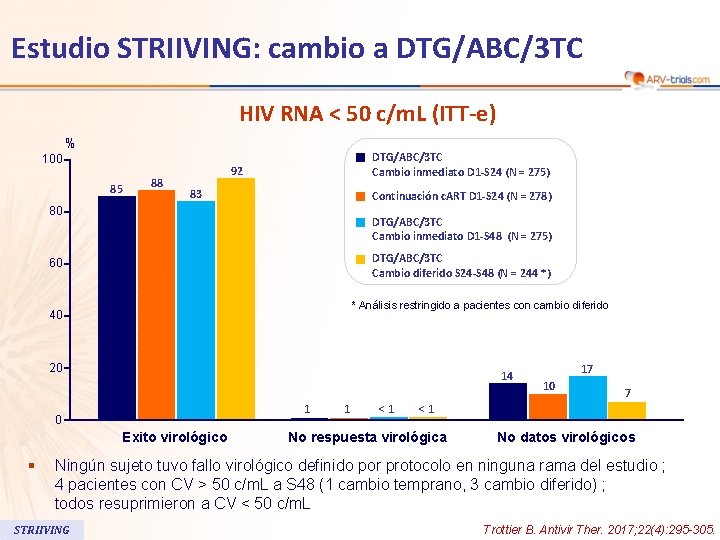
Estudio STRIIVING: cambio a DTG/ABC/3 TC HIV RNA < 50 c/m. L (ITT-e) % 100 85 88 DTG/ABC/3 TC Cambio inmediato D 1 -S 24 (N = 275) 92 83 Continuación c. ART D 1 -S 24 (N = 278) 80 DTG/ABC/3 TC Cambio inmediato D 1 -S 48 (N = 275) DTG/ABC/3 TC Cambio diferido S 24 -S 48 (N = 244 *) 60 * Análisis restringido a pacientes con cambio diferido 40 20 14 1 0 Exito virológico § 1 <1 17 10 7 <1 No respuesta virológica No datos virológicos Ningún sujeto tuvo fallo virológico definido por protocolo en ninguna rama del estudio ; 4 pacientes con CV > 50 c/m. L a S 48 (1 cambio temprano, 3 cambio diferido) ; todos resuprimieron a CV < 50 c/m. L STRIIVING Trottier B. Antivir Ther. 2017; 22(4): 295 -305.
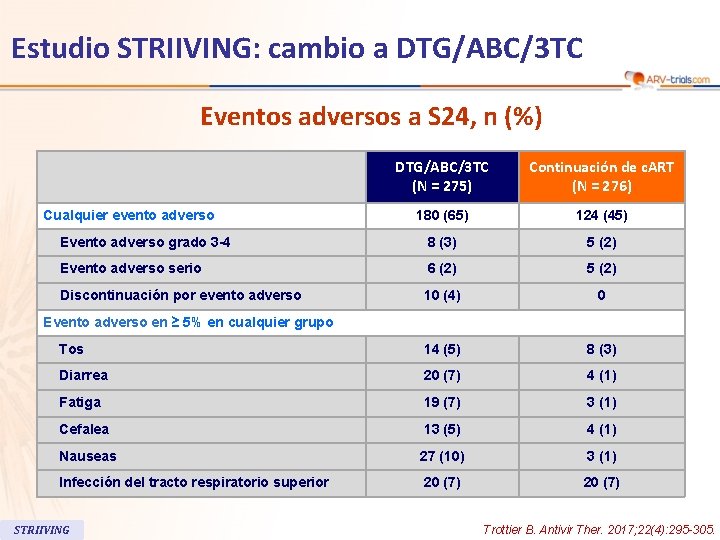
111 Estudio STRIIVING: cambio a DTG/ABC/3 TC Eventos adversos a S 24, n (%) DTG/ABC/3 TC (N = 275) Continuación de c. ART (N = 276) 180 (65) 124 (45) Evento adverso grado 3 -4 8 (3) 5 (2) Evento adverso serio 6 (2) 5 (2) Discontinuación por evento adverso 10 (4) 0 Tos 14 (5) 8 (3) Diarrea 20 (7) 4 (1) Fatiga 19 (7) 3 (1) Cefalea 13 (5) 4 (1) Nauseas 27 (10) 3 (1) Infección del tracto respiratorio superior 20 (7) Cualquier evento adverso Evento adverso en ≥ 5% en cualquier grupo STRIIVING Trottier B. Antivir Ther. 2017; 22(4): 295 -305.
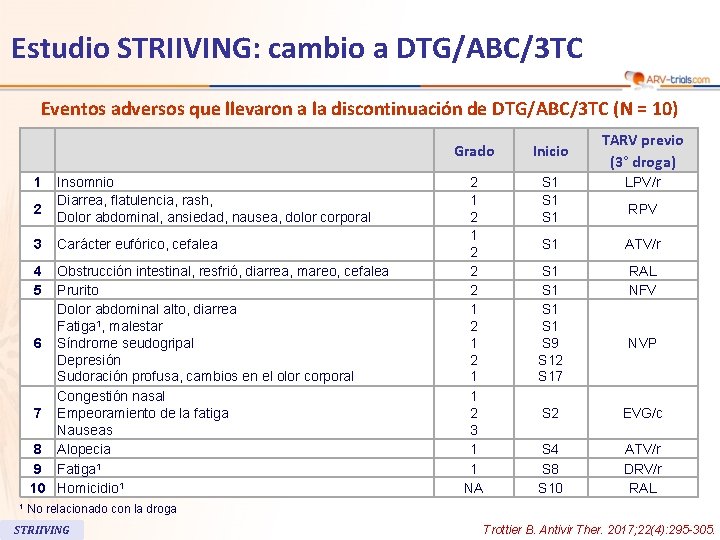
112 Estudio STRIIVING: cambio a DTG/ABC/3 TC Eventos adversos que llevaron a la discontinuación de DTG/ABC/3 TC (N = 10) 1 2 3 Insomnio Diarrea, flatulencia, rash, Dolor abdominal, ansiedad, nausea, dolor corporal Carácter eufórico, cefalea 4 5 Obstrucción intestinal, resfrió, diarrea, mareo, cefalea Prurito Dolor abdominal alto, diarrea Fatiga 1, malestar 6 Síndrome seudogripal Depresión Sudoración profusa, cambios en el olor corporal Congestión nasal 7 Empeoramiento de la fatiga Nauseas 8 Alopecia 9 Fatiga 1 10 Homicidio 1 1 TARV previo (3° droga) Grado Inicio 2 1 2 2 2 1 2 1 1 2 3 1 1 NA S 1 S 1 LPV/r S 1 ATV/r S 1 S 1 S 9 S 12 S 17 RAL NFV RPV NVP S 2 EVG/c S 4 S 8 S 10 ATV/r DRV/r RAL No relacionado con la droga STRIIVING Trottier B. Antivir Ther. 2017; 22(4): 295 -305.
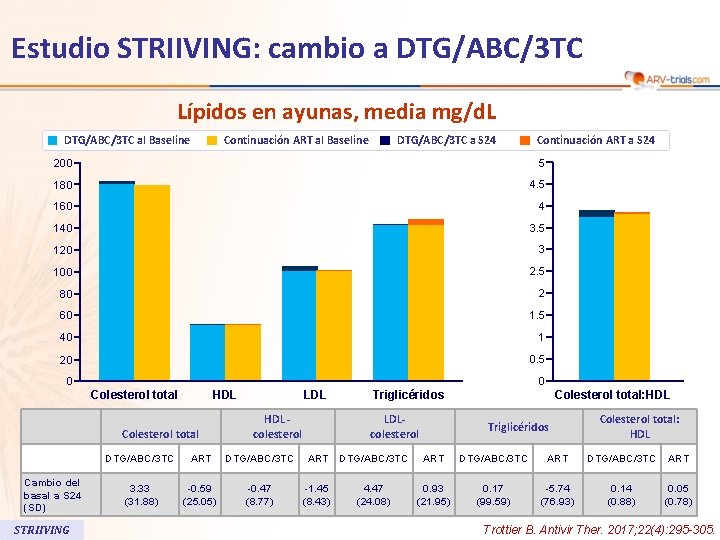
Estudio STRIIVING: cambio a DTG/ABC/3 TC Lípidos en ayunas, media mg/d. L DTG/ABC/3 TC al Baseline Continuación ART al Baseline DTG/ABC/3 TC a S 24 Continuación ART a S 24 200 5 180 4. 5 160 4 140 3. 5 120 3 100 2. 5 80 2 60 1. 5 40 1 20 0. 5 0 0 Colesterol total HDL Colesterol total Cambio del basal a S 24 (SD) STRIIVING LDL HDL colesterol DTG/ABC/3 TC ART DTG/ABC/3 TC 3. 33 (31. 88) -0. 59 (25. 05) -0. 47 (8. 77) Triglicéridos LDLcolesterol ART DTG/ABC/3 TC -1. 45 (8. 43) 4. 47 (24. 08) Colesterol total: HDL Triglicéridos Colesterol total: HDL ART DTG/ABC/3 TC ART 0. 93 (21. 95) 0. 17 (99. 59) -5. 74 (76. 93) 0. 14 (0. 88) 0. 05 (0. 78) Trottier B. Antivir Ther. 2017; 22(4): 295 -305.
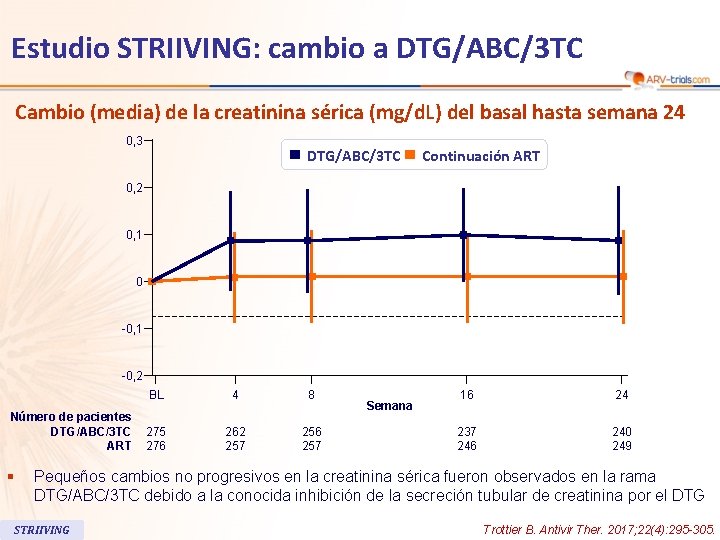
Estudio STRIIVING: cambio a DTG/ABC/3 TC Cambio (media) de la creatinina sérica (mg/d. L) del basal hasta semana 24 0, 3 DTG/ABC/3 TC Continuación ART 0, 2 0, 1 0 -0, 1 -0, 2 Número de pacientes DTG/ABC/3 TC ART § BL 4 8 275 276 262 257 256 257 Semana 16 24 237 246 240 249 Pequeños cambios no progresivos en la creatinina sérica fueron observados en la rama DTG/ABC/3 TC debido a la conocida inhibición de la secreción tubular de creatinina por el DTG STRIIVING Trottier B. Antivir Ther. 2017; 22(4): 295 -305.
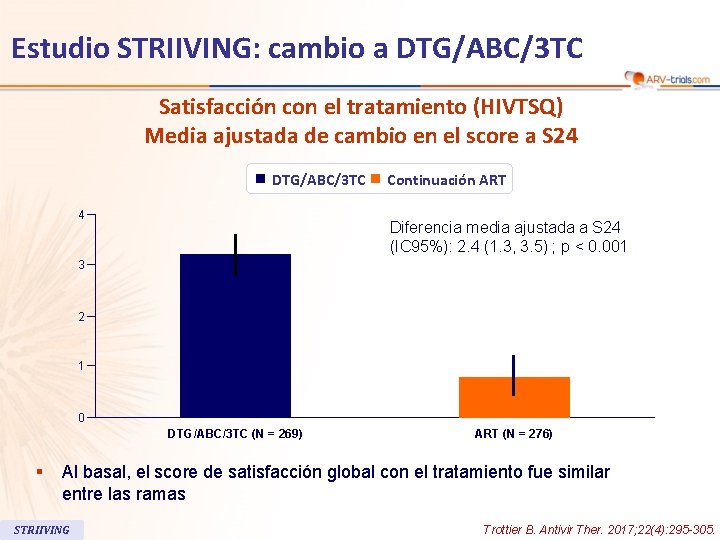
Estudio STRIIVING: cambio a DTG/ABC/3 TC Satisfacción con el tratamiento (HIVTSQ) Media ajustada de cambio en el score a S 24 DTG/ABC/3 TC 4 Continuación ART Diferencia media ajustada a S 24 (IC 95%): 2. 4 (1. 3, 3. 5) ; p < 0. 001 3 2 1 0 DTG/ABC/3 TC (N = 269) § ART (N = 276) Al basal, el score de satisfacción global con el tratamiento fue similar entre las ramas STRIIVING Trottier B. Antivir Ther. 2017; 22(4): 295 -305.

113 Estudio STRIIVING: cambio a DTG/ABC/3 TC § Conclusión – Eficacia • Similar respuesta virológica para DTG/ABC/3 TC y continuación de tratamiento actual a S 24 con no inferioridad • Las tasas de éxito se mantuvieron por 48 semanas en el grupo de cambio temprano • En el grupo de cambio tardío, la supresión virológica fue observada en 92% de los pacientes con DTG/ABC/3 TC (24 semanas post-cambio) • No hubo fallo virológico definido por protocolo en el estudio – Tolerabilidad • 4% de los sujetos discontinuaron por eventos adversos a S 24 en la rama DTG/ABC/3 TC vs 0% en el grupo de continuación • No hubieron discontinuaciones por eventos adversos en la rama de cambio temprana post semana 24 • Las tasas de discontinuación por eventos adversos en el cambio tardío fueron del 2% STRIIVING Trottier B. Antivir Ther. 2017; 22(4): 295 -305.
- Slides: 10