Calorimtrie 1 Comprendre les phnomnes thermiques Questce que





























- Slides: 42

Calorimétrie 1

Comprendre les phénomènes thermiques Qu’est-ce que l’énergie ? Comment peut-on chauffer un corps ? Comment l’énergie se transmet ? Comment isole-t-on une maison ? 2

Définition de l’énergie L’énergie est une des notions fondamentales de la physique. C’est une notion abstraite dont on sait facilement décrire les effets, mais pas la nature. Elle se présente sous différentes formes: électrique, chimique, mécanique, thermique… Son unité est le joule abrégé J. 3

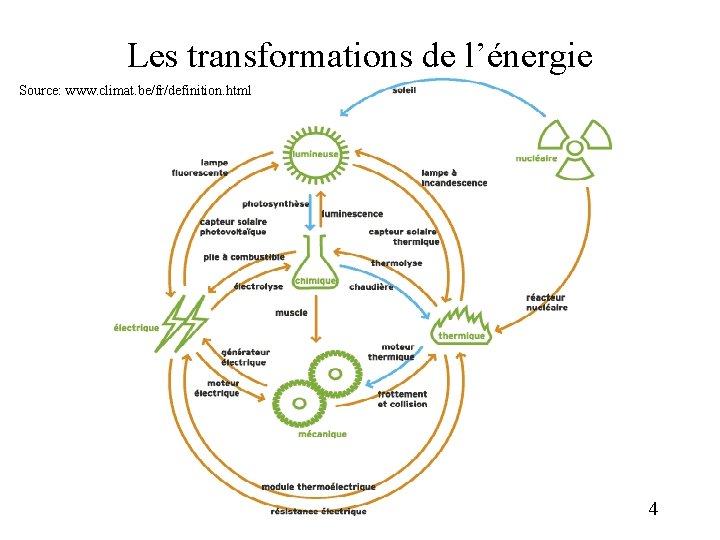
Les transformations de l’énergie Source: www. climat. be/fr/definition. html 4

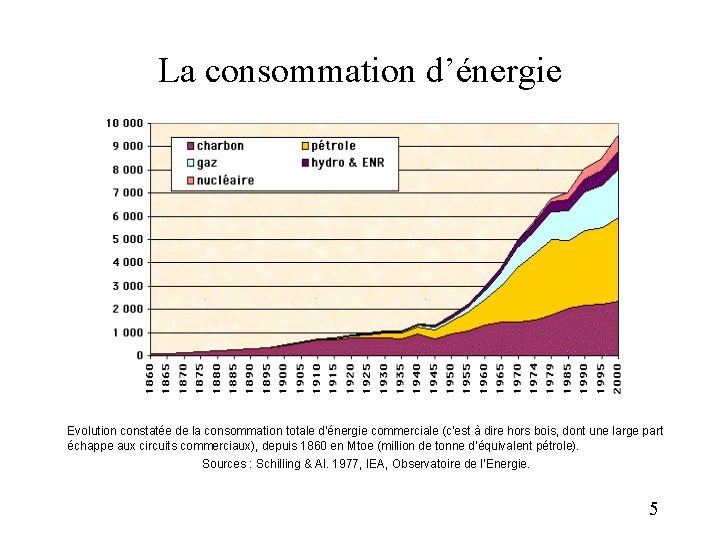
La consommation d’énergie Evolution constatée de la consommation totale d'énergie commerciale (c'est à dire hors bois, dont une large part échappe aux circuits commerciaux), depuis 1860 en Mtoe (million de tonne d’équivalent pétrole). Sources : Schilling & Al. 1977, IEA, Observatoire de l’Energie. 5

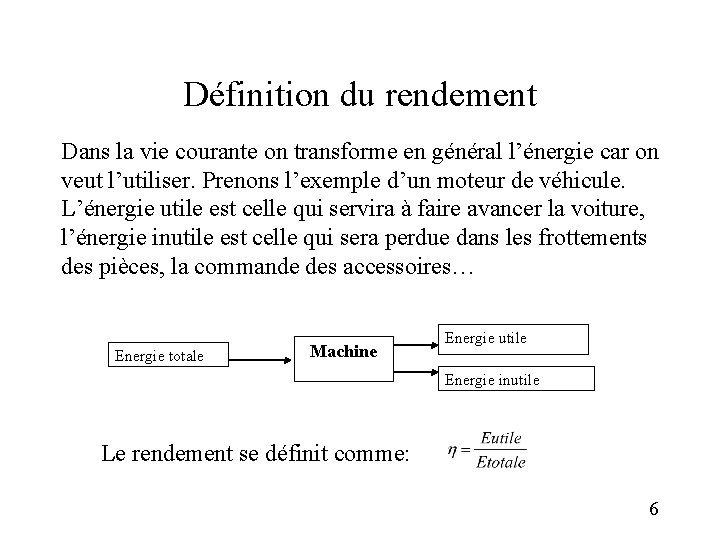
Définition du rendement Dans la vie courante on transforme en général l’énergie car on veut l’utiliser. Prenons l’exemple d’un moteur de véhicule. L’énergie utile est celle qui servira à faire avancer la voiture, l’énergie inutile est celle qui sera perdue dans les frottements des pièces, la commande des accessoires… Energie totale Machine Energie utile Energie inutile Le rendement se définit comme: 6

Définition de la puissance La puissance est la capacité à fournir une certaine énergie en un certain temps. Son unité est le Watt. 1 Watt = 1 Joule/1 seconde Nous avons tous une notion intuitive de la puissance, par exemple nous savons comparer la puissance de différents véhicules. 7

Qu’est-ce que la température? La température est une propriété de tout corps en équilibre thermique et est une mesure de l’agitation des atomes ou molécules qui constitue le corps. On parle d’une variable d’état macroscopique (cf livre page 462 -464) Elle se mesure avec des instruments appelés thermomètres. On trouve deux échelles courantes de températures: les degrés Celsius TC et les degrés Kelvin Tk La relation entre les deux échelles est: Tk = TC +273, 15 8

Modifier la température d’un corps Si on fournit à un corps une certaine quantité de chaleur alors on peut observer une augmentation de sa température. Comment peut-on quantifier ce changement de température? On a pu remarquer que le lien entre chaleur fournie et le changement de température s’exprimait comme: Q = m c T Q est la quantité de chaleur en joule, m est la masse du corps en kg, c est la chaleur spécifique du corps en J/kg. K T = (Tf - Ti ) la température finale moins la température initiale. 9

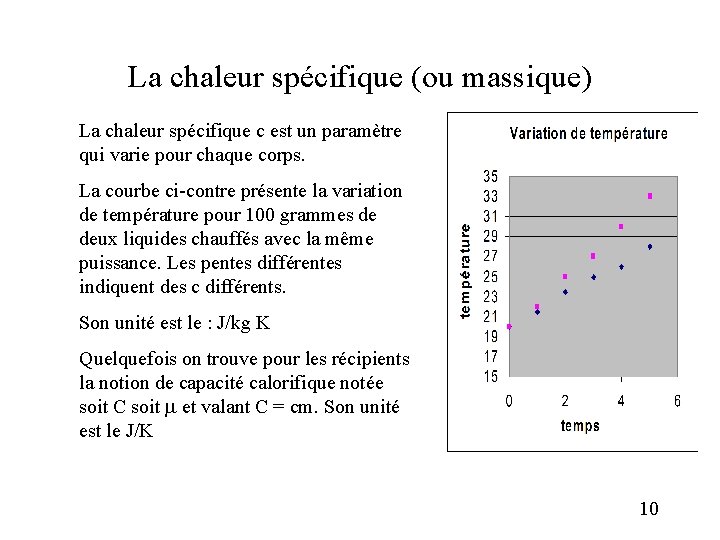
La chaleur spécifique (ou massique) La chaleur spécifique c est un paramètre qui varie pour chaque corps. La courbe ci-contre présente la variation de température pour 100 grammes de deux liquides chauffés avec la même puissance. Les pentes différentes indiquent des c différents. Son unité est le : J/kg K Quelquefois on trouve pour les récipients la notion de capacité calorifique notée soit C soit et valant C = cm. Son unité est le J/K 10

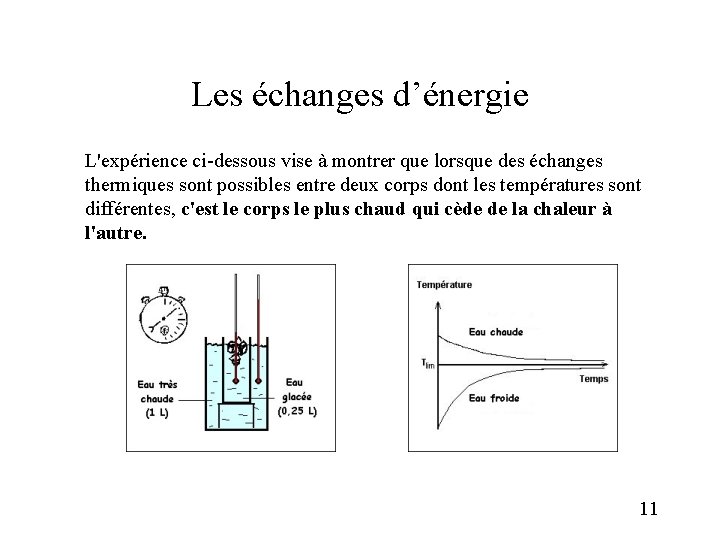
Les échanges d’énergie L'expérience ci-dessous vise à montrer que lorsque des échanges thermiques sont possibles entre deux corps dont les températures sont différentes, c'est le corps le plus chaud qui cède de la chaleur à l'autre. 11

La conservation de l’énergie Ce qui s’échange entre les deux corps de l’expérience précédente est une certaine quantité de chaleur. La loi de la conservation de l’énergie nous donne: Q 1+ Q 2 = 0 Cette relation nous permet de calculer la température finale Tf avec l’équation suivante: m 1 c 1(Tf –T 1) + m 2 c 2 (Tf –T 2) = 0 12

Modifier l’état d’un corps Apporter ou retirer de l’énergie peut aussi faire changer d’état un corps. Il existe 3 états de la matière: l’état solide, l’état liquide et l’état gazeux. Les changements entre ces états se font à une température bien spécifique à chaque corps, appelées température de fusion TF et température d’ébullition Tv vaporisation Gaz fusion Solide Liquide TF Tv liquéfaction solidification 13

Changements d’états et énergie La relation qui permet de connaître le lien entre énergie et changement d’état s’écrit: Q = ± m LF, V Le signe ± indique l’énergie est soit positive s’il faut fournir de l’énergie au corps, soit négative s’il faut enlever de l’énergie au corps. Le terme LF, V s’appelle la chaleur latente de fusion (LF) ou chaleur latente de vaporisation (Lv). Ces termes sont spécifiques à chaque corps. 14

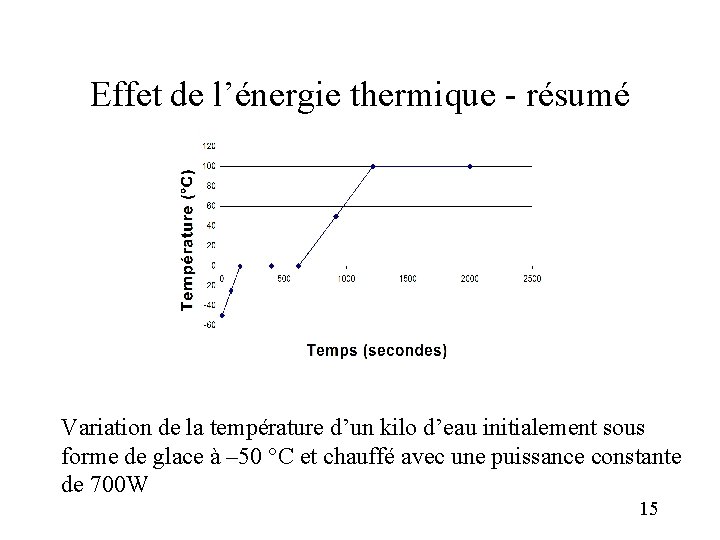
Effet de l’énergie thermique - résumé Variation de la température d’un kilo d’eau initialement sous forme de glace à – 50 °C et chauffé avec une puissance constante de 700 W 15

Et la loi de conservation de l’énergie? Si nous mélangeons dans un récipient bien isolé des corps à des températures et des états différents, que va-t-il se passer? La loi de conservation de l’énergie nous dit que les corps vont s’échanger de l’énergie et que la somme de tous les échanges vaudra toujours zéro. Le mélange va évoluer vers une température finale qui tiendra compte de tous les échanges énergétiques. Qi = 0 16

Les transferts de chaleur 17

Types de transferts Jusqu’à maintenant nous sommes intéressés à calculer les énergies en jeu lors des échanges lorsque les corps en présence arrivaient à un équilibre thermique, sans nous préoccuper des mécanismes de transfert de la chaleur. Ces mécanismes sont de plusieurs sortes • Transferts par convection • Transferts par rayonnement • Transferts par conduction 18

Les transferts par convection Ce mécanisme existe dans les liquides et les gaz. Il y a déplacement de matière. Ce sont les mécanismes responsables de nombreux phénomènes météo 19

Les transferts par rayonnement Le rayonnement est un transfert de chaleur pouvant s’effectuer à travers le vide (par transport de photons). Le flux de chaleur (en Watt) émis par une surface d’un m 2 à la température T vaut: = T 4 est l’émissivité, valeur comprise entre 0 et 1, elle est proche de zéro pour une surface blanche brillante et proche de 1 pour une surface noire. est la constante de Stefan-Boltzmann = 5. 67 x 10 -8 W/m 2 K 4 20

Transfert par conduction Ce sont les mécanismes de perte les plus importants dans une maison. A chaque instant un flux de chaleur se crée de la zone la plus chaude vers la zone la plus froide. Le flux de chaleur en Watt se calcule comme : T 1 e T 2 S = surface de la paroi k = coefficient de transmission thermique (W/m 2 K) R = résistance thermique R= e/ e = épaisseur de la paroi en mètre = coefficient de conductivité thermique (W/m. K) 21

Transferts à travers plusieurs parois Lorsque plusieurs corps de nature différente composent une paroi, le flux de chaleur va dépendre de la composition de toutes les parois selon la formule ci-dessous. = ktot T R tot = (ei / i) = Ri ktot = 1/ R tot T 1 e 2 e 3 e 4 1 2 3 4 T 2 Cette formule permet de connaître l’efficacité d’une isolation. 22

La dilatation thermique des solides et des liquides 23

La dilatation linéique La plupart des matériaux se dilatent lorsqu’ils sont soumis à des variations de température. On peut étudier la dilatation d’un solide en fonction de la variation d’une dimension linéraire quelconque. L = L 0 T (mètres) L = la variation de longueur en mètres L 0 = la longueur initiale en mètres T = la variation de température (en kelvin ou °C) = le coefficient de dilatation linéique (en K-1) 24

La dilatation volumique Pour les solides et les liquides, on peut étudier la variation de volume avec la loi suivante: Dilatation volumique V = V 0 T (en mètres 3) V = la variation de volume en m 3 V 0 = volume initial en m 3 T = la variation de température (en Kelvin ou °C) = le coefficient de dilatation volumique (en K-1) 25

Relation entre et pour les solides En général, =3 Examinons un cube d’arrête L 0 et de volume initial V 0= L 03 Son volume après dilatation est: V = (L 0 + L)3 = L 03 + 3 L 02 L + 3 L 0 L 2 + L 3 Dans cette expression on peut négliger les deux derniers termes qui sont beaucoup plus petits. On trouve finalement: V 3 L 02 L = 3 L 02 L 0 T = 3 V 0 T 26

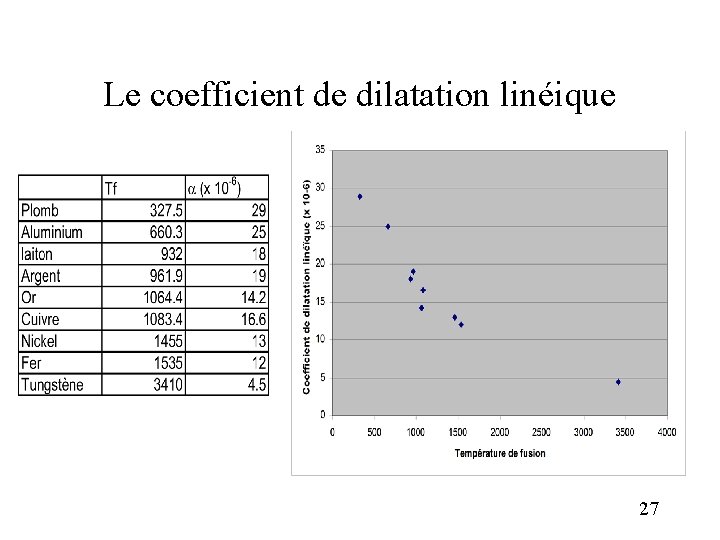
Le coefficient de dilatation linéique 27

La masse volumique • En général pour tous les corps: – La masse volumique du corps sous forme solide est supérieure à la masse volumique sous forme liquide. – La masse volumique diminue si la température augmente (la même masse occupe un plus grand espace) 28

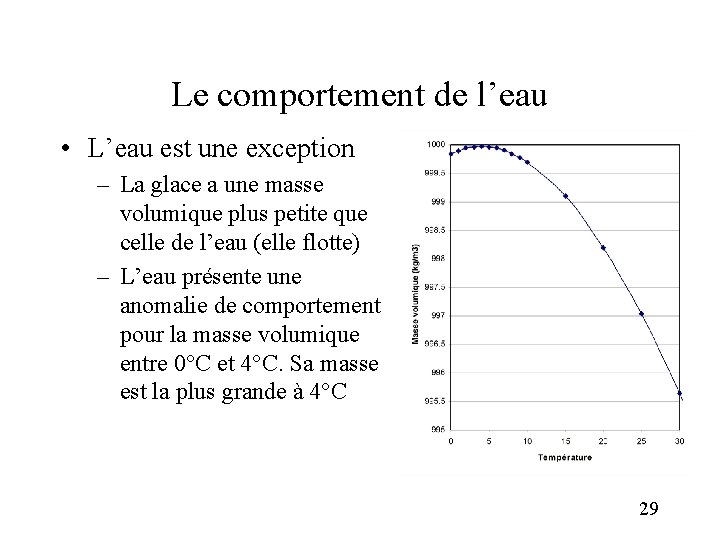
Le comportement de l’eau • L’eau est une exception – La glace a une masse volumique plus petite que celle de l’eau (elle flotte) – L’eau présente une anomalie de comportement pour la masse volumique entre 0°C et 4°C. Sa masse est la plus grande à 4°C 29

La loi des gaz 30

Pourquoi les gaz sont différents? Un gaz se comporte très différemment d’un solide ou d’un liquide pour une raison fondamentale : les interactions entre les atomes ou les molécules deviennent très faibles et peuvent être négligées. C’est pour cela qu’un gaz par exemple remplira toujours un récipient en entier. On a donc toujours à tenir compte de 3 paramètres: • Le volume occupé V en m 3 • La température T en degré Kelvin • La pression sur les parois du récipient P en Pascal 31

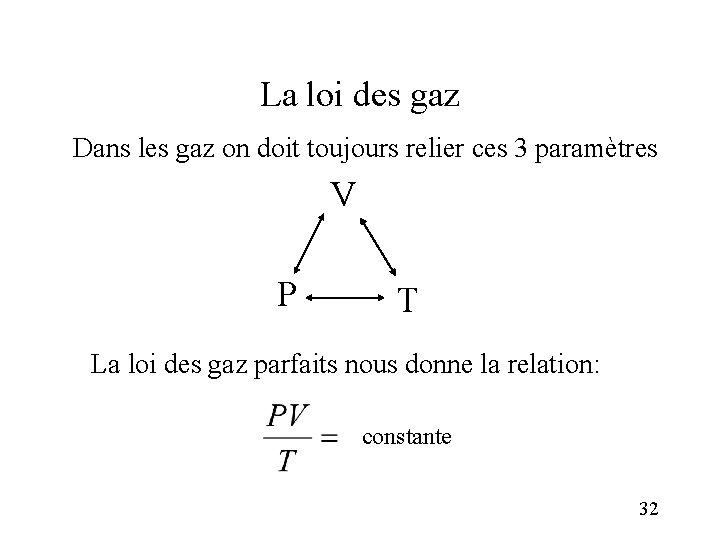
La loi des gaz Dans les gaz on doit toujours relier ces 3 paramètres V P T La loi des gaz parfaits nous donne la relation: constante 32

Et si un des paramètres reste constant Si un des 3 paramètres (P, V, T) reste constant on peut déduire 3 formes simplifiées qui, historiquement ont été découvertes avant la loi des gaz parfaits. Ce sont les lois de • Charles • Gay- Lussac • Boyle- Mariotte 33

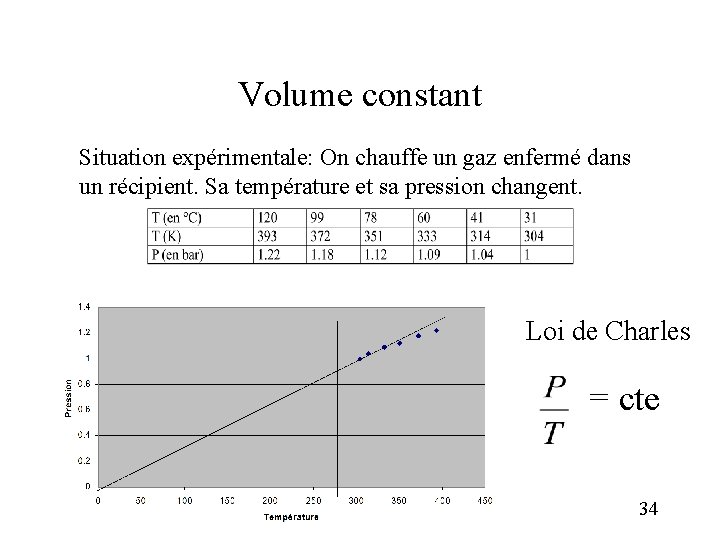
Volume constant Situation expérimentale: On chauffe un gaz enfermé dans un récipient. Sa température et sa pression changent. Loi de Charles = cte 34

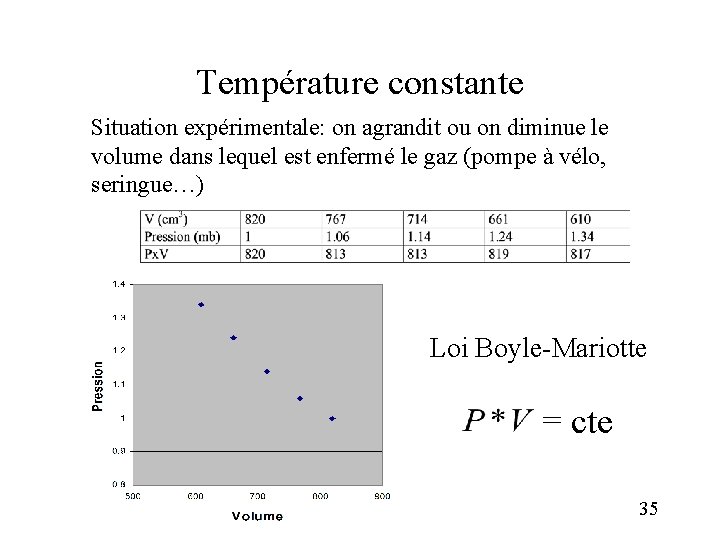
Température constante Situation expérimentale: on agrandit ou on diminue le volume dans lequel est enfermé le gaz (pompe à vélo, seringue…) Loi Boyle-Mariotte = cte 35

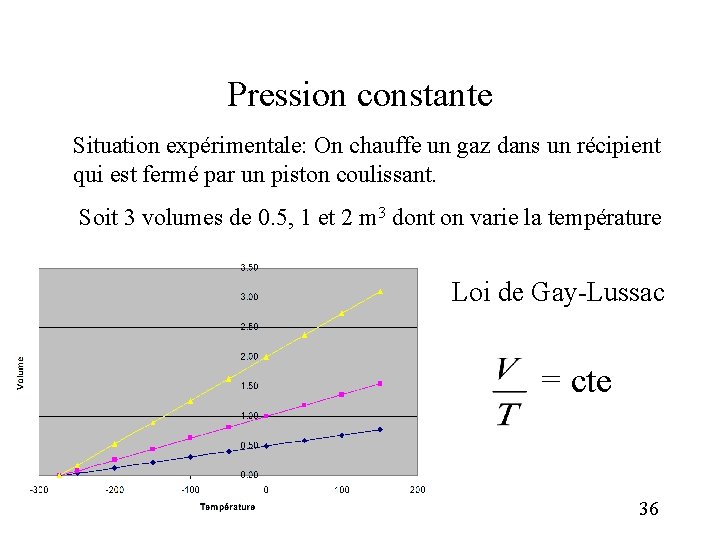
Pression constante Situation expérimentale: On chauffe un gaz dans un récipient qui est fermé par un piston coulissant. Soit 3 volumes de 0. 5, 1 et 2 m 3 dont on varie la température Loi de Gay-Lussac = cte 36

Que vaut la constante dans la loi de gaz n= le nombre de moles R= la constante des gaz parfait = 8. 31 J/moles. K 37

Qu’est-ce qu’une mole Une mole est une quantité de matière. Elle corespond à un certain nombre de molécules. Une mole = 6. 022 x 1023 molécules. Ce nombre s’appelle le nombre d’Avogadro On calcule la masse d’une mole (appelée masse molaire) en s’intéressant à la composition chimique de la molécule. • On cherche d’abord la masse atomique de la molécule • On exprime cette masse en gramme. 38

Quelle volume occupe une mole de gaz ? Ce volume dépendra de la pression et de la température. On définit des conditions standard qui sont: 0 °C et 1 atm Quel volume occupe une mole de gaz dans ces conditions ? On sait que PV = n. RT. Que vaut V pour n = 1 ? V = RT/P On trouve que le volume occupé est toujours de 22. 4 litres. STP = Standard température and pressure T = 273 K et P = 1. 013 x 105 Pascal 39

L’interprétation cinétique de la pression La théorie cinétique met en relation des grandeurs telles que la pression avec le comportement des molécules. Paroi Les molécules frappent en permanence la paroi. L’effet sur la paroi dépend de: • la vitesse moyenne des molécules • Leur densité On peut calculer avec la théorie cinétique que: P = 1/3 v 2 qmoy vqmoy= vitesse quadratique moyenne 40

L’interprétation cinétique de la température A quel paramètre microscopique correspond la température ? La température est elle uniquement liée à la vitesse moyenne des molécules dans le gaz. Elle est une mesure de l’énergie cinétique moyenne. L’énergie cinétique moyenne est par définition: K =1/ mv 2 qmoy La théorie cinétique nous indique K = 3/2 k T où k = la constante de Boltmann et vaut: 1. 38 x 10 -23 J/K 41

Variation des paramètres dans ce modèle • Dans ce modèle on comprend pourquoi les paramètres sont tous dépendants: – Si on diminue le volume à T = constant, alors la densité augmente, donc la pression aussi – Si on chauffe un gaz, on augmente la vitesse moyenne des molécules, donc aussi la pression 42