Calore Marina Cobal Dipt di Fisica Universita di

Calore Marina Cobal - Dipt. di Fisica Universita' di Udine 1

Calore e Temperatura n n La Temperatura riflette il movimento casuale delle particelle, ed è quindi correlata all’energia cinetica delle molecole Il Calore coinvolge un trasferimento di energia tra due oggetti a temperatura differente Marina Cobal - Dipt. di Fisica Universita' di Udine 2

Flusso di Calore Il Calore fluisce da un corpo caldo ad uno freddo fino a quando non raggiungono la stessa temperatura Marina Cobal - Dipt. di Fisica Universita' di Udine 3
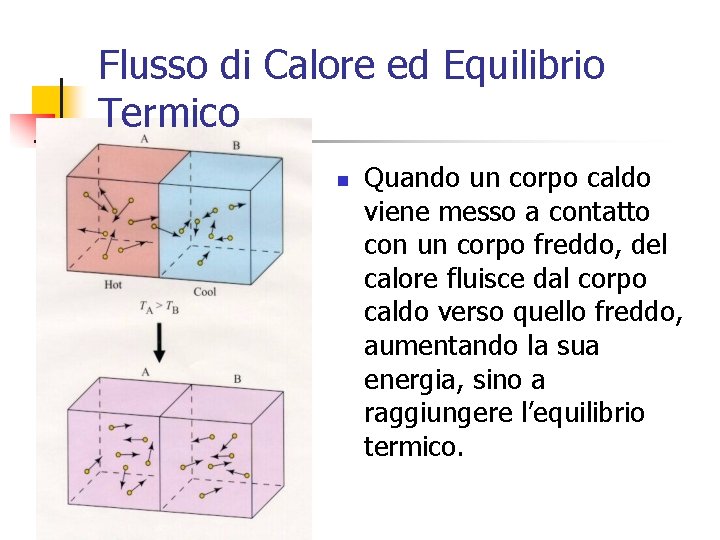
Flusso di Calore ed Equilibrio Termico n Quando un corpo caldo viene messo a contatto con un corpo freddo, del calore fluisce dal corpo caldo verso quello freddo, aumentando la sua energia, sino a raggiungere l’equilibrio termico.

Calore Scambiato n Un processo si dice n Esotermico : se il calore viene emesso dal sistema verso l’ambiente n Endotermico : se il calore viene assorbito dal sistema ed emesso dall’ambiente Marina Cobal - Dipt. di Fisica Universita' di Udine 5

Energia, Lavoro e Calore n n n Un sistema può scambiare energia con l’ambiente mediante n Calore scambiato n Lavoro eseguito (dal sistema o dall’ambiente) Scaldando un corpo, aumentiamo la sua capacita’ di compiere lavoro e quindi aumentiamo la sua energia Anche compiendo lavoro sul sistema aumentiamo la sua energia, ad esempio comprimendo un gas o tirando una molla. Marina Cobal - Dipt. di Fisica Universita' di Udine 6

Calore e Lavoro n Joule mostrò come il Lavoro e il Calore fossero convertibili l’uno nell’altro n Dopo aver variato l’Energia di un sistema, questo non “ricorda” se è stato eseguito del lavoro o se è stato scambiato del calore Marina Cobal - Dipt. di Fisica Universita' di Udine 7

L’Esperimento di Joule n Joules provò l’equivalenza tra calore e lavoro meccanico Il lavoro eseguito per far ruotare le pale, causa un aumento della temperatura dell’acqua n Joules mostrò anche la quantità di calore prodotto era proporzionale alla quantità di lavoro Marina Cobal - Dipt. di Fisica Universita' di Udine 8
Lavoro: Energia in Transito n n n Simbolo: w Il Lavoro e’ energia ‘ordinata’ che puo’ essere utilizzata per sollevare un peso nell’Ambiente Non puo’ essere immagazzinata come Lavoro. Esiste SOLAMENTE durante il processo in cui viene eseguito il lavoro. 9

Calore: Energia per giungere all’Equilibrio n n n Simbolo: q Il Calore e’ energia ‘disordinata’ che viene trasferita tra sistema e ambiente per ristabilire l’equilibrio termico. NON puo’ essere immagazzinato come Calore. Esiste SOLAMENTE durante il processo in cui viene scambiato. 10

Calore Contenuto? ? ? Non si puo’ parlare di Calore Contenuto in un corpo!! Solo di Energia contenuta Marina Cobal - Dipt. di Fisica Universita' di Udine 11

Convenzione del Segno n n Per convenzione, Lavoro e Calore sono negativi se diminuiscono l’energia del sistema, positivi se l’aumentano Lavoro n n n > 0 se e’ fatto sul sistema < 0 se e’ fatto dal sistema Calore n n > 0 se e’ assorbito dal sistema < 0 se e’ emesso dal sistema Marina Cobal - Dipt. di Fisica Universita' di Udine 12
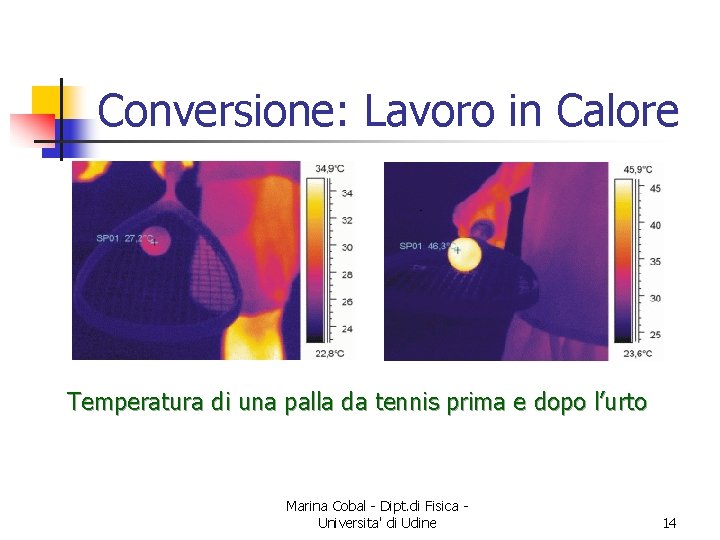
Conversione: Lavoro in Calore Temperatura di una palla da tennis prima e dopo l’urto Marina Cobal - Dipt. di Fisica Universita' di Udine 14

Calore e Lavoro non si Conservano n n n Il Lavoro non è una funzione di stato, e dipende dal cammino. Essendo il Lavoro e il Calore equivalenti in Termodinamica, neanche il Calore è una funzione di stato Il Calore è una particolare forma di energia e quindi non sorprende che non sia una funzione di stato. Marina Cobal - Dipt. di Fisica Universita' di Udine 15

Energia Interna n n Se Calore e Lavoro non esistono al di fuori del processo in cui vengono trasferiti, cosa diventano? L’evidenza sperimentale portava a concludere che ogni corpo potesse immagazzinarel’energia internamente, senza trasformarla in energia cinetica totale del corpo ponendolo in movimento. La Termodinamica postula l’esistenza di una funzione U chiamata Energia. Interna E’ la somma dell’Energia Cineticae Potenziale. Molecolare (Energia traslazionale, rotazionale, vibrazionale, …) 16

Energia Interna n n L’energia Interna PUO’ venire immagazzinata Esiste una Ui prima del processo e una Uf dopo il processo. Esiste quindi un U = Uf - Ui U e’ una funzione di stato U si comporta come una “banca”. Eseguendo lavoro sul sistema, U immagazzina una quantità equivalente di energia. Questa poi può essere ceduta sotto forma di lavoro, o di calore o in altro modo Marina Cobal - Dipt. di Fisica Universita' di Udine 17

Prima Legge della Termodinamica n Nonostante il Calore e il Lavoro non siano delle funzioni di stato, sperimentalmente si osserva che la loro somma è una variazione di una funzione di stato chiamata Energia Interna DU = q+w

U = q + w n Il Primo principio della Termodinamica racchiude più osservazioni sperimentali n n Calore e Lavoro sono equivalenti Esiste una funzione di stato chiamata U che rappresenta l’energia “interna” del sistema Se il sistema è isolato, q = w = 0, per cui U = 0: l’energia si conserva Notate che non scriviamo q o w Marina Cobal - Dipt. di Fisica Universita' di Udine 19

Corollario L’Energia dell’Universo è costante Marina Cobal - Dipt. di Fisica Universita' di Udine 20

Il Primo Principio in Forma Differenziale n n Abbiamo gia’ visto come spesso sia utile considerare dei cambiamenti infinitesimi su un sistema, invece di cambiamenti finiti Il primo principio U = q forma differenziale diventa +w in d. U = dq + dw Marina Cobal - Dipt. di Fisica Universita' di Udine 21

Energia Interna n U = U(p, V, T) L’Energia interna U e’ una funzione di Stato. La termodinamica ci assicura che DEVE essere esprimibile in funzione delle altre variabili termodinamiche n L’equazione di stato che lega p, V e T non fornisce alcuna informazione su U, che deve quindi essere ricavata separatamente. n Due gas possono seguire la legge dei gas ideali, ma avere un comportamento di U Marina Cobal - Dipt. di Fisica - diverso Universita' di Udine 22

U per un Gas Ideale Monoatomico n Dalla teoria cinetica dei Gas, abbiamo ottenuto che per un gas ideale monoatomico n Lo Zero delle energie e’ imprecisato, ma non ha importanza in Termodinamica, poiche’ interessano solo le variazioni di Energia n Dipende SOLO da T, non da V o p Marina Cobal - Dipt. di Fisica Universita' di Udine 23

Unita’ di misura n n Cal: definita come la quantità di calore che serve per portare 1 kg di acqua da 14, 5°C a 15, 5°C Joule (1818 -1889) vede che lavoro-energia e calore sono la stessa cosa (circa metà dell’ 800) n trasforma lavoro in calore e misura i risultati Marina Cobal - Dipt. di Fisica Universita' di Udine 24

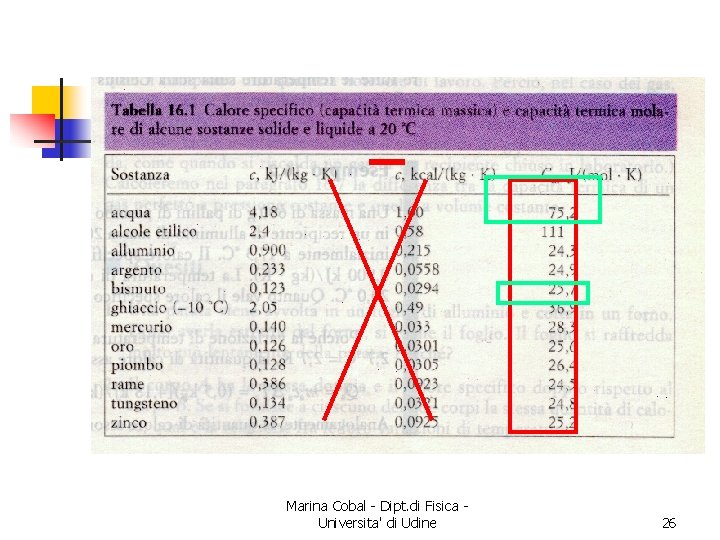
Calori specifici n Per alzare la temperatura di un corpo occorre dargli energia n n n si dà energia alle molecole Si può usare approssimativamente la relazione empirica la “costante” c è detta “calore specifico” Marina Cobal - Dipt. di Fisica Universita' di Udine 25
Marina Cobal - Dipt. di Fisica Universita' di Udine 26

Trasmissione del calore n In sistemi complessi n conduzione n n n da atomo ad atomo fortemente dipendente dai tipi di struttura atomica: si va da ottimi “conduttori” ad ottimi “isolanti” nei sistemi fluidi è esaltata dalla convezione n rimescolamento del fluido Nel vuoto n irraggiamento Marina Cobal - Dipt. di Fisica Universita' di Udine 27

Trasmissione del calore n Legge empirica per la trasmissione per conduzione Marina Cobal - Dipt. di Fisica Universita' di Udine 28
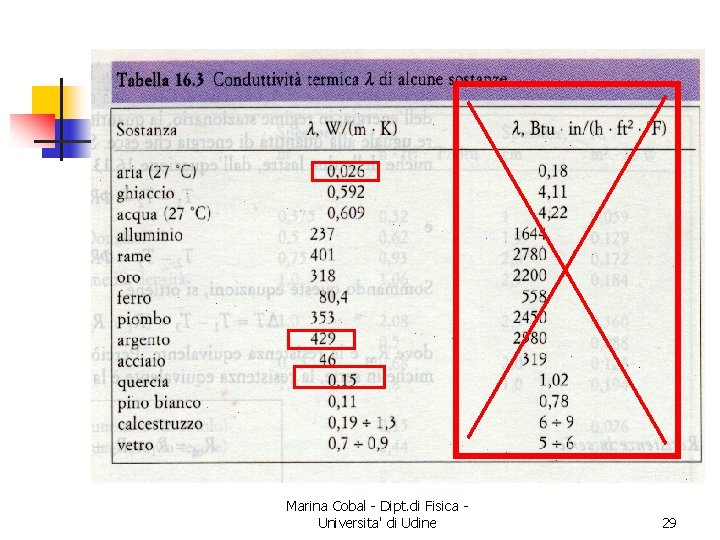
Marina Cobal - Dipt. di Fisica Universita' di Udine 29

Conduzione n Avviene per interazione fra atomo ed atomo n soprattutto tramite elettroni n n mobilissimi e velocissimi quindi un buon conduttore termico è anche un buon conduttore elettrico! Marina Cobal - Dipt. di Fisica Universita' di Udine 30

Convezione n n n Ristretta ai fluidi Di solito la densità di un fluido diminuisce con l’aumentare della temperatura Il fluido si sposta e viene rimpiazzato da altro a temperatura minore n n pentole e termosifoni Il meccanismo può divenire molto efficiente Marina Cobal - Dipt. di Fisica Universita' di Udine 31

Irraggiamento n Energia elettromagnetica (onde elettromagnetiche) irraggiate nello spazio n luce, X, onde radio, infrarossi, . . . n Sole, grill, barbecue n Principale meccanismo di trasmissione n Unico possibile nel vuoto dell’energia in tutto l’Universo Marina Cobal - Dipt. di Fisica Universita' di Udine 32

Irraggiamento n La quantità di energia irraggiata è proporzionale alla IV potenza della temperatura assoluta n n n è la legge (empirica) di Stefan-Boltzmann il coefficiente è l’emittenza della superficie Se si ha un corpo nero Marina Cobal - Dipt. di Fisica Universita' di Udine 33

Irraggiamento n Ecco un esempio Marina Cobal - Dipt. di Fisica Universita' di Udine 34

I cambiamenti di stato n Quando energie cinetiche e potenziali medie sono circa uguali. . . n n ad una temperatura ben determinata… . . . fornire energia significa aumentare le energie potenzialisenza variare le energie cinetiche n n si spezzano legami molecolari da solido si passa a liquido, o a vapore è il cambiamento di stato Marina Cobal - Dipt. di Fisica Universita' di Udine 35

I cambiamenti di stato n Se i legami sono regolari (stessa energia) si ha la fusione n n è il caso dei cristalli Se i legami sono casuali (energie diverse) si ha un progressivo rammollimento n Marina Cobal - Dipt. di Fisica Universita' di Udine è il caso dei vetri 36
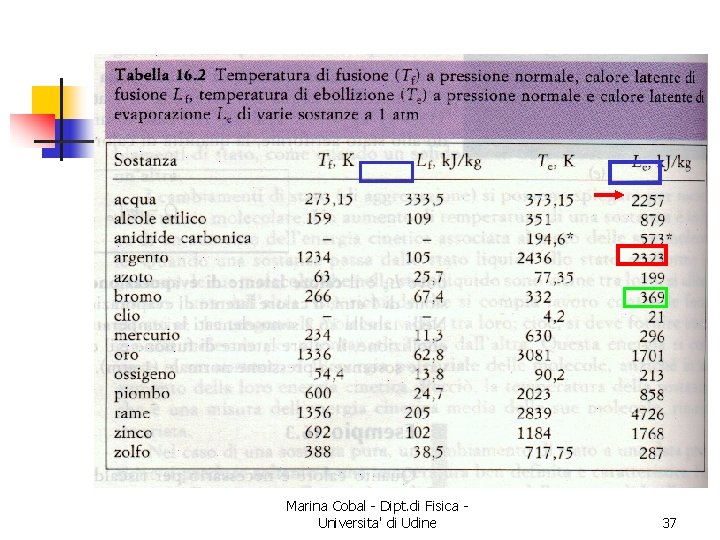
Marina Cobal - Dipt. di Fisica Universita' di Udine 37

La termodinamica Marina Cobal - Dipt. di Fisica Universita' di Udine 38

La termodinamica n n In termodinamica si prescinde dai dettagli del sistema Si parte da una serie di principi astratti Si traggono conclusioni di tipo molto generale Esempi di sistemi termodinamici n n n una batteria una soluzione chimica …ed anche un gas perfetto Marina Cobal - Dipt. di Fisica Universita' di Udine 39

Lo stato termodinamico Marina Cobal - Dipt. di Fisica Universita' di Udine 40

Definizione di stato n Un sistema generico viene descritto da una serie di parametri globali n n macroscopici Se i parametri n n non variano nel tempo hanno lo stesso valore in tutti i punti dello spazio saremo in uno stato termodinamico Marina Cobal - Dipt. di Fisica Universita' di Udine 41

Definizione di stato Attenzione n Raramente ci troviamo in stati termodinamici n ad esempio l’aria in una stanza di solito non lo è n stato termodinamico (approssimato) n n n umidità del 100% 37°C possibilmente da una settimana Marina Cobal - Dipt. di Fisica Universita' di Udine 42

Definizione di stato n In generale i parametri n n definiscono uno stato termodinamico sono legati fra loro da un’ equazione di stato Marina Cobal - Dipt. di Fisica Universita' di Udine 43

Definizione di stato n Nel caso del gas perfetto Parametri n Equazione di stato n Due parametri indipendenti n n il terzo lo si deduce dall’equazione di stato Marina Cobal - Dipt. di Fisica Universita' di Udine 44
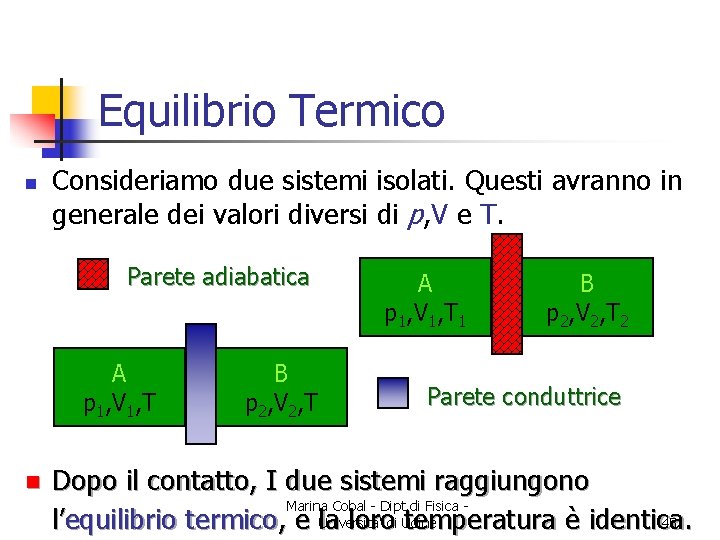
Equilibrio Termico n Consideriamo due sistemi isolati. Questi avranno in generale dei valori diversi di p, V e T. Parete adiabatica A p 1, V 1, T n B p 2, V 2, T A p 1, V 1, T 1 B p 2, V 2, T 2 Parete conduttrice Dopo il contatto, I due sistemi raggiungono Marina Cobal - Dipt. di Fisica Universita' 45. l’equilibrio termico, e la lorodi Udine temperatura è identica
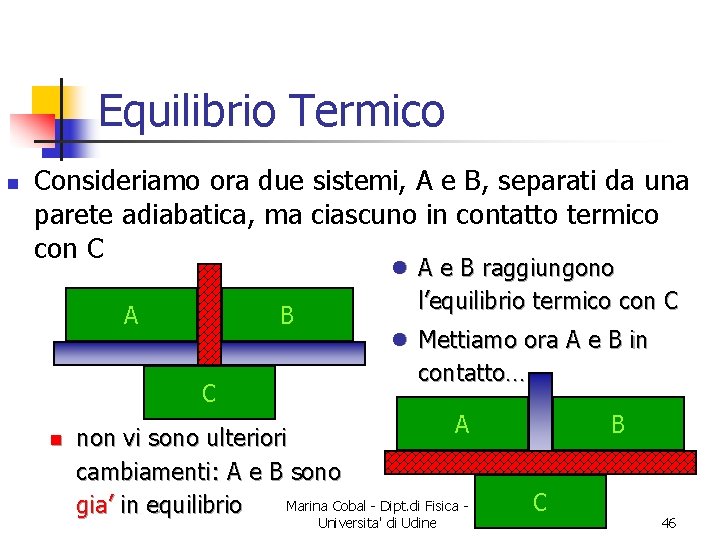
Equilibrio Termico n Consideriamo ora due sistemi, A e B, separati da una parete adiabatica, ma ciascuno in contatto termico con C l A e B raggiungono A B C n l’equilibrio termico con C l Mettiamo ora A e B in contatto… A non vi sono ulteriori cambiamenti: A e B sono Marina Cobal - Dipt. di Fisica gia’ in equilibrio Universita' di Udine B C 46

Principio Zero della Termodinamica ASSIOMA: due sistemi in equilibrio termico con un terzo, sono in equilibrio tra loro. n Il principio zero della termodinamica e’ stato enunciato dopo il primo e secondo principio. Ci si e’ resi conto della sua necessita’ quando si e’ iniziato a costruire l’edificio della Termodinamica in modo logico. n Il Termometro funziona grazie a questo principio Marina Cobal - Dipt. di Fisica Universita' di Udine 47

Equilibrio Un sistema è in equilibrio se i valori delle grandezze che lo caratterizzano rimangono costanti nel tempo n n Equilibrio meccanico: nulla si muove. Forze in equilibrio Equilibrio chimico: composizione costante Equilibrio termico: temperatura costante Equilibrio termodinamico: termico+chimico+meccanico Marina Cobal - Dipt. di Fisica Universita' di Udine 48
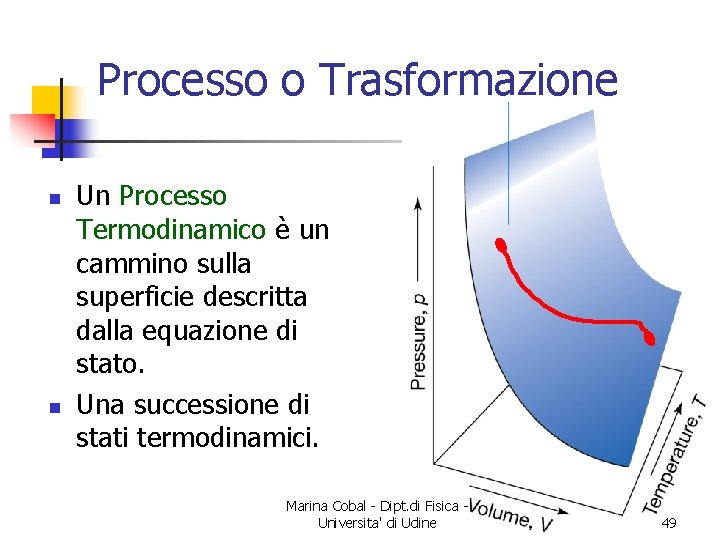
Processo o Trasformazione n n Un Processo Termodinamico è un cammino sulla superficie descritta dalla equazione di stato. Una successione di stati termodinamici. Marina Cobal - Dipt. di Fisica Universita' di Udine 49
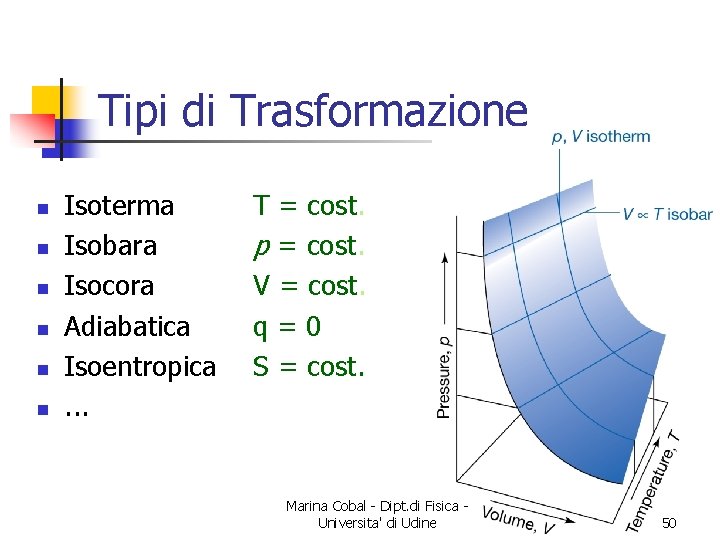
Tipi di Trasformazione n n n Isoterma Isobara Isocora Adiabatica Isoentropica. . . T = cost. p = cost. V = cost. q=0 S = cost. Marina Cobal - Dipt. di Fisica Universita' di Udine 50
- Slides: 49