C N BNG HO HC CHNG 8 Copyright

C N BẰNG HOÁ HỌC CHƯƠNG 8 Copyright © 1999 by Harcourt Brace & Company All rights reserved. Requests for permission to make copies of any part of the work should be mailed to: Permissions Department, Harcourt Brace & Company, 6277 Sea Harbor Drive, Orlando, Florida
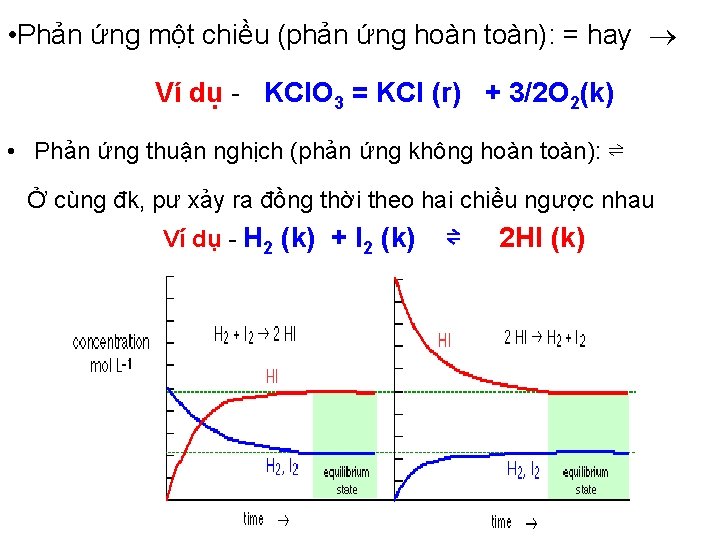
• Phản ứng một chiều (phản ứng hoàn toàn): = hay Ví dụ - KCl. O 3 = KCl (r) + 3/2 O 2(k) • Phản ứng thuận nghịch (phản ứng không hoàn toàn): ⇌ Ở cùng đk, pư xảy ra đồng thời theo hai chiều ngược nhau Ví dụ - H 2 (k) + I 2 (k) ⇌ 2 HI (k)

Phản ứng đồng thể - pư trong thể tích 1 pha HCl(dd) + Na. OH(dd) = Na. Cl (dd) + H 2 O(l) Phản ứng dị thể - pư diễn ra trên bề mặt phân chia pha Zn (r) + 2 HCl (dd) = Zn. Cl 2(dd) + H 2(k) Phản ứng đơn giản - pư diễn ra qua 1 giai đoạn (1 tác dụng cơ bản) Ví dụ: H 2(k) + I 2(k) = 2 HI (k) Phản ứng phức tạp – pư diễn ra qua nhiều giai đoạn ( nhiều tác dụng cơ bản) Các giai đoạn : nối tiếp , song, thuận nghịch…

Phân tử số - là số tiểu phân của chất phản ứng tương tác gây nên biến đổi hoá học trong 1 tác dụng cơ bản. (nguyên dương, 3) Đối với pư đơn giản PTS=1 → pư đơn phân tử I 2 (k) = 2 I(k) PTS=2 → pư lưỡng phân tử H 2(k) + I 2(k) = 2 HI (k) PTS=3 → pư tam phân tử 2 NO (k) + O 2(k) = 2 NO 2(k) Định luật tác dụng khối lượng (M. Guldberg và P. Waage ) Ở nhiệt độ không đổi, pư đồng thể, đơn giản: a. A + b. B = c. C + d. D Tốc độ phản ứng : v = k. Ca. A. Cb. B

Cân bằng hóa học Phản ứng của hệ khí lý tưởng (pư đơn giản ): a. A (k) + b. B(k) =0 C 0 A CA ⇌ C 0 B Cb vt = vn (CA)cb=const G=0 (PA)cb=const c. C(k) 0 Cc d. D(k) 0 (mol/l ) CD (CB)cb=const (Cc)cb=const (CD)cb =const (PB)cb=const (PC)cb=const (PD)cb =const v vt vt = vn vn 0 + cb

Nhận xét về trạng thái cân bằng hoá học • Trạng thái cbhh là trạng thái cân bằng động. • Trạng thái cân bằng ứng với Gpư= 0. • Dấu hiệu của trạng thái cân bằng hoá học: Ø Tính bất biến theo thời gian Ø Tính linh động Ø Tính hai chiều. (A’=0)
Examples of Chemical Equilibria Sự tạo thành thạch nhũ Ca. CO 3(r) + H 2 O(l) + CO 2(k) Ca 2+(dd) + 2 HCO 3 -(dd)

Hằng số cân bằng cho phản ứng đồng thể Hệ khí lý tưởng a. A(k) + b. B(k) ⇌ c. C(k) + d. D(k) (pư đơn giản ) Khi trạng thái đạt cân bằng: vt = vn • K – hằng số ở nhiệt độ xác định: hằng số cân bằng.
![Xác định K 2 NOCl(K) 2 NO(k) + Cl 2(k) [NOCl] [NO] [Cl 2] Xác định K 2 NOCl(K) 2 NO(k) + Cl 2(k) [NOCl] [NO] [Cl 2]](http://slidetodoc.com/presentation_image_h/9bdae0e5a4dafe061e13675b34b9acd6/image-9.jpg)
Xác định K 2 NOCl(K) 2 NO(k) + Cl 2(k) [NOCl] [NO] [Cl 2] Ban đầu Phản ứng Cân bằng 2. 00 - 0. 66 1. 34 0 +0. 66 0 +0. 33

Hằng số cân bằng cho phản ứng đồng thể (Dung dịch lỏng , loãng) a. A(dd) + b. B(dd) ⇌ c. C(dd) + d. D(dd)
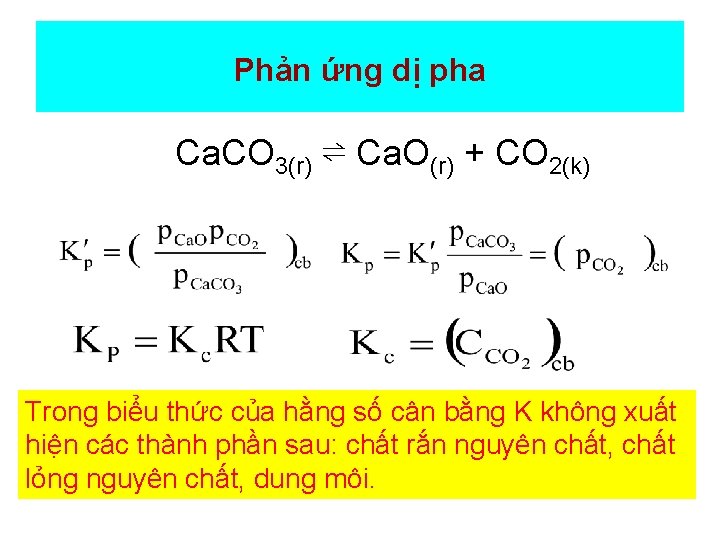
Phản ứng dị pha Ca. CO 3(r) ⇌ Ca. O(r) + CO 2(k) Trong biểu thức của hằng số cân bằng K không xuất hiện các thành phần sau: chất rắn nguyên chất, chất lỏng nguyên chất, dung môi.
![Mg(OH)2(r) ⇌ Mg 2+(dd) + 2 OH-(dd) K = [Mg 2+]cb. [OH-]2 cb = Mg(OH)2(r) ⇌ Mg 2+(dd) + 2 OH-(dd) K = [Mg 2+]cb. [OH-]2 cb =](http://slidetodoc.com/presentation_image_h/9bdae0e5a4dafe061e13675b34b9acd6/image-12.jpg)
Mg(OH)2(r) ⇌ Mg 2+(dd) + 2 OH-(dd) K = [Mg 2+]cb. [OH-]2 cb = T Mg(OH)2 - Tích số tan CH 3 COOH(dd) + H 2 O ⇌ CH 3 COO- (dd) + H 3 O+ Hằng số điện ly của axit NH 4 OH (dd) = NH 4+ (dd) + OH-(dd) Hằng số điện ly của baze CH 3 COONa (dd) + 2 H 2 O ⇌ CH 3 COOH (dd) + Na. OH(dd) CH 3 COO- (dd) + 2 H 2 O ⇌ CH 3 COOH (dd) + OH- (dd) Hằng số thuỷ phân

NHẬN XÉT về Kp và Kc Ø Là hằng số ở nhiệt độ nhất định, chỉ phụ thuộc vào bản chất pư và nhiệt độ, chứ không phụ thuộc vào nồng độ hoặc áp suất riêng phần của chất pư ØPhụ thuộc vào cách thiết lập các hệ số trong ptpư. ØHằng số cân bằng Kp , Kc không có thứ nguyên. ØHằng số cân bằng không phụ thuộc vào chất xúc tác ØHằng số cân bằng có giá trị càng lớn thì hiệu suất pư càng cao.
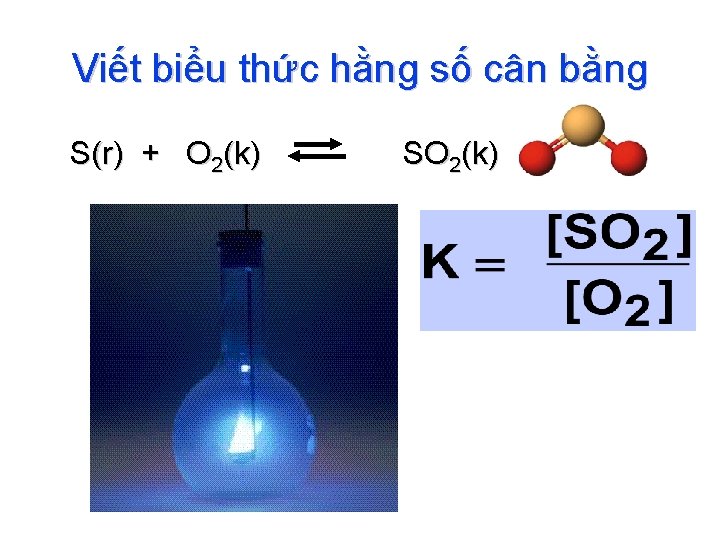
Viết biểu thức hằng số cân bằng S(r) + O 2(k) SO 2(k)
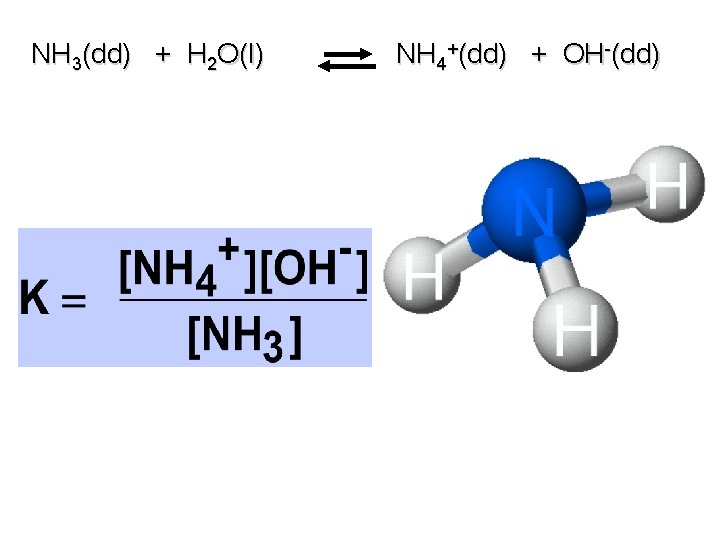
NH 3(dd) + H 2 O(l) NH 4+(dd) + OH-(dd)
![S(r) + O 2(k) SO 2(k) K 1 = [SO 2] / [O 2] S(r) + O 2(k) SO 2(k) K 1 = [SO 2] / [O 2]](http://slidetodoc.com/presentation_image_h/9bdae0e5a4dafe061e13675b34b9acd6/image-16.jpg)
S(r) + O 2(k) SO 2(k) K 1 = [SO 2] / [O 2] SO 2(k) +1/2 O 2(k) SO 3(k)K 2 = [SO 3] / [SO 2][O 2]1/2 S(r) + 3/2 O 2(k) SO 3(k) K = ? ?
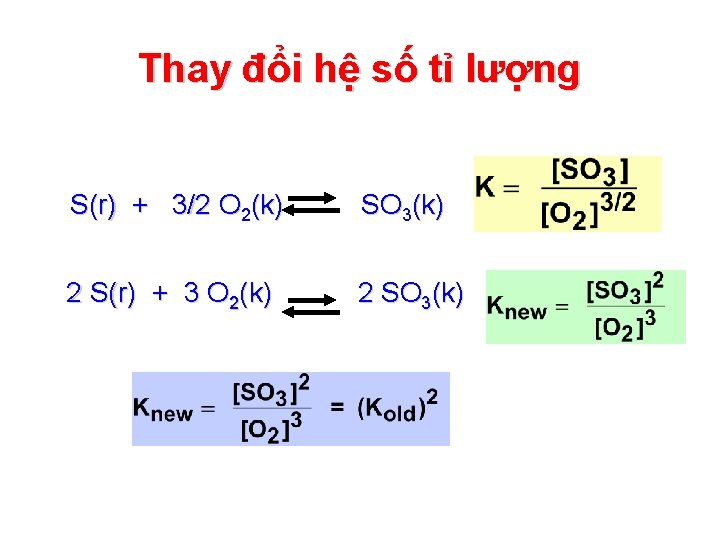
Thay đổi hệ số tỉ lượng S(r) + 3/2 O 2(k) SO 3(k) 2 S(r) + 3 O 2(k) 2 SO 3(k)
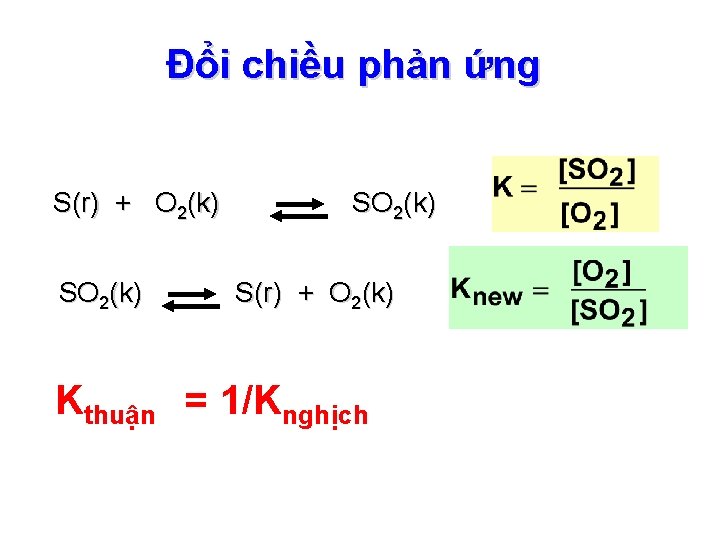
Đổi chiều phản ứng S(r) + O 2(k) SO 2(k) S(r) + O 2(k) Kthuận = 1/Knghịch

Quan hệ giữa hằng số cân bằng và G PHẢN ỨNG ĐỒNG THỂ a. A + b. B ⇌ c. C + d. D üKhí lý tưởng Khi phản ứng đạt trạng thái cân bằng: GT = 0 üDungdịch lỏng, loãng Khi phản ứng đạt trạng thái cân bằng: GT = 0 Kp = f(bc pư, T) Kp f(C)

Quan hệ giữa hằng số cân bằng và G Phản ứng dị pha : a. A + b. B ⇌ c. C Chất khí [] → P (atm) Dung dịch loãng [] → C (mol/l) Rắn nc, lỏng nc, dung môi (H 2 O) → 1 + d. D

• Nếu Q < K → G < 0 → phản ứng xảy ra theo chiều thuận • Nếu Q > K → G > 0 → phản ứng xảy ra theo chiều nghịch • Nếu Q = K → G = 0 → hệ đạt trạng thái cân bằng Ví dụ : Tính hằng số cân bằng của phản ứng: 2 NO 2(k) ở 298 K khi biết Giải: ↔ N 2 O 4(k)
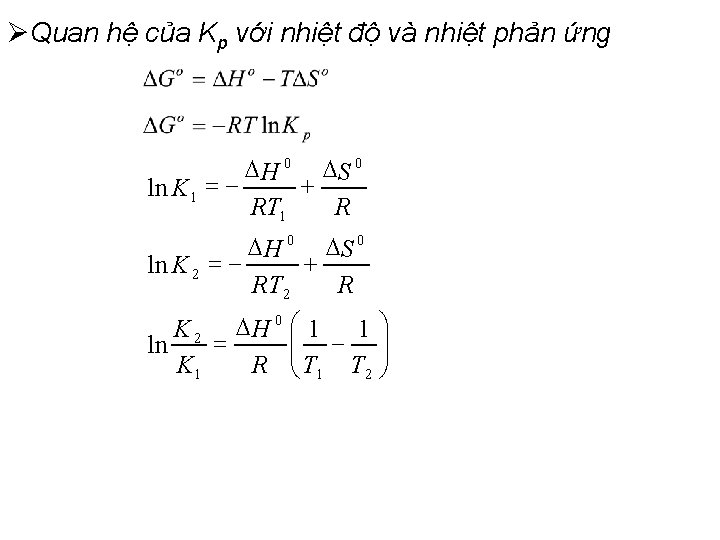
ØQuan hệ của Kp với nhiệt độ và nhiệt phản ứng ln K 1 = ln K 2 = - H 0 RT 1 H 0 RT 2 + + S 0 R K 2 H 0 æ 1 1 ö çç - ÷÷ = ln K 1 R è T 1 T 2 ø

Ví dụ NO(k) + ½ O 2(k) ⇌ NO 2(k) Tính Kp ở 3250 C? • Biết: H 0 = -56, 484 k. J và Kp = 1, 3. 106 ở 250 C K 598 H 0 æç 1 1 ö÷ = ln ç K 298 R è T 298 T 598 ÷ø K 598 56484 æ 1 1 ö =ç ÷ = -11, 437 ln 6 8, 314 è 298 598 ø 1, 3. 10 ln K 325 = 2. 64 K 325 = 14. 02

Nguyên lý chuyển dịch cân bằng Le Chatelier Phát biểu: Một hệ đang ở trạng thái cân bằng mà ta thay đổi một trong các thông số trạng thái của hệ (nồng độ, nhiệt độ, áp suất) thì cân bằng sẽ dịch chuyển theo chiều có tác dụng chống lại sự thay đổi đó. n =0 áp suất chung không ảnh hưởng đến trạng thái cân bằng.
![N 2(k) + 3 H 2(k) ⇌ 2 NH 3(k) ; H<0 [N 2] N 2(k) + 3 H 2(k) ⇌ 2 NH 3(k) ; H<0 [N 2]](http://slidetodoc.com/presentation_image_h/9bdae0e5a4dafe061e13675b34b9acd6/image-25.jpg)
N 2(k) + 3 H 2(k) ⇌ 2 NH 3(k) ; H<0 [N 2] ↑ [NH 3] ↓ P↑ T↓ cân bằng chuyển dịch theo chiều thuận
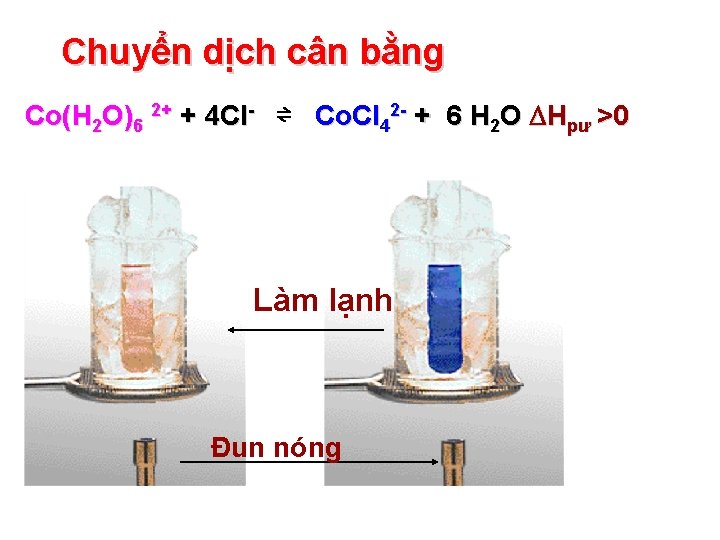
Chuyển dịch cân bằng Co(H 2 O)6 2+ + 4 Cl- ⇌ Co. Cl 42 - + 6 H 2 O Hpư >0 Làm lạnh Đun nóng

- Slides: 27