c Chp 7 Transformations associes des ractions acidobasiques

c Chp. 7 Transformations associées à des réactions acido-basiques en solution aqueuse I. Autoprotolyse de l'eau. 1. Réaction d’autoprotolyse de l’eau
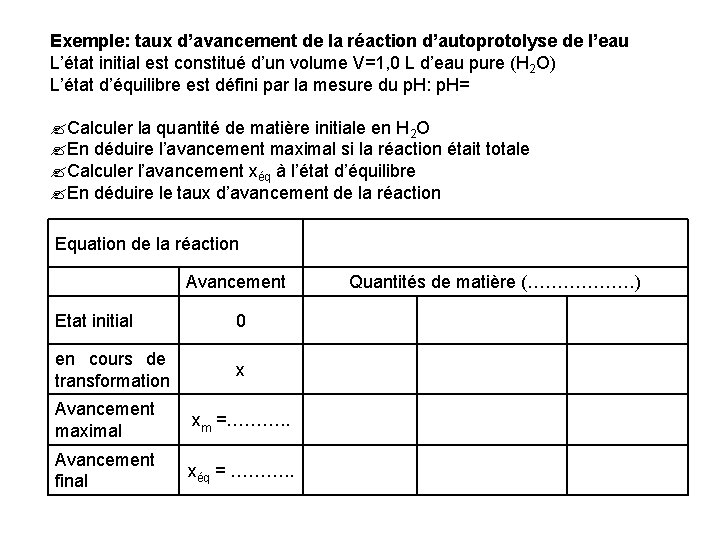
Exemple: taux d’avancement de la réaction d’autoprotolyse de l’eau L’état initial est constitué d’un volume V=1, 0 L d’eau pure (H 2 O) L’état d’équilibre est défini par la mesure du p. H: p. H= ? Calculer la quantité de matière initiale en H 2 O ? En déduire l’avancement maximal si la réaction était totale ? Calculer l’avancement xéq à l’état d’équilibre ? En déduire le taux d’avancement de la réaction Equation de la réaction Avancement Etat initial 0 en cours de transformation x Avancement maximal xm =………. . Avancement final xéq = ………. . Quantités de matière (………………)

c Chp. 7 Transformations associées à des réactions acido-basiques en solution aqueuses I. Autoprotolyse de l'eau. 1. Réaction d’autoprotolyse de l’eau 2. Produit ionique de l'eau Ke. 3. Échelle de p. H.
3. Échelle de p. H


c Chp. 7 Transformations associées à des réactions acido-basiques en solution aqueuses I. Autoprotolyse de l'eau. II. La constante d'acidité KA et le p. KA. 1. Définition. 2. Exemples.
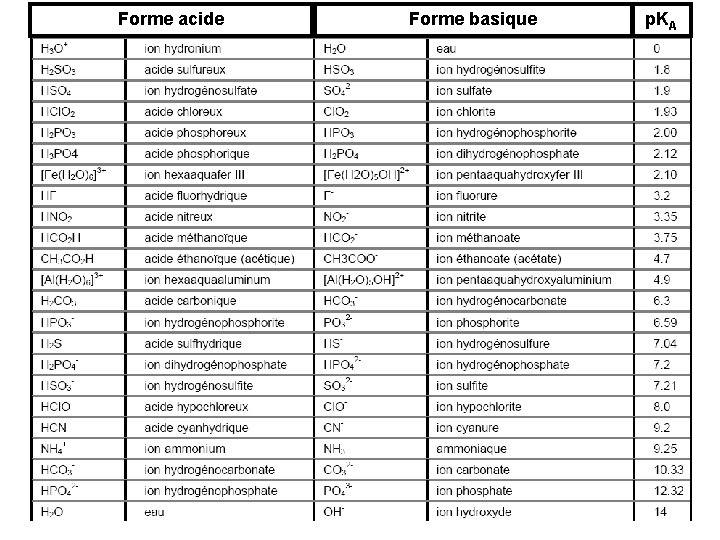
Forme acide Forme basique p. KA

c Chp. 7 Transformations associées à des réactions acido-basiques en solution aqueuses I. Autoprotolyse de l'eau. II. La constante d'acidité KA et le p. KA. III. Diagramme de prédominance et distribution des espèces acido-basiques. 1. Définition. 2. p. H d'une solution aqueuse contenant un acide A et sa base conjuguée B. 3. Domaine de prédominance.
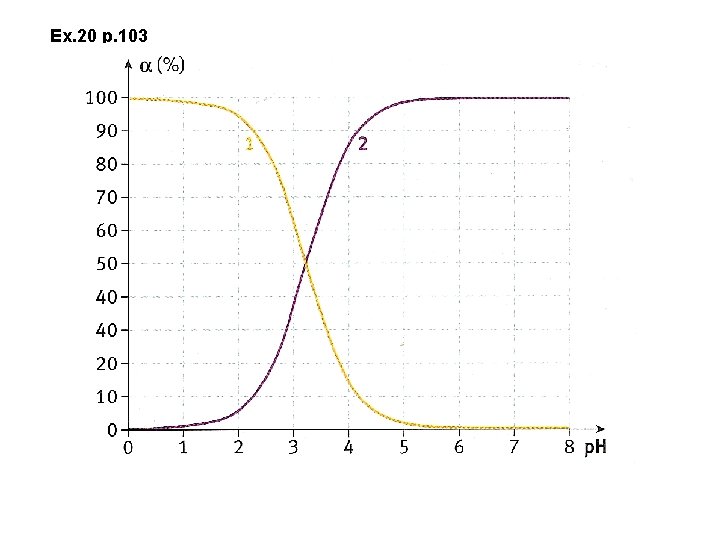
Ex. 20 p. 103

c Chp. 7 Transformations associées à des réactions acido-basiques en solution aqueuses I. Autoprotolyse de l'eau. II. La constante d'acidité KA et le p. KA. III. Diagramme de prédominance et distribution des espèces acido-basiques. 1. Définition. IV. Constante d'équilibre associée à une réaction acido-basique. 2. p. H d'une solution aqueuse contenant un acide A et sa base conjuguée B. 1. Equation de la réaction. 3. Domaine de prédominance. 2. Application Constante d'équilibre associée. 4. aux indicateurs colorés. 3. Sens de l'évolution de la transformation.

c Chp. 7 Transformations associées à des réactions acido-basiques en solution aqueuses I. Autoprotolyse de l'eau. II. La constante d'acidité KA et le p. KA. III. Diagramme de prédominance et distribution des espèces acido-basiques. IV. Constante d'équilibre associée à une réaction acido-basique. V. Comparaison du comportement des acides en solution aqueuse. 1. Forces relatives de deux acides. 2. Comparaison des p. H des solutions de deux acides de forces différentes. 3. Comparaison des constantes d'acidité.

c Chp. 7 Transformations associées à des réactions acido-basiques en solution aqueuses I. Autoprotolyse de l'eau. II. La constante d'acidité KA et le p. KA. III. Diagramme de prédominance et distribution des espèces acido-basiques. IV. Constante d'équilibre associée à une réaction acido-basique. V. Comparaison du comportement des acides en solution aqueuse. VI. Comparaison du comportement des bases en solution aqueuse. 1. Forces relatives de deux bases. 2. Comparaison des p. H des solutions de deux bases de forces différentes. 3. Comparaison des constantes d'acidité.
- Slides: 12