Buxoro Yuqori texnologiyalar muhandislik texnika instituti Umumiy kimyo

Buxoro Yuqori texnologiyalar muhandislik texnika instituti “Umumiy kimyo” kafedrasi tuzuvchi: К. E. Ro’ziyeva

Reja: 1. VI guruhning asosiy geruhcha elementlariga umumiy xarakteristika 2. Kislorodning tabiatda tarqalishi. 3. Tabiiy birikmalari. 4. Olinishi. 5. Fizikaviy va kimyoviy xossalari. 6. Allotropik shakl o’zgarishlari. 7. Ishlatilishi. 8. Ozon, xossalari. 9. Suv, xossalari. 10. Oltingugurt va uning xossalari. VI guruhning asosiy guruhcha elementlari.
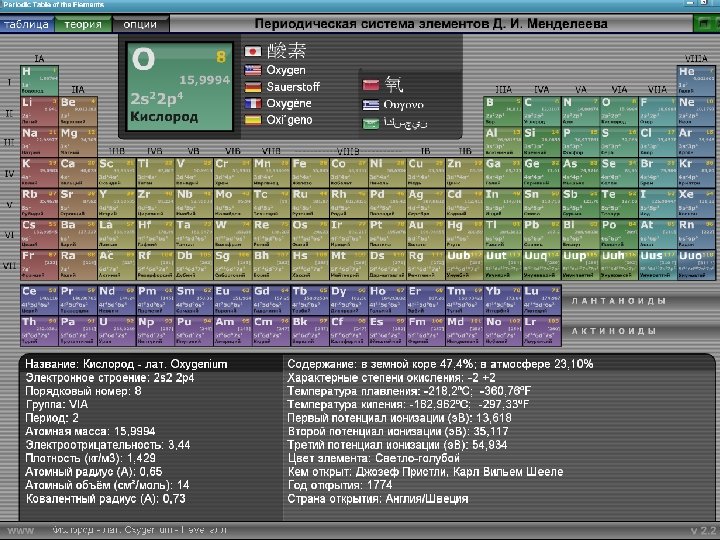

Davriy sistemaning oltinchi asosiy guruhcha elementlarining umumiy xarakteritikasi H 2 O

«Kislorod» elementiga umumiy xarakteristika • Kimyoviy belgisi : О • Davriy sistemadagi o’rni: davr II, gruppa : VIA, tartib raqami : 8 • Atom massasi : Аr(O)=16 • Kimyoviy formulasi: О 2 • Molekulyar massasi : Mr(O 2)=32 • Valentligi : II • Izotoplari: 816 O (99, 769%); Izotoplari: 817 O (0, 037%) • Izotoplari: 818 O (0, 204%)

2. Tabiatda tarqalishi Yer sharida tarqalishi jihatidan 1 o’rinni egallaydi. Kislorod – 49%, undan keyin kremniy 26%, alyuminiy 7%, temir 5%, kalsiy 4%, natriy, kaliy va magniy 2% dan, vodorod 1%. Gidrosferada 89%ni tashkil qiladi Djozef Pristli (ingliz olimi) 1774 yilda simob(II)-oksidining parchalanishidan kislorodni hosil qilib, uning xossalarini o’rgangan olim.
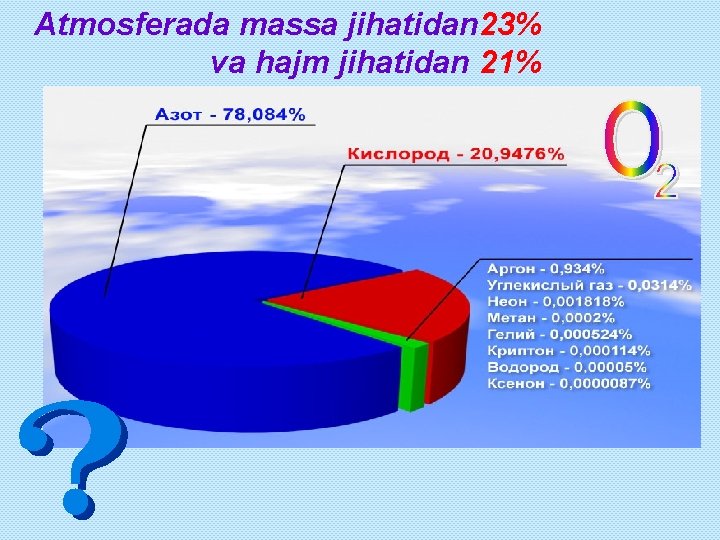
Atmosferada massa jihatidan 23% va hajm jihatidan 21%

Karl Vilgelm Sheyele Antuan Lavuaz’ye (shved kimyogari) 1772 1774 yilda tajriba o’tkazib, havoning 1/5 qismi kisloroddan tashkil topganligini aniqlagan olim. yilda kislorodni kashf qildi.

2. Laboratoriyada kaliy permanganatning parchalanishidan hosil bo’ladi. 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2↑

б) Suvning elektrolizidan: 2 H 2 O = 2 H 2↑ + O 2↑ в) Vodorod peroksidning parchalanishidan: 2 H 2 O 2 = 2 H 2 O + O 2↑ г) Kaliy xloratning parchalanishidan: 2 KCl. O 3 = 2 KCl + 3 O 2↑ д) simov(II)-oksidining parchalanishidan: 2 Hg. O = 2 Hg + O 2↑

Kislorodning fizikaviy xossalari Kislorod – hidsiz, mazasiz, gazsimon modda bo’lib, suvda kam eriydi, havodan biroz og’irroq. Tirik organizmlarda o‘rtacha hisob da taxminan 70% kislorod massasi bor. Yerdagi erkin kislorodlarning barcha mas sasi fotosintеz jarayonida kislorod ajratib chiqaradigan hayot fao liyatidan hosil bo‘lgan va saqlanmoqda. Turli moddalarning kislorod bilan oksidlanishi hayvonlar va o‘simliklarning hayot faoliyatlari uchun kе rakli enеrgiya manbaidir. Insonning xo‘jalik faoliyati kislorodning yеrda ayla nib yurishini o‘zgartiradi; masalan, yoqilg‘ilarning yonishi uchun dunyoda har yili 9 Gt (9 · 109 t) kislorod sarf bo‘ladi. Odatdagi sharoitda kislorod molеkulasi ikki atomli (O 2); sokin elеktr razryadda ozon (O 3) hosil bo‘ladi. Gaz holatidagi kislorodning zichligi 1, 429 g/sm 3(suyuq); tqayn= 182, 90 C, tsuyuq = 218, 90 C; kritik harorati CI 2, CO 2, SO 2 larning haroratidan past va 118, 840 ga tеng. Kislorod kimyoviy jihatdan eng faol (ftordan kеyin) mеtalmas elеmеntdir.

Kimyoviy xossalari: Kislorod rangsiz va hidsiz gazdir. Uning atom og’irligi 15, 9984, suyuqlanish harorati tc = − 2190, qaynash harorati tqay = − 1830. Normal sharoitda 1 l kislorod 1, 43 g keladi. 100 hajm suvda 00 da 5 hajm, 200 C da 3 hajm kislorod eriydi. Kislorodning suvda eruvchanligi azotnikidan ortiq, shuning uchun suvda kislorod miqdori azot miqdoridan ko’proq bo’ladi. Suvda erigan kislorod miqdori suvda yashaydigan hayvonlarning hayot kechirishi uchun etarlidir. Suyuq va qattiq kislorod ko’kimtir tusda bo’ladi. Kislorodning ikki allotropik shakli bor, bular kislorod va ozondir. Kislorod faol elementdir. U ko’pgina elementlar bilan birikmalar hosil qiladi va bu jihatdan ftorga o’xshaydi. Kislorod atomining tuzilishi 1 s 22 p 4, demak, ikkita toq elektronlar hisobiga uning kovalentligi 2 ga teng (sp 2 bog) bo’ladi. Bundan tashqari kislorod atomi yana ikkita elektron juftining donori bo’la oladi. Demak, uning eng yuqori kovalentligi 4 ga teng (bunda sp 3 –gibridlanish ro’y beradi). Kislorodning kovalentligi uchga ham teng bo’la olishi mumkin (sp 2 –bog’ va sp 3 – bog’). Lekin ko’pchilik birikmalarda kislorodning valentligi – 2 ga teng. 2 S + 3 O 2 = 2 SO 3↑ 4 Na + O 2 = 2 Na 2 O CH 4 + 2 O 2 = CO 2 ↑ + 2 H 2 O

Kimyoviy xossalari: Ko’pgina metallar bilan uy haroratida birikadi. 2 Ca + O 2 = 2 Ca. O 2 Zn + O 2 = 2 Zn. O metallmaslar bilan kislorod qizdirganda birikadi. 600 C da 4 P + 5 O 2 = 2 P 2 O 5 2500 C da C + O 2 = CO 2 700 -8000 C da S + O 2 = SO 2 Ko’pgina murakkab moddalar bilan ham reaksiyaga kirishadi. Masalan, oddiy sharoitda 2 NO + O 2 = 2 NO 2 qizdirganda 2 H 2 S + O 2 = 2 S + 2 H 2 O yoki 2 H 2 S + 3 O 2 = 2 SO 2 + 2 H 2 O.

6. Kislorodning ishlatilishi:
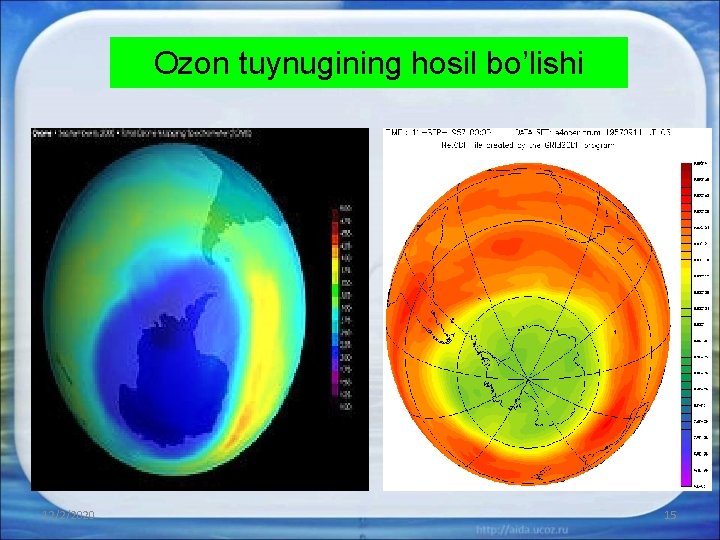
Ozon tuynugining hosil bo’lishi 12/2/2020 15

Ozon kislorodning ikkinchi allotropik shaklidir; ozonning molekulasida uch atom kislorod bo’ladi. Ozon oz miqdorda havoda uchraydi. Kuchli yashin vaqtida ba’zi organik moddalarning, masalan, daraxt smolasining chirishidan ham ozon chiqadi, shuning uchun qarag’ayzor havosida ozon ko’p bo’ladi. 1840 yilda prof. Shenbeyn elektrostatik mashina ishlayotgan vaqtida yoqimsiz hid paydo bo’lganini payqadi. U hidga sababchi gaz ozon (O 3) ekanligi aniqlandi ( «ozon» so’zi grekcha «hidli» so’zidan olingan), (10 -30 km balandlikda ulrabinafsha nurlar ta’sir etganda kisloroddan hosil bo’ladi: 3 O 2→ 2 O 3 – 289, 4 k. J) Umuman ozon atomar kislorod hosil bo’ladigan jarayonlarda (peroksidlar parchalanganda, suv radiolizga uchraganda va boshqa hollarda) hosil bo’ladi. Laboratoriyada ham elektrsizlash yo’li bilan ozon olish mumkin. Shu usulda ozon olish uchun ishlatiladigan asbob ozonator deb ataladi. Ozon ta’sirida (oltin va platinadan tashqari) barcha metallar oksidlanadi; ammiak nitrat va nitrit kislotalar aralashmasiga aylanadi, spirt yonib ketadi, rezina emiriladi, ozonning kumushga va kaliy yodid eritmasiga ta’sirini quyidagi tenglamalar bilan ko’rsatish mumkin: 2 Ag + O 3 → Ag 2 O + O 2 12/2/2020 16

Suv va uning xossalari

Kimyoviy formulasi H 2 O 12/2/2020 18

Globusga qarab suv haqida nimani bilib olish mumkin? Okeanlar yer usti suvlarining 97%, muzliklar 2. 4%, daryo, ko’l kabi kichik havzalar esa 0. 6%'ini o’zida saqlaydi.

Ko’llar Daryolar Dengizlar Okeanlar Yerdagi suv zahiralari Muzliklar Kanallar Yer osti suvlari Suv omborlari
Tabiatda uch xil agregat holatda uchraydi Suyuq • Daryo, dengiz va okean suvlari • Yomg’ir Qattiq • muz • qor Gazsimon • bug’

Bu qiziq!!! Archa og’irligi– 100 kg bo’lsa, shundan 80 kg – suv; Nartsis gulining og’irligi– 100 g bo’lsa, shundan 85 g suv Losos balig’ining og’irligi– 2 kg bo’lsa, 1, 5 kg suv.

BMT Bosh Assambleyasining qarori bilan 2005 -2015 yillar «Suv uchun» harakati Xalqaro o’n yilligi deb e’lon qilingan. 12/2/2020 hayot 23

Oltingugurt guruhchasi elementlari va ularning xossalari
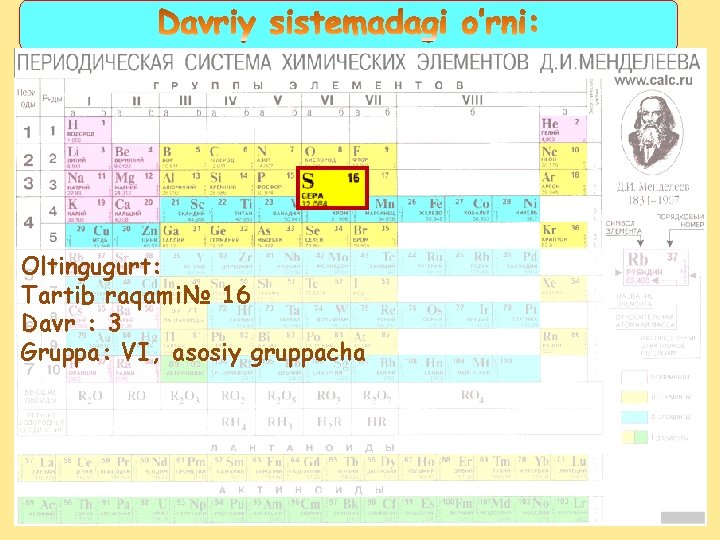
Oltingugurt: Tartib raqami№ 16 Davr : 3 Gruppa: VI, asosiy gruppacha
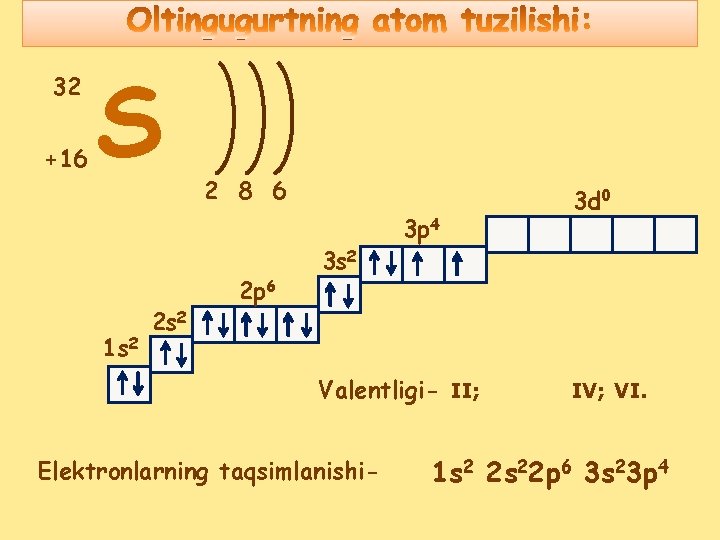
32 +16 S 1 s 2 2 8 6 2 p 6 3 s 2 3 p 4 Valentligi- II; Elektronlarning taqsimlanishi- 3 d 0 IV; VI. 1 s 2 2 s 22 p 6 3 s 23 p 4

Oltingugurt S, tartib nomeri 16, atom og'irligi 32. 064, elektron konfugurasiyasi 1 S 22 P 63 S 23 P 4; tabiiy izotoplari 1632 S, 1633 S, 1634 S, 1636 S. Oltingugurt qadimdan ma'lum element. Oltingugurtning Yer qobigidagi og'irlik miqdori 0. 05 % ni tashqil etadi. Oltingugurt tabiatda erkin (tug’ma oltingugurt) holida va birikmalar (sulfidlar va sulfatlar) holida uchraydi. Eng muhim sulfid rudalar (ularning ko’rinishlariga qarab) kolchedanlar va metall yaltiroqlar nomi bilan yuritiladi. Bular qatoriga temir kolchedani Fe. S 2, (buni pirit va oltingugurt kolchedani deb xam yuritiladi. ) Rux yaltirogi Zn. S, qo‘rg‘oshin yaltirogi Pb. S, mis kolchedani Cu. Fe. S 2, mis yaltirogi Cu 2 S kiradi. Metall sulfatlar tuz uyumlarini xosil qiladi, ba'zilari dengiz suvida erigan xolatda bo'ladi. Oltingugurt birikmalari neft konlarida va shifobaxsh suvlarda xam uchraydi.

Eng muxim sulfatlar qatoriga gips Ca. SO 4. 2 H 2 O, angidrid Ca. SO 4, achchik tuz Mg. SO 4. 2 H 2 O, kizerit Mg. SO 4. 2 H 2 O, og'ir shpat Ba. SO 4, selestin Sr. SO 4 va glauber tuzi Na. SO 4. 10 H 2 O kiradi. Organik olamda oltingugurt o‘simlik va hayvon oqsili tarkibida bo'ladi. U uglerod, kislorod, vodorod , azot va fosfor kabi hayot uchun eng zarur elementlardan biridir. Toshko‘mir tarkibida 1. 5% ga qadar oltingugurt bo'ladi. Ba'zan, oltingugurt, tarkibida oltingugurt bo'lgan gazlardan ham olinadi. Masalan, H 2 S dan oltingugurt olish uchun texnikada quyidagi reaksiyalardan foydalaniladi. 2 H 2 S + 3 O 2 = 2 SO 2 + 2 H 2 O 2 H 2 S + SO 2 = 3 S + 2 H 2 O
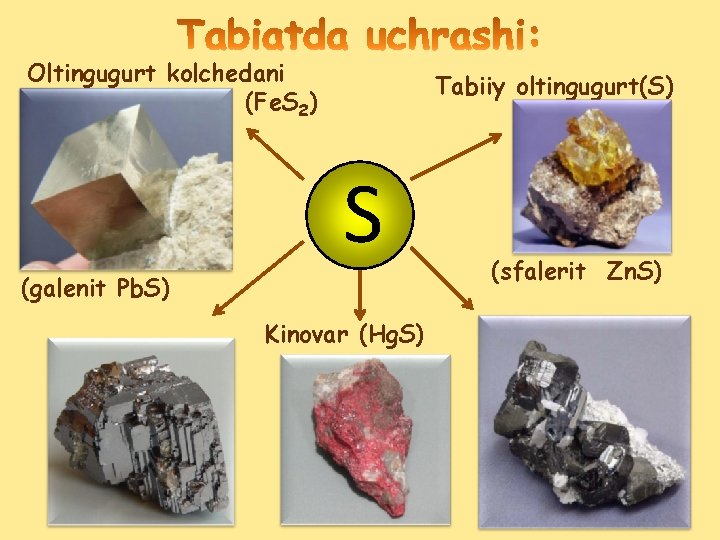
Oltingugurt kolchedani (Fе. S 2) Tabiiy oltingugurt(S) S (galenit Pb. S) Kinovar (Hg. S) (sfalerit Zn. S)


Oltingugurt allotropiyasi kristall, plastik va monoklinik

Foydalanilgan manbalar: • • • • http: //picture-world. narod. ru/pr/page_34. htm http: //vesnyanka. ucoz. ru/publ/stati/miniatjury_ehsse_zametki/36 -4 -2 http: //balkuz. ru/product_info. php? info=p 1418_ http: //radiomoon. narod. ru/ocean 1. htm http: //www. gorbushka. ru/map. html? kat=348&id=543883 http: //www. kimritorg. ru/cgibin/dsp. pl? from=20&f_id=993&catalog_id=392&event=cat_fabric&cl=search http: //www. rosbalt. ru/2008/07/22/506076. html http: //ru. wikipedia. org/wiki/Река http: //ru. wikipedia. org/wiki/Ручей http: //1 news. az/society/20080602052712967. html http: //digg. com/users/Philippeog/history/upcoming http: //times. ua/story/39603/ http: //www. sunhome. ru/journal/121947 http: //club-edu. tambov. ru/vjpusk/vjp 105/rabot/15/new_page_4. htm

E’tiboringiz uchun raxmat!
- Slides: 33