Buxoro davlat universiteti kimyo biologiya fakulteti 2 1

Buxoro davlat universiteti kimyo- biologiya fakulteti 2 -1 kim-13 guruh talabasi Muinova Niginaning alyuminiy nitrat va uning xossalari mavzusida TAYYORLAGAN KURS ISHI

Reja : 1. Kirish 2. Alyuminiy nitratning olinishi 2. 1. Labaratoriya sharoitida olinishi 2. 2. Sanoatda alyuminiy nitratning ishlab chiqarilishi 3. Alyuminiy nitrat xossalari 3. 1. Fizik va kimyoviy xossalari 3. 2. Alyuminiy nitrat kristallo gidratlari 3. 3. Alyuminiy nitrat ahamiyati , qo’llanilish sohalari

Yer qobig'i massasining 8, 8 foizi - tarqalishi bo'yicha dunyoda barcha elementlar orasida uchinchi , metallar orasida esa birinchi o'rinni egallovchi Alyuminiydan tashkil topgan

Alyuminiy Yengil va plastik , oqish metall bo’lib uni havoda qoplab oluvchi oksidlangan yupqa qatlam tufayli xira kumushrang tusga kiradi Okdis pardasini simob yordamida yo’qotish mumkin Kimyoviy jihatdan juda aktiv metall bo’lib , u tipik amfoter element sanaladi

Hozirgi kunda alyuminiyni olish uchun 1886 – yilda Geru va Xoll qo'llagan elektroliz usulidan foydalaniladi

Ø Alyuminiyni olish uchun xomashyo sifatida baksitdan foydalaniladi Al 2 O 3 *n. H 2 O Ø Avval baksitdan alyuminiy oksid olinadi , so’ngra alyuminiy oksidning suyuqlantirilgan kriolitdagi eritmasi elektroliz qilinadi Ø Suyuq aralashmada 6 – 8 % Al 2 O 3 , 92 -94 % Na 3[Al. F 6] bo’ladi. Ø Elektroliz jarayoni 900 0 C atrofida olib boriladi. Ø Suyuq aralashmadagi alyuminiy oksid Al 3+ va O 2 - ionlariga parchalanadi Al 2 O 3 2 Al 3+ + 3 O 2Ø Tok berilganda Al 3+ katodda qaytariladi , anotda O 2 oksidlanadi
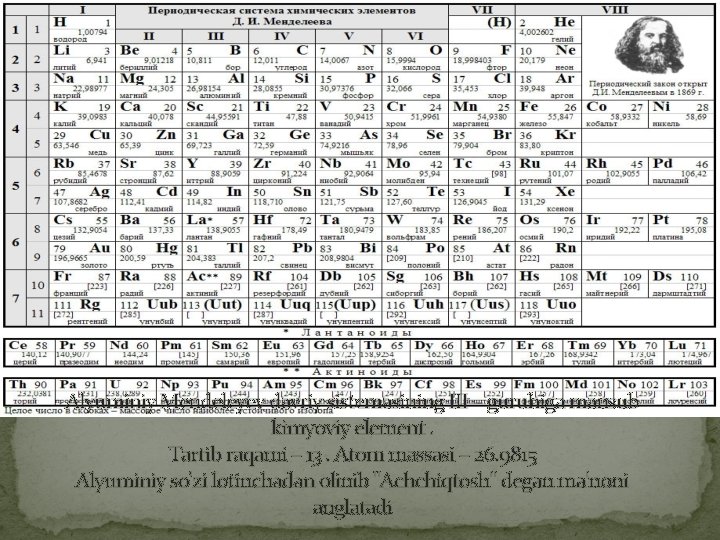
Alyuminiy Mendeleyev davriy sistemasining III – guruhiga mansub kimyoviy element. Tartib raqami – 13. Atom massasi – 26. 9815 Alyuminiy so'zi lotinchadan olinib "Achchiqtosh" degan ma'noni anglatadi

Birinchi bo'lib Hans Ersted 1825 – yilda metall holidagi alyuminiyni labaratoriyada ajratib olgan

Alyuminiy barcha barqaror birikmalarida III valentli , yuqori temperaturada ba'zan I , kamdan kam hollarda II valentli bo'lishi mumkin. Alyuminiy sirka , vino , limon kislotalari va boshqa organik moddalar ta'siriga turg'un. Alyuminiy kislorod bilan tez birikadi va zich oksid parda hosil qiladi va bu parda uni zanglashdan , turli moddalar ta'siridan saqlaydi. Alyuminiy kukuni shiddat bilan yonadi , yuqori temperaturada galogenlar bilan birikib , alyuminiy ftorid , xlorid , bromid , yodid , astatid , oltingugurt bilan sulfid , azot bilan nitrid , uglerod bilan karbid hosil qiladi.
Alyuminiy Nitrat Rangsiz , hidsiz, havoda tutovchi kristal Suvsiz holatdagisi kuchli gigroskopik xossaga ega Suvda , organik xususiyatli qutbli erituvchilarda yaxshi eriydi. Kuchli oksidlovchi modda

Alyuminiy nitrat tuzi odatdagi temperaturada Al(NO 3)3*9 H 2 O ko'rinishidagi rangsiz kristallogidrat hosil qiladi. 73, 5 0 C dan yuqori haroratda esa asta – sekinlik bilan suvini yo'qotib boradi , harorat deyarli 200 gradusga yetganda Al 2 O 3 ga qadar parchalanib ketadi. Al(NO 3)3*9 H 2 O haroratni oshirgan sari dastlab oktogidrat , so'ngra geksagidratga aylanadi.

Hozirgi kunda nitrat alyuminiyeng ko'p qo'llaniladigan soha – to'qimachilik sanoati sanaladi. Tarkibida alyuminiy nitrat mavjud bo'lgan aralashmalar yordamida matolarga ishlov berilganda , ularning qalinlik darajasi ortadi. Ushbu usul har qanday matoning xossalarini yaxshilash uchun eng qulay usul sanaladi

Kristen Vanessa Ruiz --- “Biz negadir alyuminiy nitrat tuzi haqida gapirganimizda , uning faqatgina to’qimachilik sanoati, qog’oz ishlab chiqarish , neftni qayta ishlash sohasidagi roligagina to’xtalib o’tamiz. Holbuki bu tuzning xossalari , imkoniyatlarining deyarli o’ttiz foiz darajasini ham o’rganganimizcha yo’q. Uni XXI – asrning hali ochilmagan kashfiyoti desak mubolag’a bo’lmaydi”

Alyuminiy nitratning olinishi Hozirgi kunda alyuminiy nitrat tuzini olishda bir necha usullar qo’llaniladi. Bunda reagent sifatida alyuminiy metali , nitrat kislataning suyultirilgan eritmasi , azot V oksidi , alyuminiy tuzlari , shuningdek nitrat kislata hosil qilgan tuzlar ishlatiladi.

Al(NO 3)3 ning labaratoriyada olinish usullari Labaratoriya sharoitida alyuminiy nitratni olish uchun alyuminiy nitrat kislota eritmasi bilan ta’sirlashtiriladi. Bunda nitrat kislotaning suyultirilgan eritmasidan foydalaniladi. Chunki konsentrlangan nitrat kislotada alyuminiy passivlashib qoladi.

Al(OH)3+3 HNO 3 Al(NO 3)3+3 H 2 O Ma’lumki alyuminiy tuzlari eritmasiga ishqor ta’sir ettirilganda Al(OH)3 - alyuminiy gidroksid cho’kmasi hosil bo’ladi. U p. H=4, 1 -6, 5 qiymatga ega bo’lgan kuchsiz kislotali muhitda cho’kadi. Biroq bu reaksiya kislotaning miqdori yetarli darajada bo’lgandagina oxirigacha boradi. Eritma da kislota miqdori kam bo’lganda Al(OH)2 NO 3 yoki Al. OH(NO 3)2 hosil bo’lib , Al(OH)3 cho’kmasi oxirigacha erimaydi.

Al(SO 4)3+3 Ba(NO 3)2 2 Al(NO 3)3+3 Ba. SO 4 Ushbu reaksiya kimyoviy reaksiya turlarining almashinish reaksiyasi xiliga xos bo’lib reaksiya natijasida oq rangli bariy sulfat cho’kmaga tushadi. Eritmada esa alyuminiy nitrat qoladi.

Alyuminiy nitratning sanoatda olinish usullari Sanoat miqyosida alyuminiy nitrat ishlab chiqarish uchun bir qator usullardan foydalaniladi. Bu usullar labaratoriya sharoitida olib boriladigan reaksiyalardan farqli ravishda , nisbatan tezroq boradi va tejamkorroq usullar sanaladi.

Alyuminiy (III) hamda azot (V) oksidlarining o’zaro ta’sirlashuvidan suvsiz alyuminiy nitrat tuzi olinadi • Al 2 O 3+3 N 2 O 5 2 Al(NO 3)3 Shunga o’xshash yana bir alternativ usullardan biri alyuminiy gidroksidiga azot (V) oksidining ta’sir ettirilishidir. • Al(OH)3+3 N 2 O 5 Al(NO 3)3+3 HNO 3

Hozirgi kunda alyuminiy nitrat tuzini ishlab chiqarishda bu ikki usul eng istiqbolli usullardan deb sanalib kelinmoqda. Yevropadagi , Xitoydagi bir qator alyuminiyli birikmalarni ishlab chiqaruvchi zavodlar ana shu reaksiyalardan foydalanadilar. Ikkala usul ham Al ionining amfoterlik xossasiga asoslangan bo'lib , alyuminiy nitrat olinishining eng kamchiqim ko'rinishi sanaladi.
![2 Al. Br 3+8 N 2 O 5 2 NO 2[Al(NO 3)4]+3 Br 2+6 2 Al. Br 3+8 N 2 O 5 2 NO 2[Al(NO 3)4]+3 Br 2+6](http://slidetodoc.com/presentation_image_h/3201ddcf78ffa829dab2c07b40042daa/image-21.jpg)
2 Al. Br 3+8 N 2 O 5 2 NO 2[Al(NO 3)4]+3 Br 2+6 NO 2 2 NO 2[Al(NO 3)4] 2 Al(NO 3)3+4 NO 2+O 2 Ushbu reaksiya ham so’nggi yillarda Al(NO 3)3 olishda ancha keng qo’llanilayotgan usullardan sanaladi. Reaksiya natijasida qo’shimcha mahsulot sifatida ajralib chiqadigan brom reaksiyaning dastlabki mahsuloti bo’lgan alyuminiy bromid olishda ishlatiladi
Rangsiz Qattiq Hidsiz Gigros. Fizik Xossala ri kopik Suvda eruvchan

Al(NO 3)3 • Alyuminiy hamda nitrat kislota qoldig’idan tashkil topgan noorganik birikma. • Suvda juda yaxshi eriydi. 25 C haroratda 100 g suvda 63, 7 miqdorda Al(NO 3)3 • Juda kuchli oksidlovchi xossaga ega bo’lib , alkil efirlar bilan hosil qilgan aralashmasi portlashni yuzaga keltirishi mumkin. • Monoklonnik kristall panjaraga ega. Al(NO 3)3 • 35 C temperaturada metanolda eruvchanligi 14, 45 g ni tashkil etadi. Etanolda esa xuddi shu haroratda 8, 63 g miqdorda erisa , etilenglikoldagi eruvchanligi 18, 32 g ni tashkil etadi. • Malekulasida markaziy atom azot bo’lib gibridlanishi sp 2
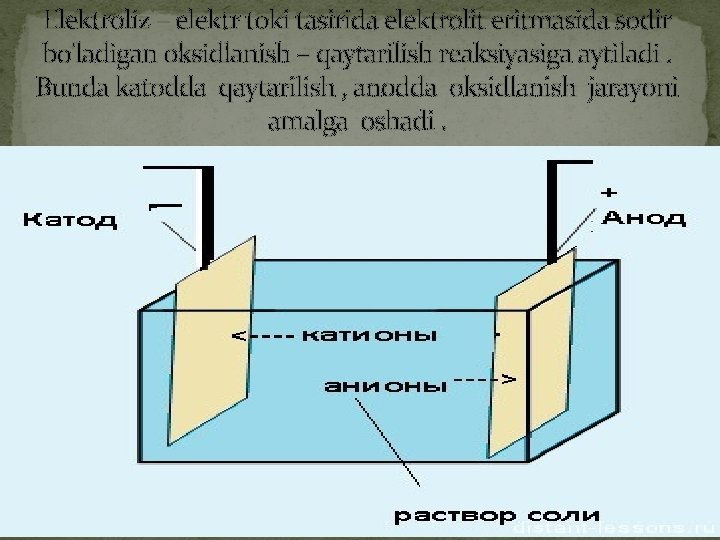
Elektroliz – elektr toki tasirida elektrolit eritmasida sodir bo'ladigan oksidlanish – qaytarilish reaksiyasiga aytiladi. Bunda katodda qaytarilish , anodda oksidlanish jarayoni amalga oshadi.

Alyuminiy nitrat elektrolizi Alyuminiy nitrat birikmasi tarkibidagi manfiy ion ya’ni kislota qoldig’i – NO 2 tarkibida kislorodning mavjudligi tufayli elektroliz vaqtida anodda OH ioni oksidlanib , gazsimon kislorod ajralib chiqadi. 4 OH 2 H 2 O+O 2 Buning sababi gidroksid ionlarining zaryadsizlanishidir. Gidroksid ionlari parchalangan sari suvning yangi malekulalari dissotdiyalanaveradi : natijada anod yaqinida vodorod ionlarining konsentratsiyasi ortib ketadi.

Alyuminiy nitrat elektrolizi Dastlab elektrolizning dissotsiyalanishini yozamiz Al(NO 3)3 Al 3++NO-3 Al(NO 3)3+2 H 2 O Al+H 2+3 HNO 3+O 2 Alyuminiyning elektrokimyoviy qatordagi aktivligi tajribada kuzatiladigan xususiyatidan kattaroq bo’ladi, chunki uning yuza qavatidagi oksid parda metallning aktivligidan kichik , agar shu parda bo’lmaganda edi , amalda bu metall aktivroq bo’lar edi. Bunday vaziyatda yuqoridagi elektroliz jarayonini quyidagicha davom ettirish mumkin 4 Al(NO 3)3 4 Al 3++12 NO-3

4 Al(NO 3)3+18 H 2 O 4 Al(OH)3+6 H 2+12 HNO 3+3 O 2 Bu hodisaning sababi oksid pardasi mavjud bo’lmagan o’ta toza alyuminiy eritmaning suvi bilan reaksiyaga kirishadi. Al+ H 2 O Al(OH)3+H 2

Alyuminiy nitrat quyidagi reaksiyalarga kirishadi.

Alyuminiy nitrat ishqor eritmalari bilan ta’sirlashadi. Reaksiya ishqorning miqdoriga qarab ikki xil ko’rinishda boradi. Al(NO 3)3+3 Na. OH Al(OH)3+3 Na. NO 3 Al(NO 3)3+4 Na. OH Na[Al(OH)4]+3 Na. NO 3 Ikkinchi reaksiyada alyuminiyli kompleks birikma hosil bo’lib u natriy tetragidroksoalyuminat deb ataladi. [Al(OH)4] – ioni faqatgina suvli eritmalarda mavjud bo’la oladi. 1)

2) Ammiakning konsentrlangan eritmasi bilan Al(NO 3)3 reaksiyaga kirishadi. Reaksiya ikki yo’nalishda boradi. Sariq suvda boradigan jarayon • Al(NO 3)3+3 NH 3+3 H 2 O Al(OH)3+3 NH 4 NO 3 Issiq suv tasirida esa quyidagicha boradi. • Al(NO 3)3+3 NH 3+3 H 2 O Al. O(OH)+3 NH 4 NO 3+H 2 O

3) Qizdirilganda parchalanib ketadi. 4 Al(NO 3)3 2 Al 2 O 3+12 NO 2+3 O 2 Bu jarayon temperatura deyarli 200 C ga qadar ko’tarilganda sodir bo’ladi.
- Slides: 31









































