bungen im Experimentalvortrag Sylvia Pross So Se 2007

Übungen im Experimentalvortrag Sylvia Pross So. Se 2007 Aluminium Silber aus Lehm? Abbildung: 1 + 2 http: //www. pacific-news. de/pn 11/rekult. html

Übersicht • • Vorkommen Eigenschaften Verwendung Geschichtliche Aspekte II Darstellung Ökologische Aspekte Schulrelevanz

Übersicht • • Vorkommen Eigenschaften Verwendung Geschichtliche Aspekte II Darstellung Ökologische Aspekte Schulrelevanz

1. Vorkommen • häufigstes Metall der Erdkruste • dritthäufigstes Element Sauerstoff Silicium Aluminium Eisen Calcium 45, 5 % 25, 7 % 8, 3 % 6, 2 % 4, 6 % • kein gediegenes Vorkommen

1. Vorkommen Sauerstoffverbindungen Verbindungen des Aluminiumtrihydroxid Al(OH)3 Hygrargillit, Bauxit Aluminiumoxidhydroxid Al. O(OH) Diaspor, Böhmit, Bauxit Dialuminiumtrioxid Al 2 O 3 Korund, Schmirgel Abbildung 3 -5

1. Vorkommen α-Aluminiumoxid („Tonerde“) Korund (Kanada, USA, Indien) • Schleif- und Poliermittel • hochfeuerfeste Keramik • Fasern • synthetische Edelsteine Schmirgel (Naxos, Kleinasien) Beimengungen von Eisenoxid und Quarz
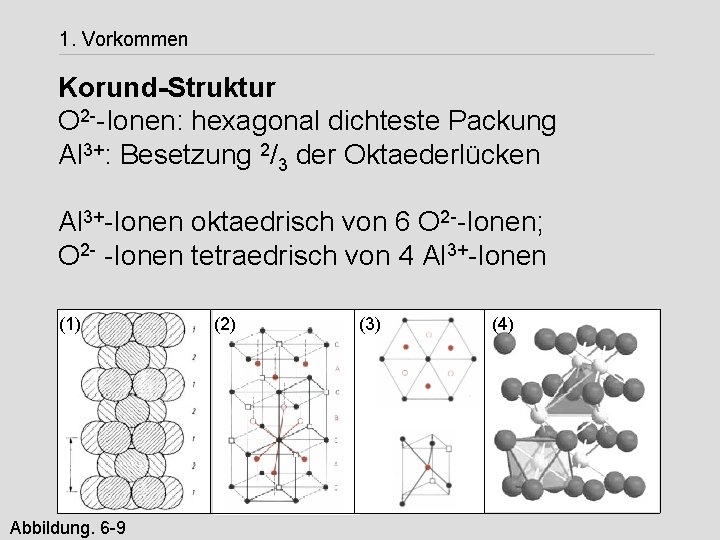
1. Vorkommen Korund-Struktur O 2 --Ionen: hexagonal dichteste Packung Al 3+: Besetzung 2/3 der Oktaederlücken Al 3+-Ionen oktaedrisch von 6 O 2 --Ionen; O 2 - -Ionen tetraedrisch von 4 Al 3+-Ionen (1) Abbildung. 6 -9 (2) (3) (4)

1. Vorkommen Edelsteine aus Aluminiumoxid und Spuren anderer Elemente Rubin Aluminiumoxid mit Spuren von Cr 3+ -Ionen Saphir Aluminiumoxid mit Spuren von Fe 3+ -Ionen & Ti 4+ -Ionen Abbildung. 10 -12
1. Vorkommen „Alumosilikate“ Feldspäte Verwitterung Tone Verwitterung Bauxite Abbildung. 13 -16 Glimmer

1. Vorkommen Bauxit 1821 Entdeckung durch Pierre Berthier bei Les Baux in der Provence Ausgangsmaterial der Aluminiumgewinnung rote Bauxite 20 -25 % Fe 2 O 3 und 1 -5 % Si. O 2, weiße Bauxite 5 % Fe 2 O 3 und 25 % Si. O 2 Abbildung. 17 -19
![1. Vorkommen Kryolith Na 3[Al. F 6] („Eisstein“) Vorkommen an der Südküste Grönlands ausgeschöpft 1. Vorkommen Kryolith Na 3[Al. F 6] („Eisstein“) Vorkommen an der Südküste Grönlands ausgeschöpft](http://slidetodoc.com/presentation_image_h2/bb3c71e5b8b673cd3d4737a53c2c86b8/image-11.jpg)
1. Vorkommen Kryolith Na 3[Al. F 6] („Eisstein“) Vorkommen an der Südküste Grönlands ausgeschöpft Technische Darstellung: Al(OH)3 (aq) + 6 HF (aq) + 3 Na. OH (aq) Na 3[Al. F 6] (s) + 6 H 2 O → Aluminiumherstellung Abbildung. 20

Übersicht • • Vorkommen Eigenschaften Verwendung Geschichtliche Aspekte II Darstellung Ökologische Aspekte Schulrelevanz
2. Eigenschaften • silberglänzendes Leichtmetall (Dichte: 2, 699 g/cm 3) • kubisch dichteste Packung • Smp. 660, 4 °C, Sdp. 2330 °C • hohe elektrische Leitfähigkeit • hohe Wärmeleitfähigkeit • hohe Dehnbarbeit • hohe Korrosionsbeständigkeit

2. Eigenschaften • Oxidschicht (Passivierung) • löslich in nicht oxidierenden Säuren Al (s) + 3 H+ (aq) Al 3+ (aq) + 11/2 H 2 (aq) • löslich in stark saurer oder alkalischer Lösung • starkes Reduktionsmittel

2. Eigenschaften Demo 1 Abflussreiniger
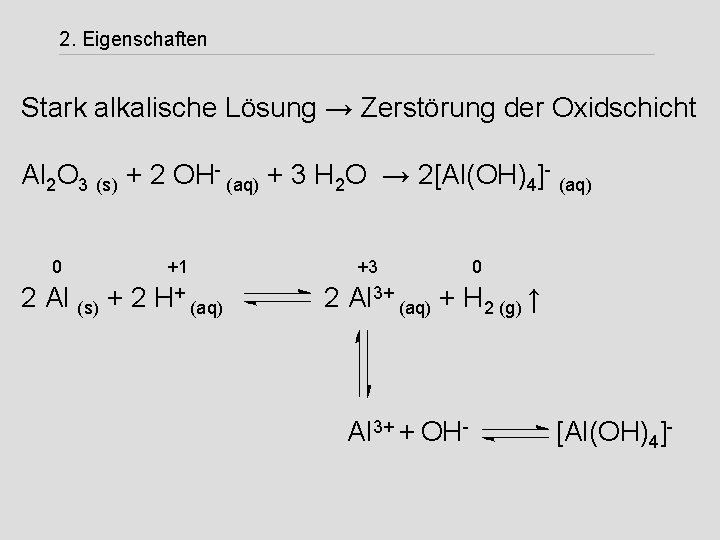
2. Eigenschaften Stark alkalische Lösung → Zerstörung der Oxidschicht Al 2 O 3 (s) + 2 OH- (aq) + 3 H 2 O → 2[Al(OH)4]- (aq) 0 2 Al (s) + 2 +1 H+ (aq) 2 +3 Al 3+ 0 (aq) + H 2 (g) ↑ Al 3+ + OH- [Al(OH)4]-

2. Eigenschaften Demo 2 Salzsäure

2. Eigenschaften Versuch 1 Reinigung von angelaufenem Silberbesteck
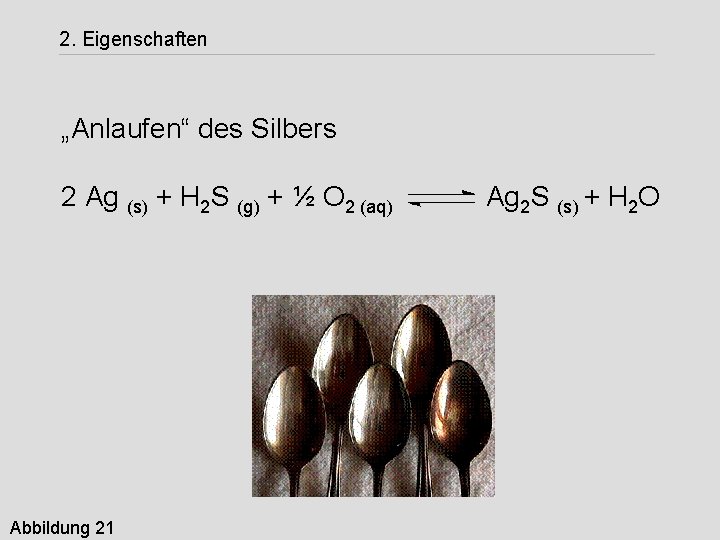
2. Eigenschaften „Anlaufen“ des Silbers 2 Ag (s) + H 2 S (g) + ½ O 2 (aq) Abbildung 21 Ag 2 S (s) + H 2 O

2. Eigenschaften Oxidation des Aluminiums Al → Al 3+(aq) + 3 e- (E°(Al/Al 3+) = -1, 66 V) Reduktion des Silbers 3 Ag+(s) + 3 e- → 3 Ag (s) (E°(Ag/Ag+) = 0, 79 V) Gesamtreaktion 2 Ag 2 S (s) + Al (s) + 4 H 2 O 4 Ag (s) + [Al(OH)4]- (aq) + 2 H 2 S (g)

Übersicht • • Vorkommen Eigenschaften Verwendung Geschichtliche Aspekte II Darstellung Ökologische Aspekte Schulrelevanz

3. Verwendung 25 % Baugewerbe 18 % Herstellung von Flugzeugen, Eisenbahnwaggons, Bussen, Autos, Fahrrädern 17 % Produktion von Containern und Verpackungsmaterial 14 % Leitungen Abbildung 22 -26

3. Verwendung Versuch 2 Aluminium-Nachweis (Morin)
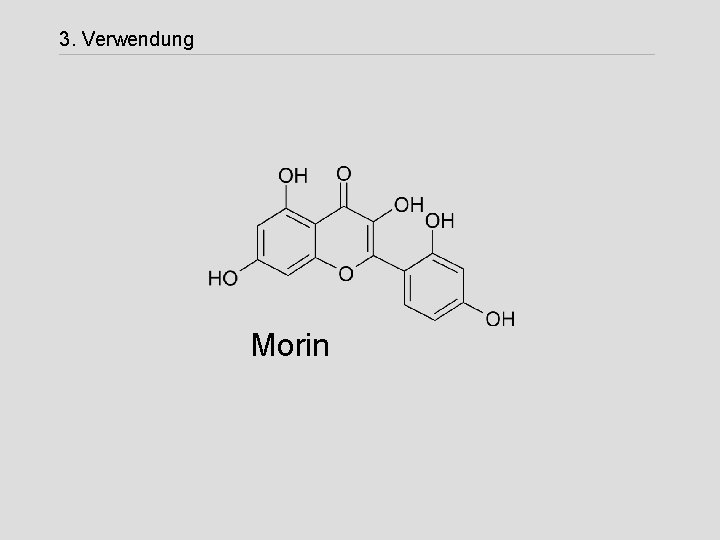
3. Verwendung Morin
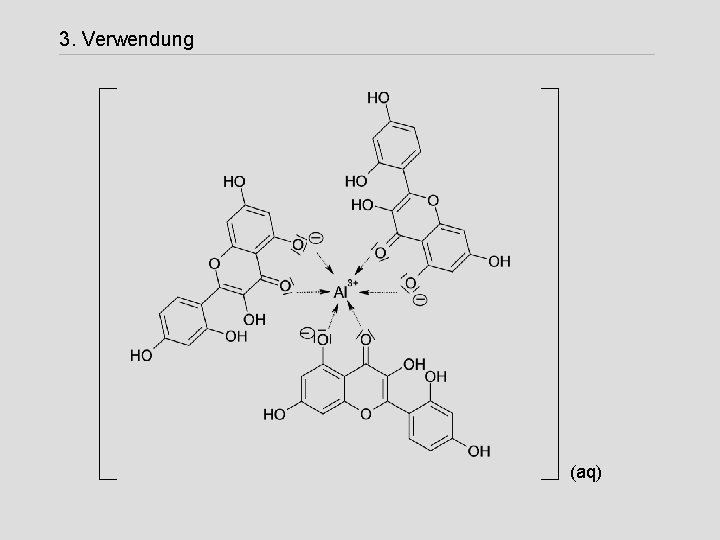
3. Verwendung (aq)
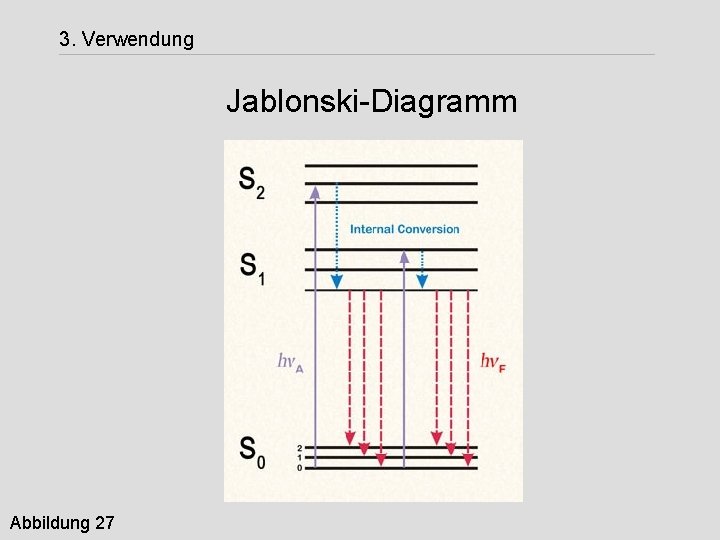
3. Verwendung Jablonski-Diagramm Abbildung 27

3. Verwendung Aluminothermie 1897 Entwicklung von Hans Goldschmidt Triebkraft: Sauerstoffaffinität des Aluminiums „Desoxidation“ des Eisens → Thermitschweißen Abbildung 28 -29 http: //www. goldschmidt-thermit. com/pictures/geschichte_document 3_co_th. jpg

3. Verwendung Reaktion: +2+3 0 3 Fe 3 O 4 (s) + 8 Al (s) +3 0 4 Al 2 O 3 (s) + 9 Fe (s) • Freisetzung von schwer reduzierbaren Metallen aus ihren Oxiden • keine Carbidbildung

3. Verwendung Versuch 3 Eloxalverfahren

3. Verwendung Eloxal-Verfahren Elektrolytische Oxidation des Aluminiums 1911 Entwicklung von de Saint Martin Verstärkung der Oxidschicht → Erhöhung des Korrosionsschutzes (beständig gegen Witterungseinflüsse, Seewasser, Säuren, Alkalilaugen) → Elektrische Isolierung Kondensatorplatten, -drähte
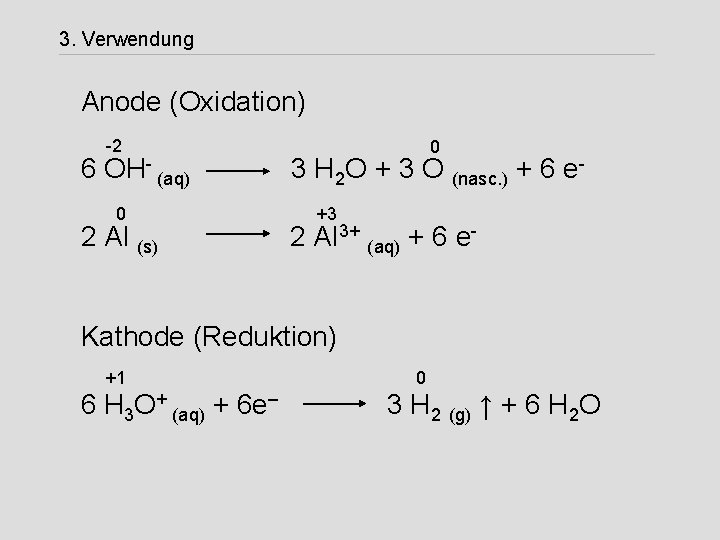
3. Verwendung Anode (Oxidation) -2 6 OH- (aq) 0 2 Al (s) 0 3 H 2 O + 3 O (nasc. ) + 6 e+3 2 Al 3+ (aq) + 6 e- Kathode (Reduktion) +1 6 H 3 O+ (aq) + 6 e– 0 3 H 2 (g) ↑ + 6 H 2 O

3. Verwendung Zwischenreaktion 2 Al (s) + 6 H 3 O+ (aq) 2 Al (s) + 3 O nasc. 2 Al 3+ (aq) + 3 H 2 (g) ↑ + 6 H 2 O Al 2 O 3 (s) Gesamtreaktion 2 Al (s) + 3 H 2 O Al 2 O 3 (s) + 3 H 2 (g) ↑

3. Verwendung Struktur leitet sich von γ-Al 2 O 3 ab: kubisch dichteste Packung Al 3+ -Ionen in oktaedrischen und tetraedrischen Lücken Oxidschicht ausschließlich oktaedrische Lücken besetzt

3. Verwendung Demo 3 Aluminium-Nachweis (Alizarin S)
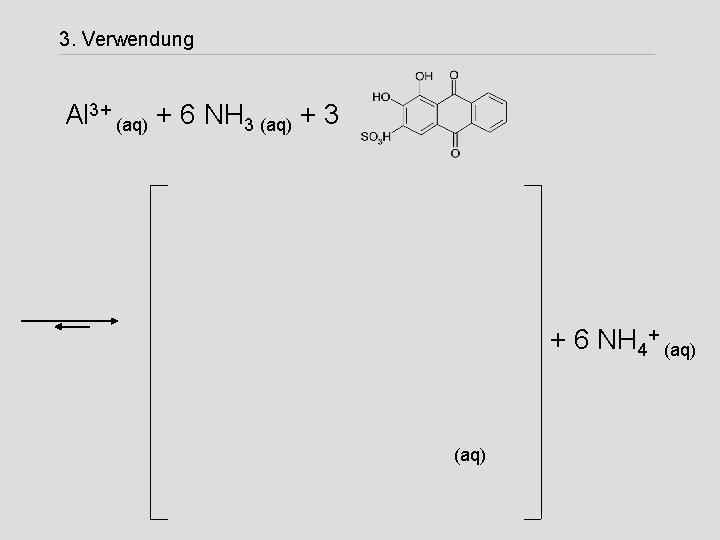
3. Verwendung Al 3+ (aq) + 6 NH 3 (aq) + 3 + 6 NH 4+ (aq)

3. Verwendung Versuch 4 Anfärben des Aluminiums
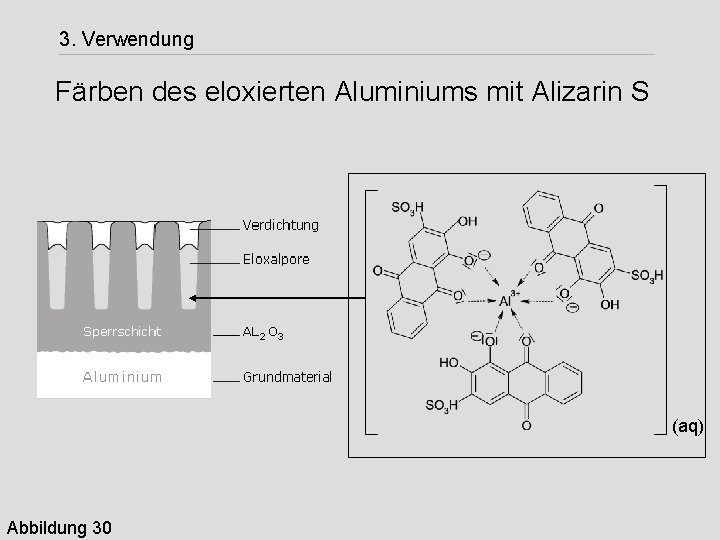
3. Verwendung Färben des eloxierten Aluminiums mit Alizarin S (aq) Abbildung 30

Übersicht • • Vorkommen Eigenschaften Verwendung Geschichtliche Aspekte II Darstellung Ökologische Aspekte Schulrelevanz

4. Geschichtliche Aspekte I 1897 Verwendung im Baugewerbe 1899 Sportwagen mit Alu-Karosserie 1900 Einzug in die Flugzeugindustrie 1916 erstes Aluminium- Flugzeug 1911 Alufolie als Schokoladenverpackung Abbildung 31 -32

Übersicht • • Vorkommen Eigenschaften Verwendung Geschichtliche Aspekte II Darstellung Ökologische Aspekte Schulrelevanz

5. Geschichtliche Aspekte II 1808 Namensgebung durch Sir Humphrey Davy 1821 Entdeckung von Bauxit durch Pierre Berthier 1825 erstmalige Isolierung von Aluminium durch Hans Christian Oersted 1827 Verbesserung des Verfahrens durch Friedrich Wöhler Abbildung 33 -34

5. Geschichtliche Aspekte II 1854 Entdeckung des ersten technisch erfolgreichen Herstellungs-Prozesses durch Henri Sainte-Claire Deville Al. Cl 3 (s) + 3 Na (s) ∆ Al (s) + 3 Na. Cl (s) 1855 Pariser Weltausstellung 1866 Erfindung des Dynamos durch Werner von Siemens http: //www. andreas-gym. de/agym 165/woehler. jpg

5. Geschichtliche Aspekte II 1886 Entwicklung eines Verfahrens zur großtechnischen Herstellung durch P. T. Herault und C. M. Hall 1887 Verbesserung des Verfahrens durch Karl Josef Bayer (Bayerverfahren) 1992 Patentanmeldung durch K. J. Bayer für den Aufschluss von Bauxit im Autoklaven Abbildung 35 -36

Übersicht • • Vorkommen Eigenschaften Verwendung Geschichtliche Aspekte II Darstellung Ökologische Aspekte Schulrelevanz

6. Darstellung Versuch 5 Amphoterie (Aluminiumhydroxid)
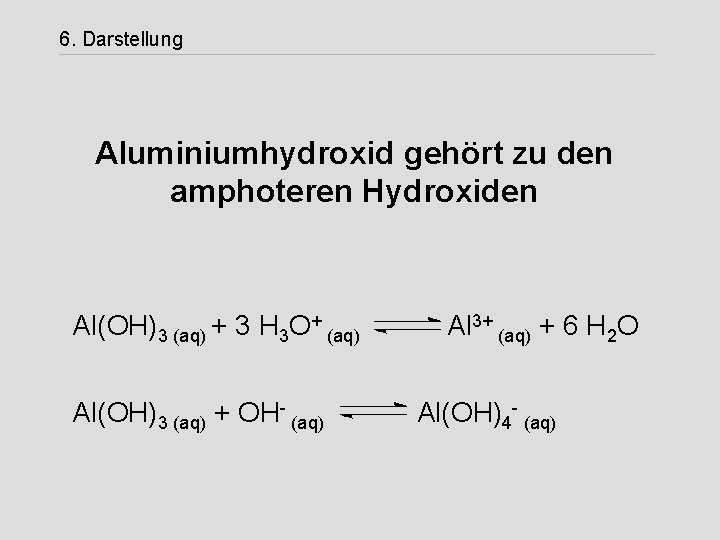
6. Darstellung Aluminiumhydroxid gehört zu den amphoteren Hydroxiden Al(OH)3 (aq) + 3 H 3 O+ (aq) Al(OH)3 (aq) + OH- (aq) Al 3+ (aq) + 6 H 2 O Al(OH)4 - (aq)
![6. Darstellung [Al(H 2 O)6]3+ (aq) + H 2 O [Al(H 2 O)6]3+ (aq) 6. Darstellung [Al(H 2 O)6]3+ (aq) + H 2 O [Al(H 2 O)6]3+ (aq)](http://slidetodoc.com/presentation_image_h2/bb3c71e5b8b673cd3d4737a53c2c86b8/image-47.jpg)
6. Darstellung [Al(H 2 O)6]3+ (aq) + H 2 O [Al(H 2 O)6]3+ (aq) + OH- (aq) Al(OH)3 (s) + OH- (aq) [Al. OH(H 2 O)5]2+ (aq) + H 3 O+ (aq) Al(OH)3 (s) ↓ [Al(OH)4]- (aq) Aluminiumsalze bei hohen und niedrigen p. H-Werten löslich
6. Darstellung Die Aluminiumgewinnung erfolgt in zwei Arbeitsgängen: 1. Gewinnung von reinem Aluminiumoxid (Al 2 O 3) aus Bauxit (Bayer-Verfahren) 2. Schmelzflusselektrolyse (Hall-Héroult-Prozess)
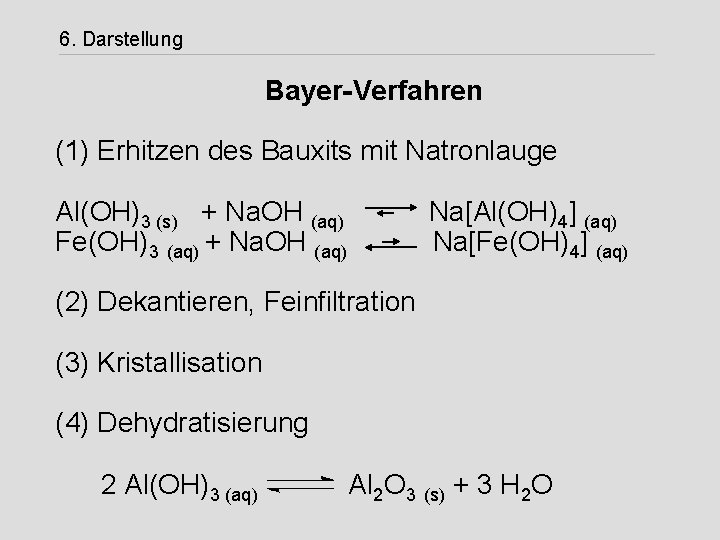
6. Darstellung Bayer-Verfahren (1) Erhitzen des Bauxits mit Natronlauge Al(OH)3 (s) + Na. OH (aq) Fe(OH)3 (aq) + Na. OH (aq) Na[Al(OH)4] (aq) Na[Fe(OH)4] (aq) (2) Dekantieren, Feinfiltration (3) Kristallisation (4) Dehydratisierung 2 Al(OH)3 (aq) Al 2 O 3 (s) + 3 H 2 O
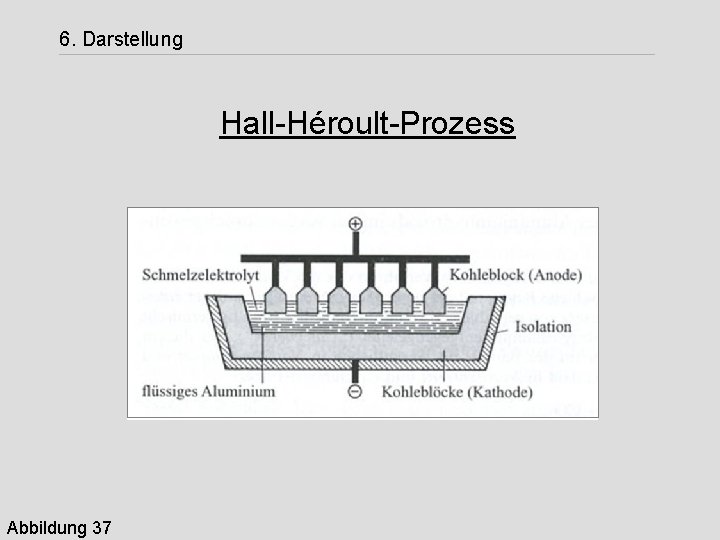
6. Darstellung Hall-Héroult-Prozess Abbildung 37

6. Darstellung Eutektisches Gemisch (Smp. 935 °C): 81, 5 % Na 3 Al. F 6 , 18, 5 % Al 2 O 3, Elektrodenvorgänge schematisiert: Schmelze: Al 2 O 3 2 Al 3+ + 3 O 2 Kathode: 2 Al 3+ + 6 e 2 Al Anode: 3 O 21½ O 2 + 6 e. Al 2 O 3 2 Al 1½ O 2

Übersicht • • Vorkommen Eigenschaften Verwendung Geschichtliche Aspekte II Darstellung Ökologische Aspekte Schulrelevanz

7. Ökologische Aspekte Abbildung 38 -44

Übersicht • • Vorkommen Eigenschaften Verwendung Geschichtliche Aspekte II Darstellung Ökologische Aspekte Schulrelevanz

8. Schulrelevanz 10 G: Fakultative Unterrichtsinhalte/ Aufgaben: • Großtechnische Elektrolysen Aluminiumgewinnung „vom Bauxit zum Aluminium“ ökologische Betrachtungen • Metalle als Werkstoffe in der Technik: Eisen, Aluminium, Kupfer • Wichtige Gebrauchsmetalle • Energie- und Ressourcenfragen • Recyclingverfahren

Aluminium Silber aus Lehm? Vielen Dank für die Aufmerksamkeit! http: //www. pacific-news. de/pn 11/rekult. html

Internet-Bildquellen: Abbildung 1: http: //www. geogr. uni-goettingen. de/kus/apsa/pn/pn 11/rekult. html Abbildung 2: http: //www. nord-sued-netz. de/index. php? option=com_docman&task=doc_download&gid=78 Abb. 4: http: //www. a-m. de/images/mineral/diaspor_gr. jpg Abb. 5: http: //tw. strahlen. org/fotoatlas/Korund 6. jpg Abb. 6 + 7 + 8: http: //www. chemie. uni-hamburg. de/ac/AKs/Prosenc/v 6. pdf Abb. 9: http: //www. fkf. mpg. de/jansen/p 430/weinmann/Chemie%20 der%20 Uebergangselemente%202006_06_19. pdf Abb. 10: http: //www. edelstein-essenzen. de/images/rubin. jpg, Abb. 11: http: //de. wikipedia. org/wiki/Saphir Abb. 12: http: //www. skielka-designschmuck. de/lexikon/saphir/index. php 3 Abb. 13 + 14: http: //www. gimizu. de/kabinett/klasse_8 g. html Abb. 15: http: //de. wikipedia. org/wiki/Kaolinit Abb. 16: http: //cc. uni-paderborn. de/lehrveranstaltungen/_aac/mineralien/grafik/bauxit. jpg Abb. 17 + 18: http: //www. geogr. uni-goettingen. de/kus/apsa/pn/pn 11/rekult. html Abb. 19: http: //www. szabozalan. hu/landscapes/gant_bauxit_mine. jpg Abb. 20: http: //umdb. um. u-tokyo. ac. jp/DKoubutu/FMPro? -db=jmiya_. fp 5&key=35&-img Abb. 21: http: //www. buetzer. info/fileadmin/pb/HTML-Files/Web. Help/Die_Adsorption_von_Gasen_und_gel_sten_Stoffen. htm Abb. 22: http: //www. heinzebauoffice. de/hbo/typ. ID_53/ob. ID_76510/kustnr_1560/module_2000/module. Page. ID_1/context_1/rehaupolytec-50. html Abb. 23: http: //www. uni-bayreuth. de/departments/ddchemie/umat/aluminium. htm Abb. 24: http: //www 1. messe-berlin. de/vip 8_1/website/Messe. Berlin/htdocs/www. innotrans. de/de/Presse/Neuheiten/index. jsp Abb. 25: http: //www. nord-sued-netz. de/index. php? option=com_docman&task=doc_download&gid=78 Abb. 26: http: //www. jbergsmann. at/DSCF 0038 -alu-schneiden-300 x 300_27 u. jpg Abb. 27: http: //icecube. berkeley. edu/~bramall/work/astrobiology/images/Jablonski-Diagram. jpg Abb. 28: http: //www. goldschmidt-thermit. com/pictures/geschichte_document 3_co_th. jpg Abb. 29: http: //www. uni-bayreuth. de/departments/ddchemie/umat/eisen/images/schiene. jpg Abb. 30: http: //www. alutecta. de/alutecta_home/0_p/alugrafikeloverd. gif

Internet-Bildquellen: Abb. 31: http: //www. konstruktionspraxis. de/sh/fachartikel/kp_sh_fachartikel_1964409. html Abb. 32: http: //www. earlyaviator. com/archive/JPL/1900. 07. 02_LZ 1_3_jpl. jpg Abb. 33: http: //www. andreas-gym. de/agym 165/woehler. jpg Abb. 34: http: //www. cozmo. dk/bio/oersted/orstptr. jpg Abb. 35 + 36: http: //www. mschaumann. de/history/Die%20 Geschichte%20 des%20 Aluminiums. htm Abb. 37: Lehrbuch der allgemeinen und anorganischen Chemie, A. Fr. Holleman; E. Wiberg, De Gruyter, 1955, 101. Auflage, New York Abb. 38 -43: http: //www. geogr. uni-goettingen. de/kus/apsa/pn/pn 11/rekult. html http: //www. nord-sued-netz. de/index. php? option=com_docman&task=doc_download&gid=78 http: //www. bgr. bund. de/DE/Themen/Min__rohstoffe/Bilder/Mir__ALCOA-Huntley__Bauxite__Mine__g, property=default. jpg http: //upload. wikimedia. org/wikipedia/commons/thumb/b/bf/Alloy_diagram_separate_crystal_building. png/400 px-Alloy_diagram_separate_crystal_building. png
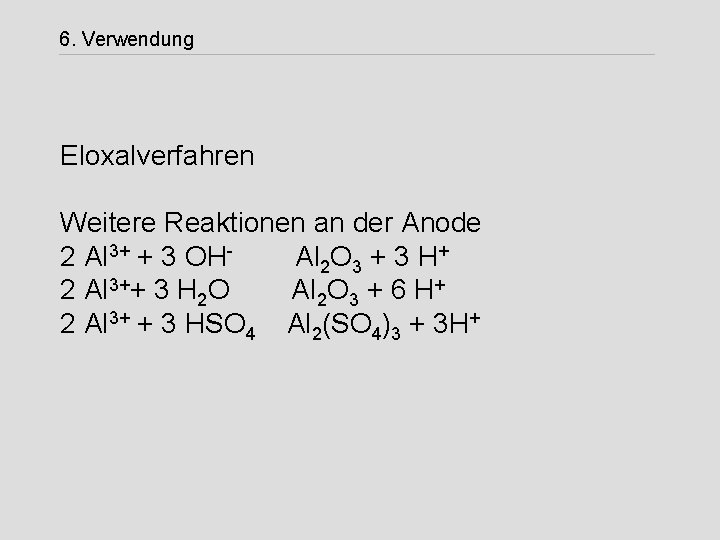
6. Verwendung Eloxalverfahren Weitere Reaktionen an der Anode 2 Al 3+ + 3 OHAl 2 O 3 + 3 H+ 2 Al 3++ 3 H 2 O Al 2 O 3 + 6 H+ 2 Al 3+ + 3 HSO 4 Al 2(SO 4)3 + 3 H+
- Slides: 59