Buka a bunn interakce v patogeneze tkovho pokozen

Buňka a buněčné interakce v patogeneze tkáňového poškození. Regulace proliferace a zániku buněk. Přednáška z patologické fyziologie 4. 10. 2004
Buňka - základní funkční jednotka - funkce: závisí na diferenciaci (proliferace, produkce látek) Diferenciace - Tkáň - specializovaná produkce látek konkrétní metabolické funkce Diferencovaná proliferační aktivita Kooperace + regulace Organismus - udržení integrity a funkce, reprodukce

Patofyziologie nemocí analyzovaná na buněčné úrovni a) Buňka reaguje na patologický stav v rámci svých funkčních a adaptačních mechanizmů (např. změna exprese receptorů, produkce cytokinů…) b) Buňka je patologickým procesem poškozena (rozvoj reakcí, které poškození buď opraví nebo kompenzují či vedou k zániku buňky) c) Primární poškození buňky (změna genomu nebo exprese – důsledek dědičných nebo získaných mutací – samotná buňka je příčinou patologického stavu)
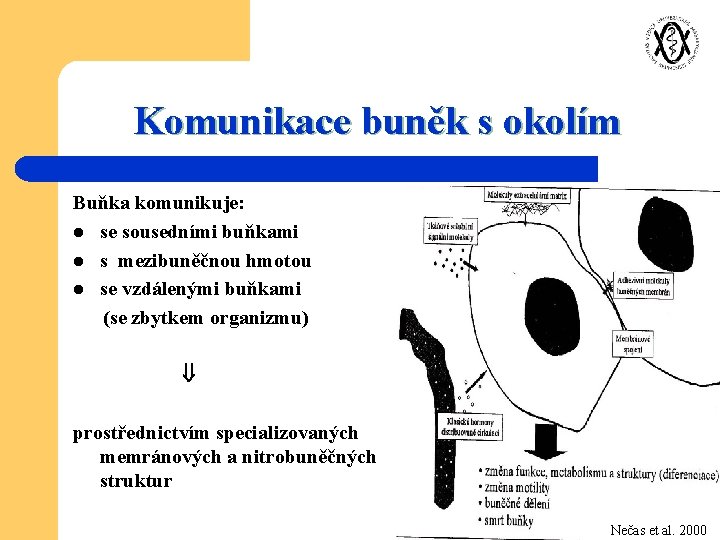
Komunikace buněk s okolím Buňka komunikuje: l se sousedními buňkami l s mezibuněčnou hmotou l se vzdálenými buňkami (se zbytkem organizmu) prostřednictvím specializovaných memránových a nitrobuněčných struktur Nečas et al. 2000
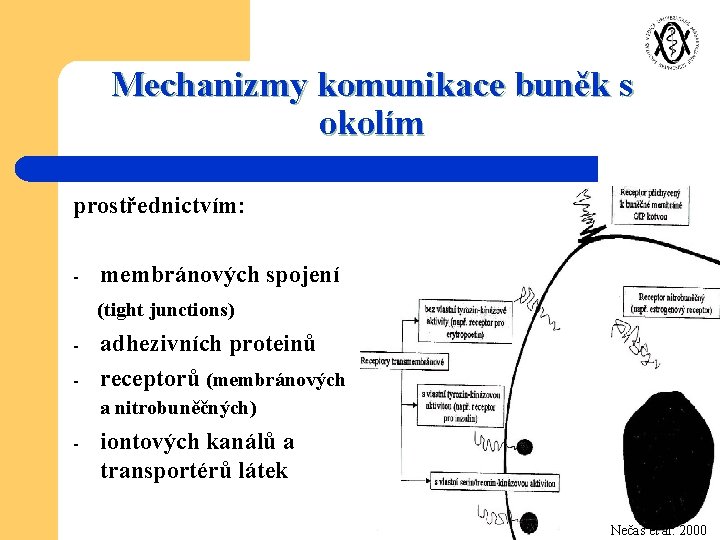
Mechanizmy komunikace buněk s okolím prostřednictvím: - membránových spojení (tight junctions) - adhezivních proteinů receptorů (membránových a nitrobuněčných) - iontových kanálů a transportérů látek Nečas et al. 2000

Transport iontů a nízkomolekulárních látek přes membránu Pasívní: l l l Difúze Facilitovaná (usnadněná) difúze sekundárně aktivní transport formou symportu nebo antiportu Iontové kanály Aktivní: l Pumpy (energie z ATP)

Prostá difúze - nízkomolekulární látky bez náboje vyjímečně - O 2, CO 2, NO voda (osmotické síly) močovina etanol - l l nevyžaduje energii rozhodující je koncentrační gradient
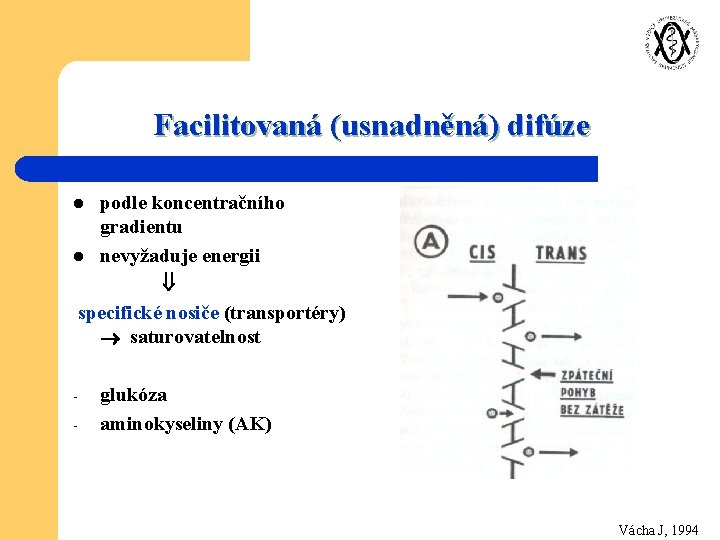
Facilitovaná (usnadněná) difúze podle koncentračního gradientu l nevyžaduje energii specifické nosiče (transportéry) saturovatelnost l - glukóza aminokyseliny (AK) Vácha J, 1994

Symport, antiport l l - přenos látek přes membránu proti jejich chemickému gradientu energii dodává gradient Na+ (přesun Na+ iontů po směru jejich elektrochemického gradientu) přenášejí vždy současně Na+ iont dovnitř buňky a jinou molekulu buď – také dovnitř = symport (např. transport glukózy a AK ze střevního lumen do enterocytu) nebo ven = antiport (vylučování Ca 2+ iontů buňkami srdečního svalu)

Příklad antiportu Cl-/HCO 3 - Antiport Cl-/HCO 3 erytrocytů – tzv. „bílkovina proužku 3“ -funkce v transportu CO 2 z tkání do plic Vácha J, 1994

Iontové kanály buněčná mebrána je prakticky neprostupná pro ionty (hydrofobní fosfolipidy) l jde o speciální póry tvořené transmembránovými glykoproteiny s centrální dutinou vyplněnou vodou l tok podle elektrochemického gradientu l mohou měnit konformaci (tím i propustnost) –vrátkování („gating“) na principu: - elektrického potenciálu – u tzv. napětově řízených kanálů - navázání specifického ligandu - mechanických sil - změn intracelulárních koncentrací Ca 2+ a H+ iontu – u „gap junctions“ l přítomnost podmiňuje existenci normálního membránového potenciálu l
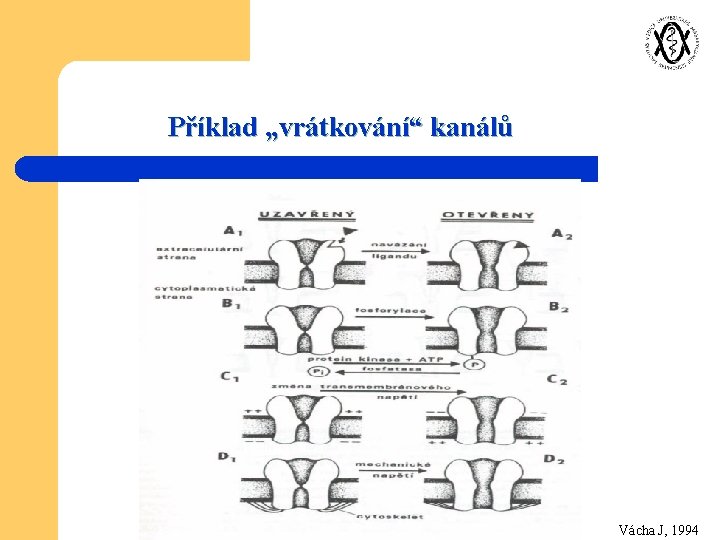
Příklad „vrátkování“ kanálů Vácha J, 1994
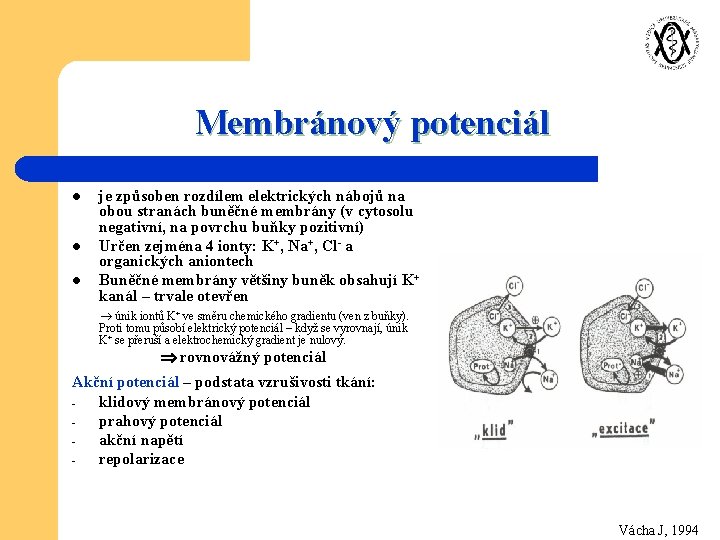
Membránový potenciál l je způsoben rozdílem elektrických nábojů na obou stranách buněčné membrány (v cytosolu negativní, na povrchu buňky pozitivní) Určen zejména 4 ionty: K+, Na+, Cl- a organických aniontech Buněčné membrány většiny buněk obsahují K+ kanál – trvale otevřen únik iontů K+ ve směru chemického gradientu (ven z buňky). Proti tomu působí elektrický potenciál – když se vyrovnají, únik K+ se přeruší a elektrochemický gradient je nulový. rovnovážný potenciál Akční potenciál – podstata vzrušivosti tkání: klidový membránový potenciál prahový potenciál akční napětí repolarizace Vácha J, 1994

Poruchy funkce iontových kanálů l Ovlivnění – léky (farmakologie) - vrozené poruchy (mutace) např. cystická fibróza – mutace genu protein CFTR (Cl- kanál) nedostatečná sekrece Cl- epitel. bb. do sekretů, které jsou viskózní ( vs. sekrece Cl- potními žlázami) Poruchy kanálů nervových a svalových buněk záchvatovitě (ztuhnutí svalů x dočasná slabost, křeče apod. ) - získané poruchy (autoprotilátky) např. myastenia gravis – Pt proti acetylcholinovému receptoru
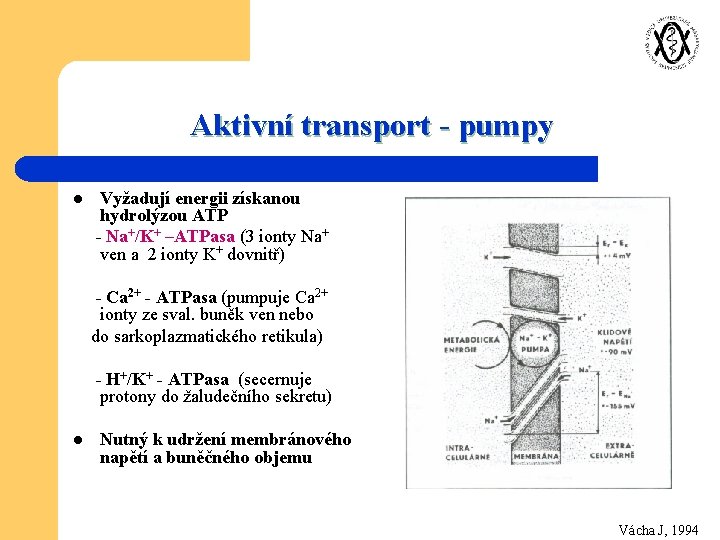
Aktivní transport - pumpy l Vyžadují energii získanou hydrolýzou ATP - Na+/K+ –ATPasa (3 ionty Na+ ven a 2 ionty K+ dovnitř) - Ca 2+ - ATPasa (pumpuje Ca 2+ ionty ze sval. buněk ven nebo do sarkoplazmatického retikula) - H+/K+ - ATPasa (secernuje protony do žaludečního sekretu) l Nutný k udržení membránového napětí a buněčného objemu Vácha J, 1994

Aktivní přenos specifickými transportéry Např. MDR (z Multi Drug Resistance) membránový protein = MDR-ATPasa (glykoprotein P) - plní funkci relat. neselektivní pumpy, kterou se buňka může zbavovat některých hydrofobních cizorodých nízkomolekul. látek - normálně přítomna v buněčných membránách jaterních, střevních, ledvinných buněk a bb. kostní dřeně - opakovaným podáním cizorodé látky – zvýší se exprese či začnou exprimovat i bb. , které ji primárně nemají zvýší se odolnost k dané látce (např. rezistence na cytostatika) l
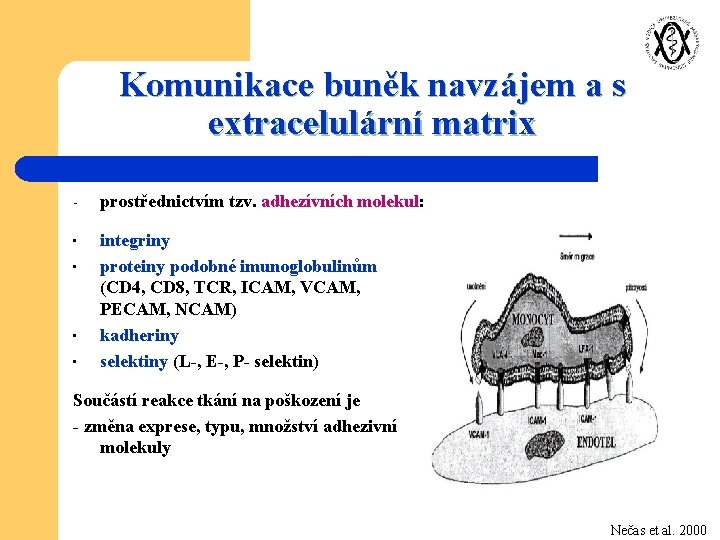
Komunikace buněk navzájem a s extracelulární matrix - prostřednictvím tzv. adhezívních molekul: • integriny proteiny podobné imunoglobulinům (CD 4, CD 8, TCR, ICAM, VCAM, PECAM, NCAM) kadheriny selektiny (L-, E-, P- selektin) • • • Součástí reakce tkání na poškození je - změna exprese, typu, množství adhezivní molekuly Nečas et al. 2000

Patologické stavy, u nichž se uplatňují adhezívní proteiny Významnou úlohu mají adhezívní proteiny v: l imunitních dějích a zánětu l při sepsi l při hojení ran l vaskularizaci tkáně l progresi nádorového růstu a tvorbě metastáz - též při ateroskleróze, trombóze, ischemickém poškození tkáně…
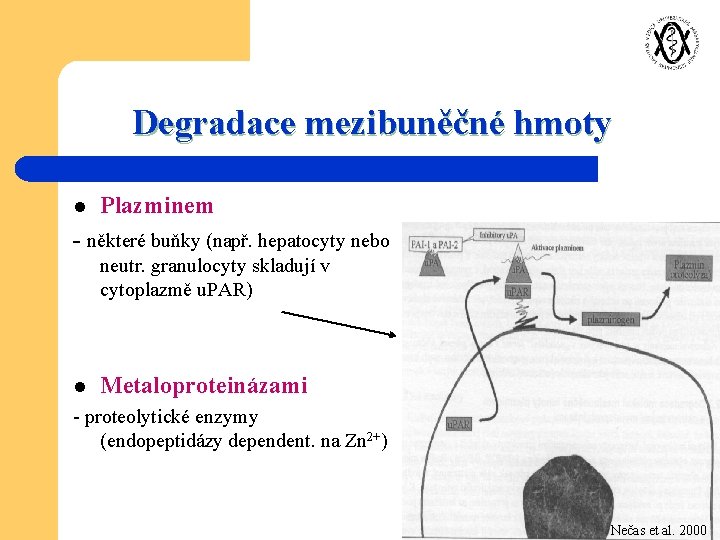
Degradace mezibuněčné hmoty l Plazminem - některé buňky (např. hepatocyty nebo neutr. granulocyty skladují v cytoplazmě u. PAR) l Metaloproteinázami - proteolytické enzymy (endopeptidázy dependent. na Zn 2+) Nečas et al. 2000

Receptorové struktury buňky a nitrobuněčné mechanizmy přenosu signálu MEMBRÁNOVÉ l Bílkoviny l Aminokyseliny TYP ODPOVĚDI: - otevření iontového kanálu - aktivace G proteinu - enzymatická aktivita akutní účinky NITROBUNĚČNÉ l steroidy l hormony štítné žlázy l retinoidy TYP ODPOVĚDI: - transkripce genu pozdní účinky

Poškození buňky a smrt buňky Příčiny poškození: l l l fyzikální chemické biologické nadměrná či nedostatečná stimulace nedostatek energie Buňky mohou být poškozeny: l l reverzibilně – řada reparačních mechanizmů ireverzibilně
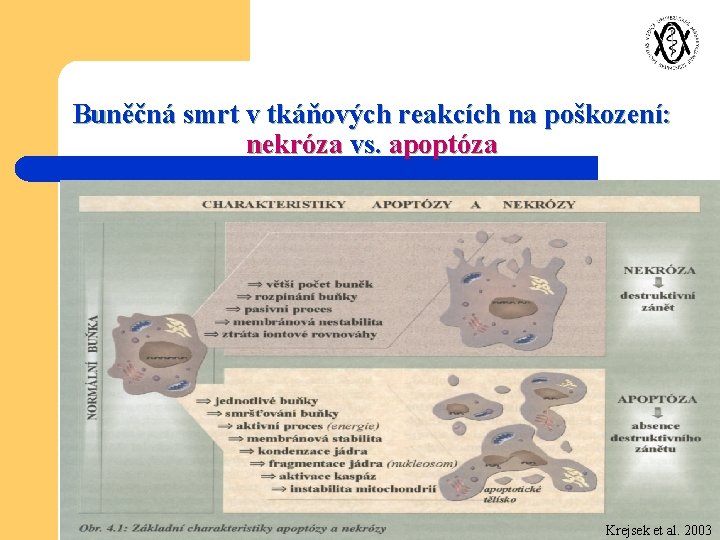
Buněčná smrt v tkáňových reakcích na poškození: nekróza vs. apoptóza Krejsek et al. 2003
Krejsek et al. 2003

Apoptóza = „programovaná buněčná smrt“ (apoptosis – z řečt. opadávání) konkrétní forma geneticky řízené buněčné smrti přísně střežený mechanizmus principem je proteolytická degradace buněčných struktur průběh je závislý na energii a udržení kontinuity cytoplazmatické membrány Nečas et al. 2000
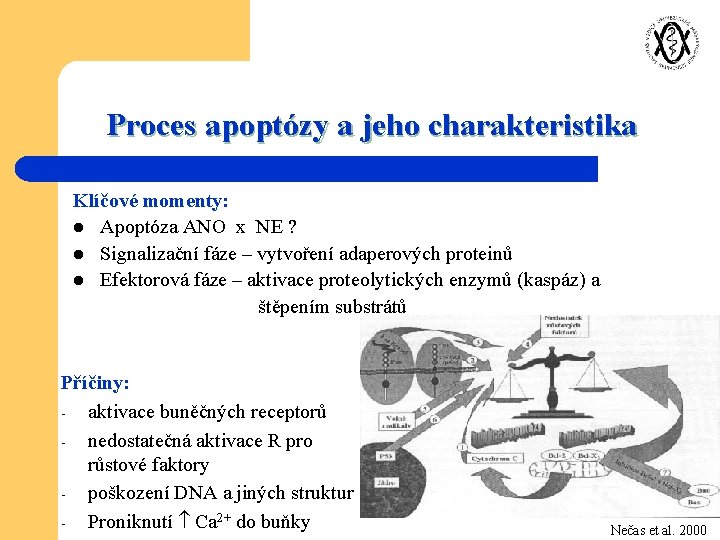
Proces apoptózy a jeho charakteristika Klíčové momenty: l Apoptóza ANO x NE ? l Signalizační fáze – vytvoření adaperových proteinů l Efektorová fáze – aktivace proteolytických enzymů (kaspáz) a štěpením substrátů Příčiny: - aktivace buněčných receptorů - nedostatečná aktivace R pro růstové faktory - poškození DNA a jiných struktur - Proniknutí Ca 2+ do buňky Nečas et al. 2000
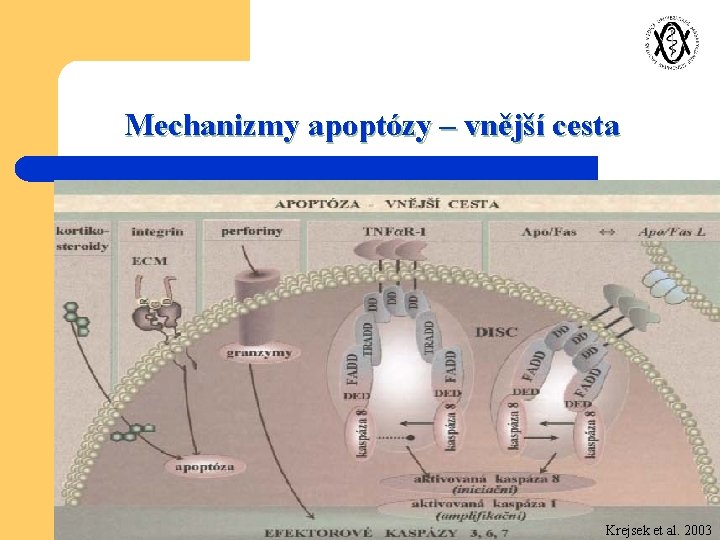
Mechanizmy apoptózy – vnější cesta Krejsek et al. 2003
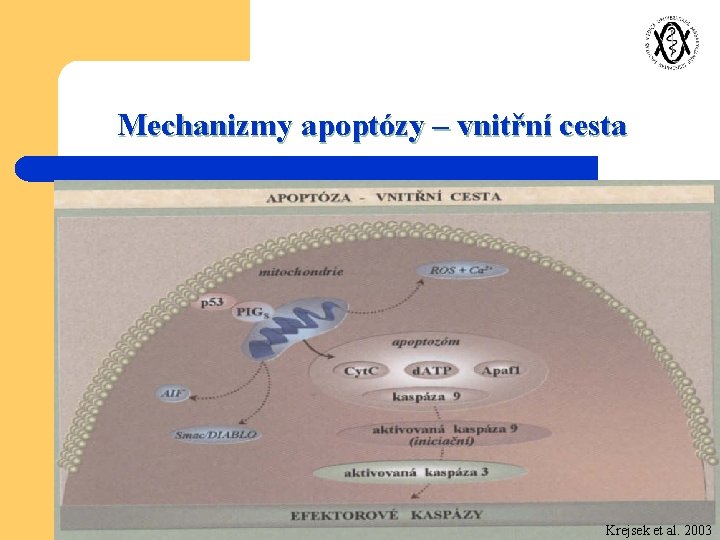
Mechanizmy apoptózy – vnitřní cesta Krejsek et al. 2003
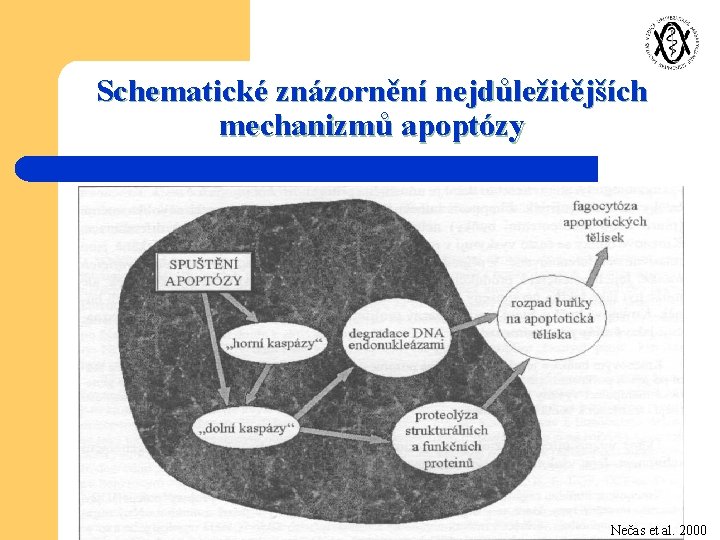
Schematické znázornění nejdůležitějších mechanizmů apoptózy Nečas et al. 2000

Vzájemné působení pro- a antiapoptotických buněčných mechanizmů Nečas et al. 2000

Náhrada zaniklých buněk l l Hypertrofie – stav, kdy se zvětší objem buněk, tedy i objem tkáně, aniž by se zvýšil počet buněk Hyperplazie – stav, kdy se zvýší počet buněk v dané tkáni a tím i její objem Regenerace – stav, kdy se doplní chybějící nebo poškozené části tkáně, přičemž se tkáň obnoví strukturně i funkčně Reparace – doplnění chybějící nebo poškozené tkáně, kdy se její struktura i funkce změní oproti stavu před poškozením

Schopnost buněk „dělit se“ l Při náhradě buněk má základní roli schopnost buněk k proliferaci (tj. k buněčnému dělení) stimulačními signály – růstové faktory: EGF, TGF, PDGF, VEGF, NGF…. . „buněčné stárnutí“

Regenerace (obnova) tkání se stálou proliferační aktivitou l l l - Epidermis, slizniční epitely Krvetvorná tkáň Spermatogonie příklad cyklicky probíhající stále obnovy díky přítomnosti „kmenových buněk“ - mají schopnost buněčné proliferace - i schopnost několikasměrné (pluri- nebo multipotentní buňky) nebo jednosměrné (unipotentní buňky) diferenciace

Regenerace (obnova) tkání s nízkou proliferační aktivitou Omezená (chybějící) schopnost regenerace l Neurony l Příčně pruhovaný sval l Játra – nízká klidová proliferační aktivita, ale vysoká schopnost regenerace diferencovaný hepatocyt se během jaterní regenerace stává „kmenovou buňkou“

Základní patofyziologické otázky l Jak? l Proč? ? ? l Přednášky můžete najít na adrese: http: //www. med. muni. cz/patfyzc. html Výuka Prof. MUDr. Anna Vašků Doc. MUDr. Lydie Izakovičová Hollá
- Slides: 34