Bra zdemir Dalton atom modeli Bohr atom modeli

Büşra Özdemir
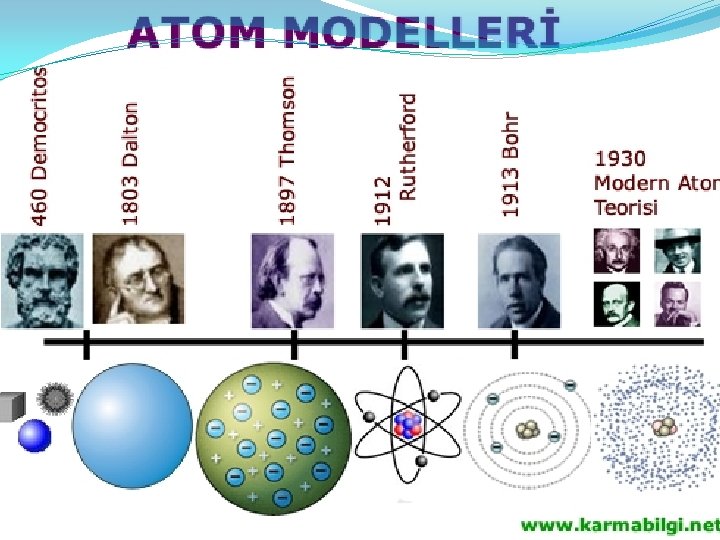

Dalton atom modeli Bohr atom modeli Thomson atom modeli Rutherford atom modeli model Modern atom modeli

Dalton atom modeli Daltona göre; Madde, atom denilen içleri dolu bölünemeyen taneciklerden oluşmuştur. Aynı elementin atomları büyüklük yönünden birbirinin aynı, farklı elementlerin atomları tamamen birbirinden farklıdır. Tepkimelerde atomlar korunur. Atomların birleşmeleri sonunda moleküller oluşur.
Rutherford atom modeli Atomların ışıma spektrumlardaki frekansların elektronların dairesel hareket frekanslarının katları olması beklenir. Atomların ışıma spektrumlarını açıklayamaz.

Bohr atom modeli, elektronların çekirdekten herhangi bir uzaklıkta bulunan tek bir yörüngede değil, belirli yörüngede olduğunu belirtir. Bir elektronun bulunduğu yer elektronun sahip olduğu enerjiye bağlıdır. Bu enerji düzeyleri çekirdeğe yakın olandan uzağa doğru 1, 2, 3. . gibi numaralar verilerek gösterilir. Enerji düzeylerinin enerjisi çekirdeğe yaklaştıkça azalır, uzaklaştıkça artar.

Modern atom modeli Atomlarda, temel enerji düzeyleri bulunmaktadır. Her enerji düzeyinde n kadar alt enerji seviyesi bulunur. Alt enerji seviyeleri s, p, d, f alt tabakalarıdır. Elektronların bulunma olasılığı en fazla olan alt enerji düzeylerine orbital denir. Orbitallerin bulunduğu alt enerji tabakasının adını alır. Bir orbitalde en fazla iki elektron bulunabilir ve bir atomda s, p, d ve f olmak üzere dört çeşit orbital vardır.

Thomson atom modeli Atom artı yüklü maddeden oluşmuştur. Elektronlar bu artı madde içinde gömülüdür ve hareket etmezler. Elektronların kütleleri çok küçüktür bu yüzden atomun tüm kütlesini bu artı yüklü madde oluşturur. Atom küre şeklindedir.
Peki atom nedir?
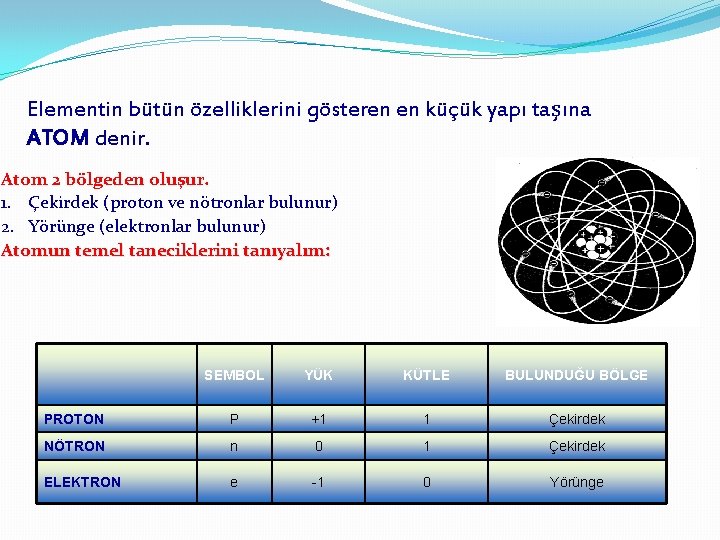
Elementin bütün özelliklerini gösteren en küçük yapı taşına ATOM denir. Atom 2 bölgeden oluşur. 1. Çekirdek (proton ve nötronlar bulunur) 2. Yörünge (elektronlar bulunur) Atomun temel taneciklerini tanıyalım: SEMBOL YÜK KÜTLE BULUNDUĞU BÖLGE PROTON P +1 1 Çekirdek NÖTRON n 0 1 Çekirdek ELEKTRON e -1 0 Yörünge
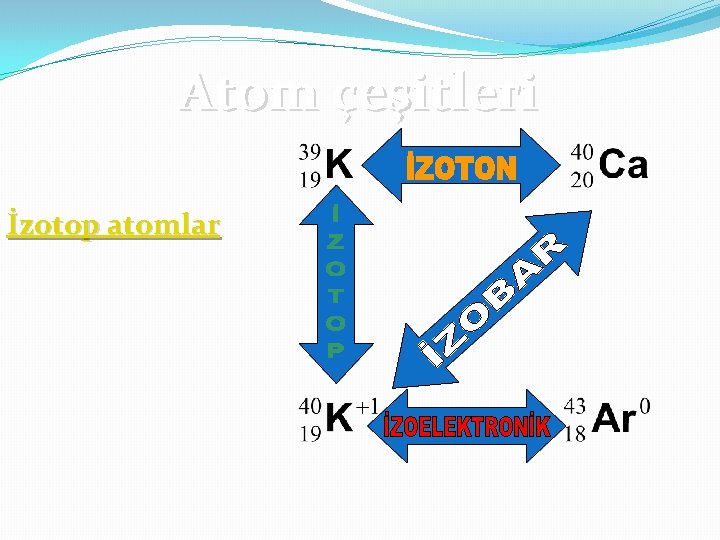
Atom çeşitleri İzotop atomlar

Atom numaraları aynı, kütle numaraları farklı olan atomlara denir. AYNI OLAN ÖZELLİKLER üAtom numaraları aynıdır. üNötr hallerinin kimyasal FARKLI OLAN ÖZELLİKLER üKütle numaraları ve nötron sayıları farklıdır. özellikleri aynıdır. üFiziksel özellikleri farklıdır. üPeriyodik cetveldeki yerleri üDoğada bulunma yüzdeleri aynıdır. (miktarları) farklıdır. üAynı element ile üGaz olanlarda yayılma oluşturdukları bileşiklerin hızları farklıdır. kimyasal formülleri aynıdır. üRadyoaktif olanlarda yarı üOrtalama atom ağırlıkları ömürler farklıdır. aynıdır. üAynı element ile oluşturdukları bileşiklerin mol kütleleri farklıdır.

Nötron sayıları aynı olan farklı element atomlarıdır. Kütle numaraları aynı olan farklı element atomlarıdır.

Elektron sayıları aynı olan taneciklerdir.
- Slides: 14