Bouwstenen van atomen massa u lading plaats Aantal
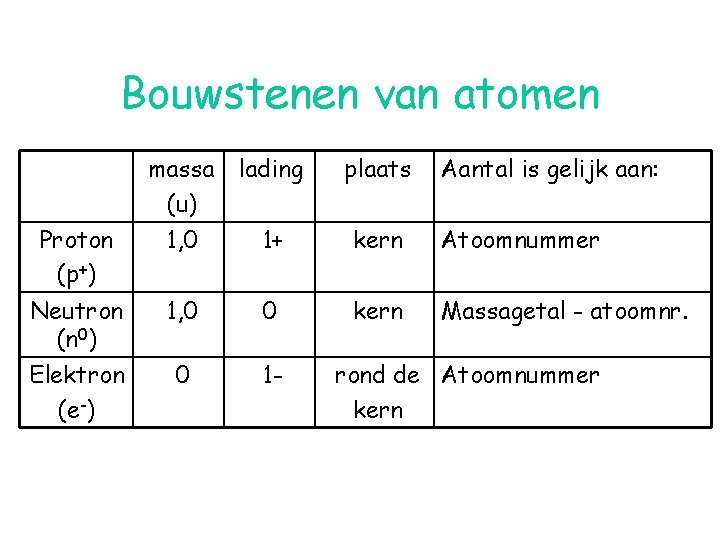
Bouwstenen van atomen massa (u) lading plaats Aantal is gelijk aan: Proton (p+) 1, 0 1+ kern Atoomnummer Neutron (n 0) 1, 0 0 kern Massagetal - atoomnr. Elektron (e-) 0 1 - rond de Atoomnummer kern

• Atoomnummer Aantal protonen in de kern • Massagetal Aantal protonen + aantal neutronen
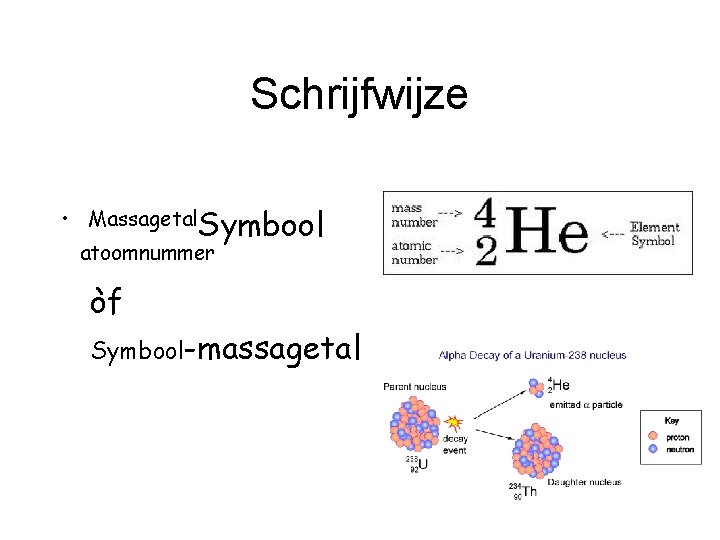
Schrijfwijze • Massagetal. Symbool atoomnummer òf Symbool-massagetal

• • Hoofdgroep 1: de alkalimetalen Hoofdgroep 2: de aardalkalimetalen Hoofdgroep (1)7: de halogenen Hoofdgroep (1)8: de edelgassen

Moleculaire stoffen • Bestaan alleen uit niet-metaal atomen • Bevatten atoombindingen • Geleiden geen stroom

Voorbeeld 3 • Systematische naam P 2 O 5 • Index P-atoom: 2 di • Index O-atoom: 5 penta • De naam wordt dan difosforpentaoxide telwoord- atoomsoort- telwoord-atoomsoort-ide

Vander. Waalsbindingen • Aantrekkende krachten tussen moleculen: cohesie. • Er geldt in het algemeen: Hoe groter de molecuulmassa, hoe sterker de Vander. Waalsbindingen, hoe hoger het smelt, - kookpunt.

Welke stoffen lossen op in water? • Hydrofiel (“houden van water”) Lossen op in water Bevatten een OH- of een NH-groep, zodat ze een H-brug kunnen vormen met water
• Hydrofoob (“angst voor water”) Lossen niet op in water Sommige stoffen zoals zeep bestaan uit een hydrofiel- en een hydrofoob- gedeelte. (C 17 H 35 COOH)
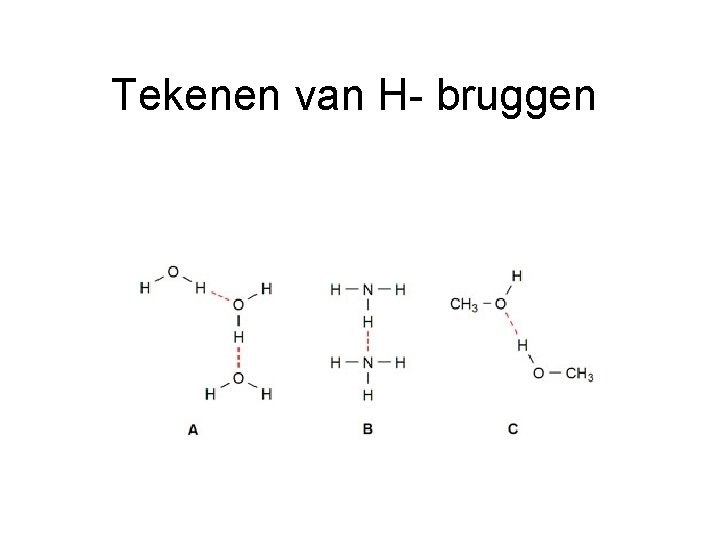
Tekenen van H- bruggen

Mengsels • Suspensie Mengsel van een vloeistof waarin kleine vaste korreltjes zweven. Voorbeelden: verf, krijt in water

Mengsels • Emulsie Mengsel van een hydrofiele vloeistof waarin kleine druppels van een hydrofobe vloeistof zweven of omgekeerd. (mayonaise, yoghurt, zonnebrandcrême) Emulgator: Zorgt ervoor dat olie en water wel mengen
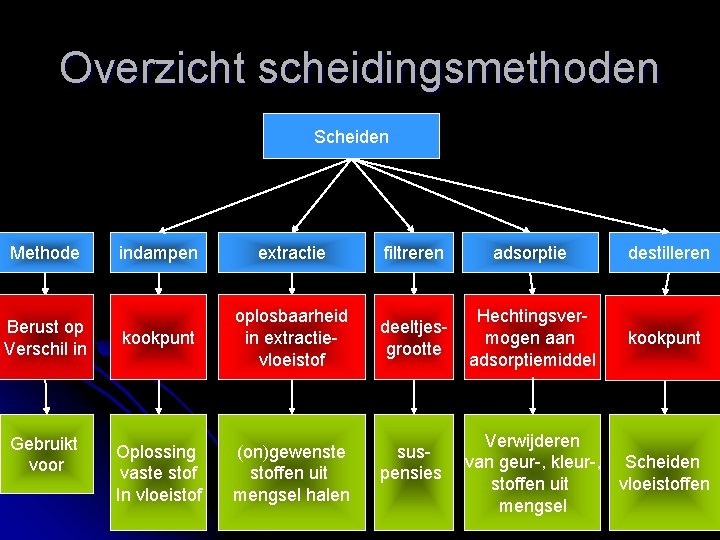
Overzicht scheidingsmethoden Scheiden Methode Berust op Verschil in Gebruikt voor indampen extractie filtreren adsorptie destilleren kookpunt oplosbaarheid in extractievloeistof deeltjesgrootte Hechtingsvermogen aan adsorptiemiddel kookpunt Oplossing vaste stof In vloeistof (on)gewenste stoffen uit mengsel halen Verwijderen van geur-, kleur-, stoffen uit mengsel Scheiden vloeistoffen suspensies

Oplosvergelijking • Bijvoorbeeld: Oplossen van suiker in water. SUIKER (s) SUIKER (aq) C 6 H 12 O 6 (s) C 6 H 12 O 6 (aq)

Significantie Kijk naar het kleinste aantal significante cijfers in de vraag en rond je antwoord (op het laatste moment) hier op af.

Rekenen met de mol • 1 Reken de gegeven hoeveelheden om naar mol. • 2 Reken met behulp van de molverhouding uit de reactie-vergelijking de hoeveelheid mol gevraagde stof uit. • 3 Reken de hoeveelheid mol om naar de gevraagde eenheid.

Oplosvergelijkingen ijzer(III)sulfaat heeft als verhoudingsformule: Fe 2(SO 4)3 Let op: géén + H 2 O in de reactievergelijking: Oplosvergelijking: Fe 2(SO 4)3 (s) 2 Fe 3+(aq) + 3 SO 42 -(aq)

Reactievergelijking • natriumoxide heeft als verhoudingsformule Na 2 O • Let op: hier wel H 2 O in de reactievergelijking Na 2 O (s) + H 2 O (l) 2 Na+(aq) + 2 OH-(aq) • (aq) : de ionen die ontstaan zijn gehydrateerd en opgelost in water • Alleen de reacties van Ba. O, Ca. O, K 2 O en Na 2 O moet je kennen

Indampvergelijkingen • Wanneer een oplossing van een zout wordt ingedampt ontstaat weer vast zout. 3 K+ (aq) + PO 43 - (aq) K 3 PO 4 (s)

Neerslagreacties • http: //www. youtube. com/watch? v=8 Rm. V wz 2 f. NGc&feature=related 1. Oplossingen van Na. Cl en Ag. NO 3 worden bij elkaar gevoegd. Er ontstaat een wit neerslag 2. Oplossingen van Na. I en Ag. NO 3 worden bij elkaar gevoegd. Er ontstaat een gelig neerslag
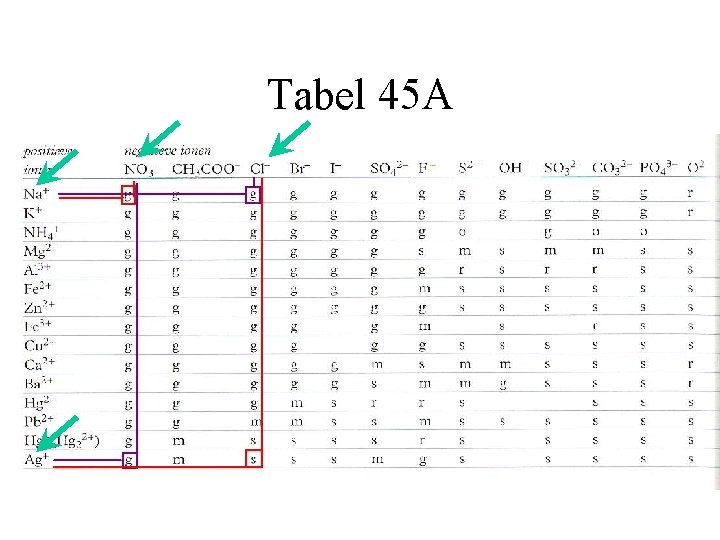
Tabel 45 A

Neerslagreactie vergelijking: • Ag+ en Cl- : de combinatie is slecht oplosbaar • Ze zullen met elkaar reageren en een neerslag vormen: neerslagreactie • De vergelijking van de reactie wordt ook ionenvergelijking genoemd • Ag+(aq) + Cl-(aq) Ag. Cl (s)

Zouthydraten • In het ionrooster zijn dan een aantal moleculen (kristal)water opgenomen. (blauw) koper(II)sulfaatpentahydraat Cu. SO 4 • 5 H 2 O • Bij het indampen van koper(II)sulfaat uit een oplossing vindt dan de volgende reactie plaats: Cu 2+ + SO 42 - + 5 H 2 O Cu. SO 4 • 5 H 2 O • Bij sterke verhitting van het hydraat verliest het zijn kristalwater: Cu. SO 4 • 5 H 2 O Cu. SO 4 + 5 H 2 O wit Watervrij kopersulfaat wordt als indicator gebruikt om water in de lucht of een andere stof aan te tonen: Cu. SO 4 + 5 H 2 O Cu. SO 4 • 5 H 2 O (EXOTHERM)

Hard water bevat veel Mg 2+ of Ca 2+- ionen. Deze ionen zorgen voor problemen omdat ze makkelijk een neerslag vormen. Vorming van hard water: Ca. CO 3 + H 2 O + CO 2 Ca 2+ + 2 HCO 3 -

Soorten dynamische evenwichten: • Homogeen evenwicht Alle stoffen in een reactie hebben dezelfde fase. • Heterogeen evenwicht Als er verschillende fasen in de reactievergelijking staan. • Verdelingsevenwicht Opgeloste (vaste) stof verdeelt zich over twee oplosmiddelen (die niet mengen) in een vaste verhouding. B. v. jood in water en benzine

Ligging van een evenwicht • Principe van Le Chatelier- Van ‘t Hoff Oefent men op een stelsel in evenwicht een dwang uit, dan zal het stelsel er zo op reageren dat de gevolgen zoveel mogelijk worden teniet gedaan

• Drukverhoging: Dan verschuift het evenwicht naar de kant met de minste gasmoleculen. • Concentratie: Toevoegen van een bepaalde stof zorgt ervoor dat deze stof verdwijnt door verschuiving van het evenwicht naar de andere kant

• Een reactie is aflopend als er een neerslag wordt gevormd of een gas ontstaat. • Een katalysator versnelt zowel de heenals teruggaande reactie. Een katalysator beïnvloed de ligging niet, enkel de snelheid van het bereiken van het evenwicht.

LET OP! • zoutzuur is een oplossing van HCl Notatie: H+ + Cl-
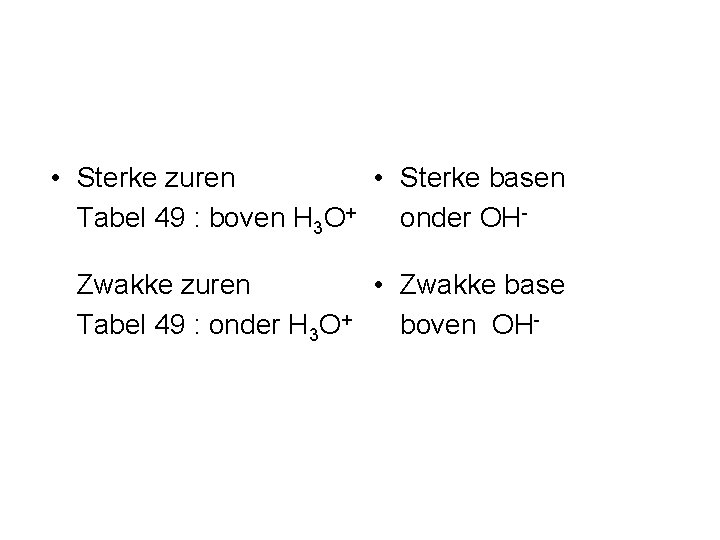
• Sterke zuren • Sterke basen Tabel 49 : boven H 3 O+ onder OHZwakke zuren • Zwakke base Tabel 49 : onder H 3 O+ boven OH-

Oplossen van een sterk zuur Bv: oplossen salpeterzuur in water HNO 3 H+ + NO 3 Alle zuurdeeltjes staan H+ af

Oplossen van een zwak zuur Bij het oplossen van ammoniumnitraat in water dan kan er een zuur ontstaan: Stap 1: NH 4 NO 3 NH 4+ + NO 3 Stap 2: NH 4+ NH 3 + H+ Niet alle zuurdeeltjes staan H + af evenwicht
![Berekeningen: De concentratie altijd in mol/l invullen! p. H = - log [H+] = Berekeningen: De concentratie altijd in mol/l invullen! p. H = - log [H+] =](http://slidetodoc.com/presentation_image_h/d72a769a7049cd88f4c6ccb18a00677c/image-34.jpg)
Berekeningen: De concentratie altijd in mol/l invullen! p. H = - log [H+] = 10 -p. H p. OH = - log [OH-] = 10 -p. OH + p. H = 14

significantie bij p. H en p. OH: Bij p. H en p. OH tellen alleen de cijfers achter de komma mee voor significantie. p. H = 0, 25 en p. OH = 13, 75 zijn beiden in 2 cijfers significant.

Drie hoofdcategorieën stoffen: ØMoleculaire stoffen: Atoombinding in molecuul (sterk), Van der Waals binding tussen moleculen (zwak), polaire (atoom)bindingen, evt. H-bruggen tussen moleculen. ØMetalen: Metaalbinding (zeer sterk), dus hoog smeltpunt, geleiden ØZouten: Ionbinding (sterk), dus hoog smeltpunt, ionen

Deeltjes die elektronen opnemen zijn oxidatoren Deeltjes die elektronen afstaan zijn reductoren Algemeen kun je stellen dat alle reacties waarbij de lading van een deeltje verandert, redoxreacties zijn. Verder zijn alle reacties waarbij elementen verdwijnen en/of ontstaan ook redoxreacties. Soms zie je dat daarbij de lading verandert (bijvoorbeeld bij het ontstaan van zouten). In andere gevallen gebeurt dat niet. Als bij een reactie elektronenoverdracht plaatsvindt spreken we van een Red. Oxreactie!

Halfreacties Elke Red. Oxreactie is op te splitsen in twee halfreacties. Eén die het afstaan van elektronen weergeeft (reductor) Eén die het opnemen van elekronen weergeeft (oxidator) We bekijken weer ons voorbeeld: 2 Fe(s) + O 2(g) 2 Fe. O(s) Halfreactie (Red) Fe (s) Halfreactie (Ox) O 2 (g) + 4 e- Fe 2+ + 2 e 2 O 2 - Totaal reactie 2 Fe (s) + O 2 (g) 2 Fe. O (s) 2 x 1 x +

Redoxvergelijkingen opstellen: 1. 2. 3. 4. 1. 2. 3. Schrijf de formules van alle deeltjes in het reactiemengsel op. (Vergeet H 2 O niet!) Ga voor ieder deeltje na m. b. v. Binas 48 of het een oxidator of reductor is. Kies uit het rijtje de sterkste oxidator en de sterkste reductor. Kijk of de reactie kan verlopen: OX moet boven RED staan. Schrijf de halfreacties op. De halfreactie van de reductor moet worden omgekeerd! Tel de twee halfreacties op, zorg ervoor dat er evenveel elektronen worden opgenomen als afgestaan. De elektronen worden bij het optellen tegen elkaar weggestreept. VEREENVOUDIGEN (links en rechts hetzelfde wegstrepen) Denk aan water wegstrepen!
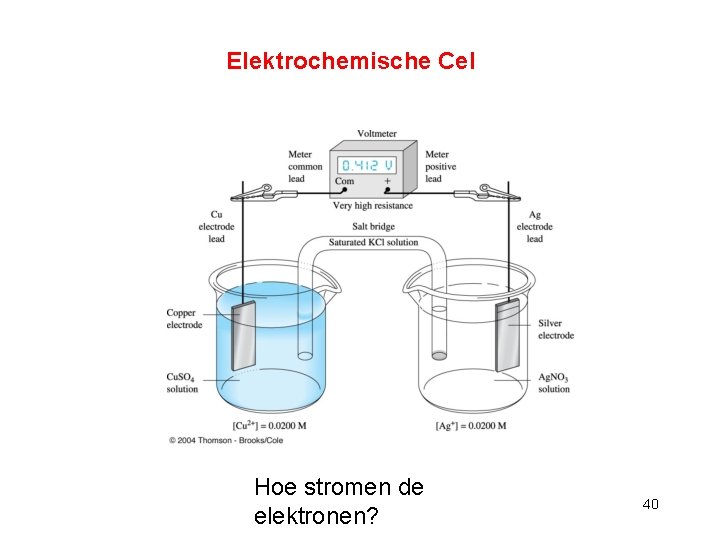
Elektrochemische Cel Hoe stromen de elektronen? 40

• De min- pool ontstaat aan de kant van de (sterkste) reductor • De plus- pool ontstaat aan de kant van de (sterkste) oxidator • Een Pt- elektrode en een C- elektrode doen nooit mee (inerte elektrode) als OX of RED

Elektrolyse • REDOX Reactie die altijd verloopt • Niet alleen ontledingsmethode • Reactie die verloopt onder invloed van een externe (gelijk)spanningsbron.
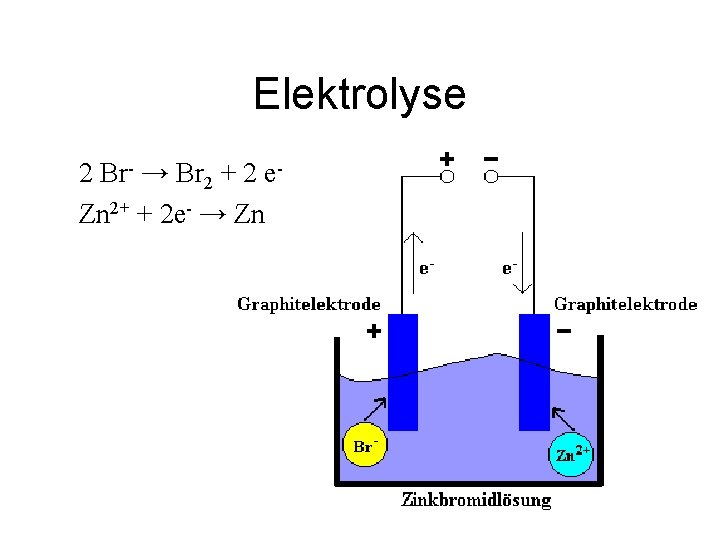
Elektrolyse 2 Br- → Br 2 + 2 e. Zn 2+ + 2 e- → Zn

Let op! • De halfreacties mag je nooit optellen! • Bij de plus- pool reageert de sterkste reductor • Bij de min- pool reageert de sterkste oxidator • Als je moet kiezen tussen Cl- (+1. 36) en H 2 O (+1. 23) als RED dan wint Cl-!!!

Naamgeving vertakte alkanen Stamnaam: langste onvertakte C-keten (de hoofdketen). Zijgroep: methyl (1 C) of ethyl ( 2 C) etc. Nummering: hoofdketen nummeren en plaats van zijgroep met nummer aangeven. (Zo laag mogelijk nummeren) C H 3 | CH 2 – CH | | CH 3 Stamnaam: pentaan Zijgroep: methyl (CH 3) Nummering: 2 (dus niet: 4) Naam: 2 -methylpentaan

Dezelfde regels gelden ook voor andere zijgroepen zoals F, Cl, Br en I. CH 3 Br | | CH 2 – CH 2 | CH 3 – CH 2 CH 3 Cl | | CH – CH 2 | | CH 3 F Stamnaam: hexaan Zijgroep: broom Nummering: 3 (dus niet: 4) Naam: 3 -broomhexaan Gecombineerd: 1 -fluor-2 -chloor-3 -methylbutaan
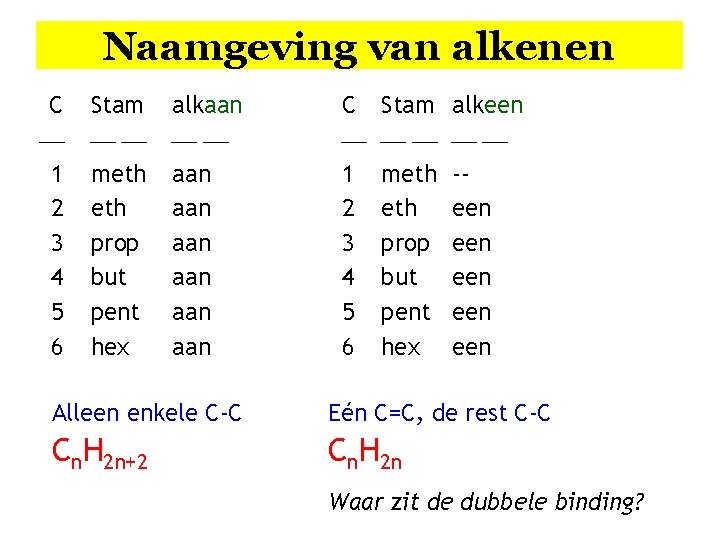
Naamgeving van alkenen C 1 2 3 4 5 6 Stam meth prop but pent hex alkaan aan aan C 1 2 3 4 5 6 Stam meth prop but pent hex alkeen -een een een Alleen enkele C-C Eén C=C, de rest C-C Cn. H 2 n+2 Cn. H 2 n Waar zit de dubbele binding?
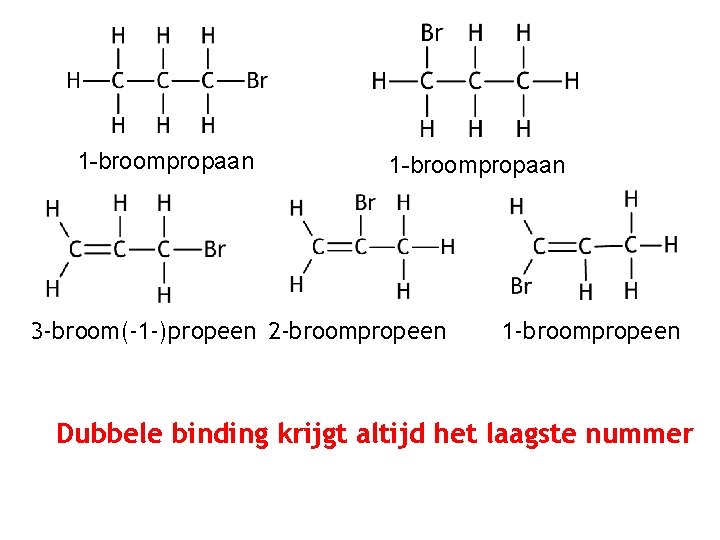
1 -broompropaan 3 -broom(-1 -)propeen 2 -broompropeen 1 -broompropeen Dubbele binding krijgt altijd het laagste nummer
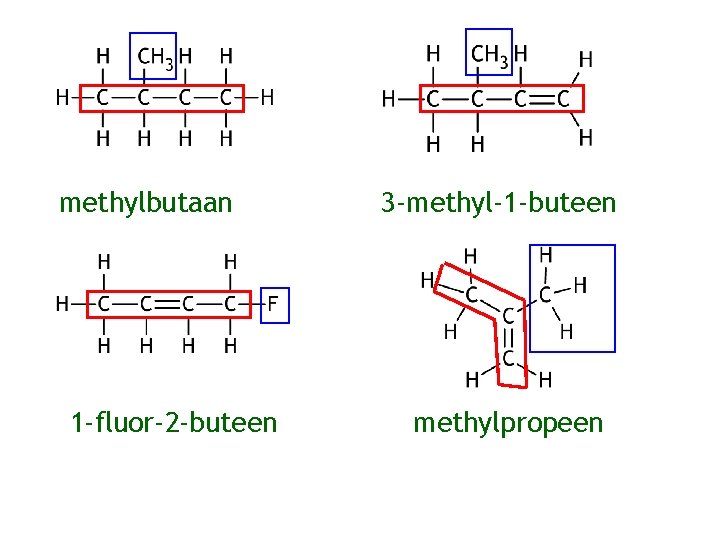
methylbutaan 1 -fluor-2 -buteen 3 -methyl-1 -buteen methylpropeen
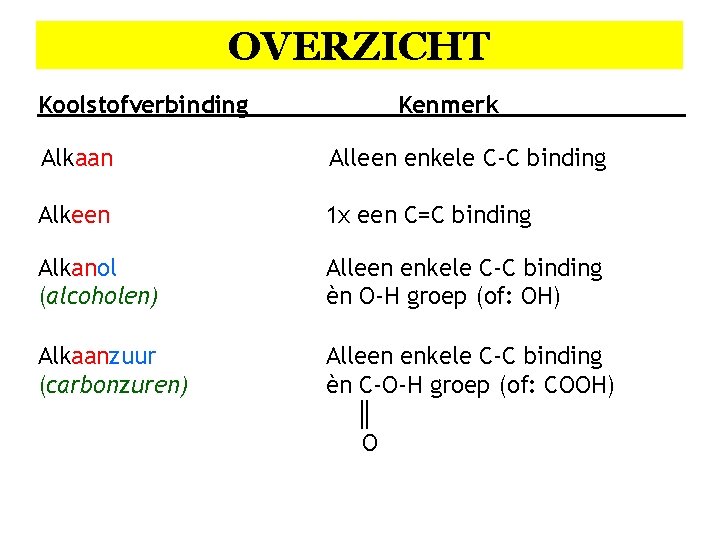
OVERZICHT Koolstofverbinding Kenmerk Alkaan Alleen enkele C-C binding Alkeen 1 x een C=C binding Alkanol (alcoholen) Alleen enkele C-C binding èn O-H groep (of: OH) Alkaanzuur (carbonzuren) Alleen enkele C-C binding èn C-O-H groep (of: COOH) ║ O
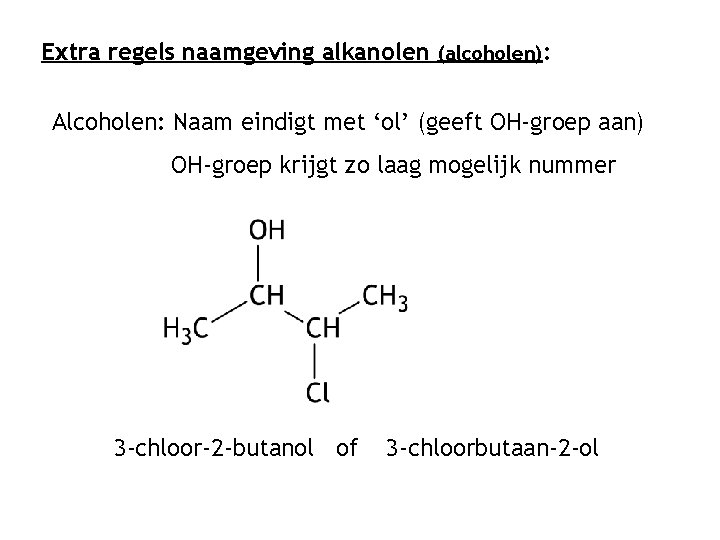
Extra regels naamgeving alkanolen (alcoholen): Alcoholen: Naam eindigt met ‘ol’ (geeft OH-groep aan) OH-groep krijgt zo laag mogelijk nummer 3 -chloor-2 -butanol of 3 -chloorbutaan-2 -ol
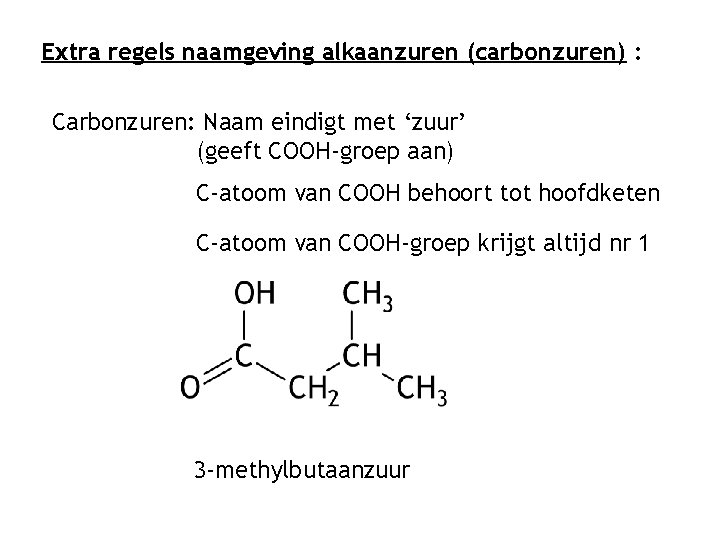
Extra regels naamgeving alkaanzuren (carbonzuren) : Carbonzuren: Naam eindigt met ‘zuur’ (geeft COOH-groep aan) C-atoom van COOH behoort tot hoofdketen C-atoom van COOH-groep krijgt altijd nr 1 3 -methylbutaanzuur
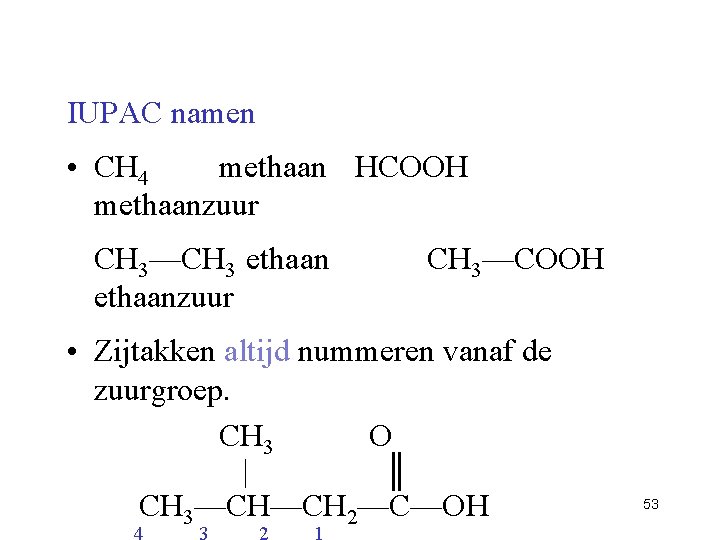
IUPAC namen • CH 4 methaan HCOOH methaanzuur CH 3—CH 3 ethaanzuur CH 3—COOH • Zijtakken altijd nummeren vanaf de zuurgroep. CH 3 O | ║ CH 3—CH—CH 2—C—OH 4 3 2 1 53
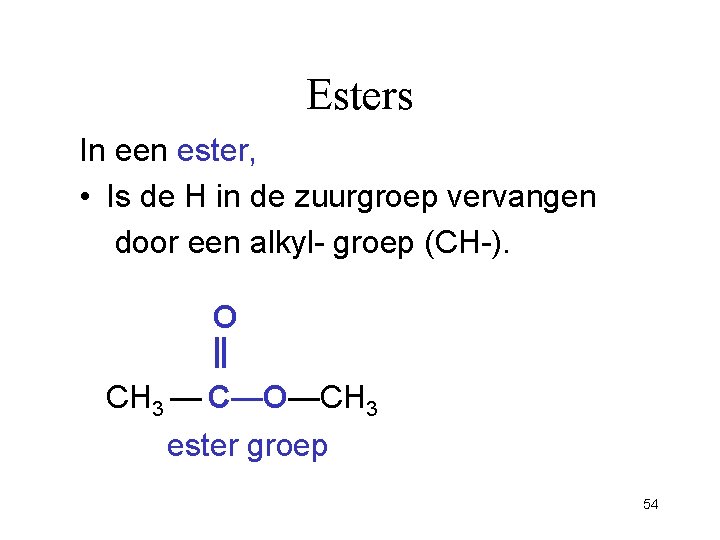
Esters In een ester, • Is de H in de zuurgroep vervangen door een alkyl- groep (CH-). O CH 3 — C—O—CH 3 ester groep 54
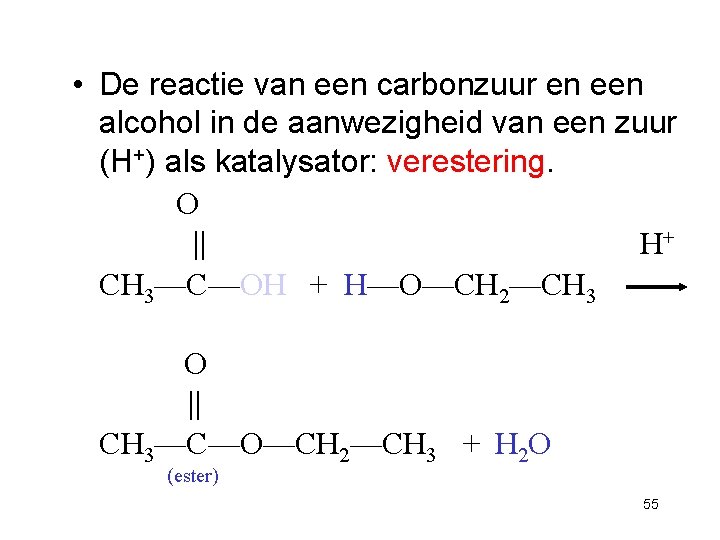
• De reactie van een carbonzuur en een alcohol in de aanwezigheid van een zuur (H+) als katalysator: verestering. O H+ CH 3—C—OH + H—O—CH 2—CH 3 O CH 3—C—O—CH 2—CH 3 + H 2 O (ester) 55
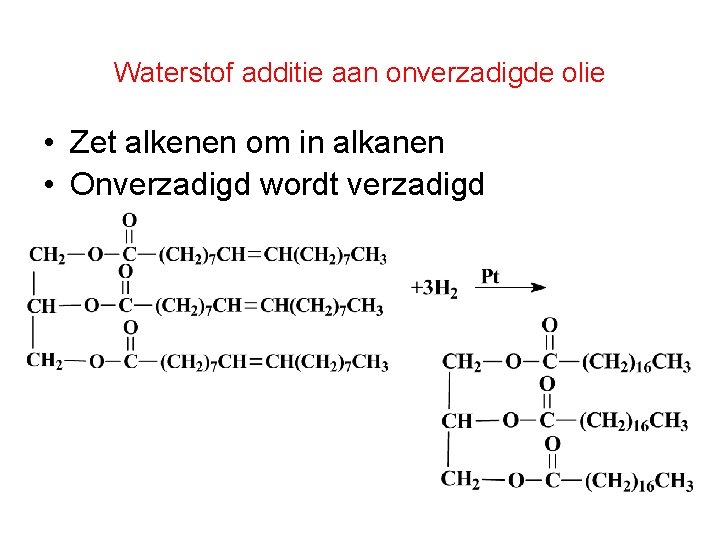
Waterstof additie aan onverzadigde olie • Zet alkenen om in alkanen • Onverzadigd wordt verzadigd
- Slides: 56