Boston College Maip Departamento de Ciencias NM 4

Boston College Maipú Departamento de Ciencias NM 4 Química Óxido-reducción: Reacciones de oxidación y reducción. Profesor: Francisco Muñoz Q Camila Álvarez
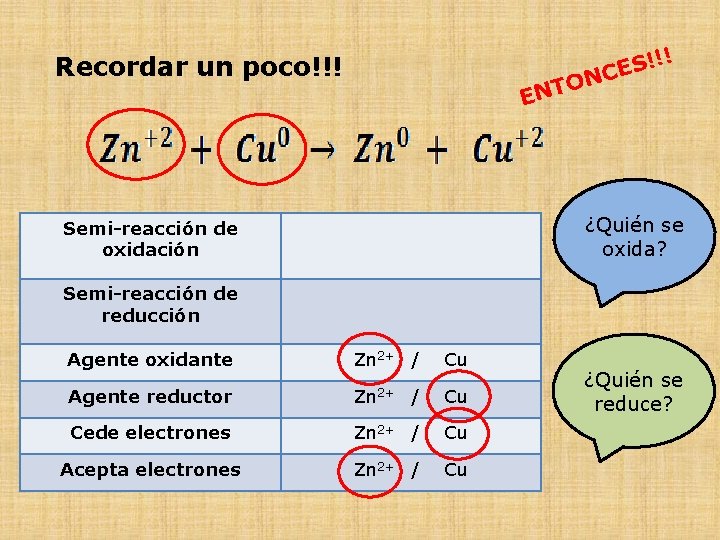
Recordar un poco!!! N O T EN !! ! S CE ¿Quién se oxida? Semi-reacción de oxidación Semi-reacción de reducción Agente oxidante Zn 2+ / Cu Agente reductor Zn 2+ / Cu Cede electrones Zn 2+ / Cu Acepta electrones Zn 2+ / Cu ¿Quién se reduce?

Objetivo: Reconocer características de las reacciones redox. 1. Reacciones redox !! ! ! O L JEMP E • Introducimos un electrodo de cobre en una disolución de Ag. NO 3. • De manera espontánea el cobre se oxidará pasando a la disolución como Cu 2+. • Mientras que la Ag+ de la misma se reducirá pasando a ser plata metálica: a) Cu 2+ + 2 e– (oxidación) b) Ag+ + 1 e– Ag (reducción) Semi-reacciones de oxidación y reducción
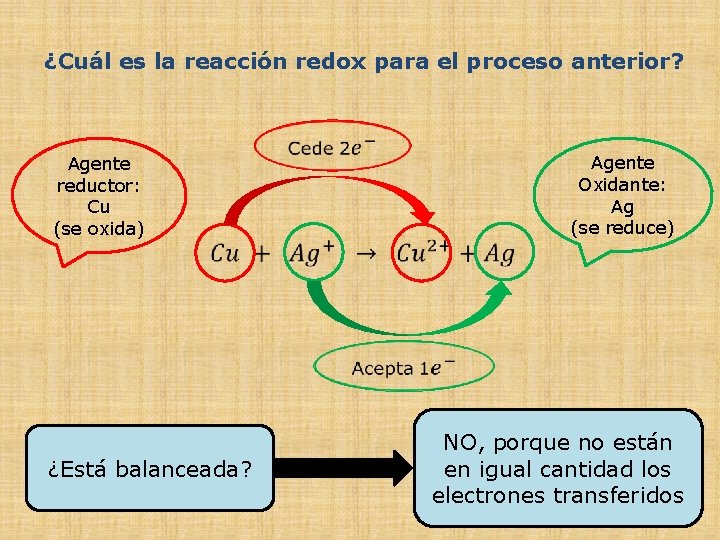
¿Cuál es la reacción redox para el proceso anterior? Agente reductor: Cu (se oxida) ¿Está balanceada? Agente Oxidante: Ag (se reduce) NO, porque no están en igual cantidad los electrones transferidos
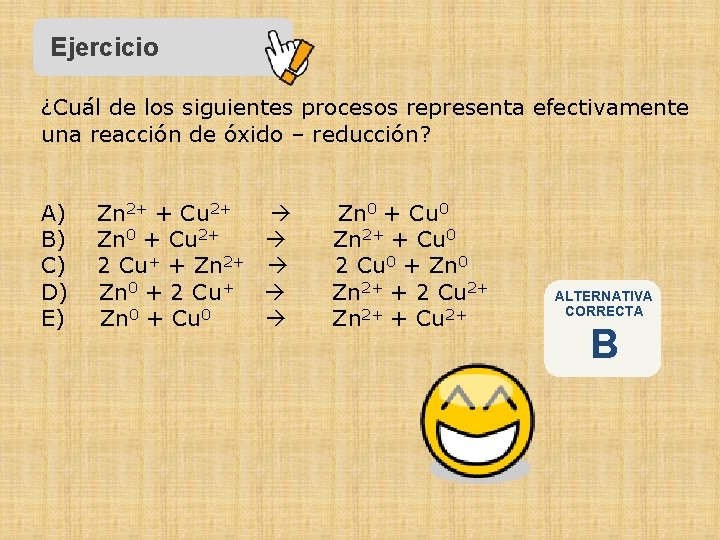
Ejercicio ¿Cuál de los siguientes procesos representa efectivamente una reacción de óxido – reducción? A) B) C) D) E) Zn 2+ + Cu 2+ Zn 0 + Cu 2+ 2 Cu+ + Zn 2+ Zn 0 + 2 Cu+ Zn 0 + Cu 0 Zn 2+ + Cu 0 2 Cu 0 + Zn 0 Zn 2+ + 2 Cu 2+ Zn 2+ + Cu 2+ ALTERNATIVA CORRECTA B
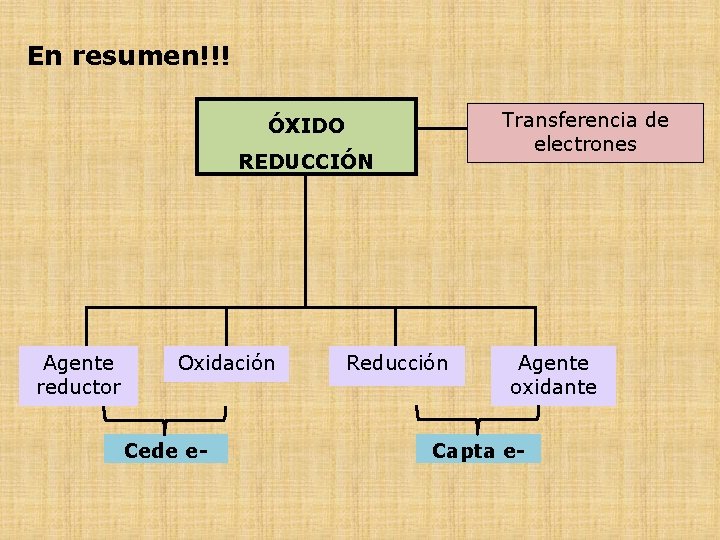
En resumen!!! Transferencia de electrones ÓXIDO REDUCCIÓN Agente reductor Oxidación Cede e- Reducción Agente oxidante Capta e-

Actividad


- Slides: 9