Boston College Maip Departamento de Ciencias NM 3
Boston College Maipú Departamento de Ciencias NM 3 Química orgánica: Estructuras de hidrocarburos y nomenclatura. Profesor: Francisco Muñoz Q
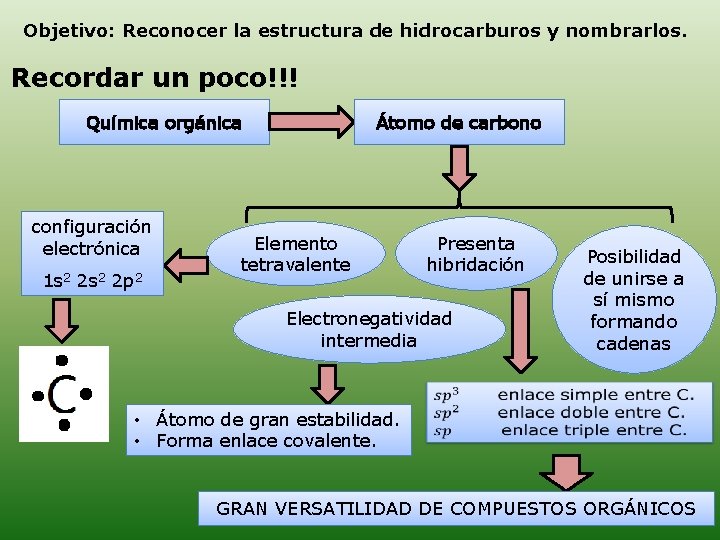
Objetivo: Reconocer la estructura de hidrocarburos y nombrarlos. Recordar un poco!!! Química orgánica configuración electrónica 1 s 2 2 p 2 Átomo de carbono Elemento tetravalente Presenta hibridación Electronegatividad intermedia Posibilidad de unirse a sí mismo formando cadenas • Átomo de gran estabilidad. • Forma enlace covalente. GRAN VERSATILIDAD DE COMPUESTOS ORGÁNICOS
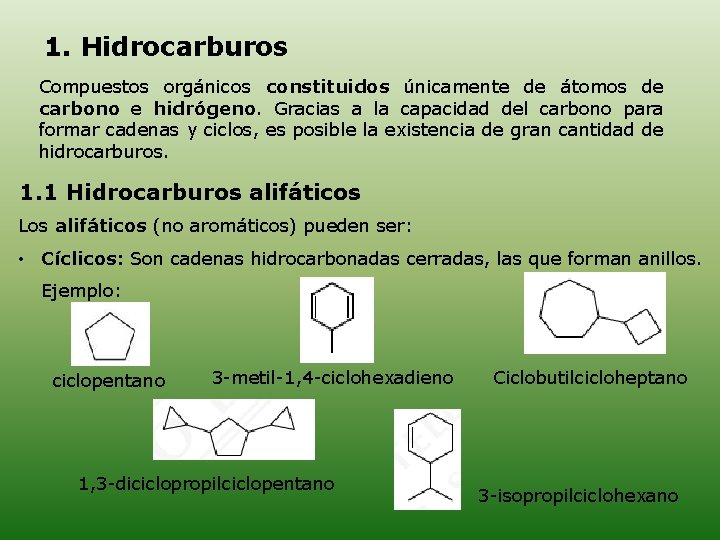
1. Hidrocarburos Compuestos orgánicos constituidos únicamente de átomos de carbono e hidrógeno. Gracias a la capacidad del carbono para formar cadenas y ciclos, es posible la existencia de gran cantidad de hidrocarburos. 1. 1 Hidrocarburos alifáticos Los alifáticos (no aromáticos) pueden ser: • Cíclicos: Son cadenas hidrocarbonadas cerradas, las que forman anillos. Ejemplo: ciclopentano 3 -metil-1, 4 -ciclohexadieno 1, 3 -diciclopropilciclopentano Ciclobutilcicloheptano 3 -isopropilciclohexano
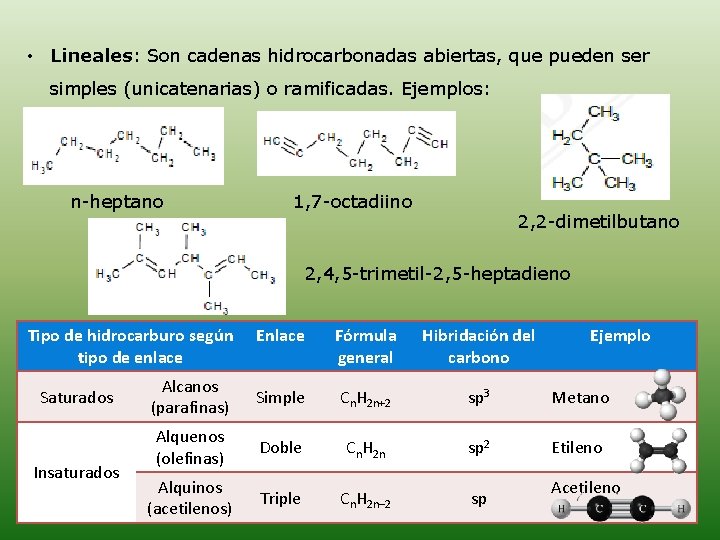
• Lineales: Son cadenas hidrocarbonadas abiertas, que pueden ser simples (unicatenarias) o ramificadas. Ejemplos: n-heptano 1, 7 -octadiino 2, 2 -dimetilbutano 2, 4, 5 -trimetil-2, 5 -heptadieno Tipo de hidrocarburo según tipo de enlace Saturados Insaturados Enlace Fórmula general Hibridación del carbono Ejemplo Alcanos (parafinas) Simple Cn. H 2 n+2 sp 3 Metano Alquenos (olefinas) Doble Cn. H 2 n sp 2 Etileno Alquinos (acetilenos) Triple Cn. H 2 n– 2 sp Acetileno
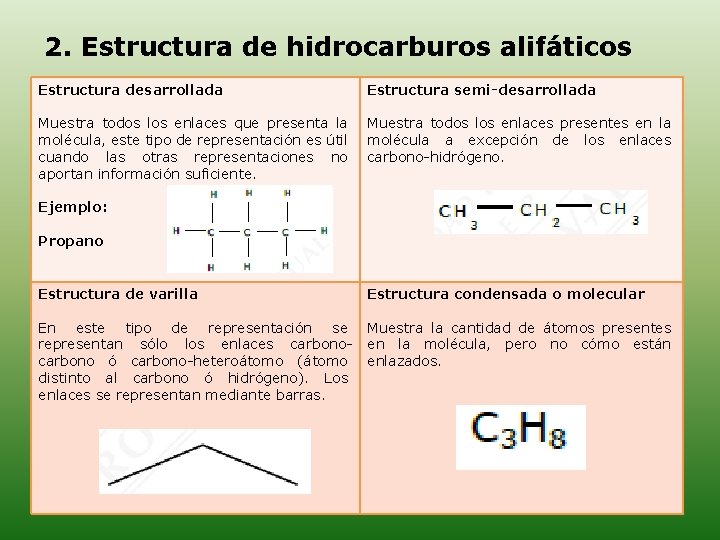
2. Estructura de hidrocarburos alifáticos Estructura desarrollada Estructura semi-desarrollada Muestra todos los enlaces que presenta la molécula, este tipo de representación es útil cuando las otras representaciones no aportan información suficiente. Muestra todos los enlaces presentes en la molécula a excepción de los enlaces carbono-hidrógeno. Ejemplo: Propano Estructura de varilla Estructura condensada o molecular En este tipo de representación se representan sólo los enlaces carbono ó carbono-heteroátomo (átomo distinto al carbono ó hidrógeno). Los enlaces se representan mediante barras. Muestra la cantidad de átomos presentes en la molécula, pero no cómo están enlazados.
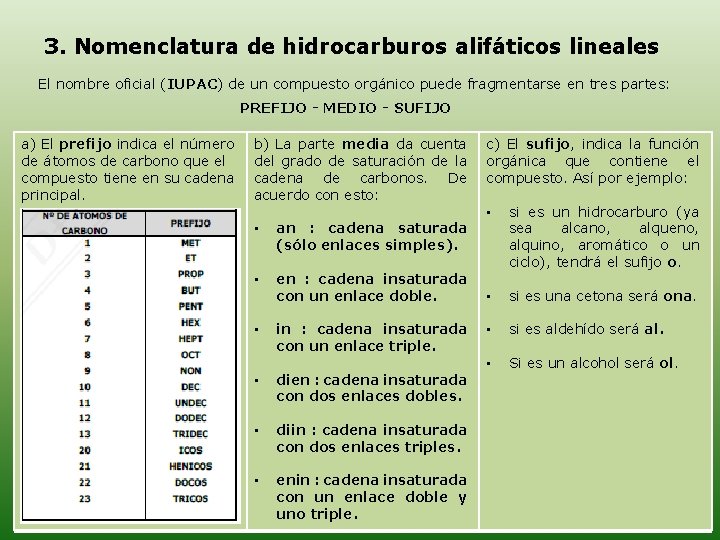
3. Nomenclatura de hidrocarburos alifáticos lineales El nombre oficial (IUPAC) de un compuesto orgánico puede fragmentarse en tres partes: PREFIJO - MEDIO - SUFIJO a) El prefijo indica el número de átomos de carbono que el compuesto tiene en su cadena principal. b) La parte media da cuenta del grado de saturación de la cadena de carbonos. De acuerdo con esto: • an : cadena saturada (sólo enlaces simples). • en : cadena insaturada con un enlace doble. • in : cadena insaturada con un enlace triple. • dien : cadena insaturada con dos enlaces dobles. • diin : cadena insaturada con dos enlaces triples. • enin : cadena insaturada con un enlace doble y uno triple. c) El sufijo, indica la función orgánica que contiene el compuesto. Así por ejemplo: • si es un hidrocarburo (ya sea alcano, alqueno, alquino, aromático o un ciclo), tendrá el sufijo o. • si es una cetona será ona. • si es aldehído será al. • Si es un alcohol será ol.
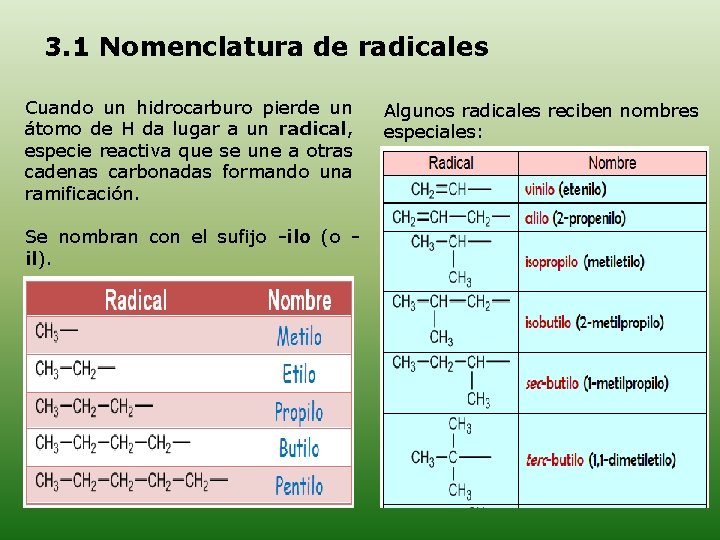
3. 1 Nomenclatura de radicales Cuando un hidrocarburo pierde un átomo de H da lugar a un radical, especie reactiva que se une a otras cadenas carbonadas formando una ramificación. Se nombran con el sufijo -ilo (o il). Algunos radicales reciben nombres especiales:
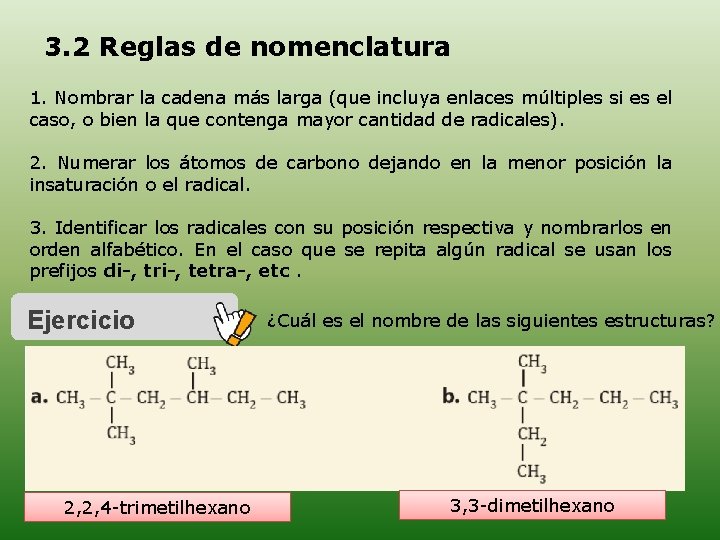
3. 2 Reglas de nomenclatura 1. Nombrar la cadena más larga (que incluya enlaces múltiples si es el caso, o bien la que contenga mayor cantidad de radicales). 2. Numerar los átomos de carbono dejando en la menor posición la insaturación o el radical. 3. Identificar los radicales con su posición respectiva y nombrarlos en orden alfabético. En el caso que se repita algún radical se usan los prefijos di-, tri-, tetra-, etc. Ejercicio 2, 2, 4 -trimetilhexano ¿Cuál es el nombre de las siguientes estructuras? 3, 3 -dimetilhexano

Actividad
- Slides: 9