Boston College Maip Departamento de Ciencias NM 2
Boston College Maipú Departamento de Ciencias NM 2 Química Estequiometría: Concepto de mol y balance de ecuaciones Profesor: Francisco Muñoz Q Camila Álvarez

Objetivo: Reconocer el concepto de mol, los términos de una ecuación química y balancear ecuaciones químicas. 1. Masa molar (MM) Se define como la masa (en gramos o kilogramos) de 1 mol de unidades (átomos o moléculas) de una sustancia. Ejercicio Determinar la masa molar de los compuestos SO 2 y Cu. SO 4 x 5 H 2 O Para calcular la masa molar es necesario contar el número átomos de cada elemento presente en la molécula y buscar su masa atómica en la tabla periódica SO 2 En el dióxido de azufre hay un átomo de S y dos átomos de O, por lo que Masa molar de SO 2 = 32, 1 g/mol + 2 (16, 0 g/mol) Masa molar = 64, 1 g/mol
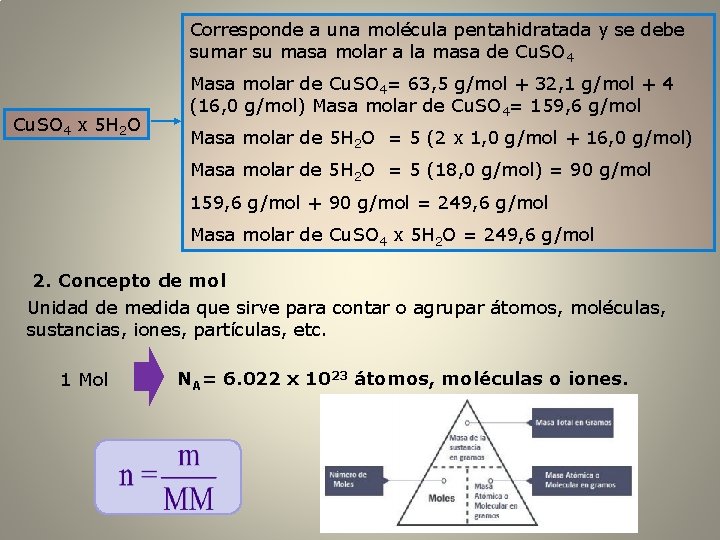
Corresponde a una molécula pentahidratada y se debe sumar su masa molar a la masa de Cu. SO 4 x 5 H 2 O Masa molar de Cu. SO 4= 63, 5 g/mol + 32, 1 g/mol + 4 (16, 0 g/mol) Masa molar de Cu. SO 4= 159, 6 g/mol Masa molar de 5 H 2 O = 5 (2 x 1, 0 g/mol + 16, 0 g/mol) Masa molar de 5 H 2 O = 5 (18, 0 g/mol) = 90 g/mol 159, 6 g/mol + 90 g/mol = 249, 6 g/mol Masa molar de Cu. SO 4 x 5 H 2 O = 249, 6 g/mol 2. Concepto de mol Unidad de medida que sirve para contar o agrupar átomos, moléculas, sustancias, iones, partículas, etc. 1 Mol NA= 6. 022 x 1023 átomos, moléculas o iones.
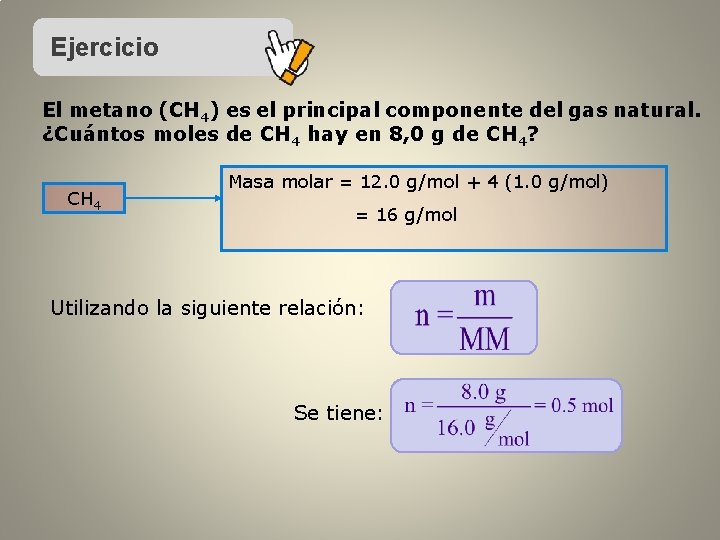
Ejercicio El metano (CH 4) es el principal componente del gas natural. ¿Cuántos moles de CH 4 hay en 8, 0 g de CH 4? CH 4 Masa molar = 12. 0 g/mol + 4 (1. 0 g/mol) = 16 g/mol Utilizando la siguiente relación: Se tiene:
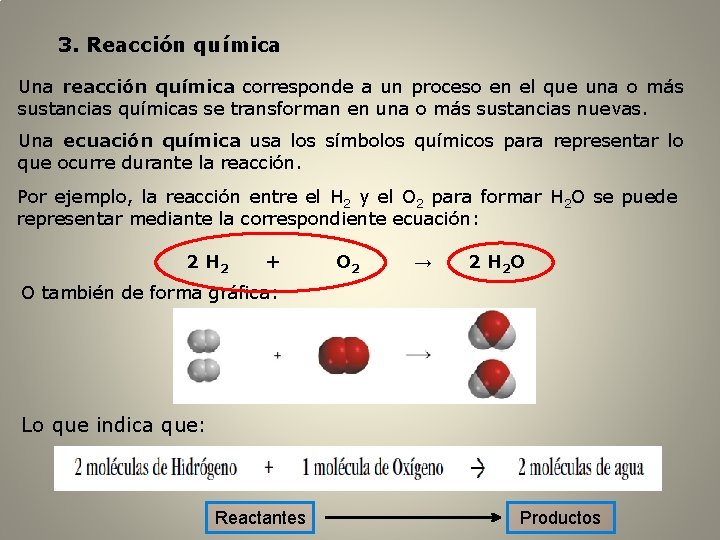
3. Reacción química Una reacción química corresponde a un proceso en el que una o más sustancias químicas se transforman en una o más sustancias nuevas. Una ecuación química usa los símbolos químicos para representar lo que ocurre durante la reacción. Por ejemplo, la reacción entre el H 2 y el O 2 para formar H 2 O se puede representar mediante la correspondiente ecuación: 2 H 2 + O 2 → 2 H 2 O O también de forma gráfica: Lo que indica que: Reactantes Productos
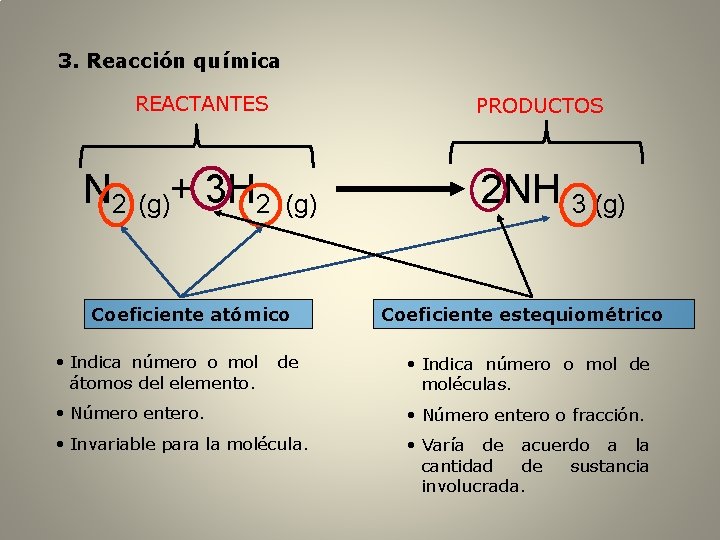
3. Reacción química REACTANTES N 2 (g)+ 3 H 2 PRODUCTOS (g) Coeficiente atómico • Indica número o mol átomos del elemento. de 2 NH 3 (g) Coeficiente estequiométrico • Indica número o mol de moléculas. • Número entero o fracción. • Invariable para la molécula. • Varía de acuerdo a la cantidad de sustancia involucrada.
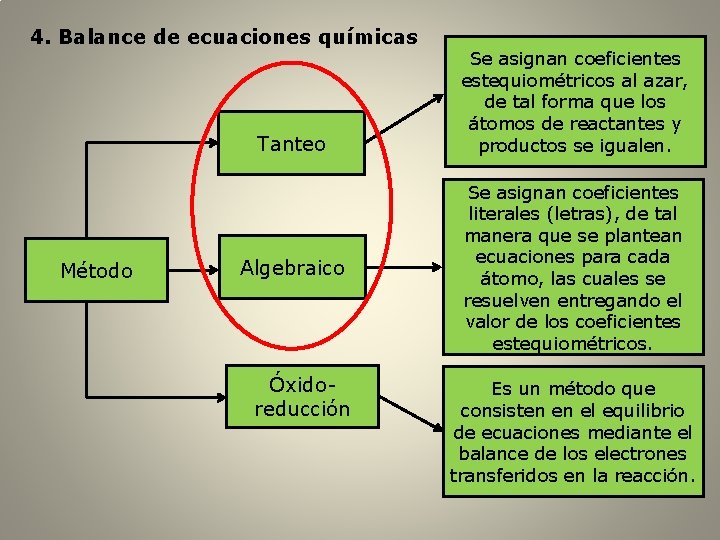
4. Balance de ecuaciones químicas Tanteo Método Algebraico Óxidoreducción Se asignan coeficientes estequiométricos al azar, de tal forma que los átomos de reactantes y productos se igualen. Se asignan coeficientes literales (letras), de tal manera que se plantean ecuaciones para cada átomo, las cuales se resuelven entregando el valor de los coeficientes estequiométricos. Es un método que consisten en el equilibrio de ecuaciones mediante el balance de los electrones transferidos en la reacción.
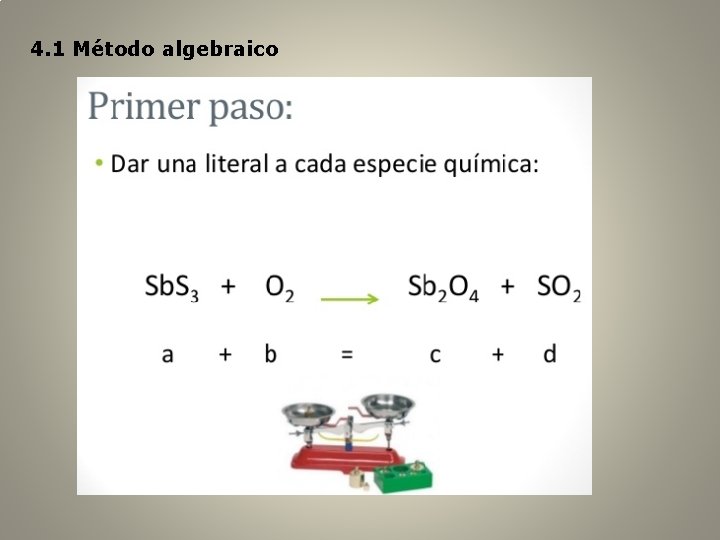
4. 1 Método algebraico




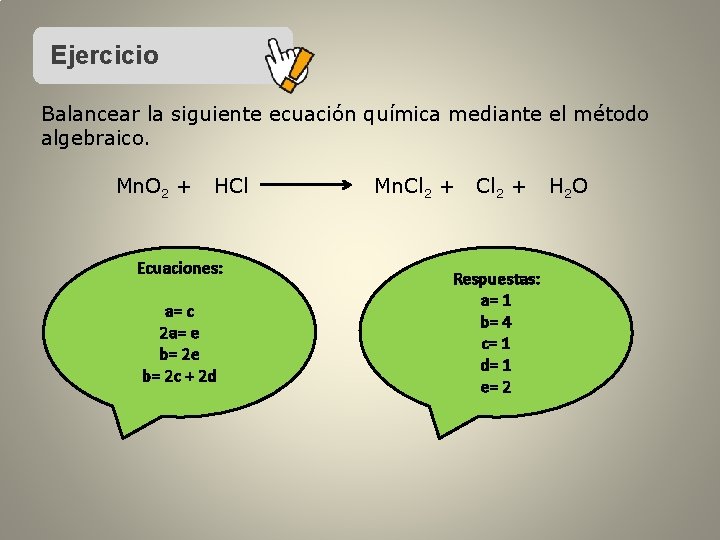
Ejercicio Balancear la siguiente ecuación química mediante el método algebraico. Mn. O 2 + HCl Ecuaciones: a= c 2 a= e b= 2 c + 2 d Mn. Cl 2 + Respuestas: a= 1 b= 4 c= 1 d= 1 e= 2 H 2 O
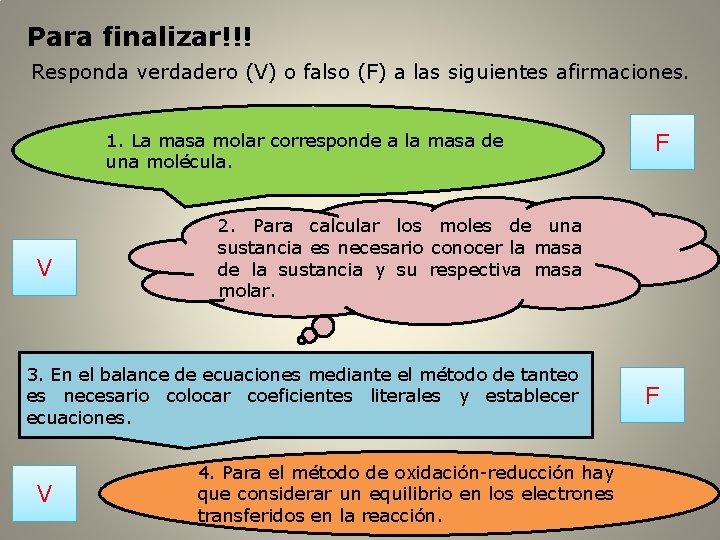
Para finalizar!!! Responda verdadero (V) o falso (F) a las siguientes afirmaciones. 1. La masa molar corresponde a la masa de una molécula. V 2. Para calcular los moles de una sustancia es necesario conocer la masa de la sustancia y su respectiva masa molar. 3. En el balance de ecuaciones mediante el método de tanteo es necesario colocar coeficientes literales y establecer ecuaciones. V F 4. Para el método de oxidación-reducción hay que considerar un equilibrio en los electrones transferidos en la reacción. F

Actividad

- Slides: 16