Boro Este es el nico elemento de la

Boro Este es el único elemento de la familia 3 A no metálico. Hay dos alótropos del boro; el boro amorfo es un polvo marrón mientras que el boro metálico es negro. La forma metálica es dura (9, 3 en la escala de Mohs) y es un mal conductor a temperatura ambiente. No se ha encontrado libre en la naturaleza.

Obtención La mayor fuente de boro son los boratos de depósitos evaporíticos, como el bórax (Na 2 B 4 O 7· 8 H 2 O, Borato de sodio o Tetraborato de sodio) que se obtiene por reducción con manganeso y, con menos importancia, la colemanita (Ca 2 B 6 O 11· 5 H 2 O Borato de calcio pentahídratado). Precipita como ácido ortobórico H 3 BO 3 alrededor de algunas fuentes y humos volcánicos, dando sasolitas. Se forman menas de boro naturales en el proceso de solidificación de magmas silicatados; estos depósitos son las pegmatitas.

Compuestos con elementos electronegativos El boro se combina con: • Halógenos, dando lugar a los haluros de boro. Estos se usan como catalizadores ácidos de Lewis • Oxígeno, produciendo ácido bórico, y ésteres de borato • Nitrógeno, obteniéndose nitruros de boro, amino-boranos y compuestos análogos a los aminoácidos

Trihaluros de boro Obtención: B 2 O 3 (S) + 3 Ca. F 2 (S) + 6 H 2 SO 4 (ac) → 2 BF 3 (g) + 3(H 3 O)(HSO 4) (ac) + 3 Ca. SO 4 (S) Estructura: Los trihaluros de boro constan de moléculas de BX 3 planas trigonales. Características físicas: El trifluoruro y el tricloruro de boro son gases, el tribromuro es un líquido volátil y el triioduro es sólido. Ácido base: Los trihaluros son ácidos de Lewis, el orden de su fuerza ácida es el siguiente: BF 3 < BCl 3 < BBr 3

Reacciones de los trihaluros • BF 3 (g) NH 3 (g) → F 3 B-NH 3 • BCl 3 (g) + 3 H 2 O (l) → B(OH)3 (ac) + 3 HCl (ac) • BF 3 (g) + F-(ac) → (BF 4)-(ac) • BCl 3 (g) + 3 H 2 O (l) → B(OH)3 (ac) + 3 HCl (ac) • BBr 3 (g) + 3 NH(CH 3)2 → B(N(CH 3)2)3 + 3 HBr (g)

Compuestos con nitrógeno El nitruro de boro se prepara calentando óxido de boro con amoniaco a altas temperaturas. B 2 O 3 (l) + 2 NH 3 (g) 2 BN (s) + 3 H 2 O (g) Características físicas: La estructura del nitruro de boro es laminar, por lo que es una sustancia resbaladiza usada como lubricante. A presiones altas cambia a una estructura cùbica. La preparaciòn de amino-boranos se lleva a cabo a partir de la reacciòn entre una base nitrogenada de Lewis y un ácido de Lewis que contenga boro: ½ B 2 H 6 + N(CH 3)3 H 3 B-N(CH 3)3 Los amino-boranos se usan en la preparación de compuestos análogos a los aminoácidos. Dichos compuestos exhiben actividad fisiològica significativa como la inhibiciòn tumoral y la reducciòn del colesterol.
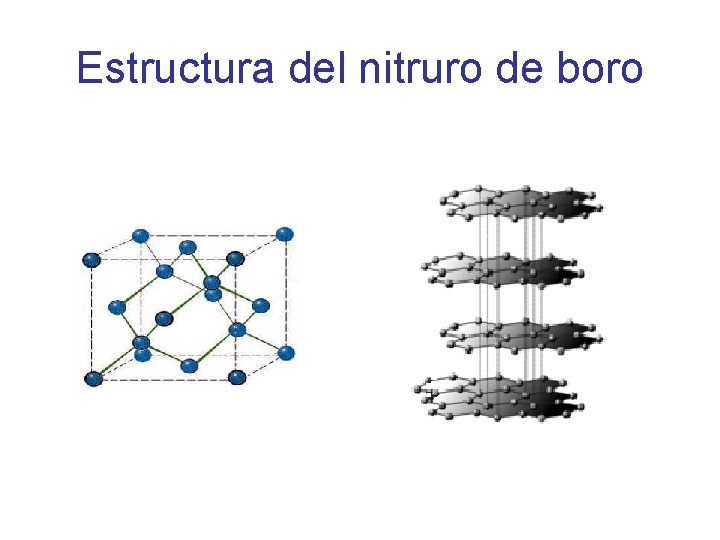
Estructura del nitruro de boro

Compuestos con oxígeno El óxido de boro más importante es el óxido bórico (B 2 O 3). Esta sustancia es el anhídrido del ácido bórico H 3 BO 3 o B(OH)3. El ácido bórico es un ácido tan débil (Ka = 5. 8 x 10 -10) que se emplean soluciones de este ácido para lavados oculares. Cuando se calienta, el ácido bórico pierde agua proceso descrito por la reacción siguiente: 4 H 3 BO 3 (s) → H 2 B 4 O 7(s) + 5 H 2 O (g) El ácido diprótico H 2 B 4 O 7, se llama ácido tetrabórico. Su sal de sodio hidratada Na 2 B 4 O 7*8 H 2 O es el bórax. Las soluciones de bórax son alcalinas, y la sustancia se emplea frecuentemente en productos para lavandería y limpieza.

Boranos Son numerosas las moléculas que contiene únicamente boro e hidrogeno, una familia de compuestos llamados boranos. El borano más sencillo es: BH 3, este compuesto reacciona consigo mismo para formar diborano (B 2 H 6). La consecuencia de esto es que le diborano es una molécula poco usual en cuanto a que los átomos de hidrogeno parecen formar dos enlaces. El diborano es una molécula altamente reactiva, que se inflama espontáneamente en el aire. La reacción es muy exotérmica. B 2 H 6(g) + 3 O 2(g) → B 2 O 3(s) + 3 H 2 O(g) ΔHº = -2030 KJ BH 3 + BH 3 → B 2 H 6 El diborano es usado en propulsores de cohetes, como agente reductor, vulcanizador de caucho, catalizador en la polimerización de hidrocarburos y acelerador de llamas. También es usado en la industria electrónica para conferir propiedades eléctricas a cristales puros.

• Otros boranos, por ejemplo el B 5 H 9 (pentaborano), también son muy reactivos. El B 10 H 14 (decaborano), es estable en el aire a temperatura ambiente, pero sufre una reacción muy exotérmica con O 2 a temperaturas altas. Se ha investigado la posibilidad de usar los boranos como combustibles sólidos para cohetes. La acidez de Brönsted de los hidruros de boro o boranos aumenta , aproximadamente, con el tamaño: B 4 H 10 < B 5 H 9 < B 10 H 14 Esta variación esta relacionada con la mayor deslocalización de la carga en los clusters de mayor tamaño. El boro y el hidrogeno forman además una serie de aniones, llamados aniones boranicos. Las sales de ión borhidruro (BH 4 -) se usan extensamente como agentes reductores. El borhidruro de sodio ( Na. BH 4) es un agente reductor ampliamente utilizado con ciertos compuestos orgánicos.

Aplicaciones • • Las fibras de boro usadas en aplicaciones mecánicas especiales, en el ámbito aeroespacial, alcanzan resistencias mecánicas de hasta 3600 MPa. El boro amorfo se usa en fuegos artificiales por su color verde. El ácido bórico se emplea en productos textiles. El boro es usado como semiconductor Los compuestos de boro tienen muchas aplicaciones en la síntesis orgánica y en la fabricación de cristales de borosilicato. Algunos compuestos se emplean como conservantes de la madera, siendo de gran interés su uso por su baja toxicidad. El B-10 se usa en el control de los reactores nucleares, como escudo frente a las radiaciones y en la detección de neutrones. Los hidruros de boro se oxidan con facilidad liberando gran cantidad de energía por lo que se ha estudiado su uso combustible


Propiedades Físicas • Gran potencial estándar de reducción negativo • Reacciona con el O 2 y forma una capa fina de Al 2 O 3 • Magnesio(1. 7 g/cm 3) Aluminio(2. 7 g/cm 3) Hierro(7. 9 g/cm 3) Oro(19. 3 g/cm 3) • Buen conductor del calor • Buen conductor de la corriente eléctrica
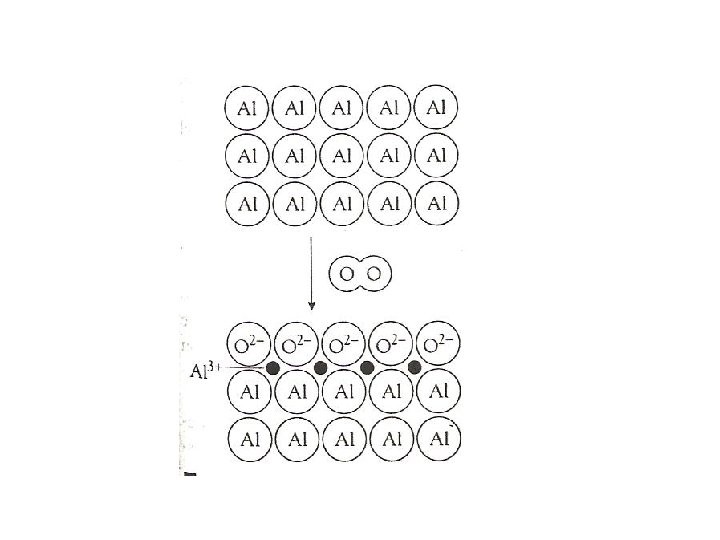

Propiedades Químicas • 4 Al(s) + 3 O 2 (g) 2 Al 2 O 3(s) • 2 Al(s) + 3 Cl 2 (g) 2 Al. Cl 3(s) • 2 Al(s) + 6 H+(ac) • 2 Al(s) + 2 OH-(ac) + 6 H 2 O(l) • [Al(OH 2)6]3+(ac) +H 2 O(l) • [Al(OH 2)5(OH)]2+(ac) + H 2 O(l) [Al(OH 2)4(OH)]+(ac) + H 3 O+(ac) • [Al(OH 2)6]3+(ac) OH- • Al(OH)3 (s) + 3 H+(ac) 2 Al 3+(ac) +3 H 2 (g) OH- 2 [Al(OH)4]-(ac) +3 H 2 (g) [Al(OH 2)5(OH)]2+(ac) + H 3 O+(ac) Al(OH)3(s) [Al(OH)4]-(ac) Al 3+(ac) + 3 H 2 O(l)
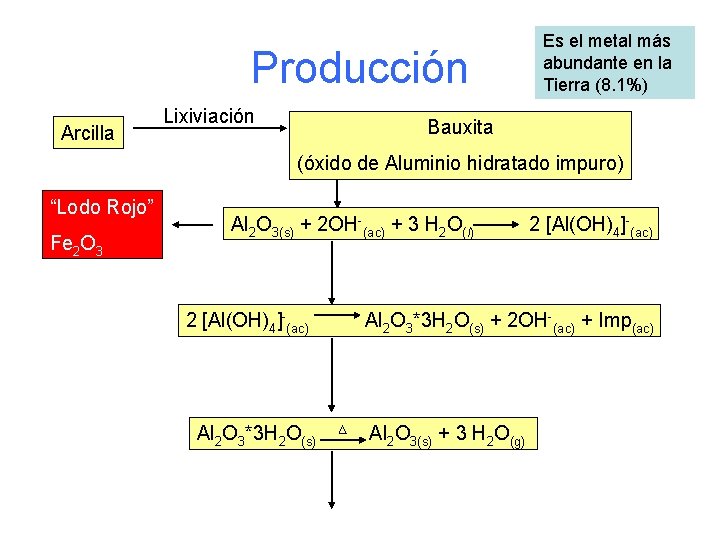
Producción Arcilla Lixiviación Es el metal más abundante en la Tierra (8. 1%) Bauxita (óxido de Aluminio hidratado impuro) “Lodo Rojo” Fe 2 O 3 Al 2 O 3(s) + 2 OH-(ac) + 3 H 2 O(l) 2 [Al(OH)4]-(ac) Al 2 O 3*3 H 2 O(s) + 2 OH-(ac) + Imp(ac) ∆ Al 2 O 3(s) + 3 H 2 O(g)
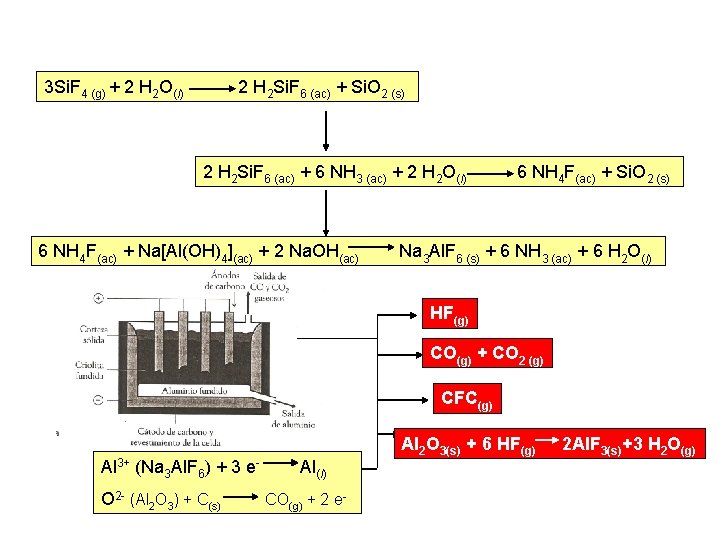
3 Si. F 4 (g) + 2 H 2 O(l) 2 H 2 Si. F 6 (ac) + Si. O 2 (s) 2 H 2 Si. F 6 (ac) + 6 NH 3 (ac) + 2 H 2 O(l) 6 NH 4 F(ac) + Na[Al(OH)4](ac) + 2 Na. OH(ac) 6 NH 4 F(ac) + Si. O 2 (s) Na 3 Al. F 6 (s) + 6 NH 3 (ac) + 6 H 2 O(l) HF(g) CO(g) + CO 2 (g) CFC(g) Al 3+ (Na 3 Al. F 6) + 3 e. O 2 - (Al 2 O 3) + C(s) Al(l) CO(g) + 2 e- Al 2 O 3(s) + 6 HF(g) 2 Al. F 3(s)+3 H 2 O(g)

DATOS Producir: • 1 Kg de Aluminio Consume: • 2 Kg Al 2 O 3 • 0. 6 Kg de carbono • 0. 1 Kg Criolita • 16 k. Wh de electricidad La obtención de: • 1 Tonelada de aluminio Produce: • 1 Kg CF 4 • 0. 1 Kg C 2 F 6
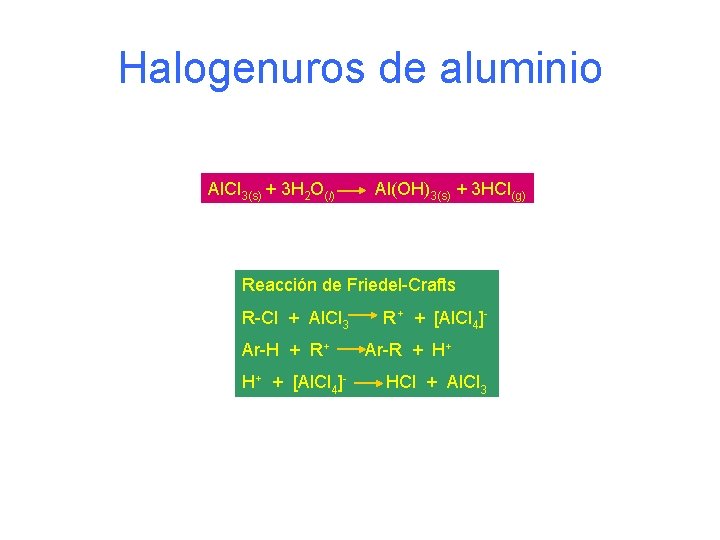
Halogenuros de aluminio Al. Cl 3(s) + 3 H 2 O(l) Al(OH)3(s) + 3 HCl(g) Reacción de Friedel-Crafts R-Cl + Al. Cl 3 Ar-H + R+ H+ + [Al. Cl 4]- R+ + [Al. Cl 4]Ar-R + H+ HCl + Al. Cl 3

Sulfato de Aluminio y Potasio (Alumbre) • Único mineral de aluminio común soluble en agua USOS • Permite la absorción permanente de un colorante sobre una tela • Detiene hemorragias (causa la coagulación de las proteínas en la superficie de las células sin matar las células)

GALIO El galio es el más abundante que los elementos litio, boro, plomo, etc. Es un elemento caro por que se encuentra muy disperso en los minerales de aluminio y de hierro. El galio, que se encuentra en cantidades de trazas en la bauxita (Al 2 O 3. x. H 2 O), se obtiene como subproducto en la refinación del aluminio. El galio es difícil de recuperar, por que las propiedades químicas de Ga 3+, Al 3+ y Fe 3+ son semejantes, debido a que tienen radios y propiedades ácido- base semejantes. Se parece al aluminio al formar óxidos y sales trivalentes, pero también unos pocos compuestos monovalentes y divalentes. Se oxida en el aire y en el agua, reacciona con los ácidos clorhídrico y nítrico y se disuelven en las soluciones alcalinas desprendiendo hidrógeno.

La reacción directa del galio con los halógenos da el haluro, este metal electropositivo reaccionan también con HCl o HBr gaseosos. 2 Ga (S) + 6 HCl (g) 2 Al. Cl 3 (s) + 3 H 2 (g) Los haluros del Ga(I) y Ga (II), como Ga. Cl y Ga. Cl 2, se pueden preparar mediante una reacción de comproporción en la que los haluros de Ga (III) se calienta con Ga metalico: 2 Ga. X 3 + Ga 3 Ga. X 2 X = Cl, Br, o I pero no F El estado de oxidación +1 es mas frecuente para el elemento más pesado galio em compuestos sólidos tales como Ga. I y Ga(Al. Cl 4) el galio (I) tiene mucho en común com el indio (I): 3 MX (s) 2 M (s) + M 3+ (aq) + 3 X- (aq) M = Ga, In

USOS La principal aplicación del galio (arseniuro de galio) es la construcción de circuitos integrados. El Ga 72 se emplea en el diagnóstico y terapia de tumores óseos. Se utiliza en aleaciones con bajo puno de fusión. Con hierro, litio, magnesio y gadolinio forma metales magnéticos. El galio se utiliza para la detección de neutrinos solares.

INDIO Metal blanco plateado, muy blando 3+ Fácilmente fundible Descubierto en 1863 El nombre proviene de la línea de color azul "índigo" característica de este elemento en un espectro Ferdinand Reich y Theodor Richter

OBTENCION Producción principal a partir de residuos de cinc Principal productor Se obtiene mediante la electrolisis de sus sales

USOS
Fosfuro de Indio: Trasmite la luz en una mezcla Indio-Fosforo Mejoró el azul en las pantallas Anti reflejante Trasmisión de luz laser

Tl Talio

Obtención • Elemento escaso; puede ser recuperado de las cenizas de chimeneas resultantes de la combustión de piritas y otros minerales sulfatados.

Tl. I – Tl. III • Tl+ ese presenta en disolución • Disolución única y lenta en H 2 SO 4 y HCl • Óxidos: sólo da lugar Tl 2 O 3; se descompone en Tl 2 O a 100 o. C

Reacciones • 2 Tl(s) + O 2(g) → Tl 2 O(s) • 2 Tl(s) + 2 H 2 O(l) → 2 Tl. OH(aq) + H 2(g) • 2 Tl(s) + 3 F 2(g) → 2 Tl. F 3(s) [] • 2 Tl(s) + 3 Cl 2(g) → 2 Tl. Cl 3(s) [] • 2 Tl(s) + 3 Br 2(l) → 2 Tl. Br 3(s) []

Algunas tiosales • -Tl 2 SO 4 • -Tl 2 CO 3 • -Tl. CO 2 CH 3

Usos • Se utiliza en raras ocasiones, excepto para la fabricación de calidades especiales de vidrio. En el pasado, los compuestos de talio encontraron aplicaciones tan diversas como veneno o golosina para ratas, lociones capilares, insecticidas.

• Aleado con mercurio forma una aleación líquida que congela a -60°C y se utiliza para termómetros de bajas temperaturas. El sulfato de talio, que es inodoro, insípido y muy venenoso, se usa para exterminar roedores e insectos.

• El sulfuro de talio se emplea en la fabricación de células fotoeléctricas sensibles a las radiaciones infrarrojas. En algunos sistemas militares de comunicación se han utilizado los cristales de bromoyoduro de talio como transmisores de la radiación infrarroja y los cristales de oxisulfuro de talio como receptores de la misma.

• En algunos equipos portátiles de escintilación se usan cristales de yoduro de sodio activados con talio para detectar radiación gamma. Las sales de talio se utilizan también para dar color verde a los fuegos de artificio.
- Slides: 36