BONDIO ONIG ADEILEDD A BONDIO Mae priodweddau ffisegol

BONDIO ÏONIG

ADEILEDD A BONDIO Mae priodweddau ffisegol sylwedd yn dibynnu ar ei adeiledd a’i fondio. Bondio sy’n pennu math yr adeiledd. Damcaniaeth sylfaenol • nwyon nobl (He, Ne, Ar, Kr, Xe a Rn) i gyd yn gymharol, neu’n gwbl, anadweithiol • mae hyn oherwydd eu hadeiledd electronol sy’n rhoi sefydlogrwydd • mae atomau heb adeiledd electronol nwy nobl yn ceisio cael un • mae amrywiaeth o ffyrdd ar gael yn ôl safle elfen yn y tabl cyfnodol.

ADEILEDD A BONDIO s. Mae priodweddau ffisegol sylwedd yn dibynnu ar ei adeiledd a’i fondio. Bondio sy’n pennu math yr adeiledd. MATHAU O FONDIO CEMEGOL bondiau cryf FFISEGOL bondiau gwan ïonig (neu electrofalent) cofalent datif (neu gyd-drefnol) metelig grymoedd van der Waals rhyngweithiad deupol-deupol bondiau hydrogen - gwannaf - cryfaf

Y BOND ÏONIG Mae bondiau ïonig yn tueddu i gael eu ffurfio rhwng elfennau sydd angen “colli” electronau ar eu hatomau i gael yr un ffurfwedd electronol â’r nwy nobl agosaf, a rhai sydd angen ennill electronau. Trosglwyddir yr electronau o’r naill atom i’r llall.
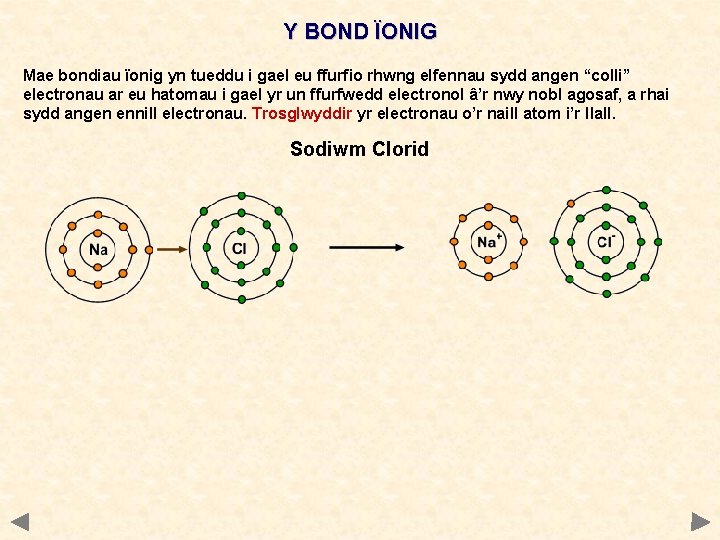
Y BOND ÏONIG Mae bondiau ïonig yn tueddu i gael eu ffurfio rhwng elfennau sydd angen “colli” electronau ar eu hatomau i gael yr un ffurfwedd electronol â’r nwy nobl agosaf, a rhai sydd angen ennill electronau. Trosglwyddir yr electronau o’r naill atom i’r llall. Sodiwm Clorid
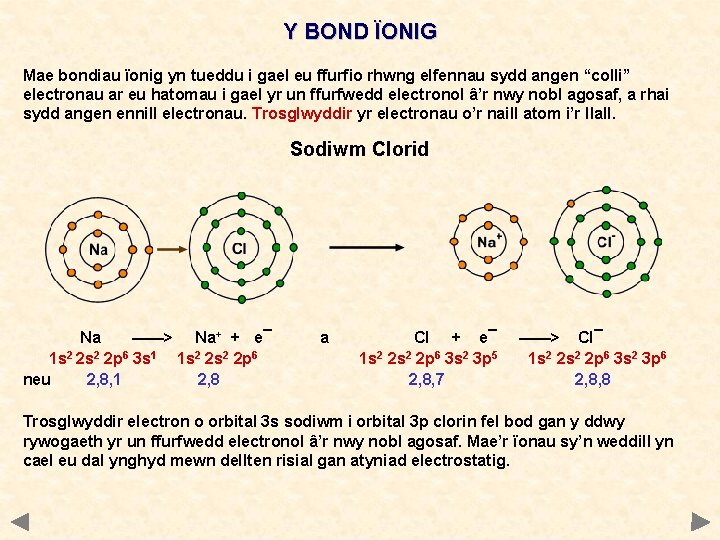
Y BOND ÏONIG Mae bondiau ïonig yn tueddu i gael eu ffurfio rhwng elfennau sydd angen “colli” electronau ar eu hatomau i gael yr un ffurfwedd electronol â’r nwy nobl agosaf, a rhai sydd angen ennill electronau. Trosglwyddir yr electronau o’r naill atom i’r llall. Sodiwm Clorid Na ——> Na+ + e¯ 1 s 2 2 p 6 3 s 1 1 s 2 2 p 6 neu 2, 8, 1 2, 8 a Cl + e¯ 1 s 2 2 p 6 3 s 2 3 p 5 2, 8, 7 ——> Cl¯ 1 s 2 2 p 6 3 s 2 3 p 6 2, 8, 8 Trosglwyddir electron o orbital 3 s sodiwm i orbital 3 p clorin fel bod gan y ddwy rywogaeth yr un ffurfwedd electronol â’r nwy nobl agosaf. Mae’r ïonau sy’n weddill yn cael eu dal ynghyd mewn dellten risial gan atyniad electrostatig.
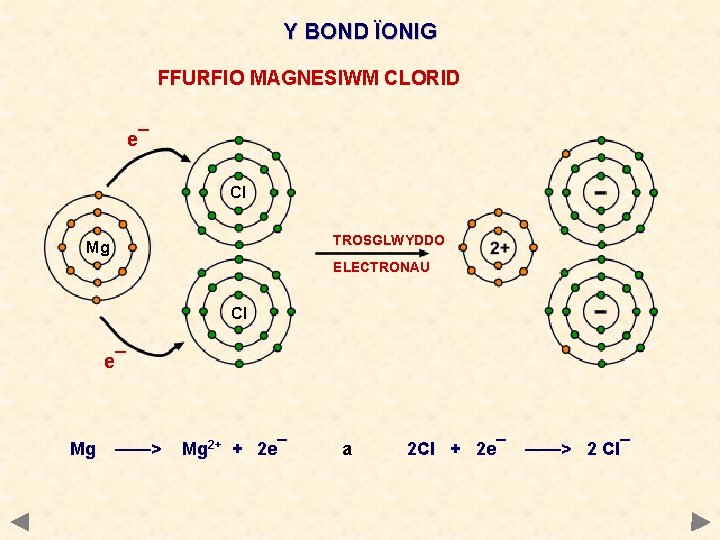
Y BOND ÏONIG FFURFIO MAGNESIWM CLORID e¯ Cl TROSGLWYDDO Mg ELECTRONAU Cl e¯ Mg ——> Mg 2+ + 2 e¯ a 2 Cl + 2 e¯ ——> 2 Cl¯

FFURFIO ÏONAU Ïonau Positif • fe’u gelwir hefyd yn gatïonau; maent yn llai na’r atom gwreiddiol. • fe’u ffurfir pan dynnir electronau oddi ar atomau. • gelwir yr egni sy’n gysylltiedig â’r broses yn egni ïoneiddiad (E. Ï). EGNI ÏONEIDDIAD 1 af Yr egni sydd ei angen i dynnu un môl o electronau (i anfeidredd) oddi ar un môl o atomau nwyol i ffurfio un môl o ïonau positif nwyol. e. e. Na(n) ——> Na+(n) + e¯ neu Mg(n) ——> Mg+(n) + e¯ Pwyntiau eraill Mae’r egnïon ïoneiddiad olynol yn mynd yn fwy wrth i’r gymhareb proton : electron gynyddu. Ceir neidiau mawr mewn gwerth pan dynnir electronau oddi ar y plisg sydd agosaf at y niwclews oherwydd bod llai o gysgodi a bod angen mwy o egni i oresgyn yr atyniad. Os yw’r gwerthoedd E. Ï yn uchel iawn, ceir bondio cofalent (e. e. beryliwm).

FFURFIO ÏONAU Ïonau Negatif • • • fe’u gelwir yn anïonau yn fwy na’r atom gwreiddiol oherwydd gwrthyriad yr electronau yn y plisgyn allanol fe’u ffurfir pan ychwanegir electronau at atomau rhyddheir egni wrth i’r niwclews dynnu electron i mewn affinedd electronol yw’r egni hwn. AFFINEDD ELECTRONOL Y newid yn yr egni pan fydd un môl o atomau nwyol yn ennill un môl o electronau (o anfeidredd) i ffurfio un môl o ïonau negatif nwyol. e. e. Cl(n) + e¯ ——> Cl¯(n) a O(n) + e¯ ——> O¯(n) Po fwyaf y wefr niwclear effeithiol (GNE), hawsaf yw tynnu’r electron i mewn.

BONDIO ÏONIG Animeiddiadau
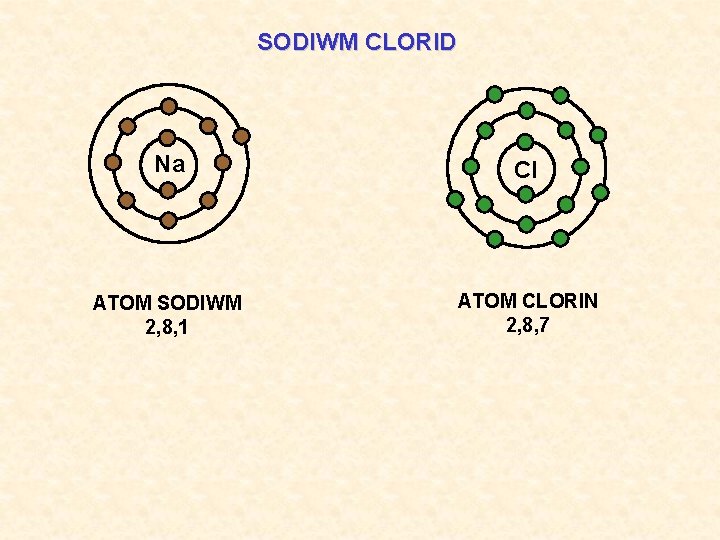
SODIWM CLORID Na Cl ATOM SODIWM 2, 8, 1 ATOM CLORIN 2, 8, 7

SODIWM CLORID Na+ Cl ÏON SODIWM 2, 8 ÏON CLORIN 2, 8, 8 Bellach, mae gan y ddwy rywogaeth blisg allanol ‘llawn’, h. y. mae ganddynt ffurfwedd electronol nwy nobl
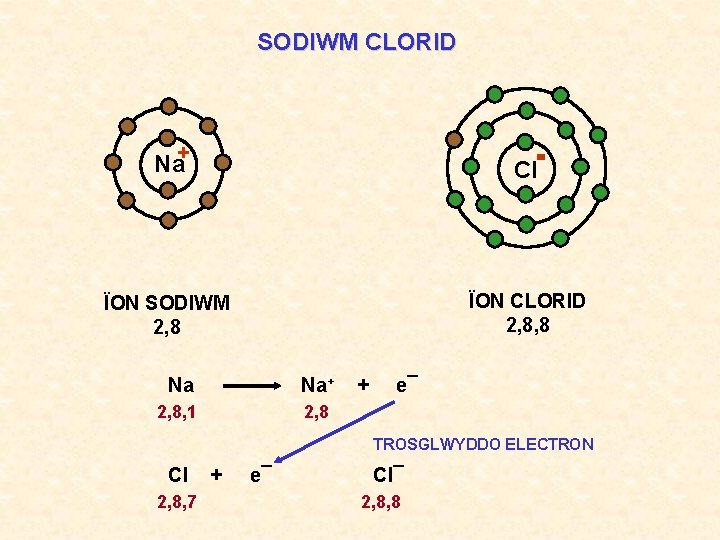
SODIWM CLORID Na+ Cl ÏON SODIWM 2, 8 ÏON CLORID 2, 8, 8 Na Na+ 2, 8, 1 2, 8 + e¯ TROSGLWYDDO ELECTRON Cl 2, 8, 7 + e¯ Cl¯ 2, 8, 8
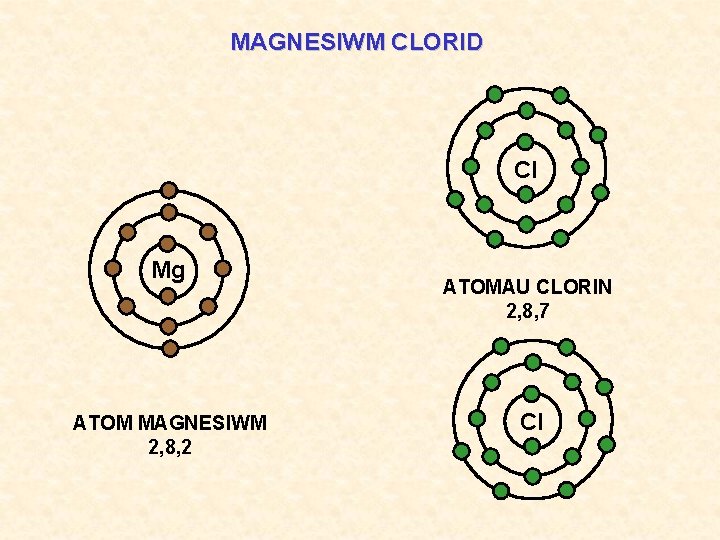
MAGNESIWM CLORID Cl Mg ATOM MAGNESIWM 2, 8, 2 ATOMAU CLORIN 2, 8, 7 Cl
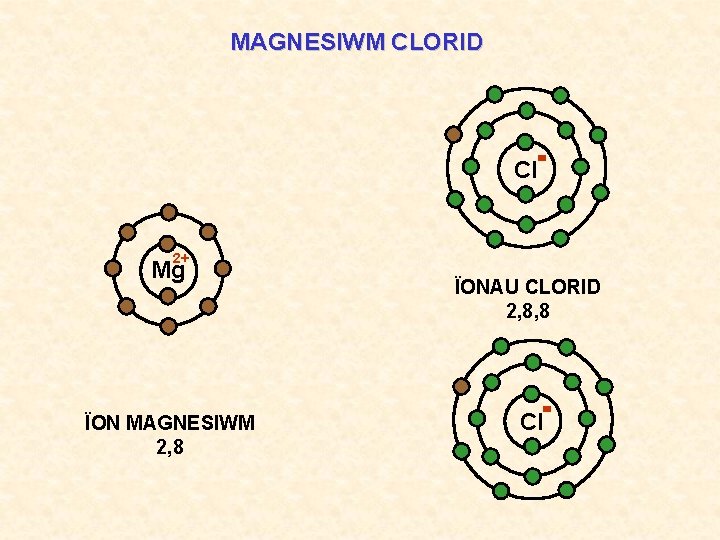
MAGNESIWM CLORID Cl 2+ Mg ÏON MAGNESIWM 2, 8 ÏONAU CLORID 2, 8, 8 Cl
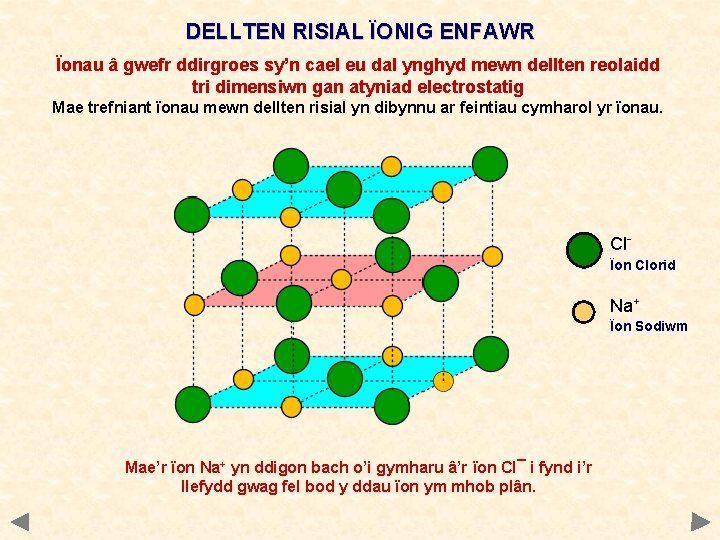
DELLTEN RISIAL ÏONIG ENFAWR Ïonau â gwefr ddirgroes sy’n cael eu dal ynghyd mewn dellten reolaidd tri dimensiwn gan atyniad electrostatig Mae trefniant ïonau mewn dellten risial yn dibynnu ar feintiau cymharol yr ïonau. ClÏon Clorid Na+ Ïon Sodiwm Mae’r ïon Na+ yn ddigon bach o’i gymharu â’r ïon CI¯ i fynd i’r llefydd gwag fel bod y ddau ïon ym mhob plân.
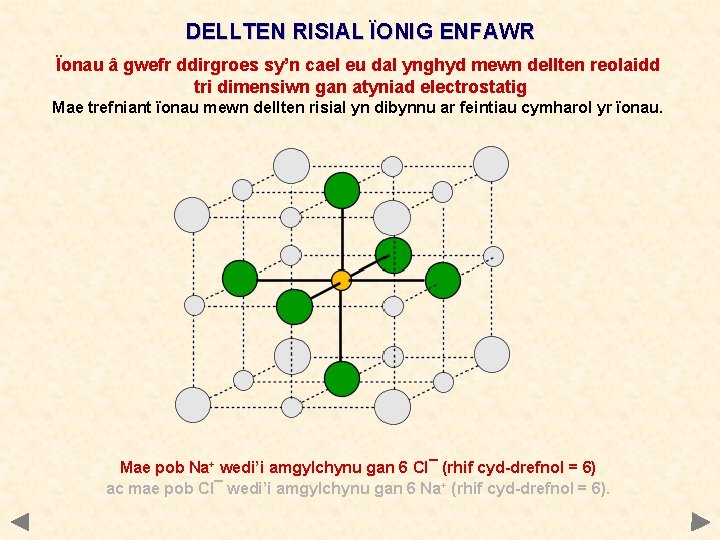
DELLTEN RISIAL ÏONIG ENFAWR Ïonau â gwefr ddirgroes sy’n cael eu dal ynghyd mewn dellten reolaidd tri dimensiwn gan atyniad electrostatig Mae trefniant ïonau mewn dellten risial yn dibynnu ar feintiau cymharol yr ïonau. Mae pob Na+ wedi’i amgylchynu gan 6 Cl¯ (rhif cyd-drefnol = 6) ac mae pob Cl¯ wedi’i amgylchynu gan 6 Na+ (rhif cyd-drefnol = 6).

Priodweddau ffisegol cyfansoddion ïonig Ymdoddbwynt Uchel iawn Cryfder Bregus iawn Rhaid cael cryn dipyn o egni i oresgyn yr atyniadau electrostatig cryf a gwahanu’r ïonau. Mae unrhyw ddadleoli yn golygu bod yr haenau yn symud ac ïonau sydd â gwefr debyg wrth ymyl ei gilydd. Mae’r gwrthyriad yn hollti’r grisial. Trydanol Ddim yn dargludo yn eu ffurf solid – mae’r ïonau wedi’u dal ynghyd yn gryf yn y ddellten. Dargludo yn eu ffurf tawdd neu mewn hydoddiant dyfrllyd – mae’r ïonau yn symudol ac yn dargludo. Hydoddedd Anhydawdd mewn hydoddyddion amholar ond yn hydawdd mewn dŵr. Dŵr oherwydd ei fod yn hydoddydd polar ac yn sefydlogi’r ïonau sydd wedi’u gwahanu. Mae angen cryn dipyn o egni i oresgyn yr atyniad electrostatig a gwahanu’r ïonau. Mae’r sefydlogrwydd a geir o gael eu hamgylchynu gan foleciwlau dŵr polar yn gwneud iawn am hyn.
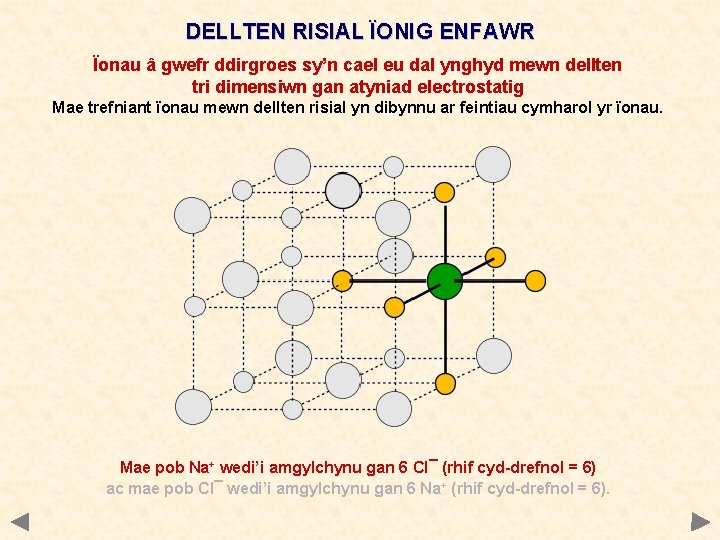
DELLTEN RISIAL ÏONIG ENFAWR Ïonau â gwefr ddirgroes sy’n cael eu dal ynghyd mewn dellten tri dimensiwn gan atyniad electrostatig Mae trefniant ïonau mewn dellten risial yn dibynnu ar feintiau cymharol yr ïonau. Mae pob Na+ wedi’i amgylchynu gan 6 Cl¯ (rhif cyd-drefnol = 6) ac mae pob Cl¯ wedi’i amgylchynu gan 6 Na+ (rhif cyd-drefnol = 6).
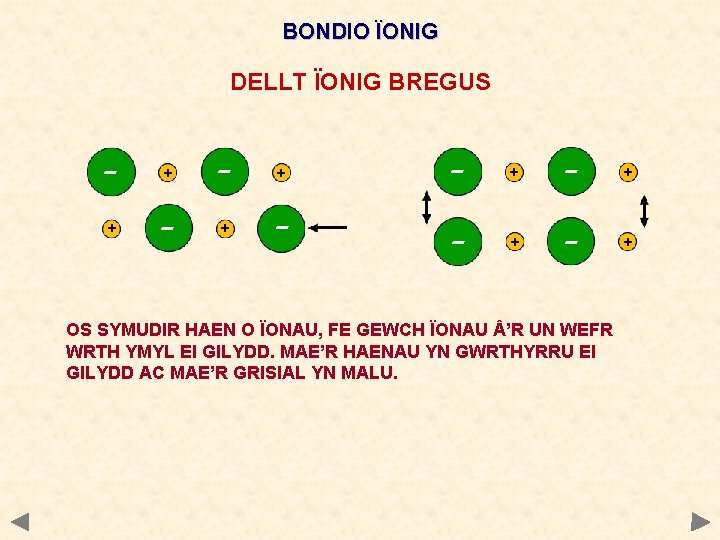
BONDIO ÏONIG DELLT ÏONIG BREGUS - + + - - + - + OS SYMUDIR HAEN O ÏONAU, FE GEWCH ÏONAU ’R UN WEFR WRTH YMYL EI GILYDD. MAE’R HAENAU YN GWRTHYRRU EI GILYDD AC MAE’R GRISIAL YN MALU.
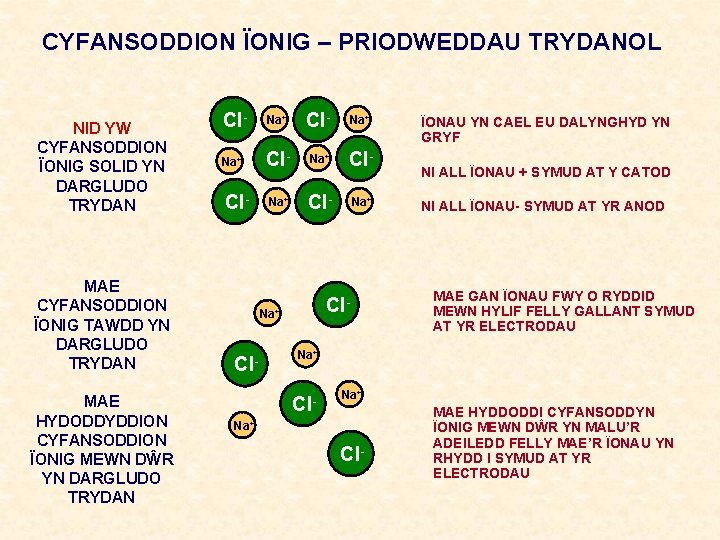
CYFANSODDION ÏONIG – PRIODWEDDAU TRYDANOL NID YW CYFANSODDION ÏONIG SOLID YN DARGLUDO TRYDAN MAE CYFANSODDION ÏONIG TAWDD YN DARGLUDO TRYDAN MAE HYDODDYDDION CYFANSODDION ÏONIG MEWN DŴR YN DARGLUDO TRYDAN Cl- Na+ Na+ Cl- Cl- Na+ Cl- ÏONAU YN CAEL EU DALYNGHYD YN GRYF NI ALL ÏONAU + SYMUD AT Y CATOD NI ALL ÏONAU- SYMUD AT YR ANOD MAE GAN ÏONAU FWY O RYDDID MEWN HYLIF FELLY GALLANT SYMUD AT YR ELECTRODAU Na+ Cl- MAE HYDDODDI CYFANSODDYN ÏONIG MEWN DŴR YN MALU’R ADEILEDD FELLY MAE’R ÏONAU YN RHYDD I SYMUD AT YR ELECTRODAU
- Slides: 21