BOLILLA 2 TRANSPORTE ELECTRONICO y FOSFORILACION OXIDATIVA Cadena


BOLILLA 2 • TRANSPORTE ELECTRONICO y FOSFORILACION OXIDATIVA • Cadena Respiratoria. Complejos. Inhibidores y desacoplantes. Síntesis de ATP. Translocasas • OTROS SISTEMAS DE TRANSPORTE: Sistema Microsomal. Oxigenasas. Catalasas • Formacion de species reactivas del oxígeno: Radicales libres. Sistemas de protección
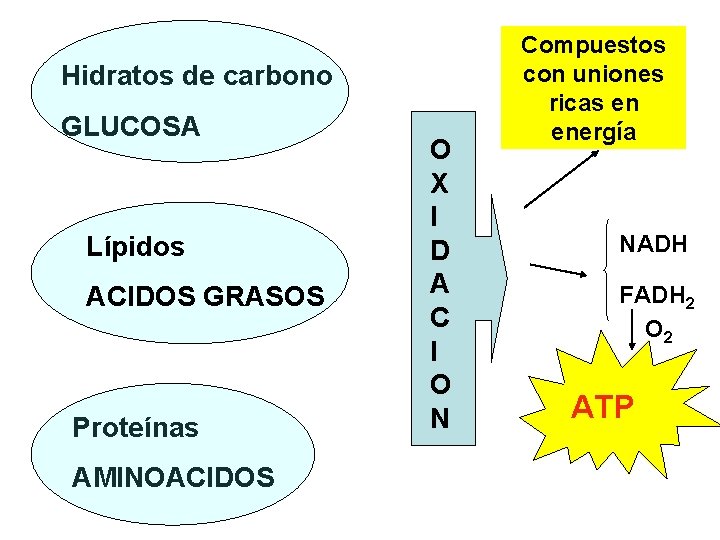
Hidratos de carbono GLUCOSA Lípidos ACIDOS GRASOS Proteínas AMINOACIDOS O X I D A C I O N Compuestos con uniones ricas en energía NADH FADH 2 O 2 ATP
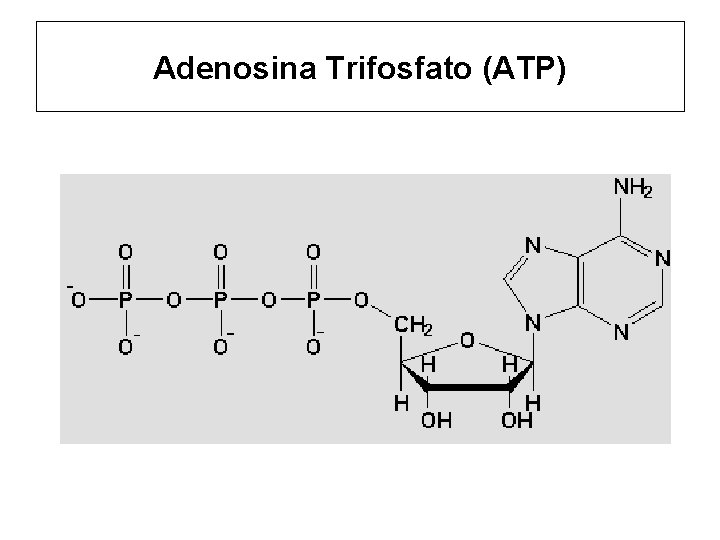
Adenosina Trifosfato (ATP)
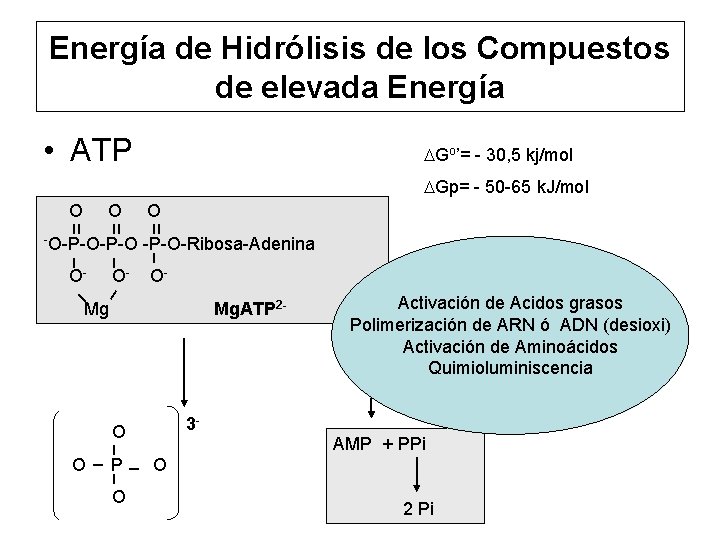
Energía de Hidrólisis de los Compuestos de elevada Energía • ATP DGo’= - 30, 5 kj/mol DGp= - 50 -65 k. J/mol O ו P ו O ו O O O װ װ װ -O-P-O-Ribosa-Adenina ו - ו O O O ו ו Mg Mg. ATP 2 - 3 - Activación de Acidos grasos Polimerización de ARN ó ADN (desioxi) Activación de Aminoácidos Quimioluminiscencia AMP + PPi O 2 Pi
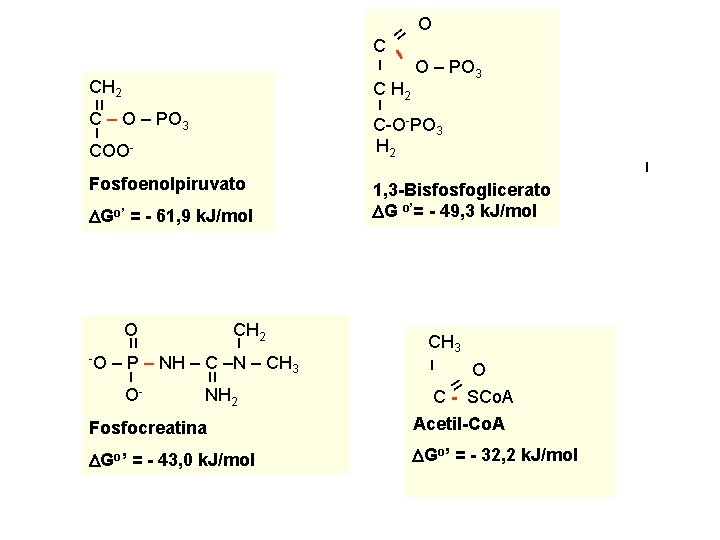
װ CH 2 װ C – O – PO 3 ו COOFosfoenolpiruvato DGo’ = - 61, 9 k. J/mol O CH 2 װ ו -O – P – NH – C –N – CH 3 ו װ ONH 2 O C ו ו O – PO 3 C H 2 ו C-O-PO 3 H 2 1, 3 -Bisfosfoglicerato DG o’= - 49, 3 k. J/mol DGo’ = - 43, 0 k. J/mol DGo’ = - 32, 2 k. J/mol װ Fosfocreatina CH 3 ו O C - SCo. A Acetil-Co. A ו
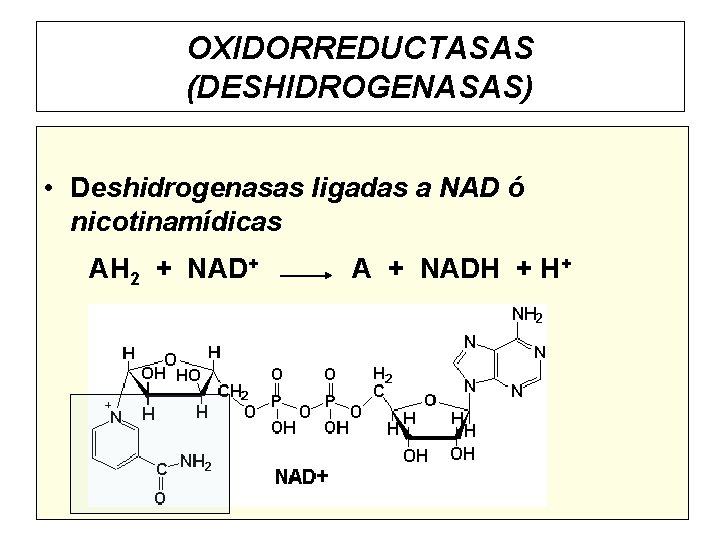
OXIDORREDUCTASAS (DESHIDROGENASAS) • Deshidrogenasas ligadas a NAD ó nicotinamídicas AH 2 + NAD+ A + NADH + H+
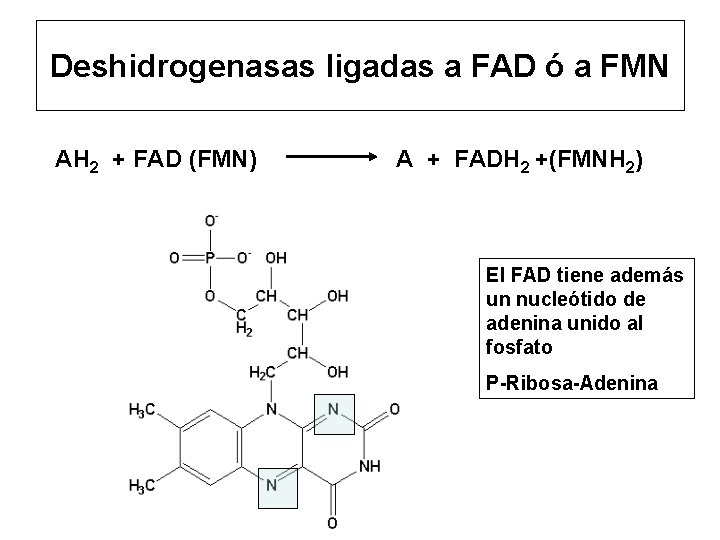
Deshidrogenasas ligadas a FAD ó a FMN AH 2 + FAD (FMN) A + FADH 2 +(FMNH 2) El FAD tiene además un nucleótido de adenina unido al fosfato P-Ribosa-Adenina
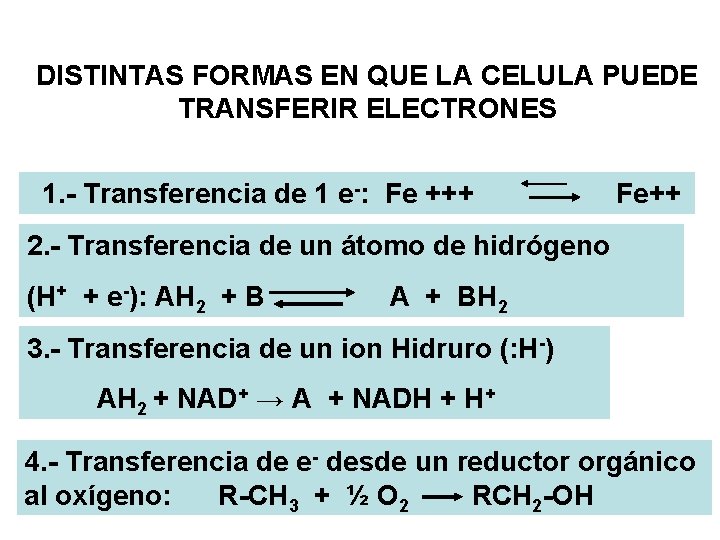
DISTINTAS FORMAS EN QUE LA CELULA PUEDE TRANSFERIR ELECTRONES 1. - Transferencia de 1 e-: Fe +++ Fe++ 2. - Transferencia de un átomo de hidrógeno (H+ + e-): AH 2 + B A + BH 2 3. - Transferencia de un ion Hidruro (: H-) AH 2 + NAD+ → A + NADH + H+ 4. - Transferencia de e- desde un reductor orgánico al oxígeno: R-CH 3 + ½ O 2 RCH 2 -OH
MECANISMOS DE SINTESIS DE ATP • FOSFORILACION A NIVEL DE SUSTRATO HIDRÓLISIS DE UNA UNION DE ALTA ENERGIA • FOSFORILACION OXIDATIVA CADENA RESPIRATORIA O 2
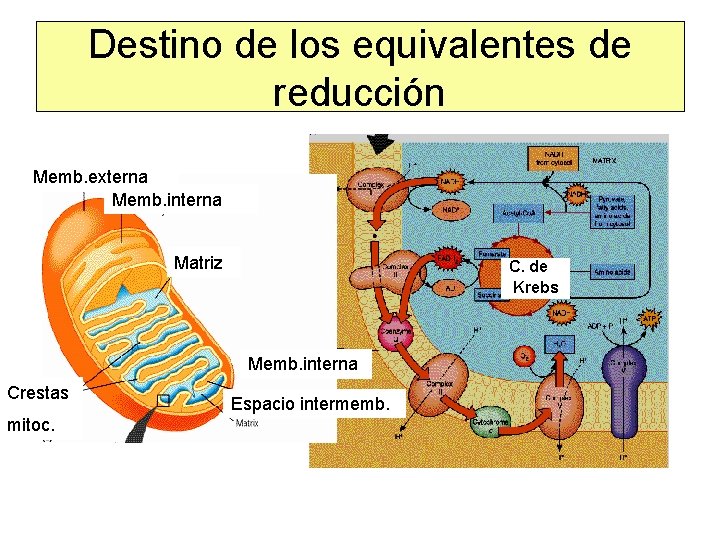
Destino de los equivalentes de reducción Memb. externa Memb. interna Matriz C. de Krebs Memb. interna Crestas mitoc. Espacio intermemb.

CADENA DE TRANSPORTE ELECTRONICO • Los componentes de la cadena se encuentran en la membrana mitocondrial interna. • Reciben equivalentes de reducción de NADH Y FADH 2 producidos en la matriz. • Los componentes se encuentran ordenados en orden creciente de sus potenciales de reducción. • El aceptor final de electrones es el oxígeno.

Potenciales de reducción estándar 2 H + + 2 e - → H 2 -0. 42 V NAD+ + H+ + 2 e- → NADH -0. 32 V S + 2 H + + 2 e - → H 2 S -0. 23 V FAD + 2 H+ + 2 e- → FADH 2 -0. 22 V Acetaldehído + 2 H+ + 2 e- → etanol -0. 20 V Piruvato + 2 H+ + 2 e- → lactato -0. 19 V Cu+ → Cu 2+ + e-0. 16 V Citocromo b (Fe 3+) + e- → citocromo b (Fe 2+) + 0. 075 V Citocromo c 1 (Fe 3+) + e- → citocromo c 1 (Fe 2+) + 0. 22 V Citocromo c (Fe 3+) + e- → citocromo c (Fe 2+) + 0. 235 V Citocromo a (Fe 3+) + e- → citocromo a (Fe 2+) + 0. 29 V Fe 3+ + e- → Fe 2+ + 0. 77 V ½ O 2 + 2 H + + 2 e - → H 2 O + 0. 82 V

COMPONENTES DE LA CADENA DE TRANSPORTE ELECTRONICO • FLAVOPROTEINAS: FMN ó FAD: Transportan 2 e- y 2 H+ • PROTEINAS FERROSULFURADAS: transportan e(Fe+++ Fe++) • COENZIMA Q ó UBIQUINONA: Quinona isoprenoide no proteica. Transporta 1 e- y libera 2 H+ a la matriz. • CITOCROMOS b, c, c 1, a, a 3: Proteínas que contienen un grupo hemo. Transportan 1 e-
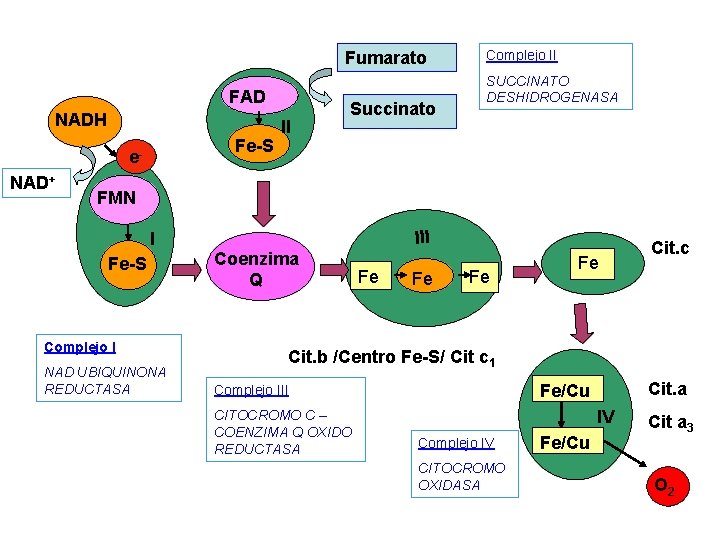
Fumarato FAD NADH Fe-S e. NAD+ II Succinato Complejo II SUCCINATO DESHIDROGENASA FMN I Fe-S Complejo I NAD UBIQUINONA REDUCTASA III Coenzima Q Fe Fe-S Fe Fe Fe Cit. c Cit. b /Centro Fe-S/ Cit c 1 CITOCROMO C – COENZIMA Q OXIDO REDUCTASA Cit. a Fe/Cu Complejo III IV Complejo IV CITOCROMO OXIDASA Fe/Cu Cit a 3 O 2
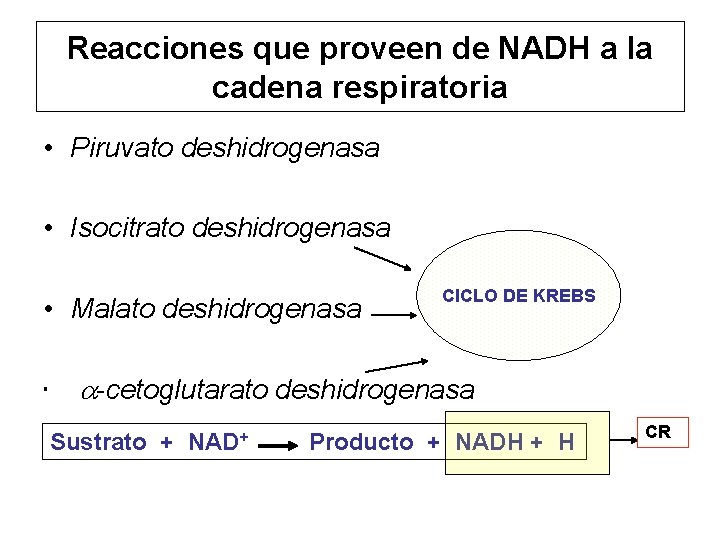
Reacciones que proveen de NADH a la cadena respiratoria • Piruvato deshidrogenasa • Isocitrato deshidrogenasa • Malato deshidrogenasa • CICLO DE KREBS a-cetoglutarato deshidrogenasa Sustrato + NAD+ Producto + NADH + H CR
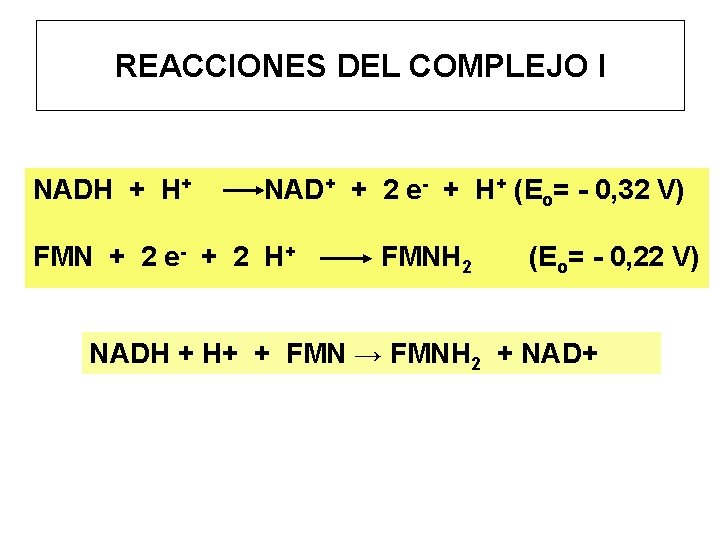
REACCIONES DEL COMPLEJO I NADH + H+ NAD+ + 2 e- + H+ (Eo= - 0, 32 V) FMN + 2 e- + 2 H+ FMNH 2 (Eo= - 0, 22 V) NADH + H+ + FMN → FMNH 2 + NAD+
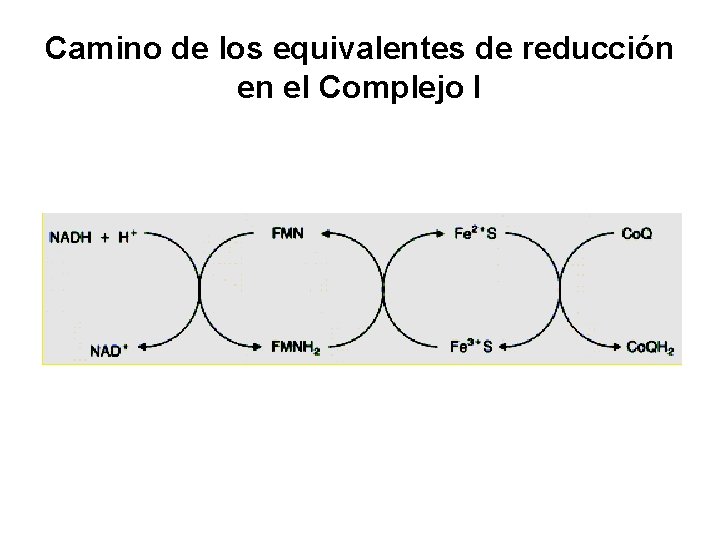
Camino de los equivalentes de reducción en el Complejo I
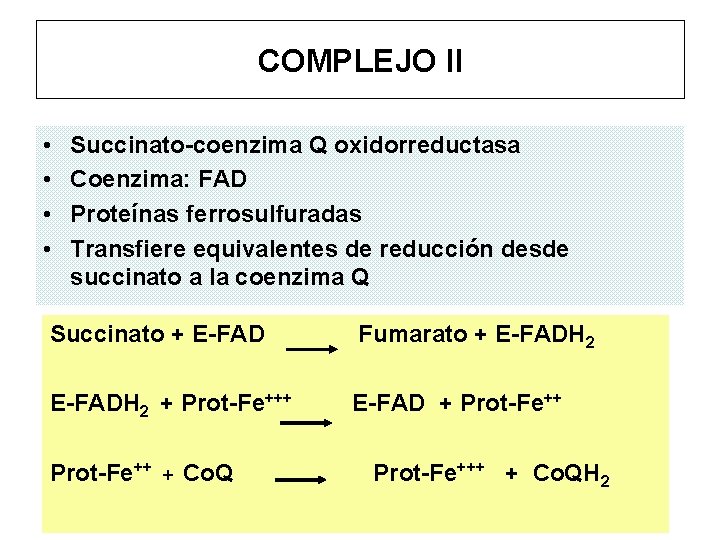
COMPLEJO II • • Succinato-coenzima Q oxidorreductasa Coenzima: FAD Proteínas ferrosulfuradas Transfiere equivalentes de reducción desde succinato a la coenzima Q Succinato + E-FAD Fumarato + E-FADH 2 + Prot-Fe+++ E-FAD + Prot-Fe++ + Co. Q Prot-Fe+++ + Co. QH 2
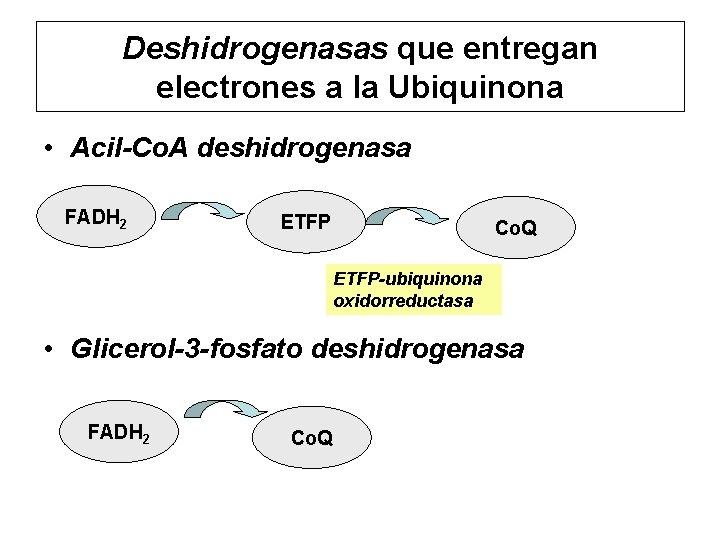
Deshidrogenasas que entregan electrones a la Ubiquinona • Acil-Co. A deshidrogenasa FADH 2 ETFP Co. Q ETFP-ubiquinona oxidorreductasa • Glicerol-3 -fosfato deshidrogenasa FADH 2 Co. Q
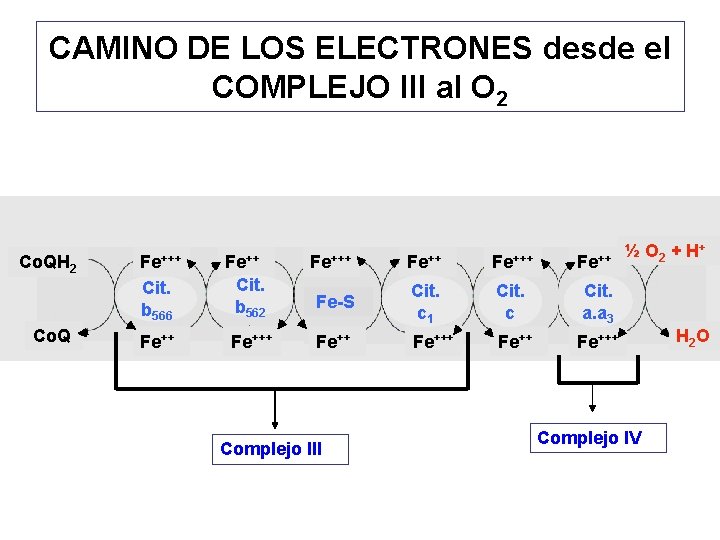
CAMINO DE LOS ELECTRONES desde el COMPLEJO III al O 2 Co. QH 2 Co. Q Fe+++ Fe++ Cit. b 566 Cit. b 562 Fe-S Cit. c 1 Cit. c Cit. a. a 3 Fe+++ Fe+++ Complejo III ½ O 2 + H+ Complejo IV H 2 O
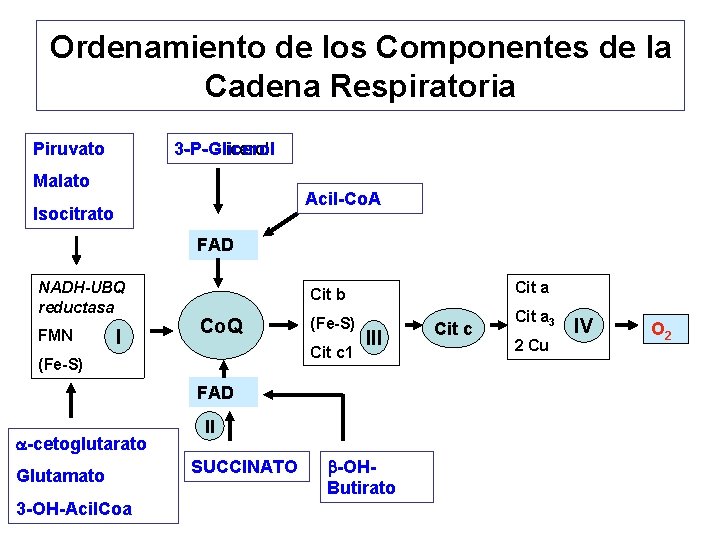
Ordenamiento de los Componentes de la Cadena Respiratoria Piruvato 3 -P-Glicerol Malato Acil-Co. A Isocitrato FAD NADH-UBQ reductasa FMN I Cit a Cit b Co. Q (Fe-S) Cit c 1 (Fe-S) III FAD a-cetoglutarato Glutamato 3 -OH-Acil. Coa II SUCCINATO b-OHButirato Cit c Cit a 3 2 Cu IV O 2
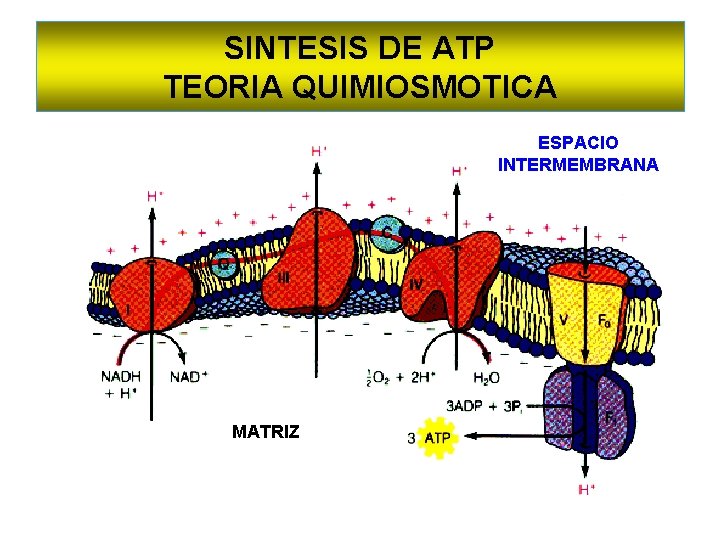
SINTESIS DE ATP TEORIA QUIMIOSMOTICA ESPACIO INTERMEMBRANA MATRIZ
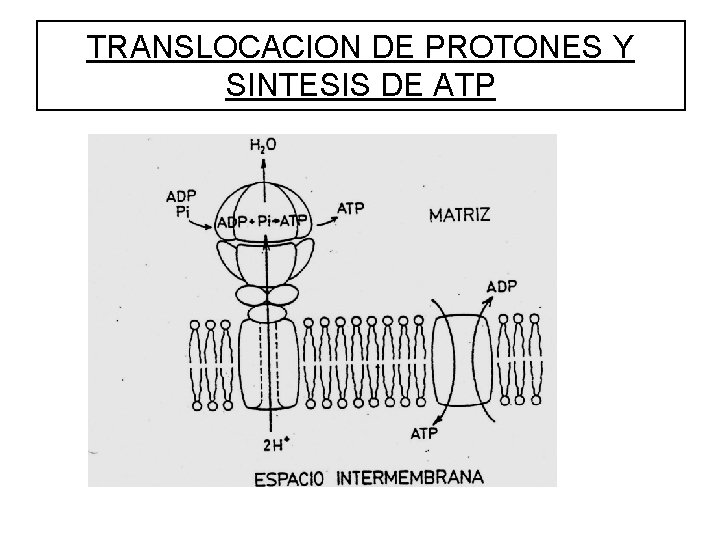
TRANSLOCACION DE PROTONES Y SINTESIS DE ATP

POSTULADOS DE LA TEORIA QUIMIOSMOTICA • Membrana mitocondrial impermeable a protones • Expulsion de H+ durante el transporte de electrones • Formación de un gradiente electroquímico (H+ y cargas positivas) • El pasaje de los H+ a través de Fo activan la ATP sintasa -Complejo I (H+ desde matriz hacia espacio interm. ) -Complejo III (H+ desde matriz, QH 2 y hacia espacio interm. ) Complejo IV (H+ desde matriz hacia espacio interm. )
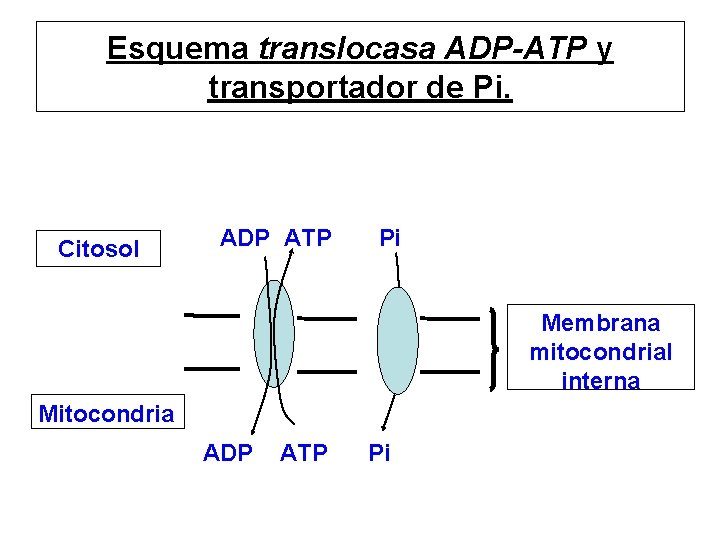
Esquema translocasa ADP-ATP y transportador de Pi. Citosol ADP ATP Pi Membrana mitocondrial interna Mitocondria ADP ATP Pi

INHIBIDORES • Inhibidores del transporte electrónico Inhiben solamente el transporte de e • Inhibidores de la fosforilación Inhiben la síntesis de ATP , indirectamente eel transporte de e • Desacoplantes Impiden la síntesis de ATP pero no inhiben el transporte de electrones • Inhibidores de la translocasa Inhiben la entrada de ADP y la salida de ATP desde la mitocondria
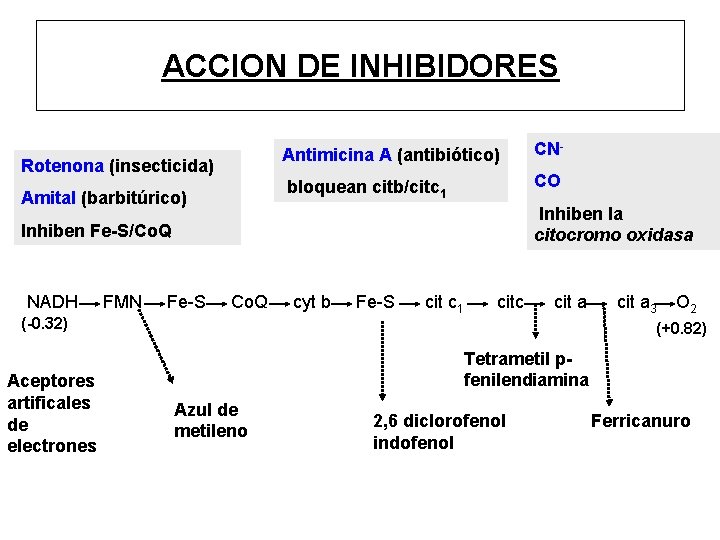
ACCION DE INHIBIDORES Rotenona (insecticida) Amital (barbitúrico) Antimicina A (antibiótico) CN- bloquean citb/citc 1 CO Inhiben la citocromo oxidasa Inhiben Fe-S/Co. Q NADH FMN Fe-S Co. Q (-0. 32) Aceptores artificales de electrones cyt b Fe-S cit c 1 citc cit a 3 O 2 (+0. 82) Tetrametil pfenilendiamina Azul de metileno 2, 6 diclorofenol indofenol Ferricanuro

INHIBIDORES DE LA FOSFORILACIÓN • Oligomicina: Bloquea el flujo de protones a través de Fo. • Se inhibe la síntesis de ATP • Se acumulan protones y se produce una fuerza inversa deteniéndose el transporte de electrones.
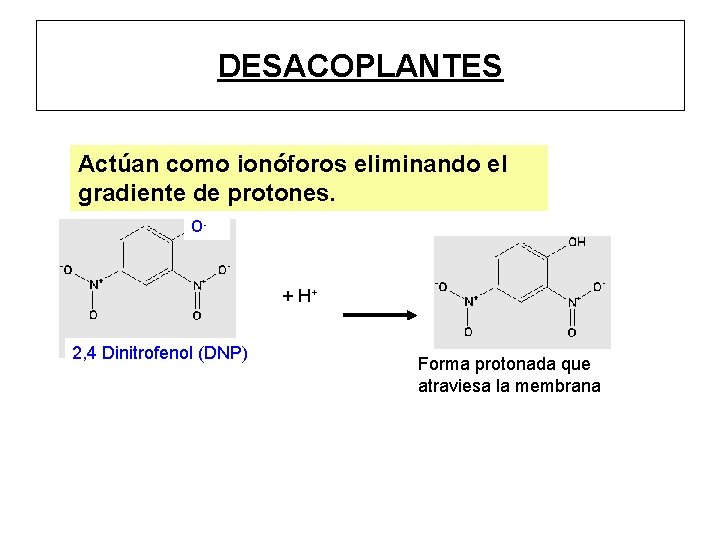
DESACOPLANTES Actúan como ionóforos eliminando el gradiente de protones. O- + H+ 2, 4 Dinitrofenol (DNP) Forma protonada que atraviesa la membrana
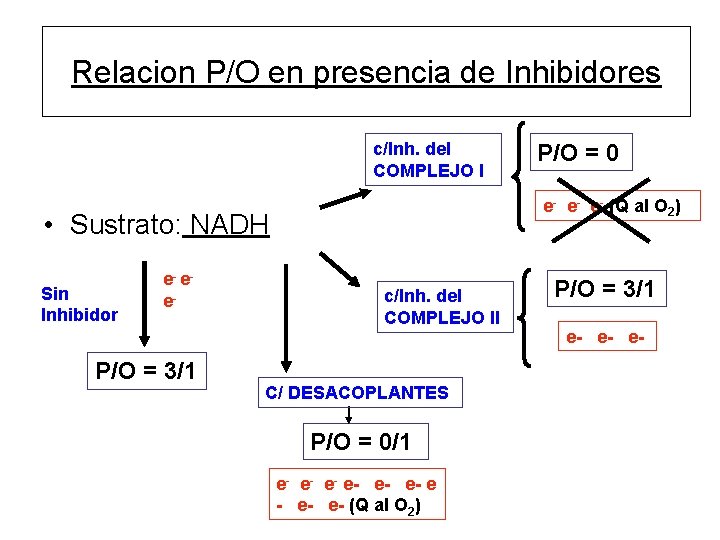
Relacion P/O en presencia de Inhibidores c/Inh. del COMPLEJO I e- e- e- (Q al O 2) • Sustrato: NADH Sin Inhibidor e- ee- P/O = 3/1 P/O = 0 c/Inh. del COMPLEJO II C/ DESACOPLANTES P/O = 0/1 e- e- e- e- (Q al O 2) P/O = 3/1 e- e- e-
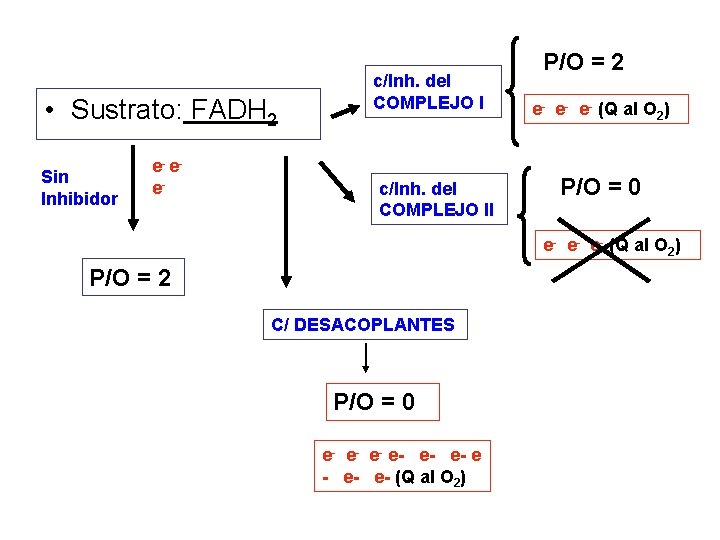
• Sustrato: FADH 2 Sin Inhibidor e- ee- c/Inh. del COMPLEJO II P/O = 2 e- e- e- (Q al O 2) P/O = 0 e- e- e- (Q al O 2) P/O = 2 C/ DESACOPLANTES P/O = 0 e- e- e- e- (Q al O 2)
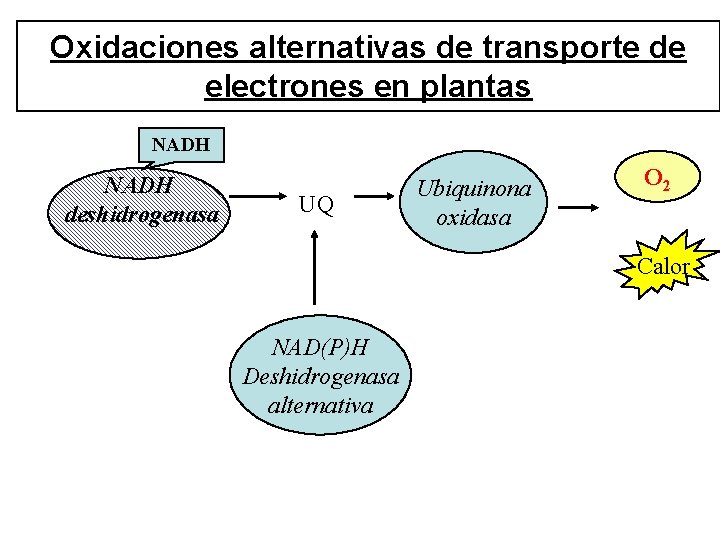
Oxidaciones alternativas de transporte de electrones en plantas NADH deshidrogenasa UQ Ubiquinona oxidasa O 2 Calor NAD(P)H Deshidrogenasa alternativa
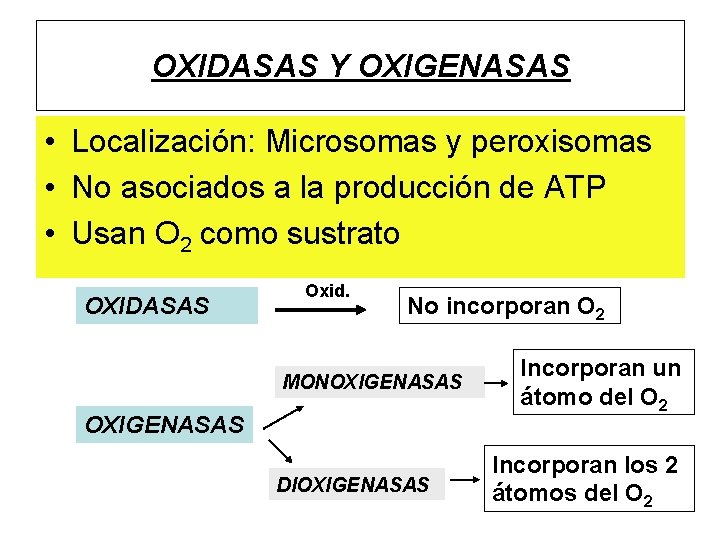
OXIDASAS Y OXIGENASAS • Localización: Microsomas y peroxisomas • No asociados a la producción de ATP • Usan O 2 como sustrato OXIDASAS Oxid. No incorporan O 2 MONOXIGENASAS DIOXIGENASAS Incorporan un átomo del O 2 Incorporan los 2 átomos del O 2
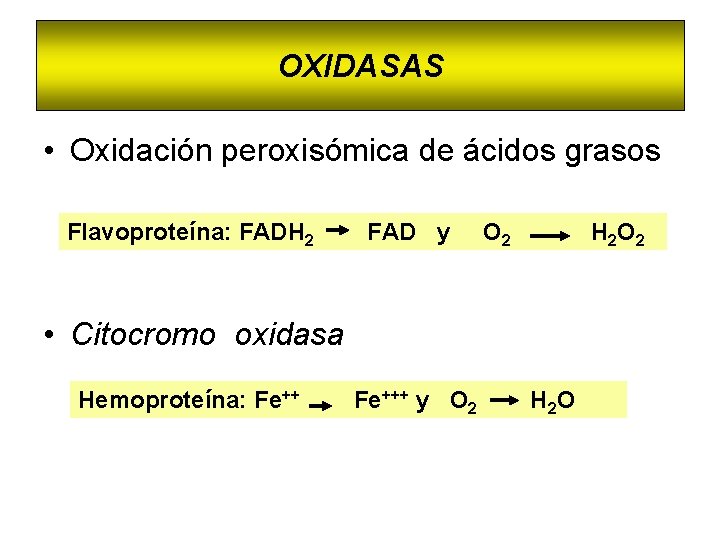
OXIDASAS • Oxidación peroxisómica de ácidos grasos Flavoproteína: FADH 2 FAD y O 2 H 2 O 2 • Citocromo oxidasa Hemoproteína: Fe+++ y O 2 H 2 O
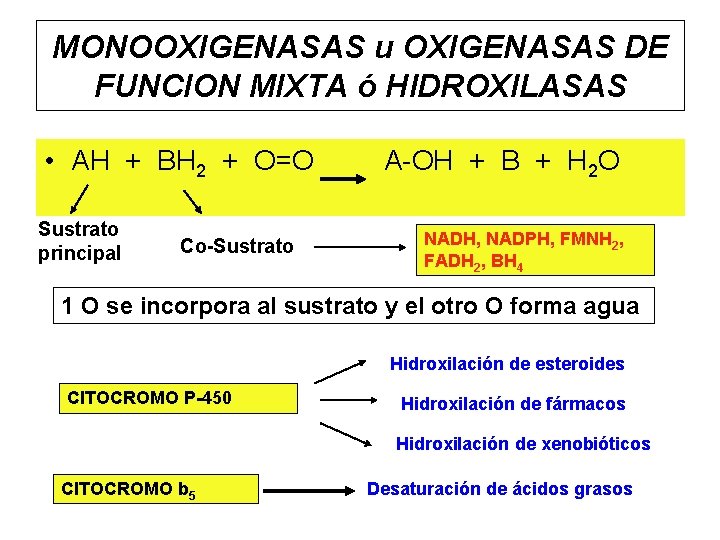
MONOOXIGENASAS u OXIGENASAS DE FUNCION MIXTA ó HIDROXILASAS • AH + BH 2 + O=O Sustrato principal Co-Sustrato A-OH + B + H 2 O NADH, NADPH, FMNH 2, FADH 2, BH 4 1 O se incorpora al sustrato y el otro O forma agua Hidroxilación de esteroides CITOCROMO P-450 Hidroxilación de fármacos Hidroxilación de xenobióticos CITOCROMO b 5 Desaturación de ácidos grasos
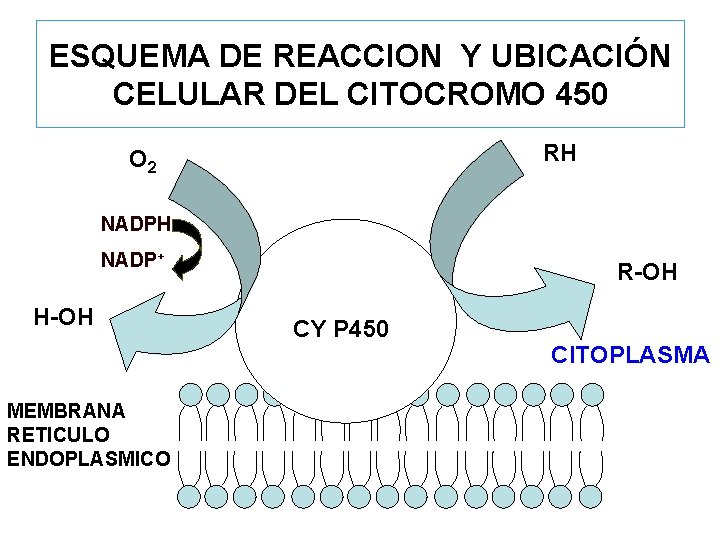
ESQUEMA DE REACCION Y UBICACIÓN CELULAR DEL CITOCROMO 450 RH O 2 NADPH NADP+ H-OH MEMBRANA RETICULO ENDOPLASMICO R-OH CY P 450 CITOPLASMA
- Slides: 37