Bolilla 1 Enzimas Caracteres generales Importancia del estudio

Bolilla 1 Enzimas Caracteres generales. Importancia del estudio de las enzimas en los alimentos. Nomenclatura y clasificación. Coenzimas. Compartimentalización de las enzimas. Cinética enzimática. Factores que afectan la actividad enzimática, temperatura, p. H, actividad de agua, radiaciones ionizantes, etc. Ecuación de Michaelis-Menten. Inhibición de enzimas, competitiva y no competitiva. Enzimas reguladoras. Enzimas alostéricas, modificación por unión covalente. Isoenzimas. Zimógenos. Enzimas endógenas y exógenas.

HISTORIA A fines del siglo XVIII: catalizadores en estudios de la digestión de la carne por secreciones del estómago. • Louis Pasteur, 1850 (fermentos de la levadura) • Eduard Buchner, 1897 (levaduras) • Fredrick Kühne fue el primero en llamar a los fermentos: ENIZMAS • James Summer, 1926 (ureasa) • John Northrop y Moses Kunitz, 1930 (pepsina, tripsina y quimotripsina) Estructura y función • 1963: 1º Secuencia de aminoácidos de la ribonucleasa pancreática bovina A • 1965: 1º Estructura por RX de la Lisozima de clara de huevo de gallina • 1983: Sidney Altman y Col. Observaron que el RNA de la ribonucleasa tiene actividad catalítica.

ENZIMAS - FUNCIÓN En los seres vivos se producen reacciones químicas para: • Transformar los nutrientes de los alimentos para obtenergía. • Transformar nutrientes simples en moléculas complejas y viceversa. • Obtener materia prima para la síntesis de nuevas moléculas. • Degradar componentes celulares una vez cumplida su vida útil. • Extraer energía desde combustibles por oxidación. • Polimerizar subunidades para formar macromoléculas.

Las transformaciones bioquímicas en los seres vivos ocurren: • a gran velocidad • con gran especificidad • en condiciones muy moderadas de temperatura, p. H, presión, etc. Un catalizador es una sustancia capaz de acelerar una reacción química sin formar parte de los productos finales ni desgastarse en el proceso.

ENZIMAS Los catalizadores biológicos son macromoléculas llamadas enzimas La mayoría de las enzimas son proteínas, con la excepción de un pequeño grupo de moléculas de RNA catalítico, llamadas ribozimas. Actividad catalítica: depende de la integridad de su conformación proteica nativa

CARACTERISTICAS DE LAS ENZIMAS PROTEINAS y RNA (Ribozimas): Estructura terciaria y cuaternaria SITIO DE UNION AL SUSTRATO: SUSTRATO Uniones no Covalentes (puente de hidrógeno, hidrofóbicas, electrostáticas) NECESITAN DE FACTORES ENZIMATICOS: ENZIMATICOS Inorgánicos (metales) y orgánicos (Coenzimas) ESPECIFICIDAD DE SUSTRATO: SUSTRATO Estéreo-especificidad y especificidad geométrica SON REGULABLES: REGULABLES La síntesis de la proteína, su actividad y degradación.

DISTRIBUCION DE LAS ENZIMAS COMPARTIMENTALIZACION: COMPARTIMENTALIZACION Diferente localización dentro de la célula. SISTEMAS MULTIENZIMATICOS: MULTIENZIMATICOS Enzimas relacionadas agrupadas formando verdaderos complejos. ENZIMAS MULTIFUNCIONALES: MULTIFUNCIONALES Una enzima que presenta varios sitios catalíticos distintos en una misma cadena polipeptídica.

Tipos de reacciones catalizadas por enzimas Ø Oxido-reducción Ø Rotura y formación de enlaces C-C Ø Reorganizaciones internas Ø Transferencia de grupos Ø Reacciones de condensación

NOMENCLATURA Y CLASIFICACIÓN DE ENZIMAS Nombre común : nombre de uso cotidiano asa + nombre del sustrato de la reacción Ejemplo: sacarasa, ureasa, amilasa, etc Nombres arbitrarios Ej: ptialina salival, pepsina del jugo gástrico, etc. Nombres según el tipo de reacción catalizada. Ej: deshidrogenasas, carboxilasas, etc.

Nombre sistemático: Unión Internacional de Bioquímica y Biología Molecular (IUBMB) Se asigna a cada enzima un nombre descriptivo y un número que permite identificarla inequívocamente Nombre común: Hexoquinasa Nombre sistemático: ATP: glucosa fosfotransferasa Código de 4 dígitos: 2. 7. 1. 1. Clase 2: transferasa Subclase 7: fosfotransferasa Subsubclase 1: fosfotransferasa con un grupo hidroxilo como aceptor N° de orden de la enzima en su subclase 1: glucosa como aceptor del grupo fosfato


1 - OXIDORREDUCTASAS: DESHIDROGENASAS, OXIDASAS, OXIGENASAS, REDUCTASAS, PEROXIDASAS 2 - TRANSFERASAS: TRANSCARBOXILASAS, TRANSMETILASAS Y TRANSAMINASAS. 3 - HIDROLASAS: ESTERASAS, FOSFATASAS, PEPTIDASAS. 4 - LIASAS: DESCARBOXILASAS, HIDRATASAS, DESAMINASAS. 5 - ISOMERASAS: EPIMERASAS, MUTASAS. 6 - LIGASAS: SINTETASAS, CARBOXILASAS

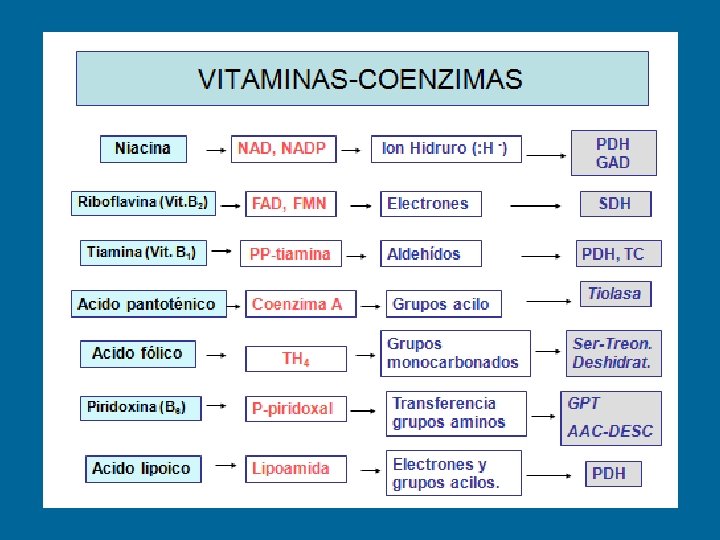
COFACTORES Según su modo de interacción con la enzima COENZIMAS Ø Unión laxa a la enzima Ø Actuaría como co-sustrato Ø Son moléculas orgánicas pequeñas Ø Muchas se encuentran libres y solo se unen a la enzima en el momento de la catálisis GRUPO PROSTÉTICO Ø Molécula orgánica no proteica Ø Se une fuertemente a la enzima Ø Solo se separa por desnaturalización IONES INORGÁNICOS Aniones - cationes

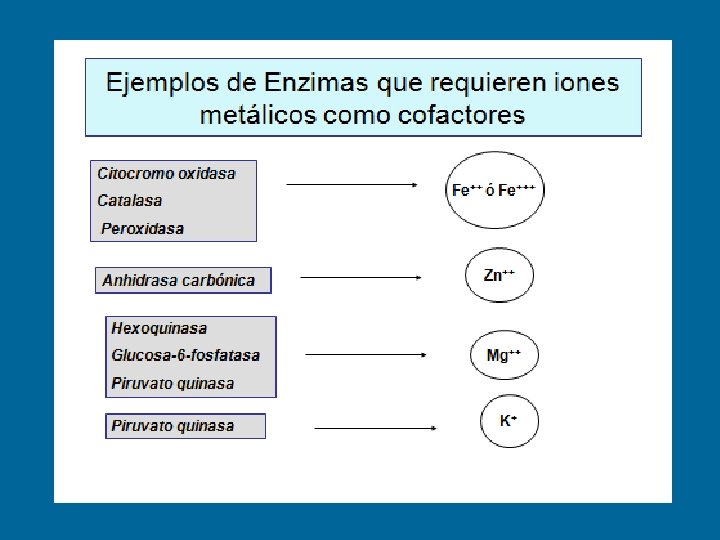
COFACTORES • Iones inorgánicos: Fe 2+ Mg 2+ Mn 2+ Zn 2+ En el caso de las coenzimas se forma un complejo: HOLOENZIMA = Enzima total APOENZIMA + Proteína Termolábil No dializa COENZIMA No proteínica Termoestable Oxidorreductasas, transferasas, isomerasas y ligasas requieren coenzimas
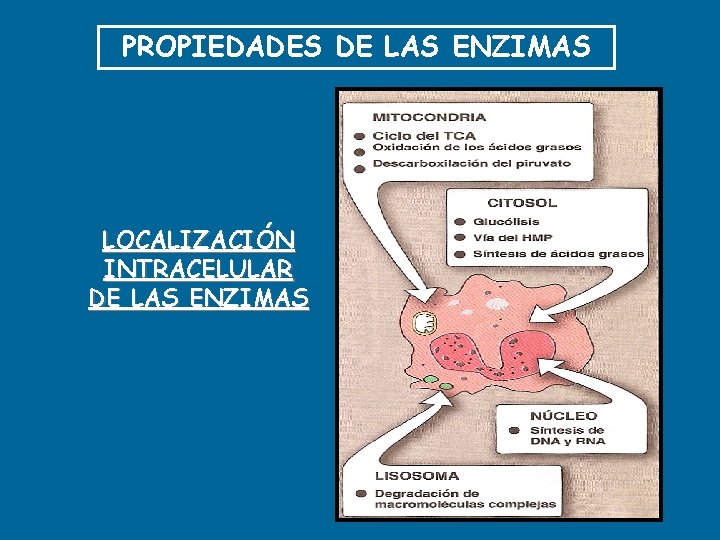
PROPIEDADES DE LAS ENZIMAS LOCALIZACIÓN INTRACELULAR DE LAS ENZIMAS
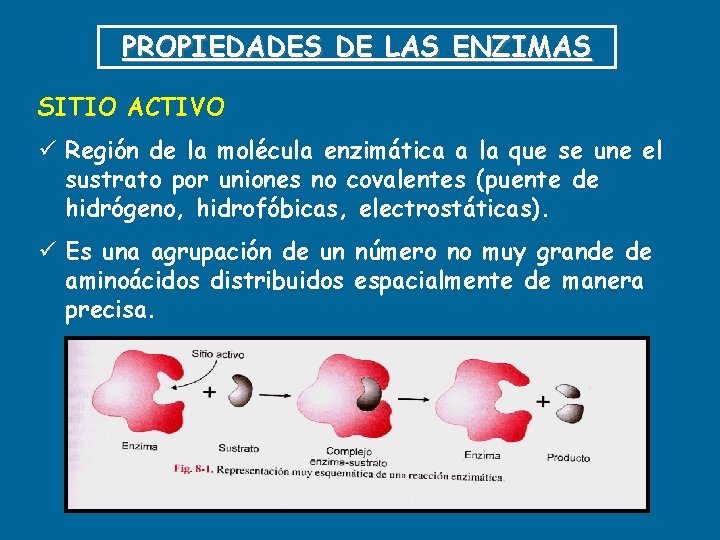
PROPIEDADES DE LAS ENZIMAS SITIO ACTIVO ü Región de la molécula enzimática a la que se une el sustrato por uniones no covalentes (puente de hidrógeno, hidrofóbicas, electrostáticas). ü Es una agrupación de un número no muy grande de aminoácidos distribuidos espacialmente de manera precisa.
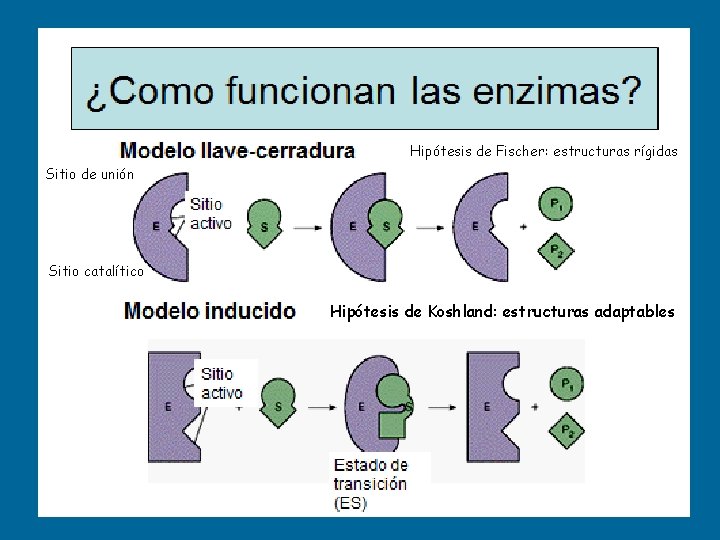
Hipótesis de Fischer: estructuras rígidas Sitio de unión Sitio catalítico Hipótesis de Koshland: estructuras adaptables

ZIMÓGENOS Algunas enzimas se sintetizan en la célula de origen al estado de PRECURSORES INACTIVOS llamados zimógenos, proenzimas o preenzimas SISTEMAS MULTIENZIMÁTICOS 1. Varias enzimas diferentes cuyas acciones se complementan. 2. Están ordenados, generalmente en membranas, de modo que el producto de la reacción catalizada por la primera enzima es recibido como sustrato por la segunda y así sucesivamente. 3. Las transformaciones se producen según la secuencia establecida por la disposición espacial de los catalizadores. Ej: Cadena Respiratoria ENZIMAS MULTIFUNCIONALES Presentan varios sitios catalíticos distintos en una misma cadena polipeptídica. Ejemplo: ácido graso sintetasa.

Catálisis enzimática • Las células y organismos vivos deben realizar distintos tipos de trabajo para permanecer vivos y reproducirse. • La síntesis continua de componentes celulares requiere de trabajo químico • La acumulación y retención de sales contra un gradiente de concentración implica la realización de un trabajo osmótico • La contracción muscular o el movimiento bacteriano representa un trabajo mecánico

Determinación de la actividad enzimática Se puede determinar, midiendo: v La cantidad de producto formado v O de sustrato consumido v En un tiempo dado v Como una sumatoria de todos los factores requeridos para la reacción

ACTIVIDAD ESPECÍFICA Ø Es una expresión que indica la pureza relativa de una preparación enzimática. Ø Relaciona Actividad Enzimática, no con el volumen de muestra, sino con el total de proteínas existentes en la misma. Ø Se define como: UNIDADES DE ENZIMA POR MG DE PROTEÍNAS PRESENTES EN LA MUESTRA

ACTIVIDAD ENZIMATICA Unidades Internacionales Cantidad de enzima que cataliza la transformación de 1 μmol (10 -6 mol) de Sustrato por minuto: E Sustrato Producto mmol de S transformados U. I. = minuto Siempre bajo condiciones definidas de p. H y temperatura


ü Para todo ello, los seres vivos requieren y utilizan la energía de su entorno ü La cantidad de energía realmente transformable en trabajo se denomina energía libre ü y ésta siempre será ligeramente inferior a la variación de energía total, ya que una parte de la misma se disipa en forma de calor

ü La variación de energía libre ( G) de una reacción química es una expresión cuantitativa de lo lejos que se encuentra el sistema del equilibrio. ü Aquellas reacciones que liberan energía libre se denominan exergónicas. ü Dado que los productos de estas reacciones tienen menor energía libre que los reactivos, G es negativa. ü Aquellas reacciones en las que los productos poseen mayor energía libre que los reactivos son endergónicas y G es positiva.
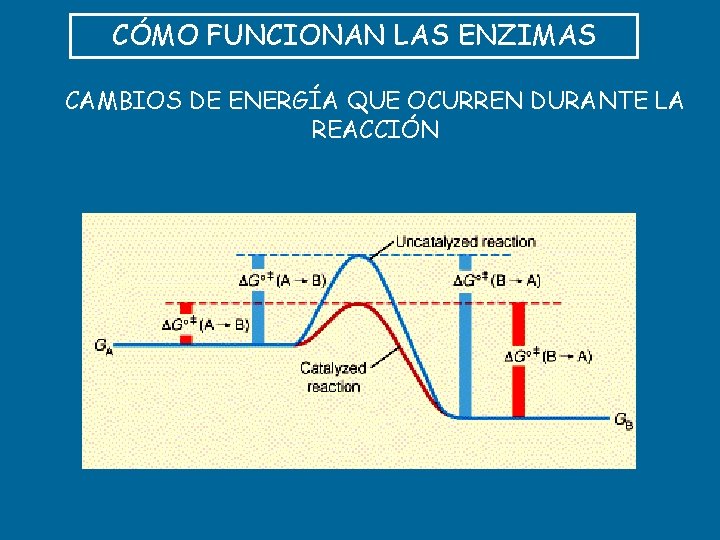
CÓMO FUNCIONAN LAS ENZIMAS CAMBIOS DE ENERGÍA QUE OCURREN DURANTE LA REACCIÓN
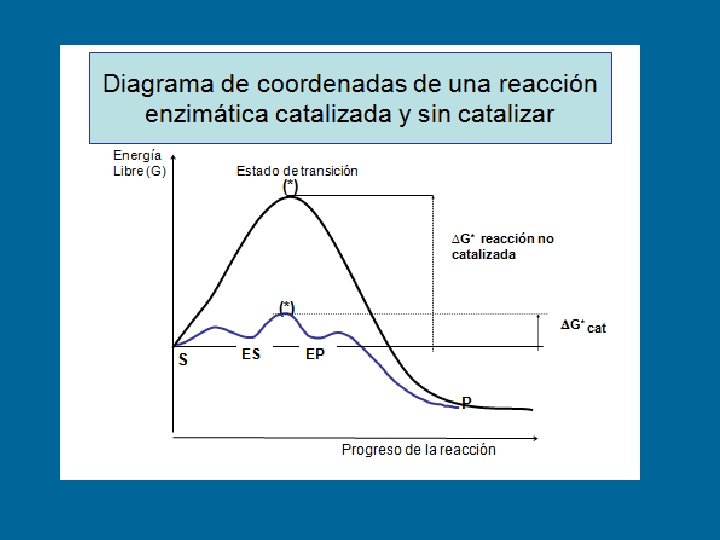

v El estado de transición o barrera de activación, activación representa los cambios que se generan en la molécula del S. v Las barreras de activación son importantes para la estabilidad de las biomoléculas. v Es por esto que las reacciones sin catalizar tienden a ser muy lentas. v Todas las moléculas biológicas son muy estables al p. H neutro, temperatura suave y ambiente acuoso en el interior de las células. v Todas las reacciones químicas celulares se llevan a cabo porque las enzimas actúan disminuyendo la barrera energética entre el S y el P
- Slides: 30