Bolilla 1 Enzimas Caracteres generales Importancia del estudio

Bolilla 1 Enzimas Caracteres generales. Importancia del estudio de las enzimas en los alimentos. Nomenclatura y clasificación. Coenzimas. Compartimentalización de las enzimas. Cinética enzimática. Factores que afectan la actividad enzimática, temperatura, p. H, actividad de agua, radiaciones ionizantes, etc. Ecuación de Michaelis-Menten. Inhibición de enzimas, competitiva, no competitiva y acompetitiva. Enzimas reguladoras. Enzimas alostéricas, modificación por unión covalente. Isoenzimas. Zimógenos. Enzimas endógenas y exógenas.

INHIBIDORES REVERSIBLES • Sustancias que producen un cambio de la capacidad catalítica de la enzima pero su acción no es permanente, el complejo [EI] se disocia rápidamente. • La inhibición reversible puede ser: COMPETITIVA NO COMPETITIVA ACOMPETITIVA

INHIBIDORES REVERSIBLES COMPETITIVOS
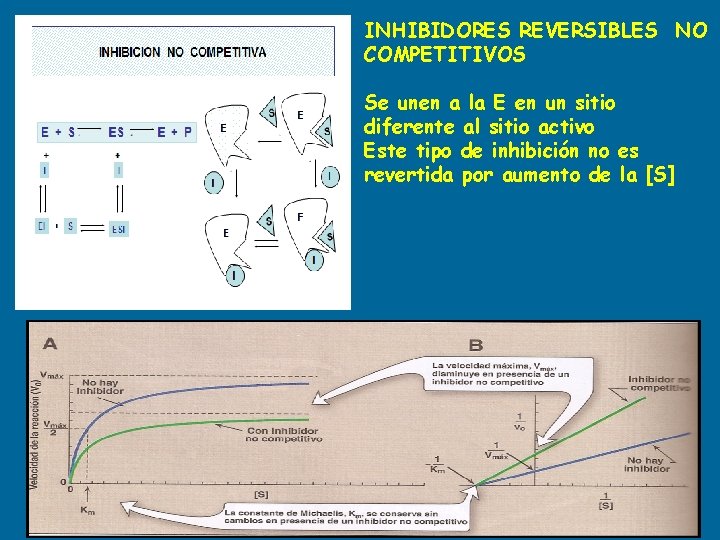
INHIBIDORES REVERSIBLES NO COMPETITIVOS Se unen a la E en un sitio diferente al sitio activo Este tipo de inhibición no es revertida por aumento de la [S]

INHIBIDORES REVERSIBLES NO COMPETITIVOS • La unión S-E no esta afectada, porque el I se une a la E libre o al [ES]. • Una vez formado el [ESI] la enzima se inactiva. • El valor de Km no se modifica, pues el S reacciona con la E igual que en ausencia del I. • Ejemplos: reactivos que se unen a grupos –SH de cisteína, indispensables para algunas enzimas, iones metálicos (Cu 2+, Hg 2+ y Ag 2+). • Otros I se unen a los metales componentes de la E, por ejemplo: cianuro se une fuertemente al Fe de los citocromos, catalasas y así bloquean su actividad.

INHIBIDORES ACOMPETITIVOS § Son inhibidores reversibles. § El I se une al complejo ES ESI § Hay 2 reacciones que producen: 1 - ESI 2 - P § Este tipo de inhibición se da en casos en los cuales participan varios sustratos en la reacción. § No es revertida por aumento de la [S].




REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA Ø La AE en las células se ajustan a las necesidades fisiológicas, cambiantes permanentemente. Ø A [S] bajas, la AE es proporcional a los niveles de S. Ø En condiciones fisiológicas, la [S] se encuentra por debajo o próxima al Km, así los niveles de S, determinarán la mayor o menor AE. Ø A mayor [S] mayor AE Ø La E que cataliza la primera etapa de una vía metabólica suele ser reguladora.

• Los seres vivos han generado mecanismos para regular las rutas bioquímicas. • La regulación es esencial por las siguientes razones: Ø Mantenimiento de un estado ordenado no hay desperdicio de recursos. Ø Conservación de la energía utilización de la En suficiente en las células, para consumir los nutrientes según sus necesidades energéticas. Ø Respuesta a variaciones ambientales son los ajustes rápidos que deben realizar las células (p. H, [S], T°C), por su capacidad de aumentar o disminuir la velocidad de las reacciones específicas.
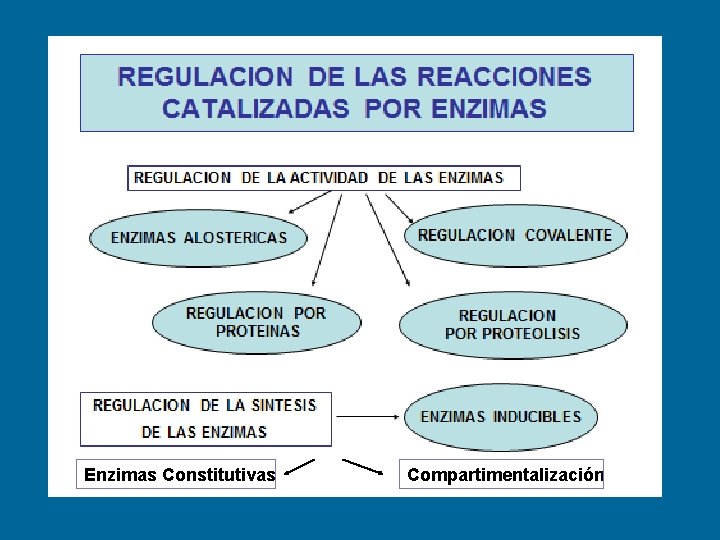
Enzimas Constitutivas Compartimentalización
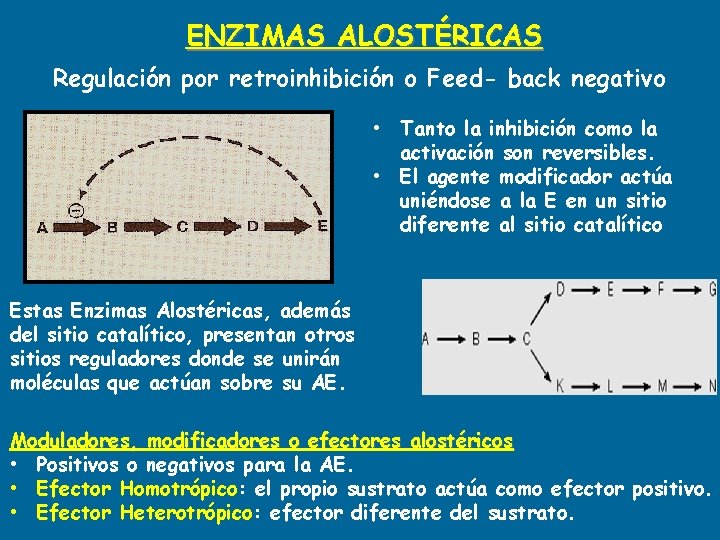
ENZIMAS ALOSTÉRICAS Regulación por retroinhibición o Feed- back negativo • Tanto la inhibición como la activación son reversibles. • El agente modificador actúa uniéndose a la E en un sitio diferente al sitio catalítico Estas Enzimas Alostéricas, además del sitio catalítico, presentan otros sitios reguladores donde se unirán moléculas que actúan sobre su AE. Moduladores, modificadores o efectores alostéricos • Positivos o negativos para la AE. • Efector Homotrópico: el propio sustrato actúa como efector positivo. • Efector Heterotrópico: efector diferente del sustrato.
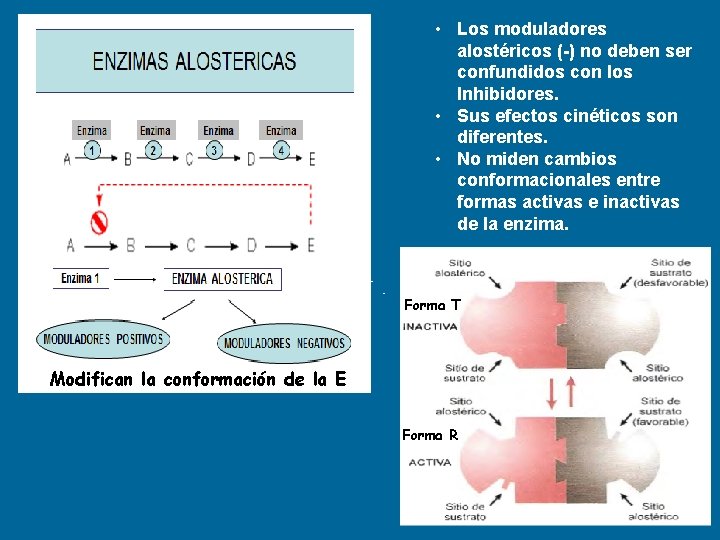
• Los moduladores alostéricos (-) no deben ser confundidos con los Inhibidores. • Sus efectos cinéticos son diferentes. • No miden cambios conformacionales entre formas activas e inactivas de la enzima. Forma T Modifican la conformación de la E Forma R
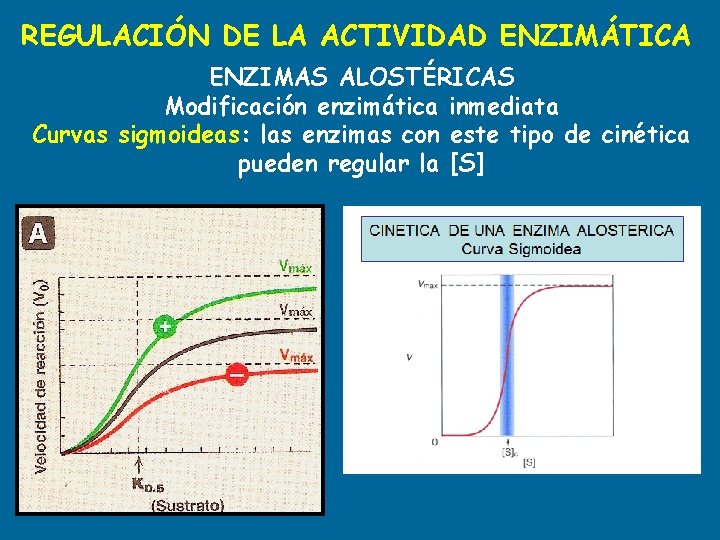
REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA ENZIMAS ALOSTÉRICAS Modificación enzimática inmediata Curvas sigmoideas: las enzimas con este tipo de cinética pueden regular la [S]


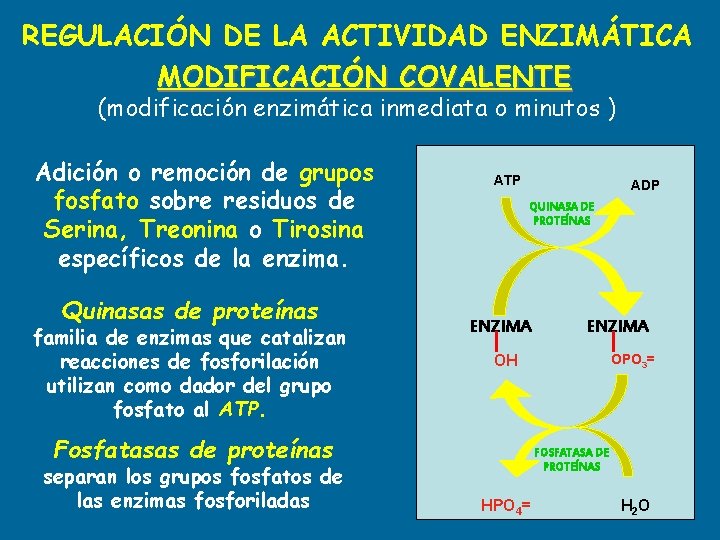
REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA MODIFICACIÓN COVALENTE (modificación enzimática inmediata o minutos ) Adición o remoción de grupos fosfato sobre residuos de Serina, Treonina o Tirosina específicos de la enzima. Quinasas de proteínas familia de enzimas que catalizan reacciones de fosforilación utilizan como dador del grupo fosfato al ATP ADP QUINASA DE PROTEÍNAS ENZIMA OPO 3= OH Fosfatasas de proteínas separan los grupos fosfatos de las enzimas fosforiladas ENZIMA FOSFATASA DE PROTEÍNAS HPO 4= H 2 O
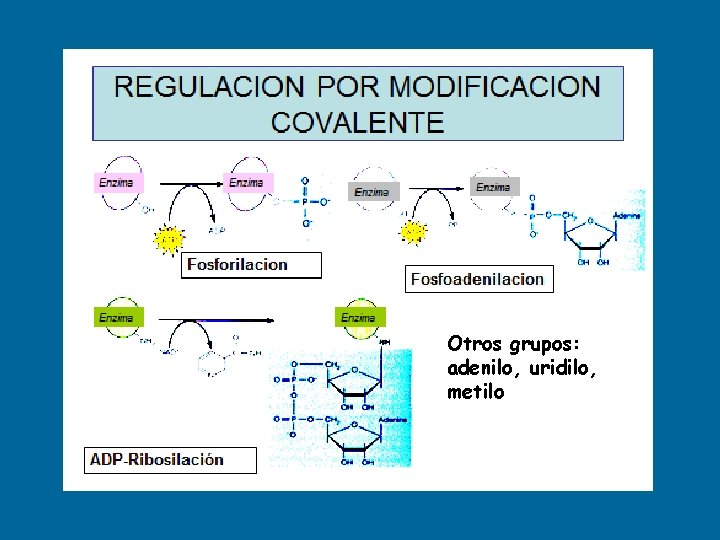
Otros grupos: adenilo, uridilo, metilo

Glucógeno fosforilasa



REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA INDUCCIÓN Y REPRESIÓN DE LA SÍNTESIS ENZIMÁTICA A NIVEL GÉNICO (modificación enzimática en horas o días) INDUCCIÓN síntesis enzimática aumentada REPRESIÓN síntesis enzimática disminuida CONSECUENCIA cambios en la población total de sitios activos. Una enzima puede responder a más de un tipo de regulación





Enzimas diagnósticas de enfermedades cardíacas • Creatina Quinasa (CK o CPK) • Lactato deshidrogenasa (LDH) • Aspartato amino transferasa (ASATGOT) • Alanina amino transferasa (ALAT- GPT) • Otros marcadores: proteínas como mioglobina, troponinas, proteína de enlace de ácidos grasos (FABP), enzima glucógeno fosforilasa.

Enzimas relacionadas con las enfermedades hepáticas • Transaminasas (ALAT y ASAT) • Fosfatasa alcalina (FAL) • Gama- glutamil- transferasa (GGT)

Enzimas relacionadas con daño pancreático • • Amilasa sérica y urinaria Lipasa Tripsinógeno sérico y urinario Quimotripsina y elastasa en heces
- Slides: 30