Bohrov model atoma vodika Niels Bohr 1913 Bohrovi

Bohrov model atoma vodika (Niels Bohr 1913) Bohrovi postulati: 1. Elektron se kreće po kružnoj putanji oko jezgre 2. Angularni momemt (kutna količina gibanja) elektrona može poprimiti samo diskretne vrijednosti L=nħ gdje je n =1, 2, 3, . . . i ħ =h/(2 p) reducirana Planckova konstanta! 3. Elektron emitira (apsorbira) zračenje samo pri prelazu iz jedne putanje u drugu. Tada emitira (apsorbira) foton energije hn = E-E’ gdje su E i E’ energije tih dviju putanja!
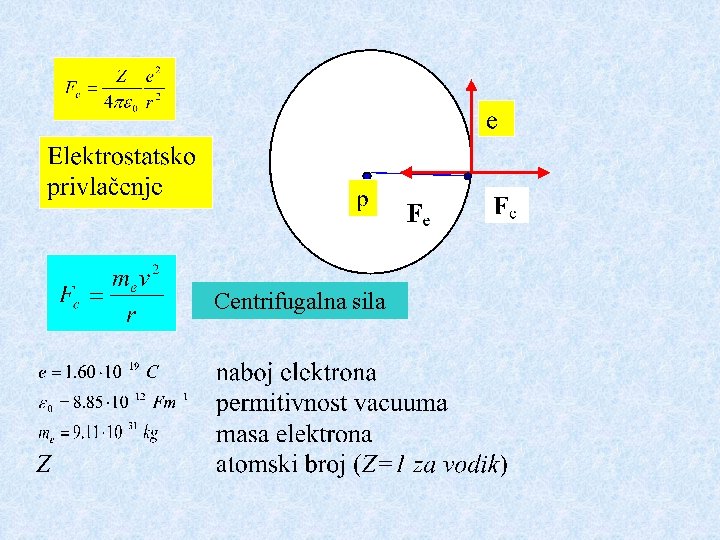
Centrifugalna sila




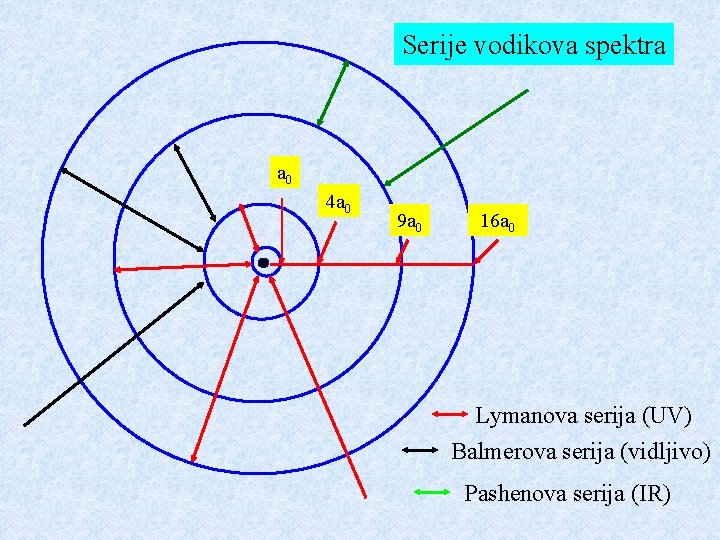
Serije vodikova spektra a 0 4 a 0 9 a 0 16 a 0 Lymanova serija (UV) Balmerova serija (vidljivo) Pashenova serija (IR)

E=hn (e. V) n 0 Paschenova serija 4 3 E 3=-13. 6/9=-1. 49 e. V 2 E 2=-13. 6/4=-3. 39 e. V 1 E 1=-13. 6 e. V Balmerova serija Lymanova serija Termovi (energetski nivoi) vodika i prijelazi elektrona koji uzrokuju serije u emisijskom spektru vodika
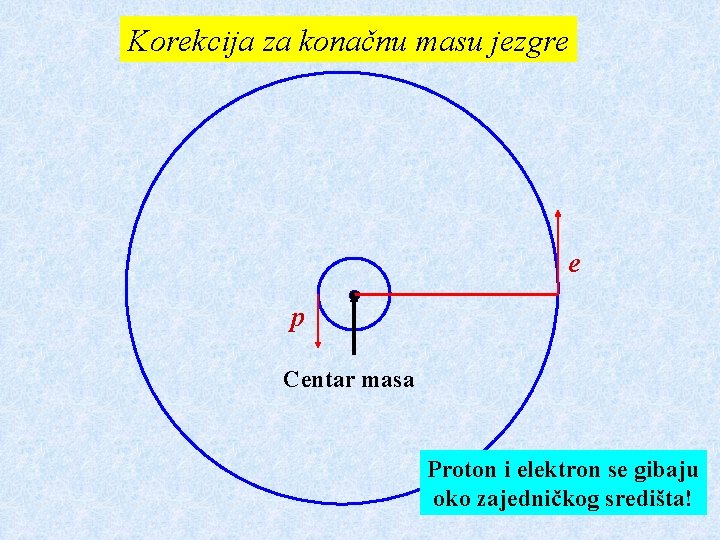
Korekcija za konačnu masu jezgre e p Centar masa Proton i elektron se gibaju oko zajedničkog središta!





Pitanja Bohrov model atoma vodika • Koji su Bohrovi postulati? • Što objašnjava Bohrov model? • Što je. Bohr kvantizirao? • Koj Bohrov postulat govori o kvantizaciji i kako on glasi? • Što je posljedica Bohrovih postulata? • Kako je u Bohrovu modelu kvantiziran radius putanje elektrona? • Koja je razlika Rydbergove konstante za beskonačnu masu i za vodikov atom? • Što je to reducirana masa i zašto je ona potrebna? • Kako je Bohr modificirao svoj drugi postulat? Zašto? • Koje su prednosti a koj nedostaci Bohrova modela? • Koje linije se mogu opaziti u vidljivom dijelu vodikova spektra? • Kako je u Bohrovom modelu kvantizirana energija? • Kako je u Bohrovom modelu kvantizirana brzina elektrona?
- Slides: 14