BOCIO Y ENFERMEDAD TIROIDEA NODULAR Prof Dra Mara

BOCIO Y ENFERMEDAD TIROIDEA NODULAR Prof. Dra. María Beatriz Casadio 2014

BOCIO n Aumento de tamaño de la glándula tiroides 2º a defectos de biosíntesis, deficiencia de yodo, enfermedad autoinmunitaria y enfermedades nodulares. n Defectos de la biosíntesis y deficiencia de yodo reducción de síntesis de hormonas tiroideas aumento de la TSH, que estimula el incremento de la tiroides como mecanismo compensador para superar el bloqueo de la síntesis hormonal. n En la enfermedad de Graves, el bocio se debe a los

NÓDULO TIROIDEO PRESENTACIÓN “Lesión dentro del parénquima tiroideo que es palpable y/o ultrasonográficamente distinto del tejido tiroideo circundante” Cooper D. Thyroid 2006; 16: 1 -33 Kinder B. Curr Opin Oncol 2003; 15: 71 -77

�Enfermedad nodular : crecimiento desordenado de los folículos tiroideos combinado con desarrollo gradual de fibrosis. n Es frecuente y se encuentra en 3 a 7% de los adultos. n Con técnicas más sensibles, como ecografía, está presente en más de 25% de los adultos. n Los nódulos tiroideos pueden ser solitarios

BOCIO DIFUSO NO TOXICO n n n Aumento de tamaño difuso de la glándula tiroides en ausencia de nódulos e hipertiroidismo deficiencia de yodo. Endémico afecta a más de 5% de la población. Esporádico en regiones no endémicas, causa desconocida. Bocio juvenil en los adolescentes. > frecuencia en las mujeres por > prevalencia de enfermedad autoinmunitaria subyacente y > necesidad de yodo asociada a la gestación. Niveles de TSH normales o ligeramente aumentados, sugiere aumento de la sensibilidad a la TSH o activación de otras vías que conducen al aumento de tamaño de la

CLÍNICA n n El yoduro ejerce acciones directas sobre los vasos tiroideos e indirecta por medio de sustancias vasoactivas como las endotelinas y el óxido nítrico. El bocio endémico también es causado por bociógenos ambientales como la mandioca, que contiene un tiocianato, verduras de la familia Crucíferas ( repollo y coliflor) y leche de regiones en las que hay bociógenos en el pasto. (Efecto Wolff-Chaikoff) Los defectos de síntesis hormonal también provocan bocio: anomalías de los pasos de la síntesis hormonal, transporte de yodo (NIS, simporter Na-I), síntesis de Tg, organificación y acoplamiento (TPO, Ac antiperoxidasa) y regeneración de yoduro (deshalogenasa). Función tiroidea conservada, la > asintomáticos.

Exploración: n Glándula aumentada, simétrica, blanda, sin nódulos. n El bocio se define como un lóbulo lateral con un volumen superior al pulgar del paciente. n El agrandamiento notable puede causar compresión traqueal o esofágica. n El bocio retroesternal puede obstruir el estrecho torácico superior. n Signo de Pemberton: síntomas de desfallecimiento con signos de congestión facial y obstrucción venosa yugular al elevar los brazos por encima de la cabeza, maniobra que desplaza la tiroides al estrecho torácico superior.

DIAGNÓSTICO n n n n Para evaluar el bocio retroesternal se usan medidas del flujo respiratorio y TC o resonancia magnética. Pruebas de función tiroidea para excluir tirotoxicosis o hipotiroidismo. En deficiencia de yodo: T 4 total baja, T 3 y TSH normales, (refleja el aumento de la conversión de T 4 en T 3). TSH baja, en el anciano, sugiere enfermedad de Graves no diagnosticada. Ac anti TPO para identificar enfermedad tiroidea autoinmunitaria. Los valores urinarios bajos de yodo (<10 pg/100 mi). Gammagrafía muestra aumento de la captación en el déficit de yodo y la dishormonogénesis.
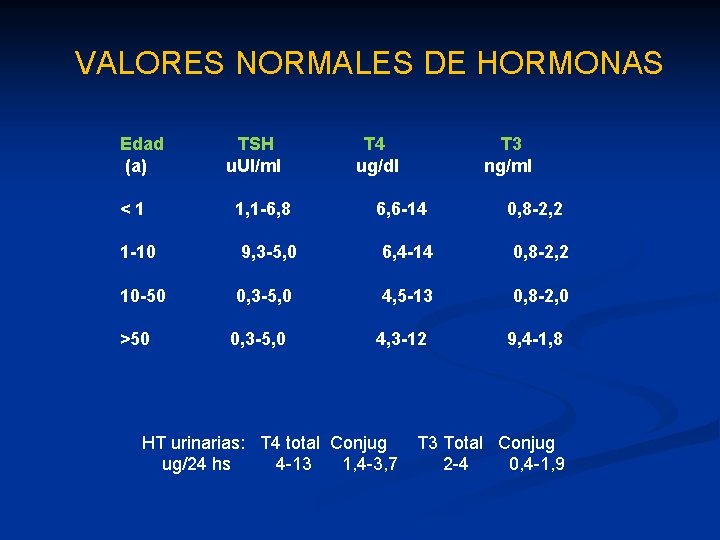
VALORES NORMALES DE HORMONAS Edad (a) <1 TSH u. UI/ml 1, 1 -6, 8 T 4 ug/dl T 3 ng/ml 6, 6 -14 0, 8 -2, 2 1 -10 9, 3 -5, 0 6, 4 -14 0, 8 -2, 2 10 -50 0, 3 -5, 0 4, 5 -13 0, 8 -2, 0 >50 0, 3 -5, 0 4, 3 -12 HT urinarias: T 4 total Conjug ug/24 hs 4 -13 1, 4 -3, 7 9, 4 -1, 8 T 3 Total Conjug 2 -4 0, 4 -1, 9

TRATAMIENTO n n n n Yodo o sustitución con hormonas tiroideas inducen regresión. Tomar precauciones al instaurar el tratamiento supresor con tiroxina, si la TSH basal esta normal a baja. En jóvenes dosis inicial de 100 pg/día. En ancianos 50 pg/d í a. Regresión en 3 a 6 meses < al 33% en ancianos y en los que tienen algún grado de enfermedad nodular o fibrosis. Cirugía indicada en compresión traqueal o de obstrucción del estrecho torácico superior. Después de la cirugía tratamiento supresor suave con levotiroxina para prevenir reaparición del bocio. I 131 radiactivo reduce el bocio en 50% de los pacientes. Seguimiento posterior para descartar desarrollo de

BOCIO MULTINODULAR NO TOXICO 12 % de los adultos. > frecuencia en mujeres y su prevalencia aumenta con la edad. n Común en regiones con déficit de yodo. n Variación en el tamaño de los nódulos. n Histología: regiones hipercelulares, áreas quísticas llenas de coloide, fibrosis extensa y áreas de hemorragia o infiltración linfocítica. n La TSH, no elevada, puede contribuir al proceso. Clínica: n Asintomáticos y eutiroideos, aumento de tamaño en cuello. n Los sintomáticos suelen ser grandes o contienen áreas fibróticas que causan compresión. n Dolor repentino se debe a hemorragia en el interior de n

DIAGNÓSTICO n n n Medir TSH para excluir hipertiroidismo o hipotiroidismo subclínico, la función tiroidea suele ser normal. Desviación de la tráquea frecuente, pero la compresión debe superar 70% del diámetro para que afecte vías respiratorias. Pruebas de función pulmonar para valorar efectos de la compresión. TC o IRM para evaluar anatomía del bocio y extensión retroesternal. Tránsito intestinal con bario para ver compresión esofágica.

TRATAMIENTO q q q q Levotiroxina en dosis bajas (50 pg ) Evitar medios de contraste y sustancias con yodo debido al riesgo de inducir fenómeno Jod-Basedow: > producción de hormona tiroidea por nódulos autónomos. Yodo radiactivo (I 131 ) reduce el bocio y puede suprimir regiones de autonomía. Dosis de I 131, según tamaño y captación de. En la mayoría reducción de 40 a 50%. Ante compresión aguda tto con glucocorticoides o cirugía. Hipotiroidismo inducido por radiación < frecuente que tras tratamiento de enfermedad de Graves. Tirotoxicosis autoinmunitaria postratamiento hasta en 5%.

BOCIO MULTINODULAR TOXICO n n n n Patogenia similar al no tóxico pero este presenta autonomía funcional Presentación clínica como hipertiroidismo subclínico o tirotoxicosis leve. Paciente anciano consulta con FA o palpitaciones, taquicardia, nerviosismo, temblores o pérdida de peso. Exposición reciente al yodo puede desencadenar o exacerbar la tirotoxicosis. Nivel de TSH bajo, T 4 normal o poco aumentada; T 3 más elevada que T 4. Gammagrafía tiroidea muestra captación heterogénea. Captación de yodo radiactivo de 24 h puede no estar aumentada.

TRATAMIENTO n Antitiroideos, en combinación con BB, pueden normalizar la función tiroidea y tratar la tirotoxicosis, pero estimula el crecimiento del bocio. n Yodo radiactivo para tratar áreas de autonomía y reducir el volumen. n Cirugía: tto definitivo de la tirotoxicosis subyacente y del bocio. Los pacientes deben estar eutiroideos antes de la intervención.

TRATAMIENTO Nódulo tiroideo solitario de funcionamiento autónomo (adenoma tóxico). n La mayoría de los ptes presenta mutaciones somáticas activadoras en el gen que codifica el TSH-R. Estas potencian proliferación y función de las células foliculares. Clínica: n Tirotoxicosis leve. Nódulo tiroideo palpable y ausencia de características clínicas de enfermedad de Graves. Diagnostico: n Gammagrafía: captación focal en nódulo hiperfuncional y disminución de la captación en el resto. n Actividad de la tiroides suprimida. n

TRATAMIENTO n n n Ablación con yodo radiactivo de elección, el I 131 se concentra en el nódulo hiperfuncional con mínima captación y lesión del tejido tiroideo normal. Las dosis grandes de yodo radiactivo corrigen la tirotoxicosis en 75% de los pacientes en 3 meses. En menos de 10% aparece hipotiroidismo durante los 5 años siguientes. Resección quirúrgica: enucleación del adenoma o lobulectomía, con lo que se preserva la función tiroidea y se reduce al mínimo el riesgo de hipoparatiroidismo y lesión de los nervios laríngeos recurrentes. Antitiroideos y BB pueden normalizar la función tiroidea, pero no es el mejor tratamiento a largo plazo. Se ha utilizado la inyección de etanol bajo guía ecográfica para la ablación de los nódulos.

TIROIDITIS

CAUSAS DE TIROIDITIS AGUDA: a) I. Bacteriana. Stafiloc. , Strept. , Enterobacter b) I. Micótica: asperg. , Cand. , Cocci. , Histop, Neumocis. c) Por radiación I 131 d) Drogas: Amiodarona (aguda o crónica) SUBAGUDA a) Víricas o granulomatosa b) T. Silenciosa (incluida del puerperio) c) Infección micobacteriana CRÓNICA a) Autoinmune: Focal, Hashimoto b) T. Riedel c) Parasitaria: Equinoc. Estrong. Cistecerc.

TIROIDITIS AGUDA n n n Poco frecuente, infección supurativa de la glándula. > frecuente en niños y adultos jóvenes. 2º causa más frecuente: presencia de un seno piriforme, que conecta la bucofarínge con la tiroides. Factores de riesgo en el anciano: bocio prolongado, degeneración en neoplasia maligna de tiroides. Clínica: dolor tiroideo, referido a garganta, oídos, bocio pequeño e hipersensible. Fiebre, disfagia y eritema sobre la glándula.

�LBT: VSG y recuento leucocítico con función tiroidea normal. �Biopsia: infiltración por PMN; el cultivo de la muestra identifica el microorganismo. �Tratamiento antibiótico según cultivo. �Complicaciones: obstrucción traqueal, septicemia, absceso retrofaríngeo, mediastinitis y trombosis venosa yugular.

TIROIDITIS SUBAGUDA n n n n De Quervain, granulomatosa o vírica. Relacionada a virus: virus de la parotiditis, coxsackie, virus de la gripe, adenovirus y echovirus. Diagnóstico: los síntomas pueden confundirse con faringitis. Incidencia máxima: entre 30 y 50 años. Mujeres-hombres: 3/1. Infiltrado inflamatorio con alteración de los folículos y células gigantes multinucleadas granulomas y fibrosis. Fase inicial: destrucción folicular se liberan Tg y H. tiroideas, con aumento de T 4 y T 3 libres circulantes, supresión de la TSH.

n n n reserva de hormonas fase de hipotiroidismo, con T 4 libre baja y aumento moderado de los niveles de TSH. La captación de yodo radiactivo se recupera o incluso aumenta por la elevación de la TSH. La hormona tiroidea y los niveles de TSH se normalizan a medida que la enfermedad cede. Clínica: tiroides dolorosa, aumentada de tamaño y fiebre. Tirotoxicosis o hipotiroidismo, dependiendo de la fase. Dolor de garganta, suele referirse hacia el maxilar inferior o el oído; exploración: pequeño bocio hipersensible. Puede desarrollarse hipotiroidismo permanente, especialmente en los que tienen autoinmunidad tiroidea.

n LBT: FT. evoluciona en 3 fases durante 6 meses: n 1) tirotóxica, 2) hipotiroidea y 3) de recuperación. n Tirotóxica: T 3 y T 4 aumentados, TSH suprimida. � Índice T 4 / T 3 > que en E. de Graves. � DX: de la ESR y captación I 131 � Rto de leucocitos aumentado y ac antitiroideos (). � TTO: AAS (600 mg cada 4 a 6 h). � Glucocorticoides, dosis inicial de 40 a 60 mg de prednisona, � Control de TSH y de T 4 libre cada 2 a 4 semanas.


TIROIDITIS SILENCIOSA n n n Pacientes con enfermedad tiroidea autoinmunitaria subyacente. Clínica: similar a tiroiditis subaguda, (excepto que no existe hipersensibilidad). 5% en mujeres tres a seis meses después de un embarazo. Fase de tirotoxicosis, dura 2 y 4 semanas, seguida de hipotiroidismo de 4 a 12 semanas, resolución. Ac. anti-TPO antes del parto.

TIROIDITIS SILENCIOSA n n n n Seguimiento anual, (en algunos se desarrolla un hipotiroidismo permanente). 3 veces > en mujeres con DBT 1. Captación de yodo radiactivo inicialmente suprimida. Bocio indoloro, ESR normal y Ac. TPO. No está indicado tratamiento con glucocorticoides. Síntomas graves: propranolol, 20 a 40 mg/ 3 -4 veces/día. Sustitución con tiroxina en la fase hipotiroidea,

TIROIDITIS INDUCIDA POR FÁRMACOS El IFN-a, que se utiliza para tratar hepatitis crónicas B o C y cánceres de la sangre y la piel, origina disfunción tiroidea hasta en 5% de pacientes. n Tiroiditis indolora, hipotiroidismo y enfermedad de Graves. n > frecuencia en mujeres con anticuerpos contra TPO. n

TIROIDITIS CRONICA n n Tiroiditis focal en 20 a 40% de los eutiroideos. Ac. anti TPO 4 a 10 veces más frecuentes en mujeres. Causa más manifiesta: Tiroiditis de Hashimoto, trastorno autoinmunitario, se manifiesta como bocio de consistencia firme de tamaño variable. La tiroiditis de Riedel ocurre en mujeres de edad madura. Se manifiesta como bocio indoloro con síntomas por compresión de esófago, tráquea, venas del cuello o nervios laríngeos recurrentes. Fibrosis densa que se puede extender al exterior de la cápsula tiroidea. Es rara la disfunción tiroidea. El bocio es duro, no hipersensible, asimétrico y fijo, lo que despierta sospecha de malignidad.

El diagnóstico requiere biopsia abierta. n Tratamiento: quirúrgico de los síntomas de compresión. Beneficioso el tamoxifeno. n Relación entre tiroiditis de Riedel y fibrosis idiopática en otros sitios (retroperitoneo, mediastino, árbol biliar, pulmón y órbita). n

NÓDULO TIROIDEO

PRESENTACIÓN n Nódulo tiroideo n Solo 5% a 10% serán malignos n< 2 cm n > 4 cm 3% 16% 30% TODOS LOS MAYORES A 1 CM PALPABLES O NO DEBEN ESTUDIARSE Cooper D. Thyroid 2006; 16: 1 -33 Kinder B. Curr Opin Oncol 2003; 15: 71 -77





PRESENTACIÓN n Manifestaciones Disfagia n Dolor n Disnea n Disfonía n 27. 3% 21. 7% 7. 7% 0. 7 - 7% ¿ Criterios clínicos de malignidad ? Cooper D. Thyroid 2006; 16: 1 -33 Kinder B. Curr Opin Oncol 2003; 15: 71 -77

DIAGNÓSTICO n Sospecha clínica de malignidad n Alta n n n Historia familiar de medular o NEM Crecimiento rápido Fijo a estructuras adyacentes Asociado a adenopatías Parálisis cordal Moderada n Edad (<20 años ó >70 años) n n n Incluye lesiones < 1 cm Hasta 50% malignos) Masculino Tamaño > 4 cm Asociado a sintomatología Historia de exposición a radiaciones Sakorafas G. Cancer Treat Rev 2006; 32: 191 -202

DIAGNÓSTICO n BAAF Martin y Ellis 1930 n Crockford y Bain 1979 n Miller y Hamburger 1979 n número de pacientes llevados a cirugías diagnósticas 60 -85% Nguyen G. Cytojournal 2005; 2: 12 -25 Landsford C. Cancer Control 2006; 13: 89 -98

DIAGNÓSTICO n BAAF n Actualmente Gold Standard n. S n. E n VPP n VPN n Certeza n FN n n n 90% 72% 46% 97% 80% 5% Quistes Tamaño < 10 y > 30 mm Antecedente de RT? S sensibilidad, E especificidad, VPP valor predictivo positivo, VPN valor predictivo negativo, FN falsos negativos

DIAGNÓSTICO n BAAF n Categorías n Benigno 70 % 4% 10 % n Maligno n Sospechosa n Solo 20% serán malignos n Inadecuada n n 16 % Hasta 50% diagnósticas cuando se repiten USG Nguyen G. Cytojournal 2005; 2: 12 -25 Landsford C. Cancer Control 2006; 13: 89 -98

DIAGNÓSTICO n BAAF n Contraindicaciones n Diátesis n hemorrágica Complicaciones n Siembra en el trayecto 0. 14% (4912 pacientes) n Hematoma n Punción traqueal n Infección Nguyen G. Cytojournal 2005; 2: 12 -25 Landsford C. Cancer Control 2006; 13: 89 -98
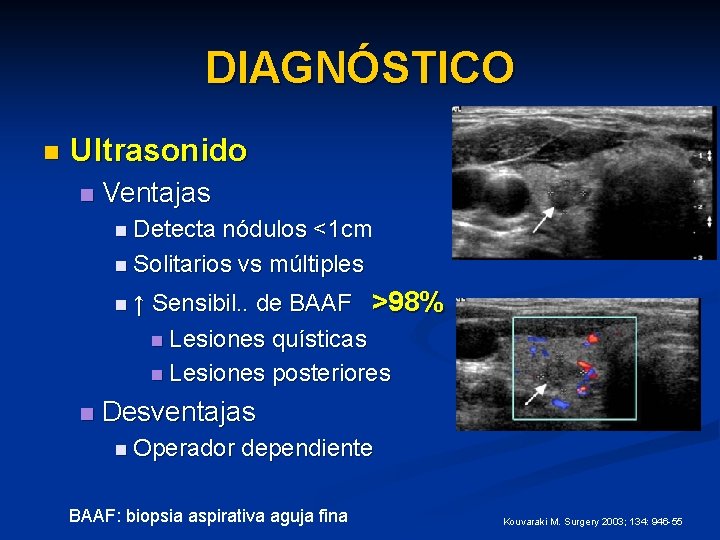
DIAGNÓSTICO n Ultrasonido n Ventajas n Detecta nódulos <1 cm n Solitarios vs múltiples n↑ n Sensibil. . de BAAF >98% n Lesiones quísticas n Lesiones posteriores Desventajas n Operador dependiente BAAF: biopsia aspirativa aguja fina Kouvaraki M. Surgery 2003; 134: 946 -55








DIAGNÓSTICO n Ultrasonido n Características sonográficas de malignidad n Nódulo n n n S 18. 2% E 88% Ganglios n n Sólido Hipoecogénico Microcalcificaciones Hipervascularidad Tamaño Posición del hilio Redondos S 52 a 77% E 93 a 95% Utilidad? Kouvaraki M. Surgery 2003; 134: 946 -55

DIAGNÓSTICO n Ultrasonido n Preoperatorio n Detección n de adenopatías 20 a 30% ocultas Cambia manejo? Seguimiento n Pacientes ya tratados n Nódulos benignos n Crecimiento n >20% del volumen ó 2 mm en dos dimensiones
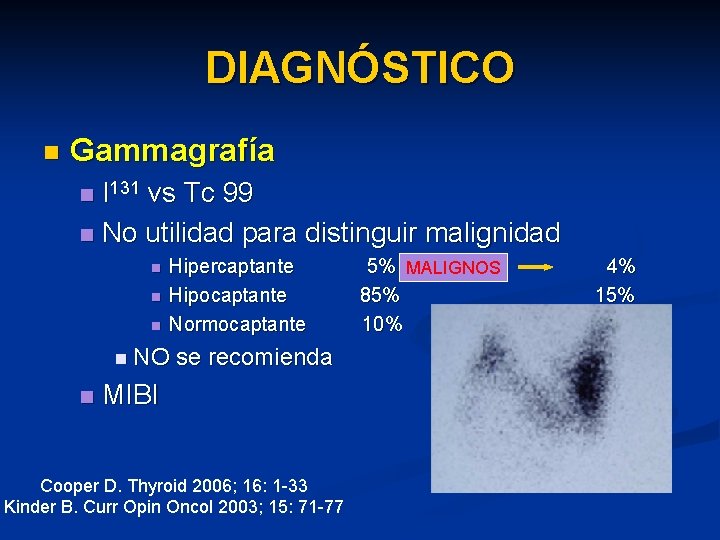
DIAGNÓSTICO n Gammagrafía n I 131 vs Tc 99 n No utilidad para distinguir malignidad n n n Hipercaptante Hipocaptante Normocaptante n NO n se recomienda MIBI Cooper D. Thyroid 2006; 16: 1 -33 Kinder B. Curr Opin Oncol 2003; 15: 71 -77 5% MALIGNOS 85% 10% 4% 15%

DIAGNÓSTICO n Laringoscopía n Parálisis cordal en pacientes llevados a tiroidectomía n 4% global n n n 71% 0. 3% Utilidad como predictor de enfermedad extratiroidea n n n Invasión extratiroidea Sin invasión S 76% E 100% Asintomáticos 67% n Utilidad de cambios de voz como indicador de parálisis n S 33% n E 75% Randolph GW. Surgery 2006; 139: 357 -62

DIAGNÓSTICO n Laringoscopía n Si hay parálisis cordal considerar enfermedad extensa n Estudios n n En n n de extensión preoperatorios TAC IRM Imagen de tórax quirófano Broncoscopía Esofagoscopía Hasta 85% serán positivas para invasión Randolph GW. Surgery 2006; 139: 357 -62

DIAGNÓSTICO n TAC Efecto de contraste sobre captación posterior de I 131 Puede retardar ablación de 6 a 8 semanas n Niveles ganglionares poco accesibles al US n n Niveles laterales n Retrofaríngeos, retrotraqueales, retroesternales SOLO RECOMENDADA CUANDO SE CONFIRMA MALIGNIDAD Cooper D. Thyroid 2006; 16: 1 -33 Kinder B. Curr Opin Oncol 2003; 15: 71 -77

DIAGNÓSTICO RMN n No estudios que avalen utilidad n Mejor resolución espacial n n Nódulos n 4 mm NO se recomienda de rutina Cooper D. Thyroid 2006; 16: 1 -33 Kinder B. Curr Opin Oncol 2003; 15: 71 -77
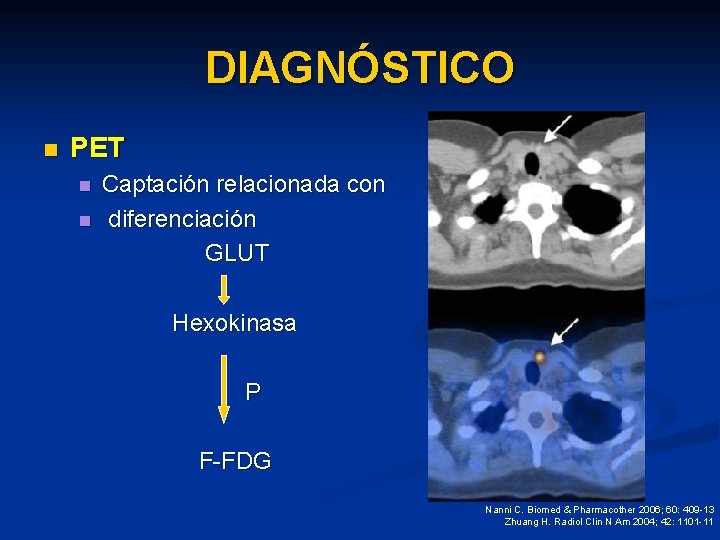
DIAGNÓSTICO n PET n n Captación relacionada con diferenciación GLUT Hexokinasa P F-FDG Nanni C. Biomed & Pharmacother 2006; 60: 409 -13 Zhuang H. Radiol Clin N Am 2004; 42: 1101 -11

DIAGNÓSTICO n PET n Principalmente útil en los que no captan I n Mayor sensibilidad cuando TSH n VPP 75% a 96% n Tg y rastreo (-) n PET-CT n n A 78% A 93% FN bien diferenciados que captan I FP Nanni C. Biomed & Pharmacother 2006; 60: 409 Zhuang H. Radiol Clin N Am 2004; 42: 1101 -11
DIAGNÓSTICO n PET n n Estudios en lesiones indeterminadas n Si negativo evita cirugía 66% Utilidad pronostica? Pacientes I 131 (-) n Dificultad para identificar enfermedad metastásica n Peor pronóstico Opción de identificación y tratamiento

CLASIFICACIÓN n Tumor Solitario Tumor Multifocal El Mayor Determina la Clasificación n TX: El Tumor Primario No puede ser Evaluado n T 0: No hay Evidencia de Tumor Primario n T 1: Tumor de 1 cm. o Menos en su Dimensión Mayor. Limitado a la Tiroides

CLASIFICACIÓN n T 2: Tumor de Más de 1 cm. No Más de 4 cm. en su Dimensión Mayor Limitado a la Tiroides n T 3: Tumor de Más de 4 cm. en su Dimensión Mayor – Limitado a la Tiroides n T 4: Tumor de Cualquier Tamaño Se Extiende Fuera de la Cápsula Tiroidea

CLASIFICACIÓN n T 2: Tumor de Más de 1 cm. No Más de 4 cm. en su Dimensión Mayor Limitado a la Tiroides n T 3: Tumor de Más de 4 cm. en su Dimensión Mayor – Limitado a la Tiroides n T 4: Tumor de Cualquier Tamaño Se Extiende Fuera de la Cápsula Tiroidea

GANGLIOS n Son los Ganglios Cervicales y los Mediastínicos Superiores. n NX: Ganglios L. Regionales No pueden ser Evaluados n N 0: No hay MTTS Ganglionar Linfática Regional n N 1: Metástasis Ganglios Linfáticos Regionales n N 1 a: Metástasis a Ganglio(s) Linfático(s) Cervical(es) Ipsilateral(es) n N 1 b: Metástasis a Ganglio(s) Linfático(s) Mediastínico(s) o Cervical(es) Bilateral(es) de Línea Media o Contralateral(es)


CÁNCER DE TIROIDES

elobservadordellitoral. com Detectan 2. 800 casos de cáncer de tiroides por año n Publicado el 24 de febrero de 2011 n El trabajo difundido por la Asociación de Pacientes con Cáncer de Tiroides de la República Argentina (ACTIRA) añadió que esa enfermedad es de mayor prevalencia entre las mujeres, y que su detección se realiza con un examen clínico del cuello.

EPIDEMIOLOGÍA n Neoplasia más frecuente de CYC n n Tumor endócrino más común Solo 1% de todos los tumores malignos 1 -5% mujeres n 0. 5% hombres n n Incidencia mundial 1 x 100 000 H n 2. 6 x 100 000 M n Sherman S. Lancet 2003; 361: 501 -11 Vini L. Lancet Oncol 2002; 3: 407 -14

EPIDEMIOLOGÍA Incidencia n n 14. 6% en los últimos 40 años n 6. 6% anual 1998 -2002 Mejor detección? n Asociada a radiación? n n Mortalidad 21% Baker S. Eur J Radiol 2006; 60: 67 -69
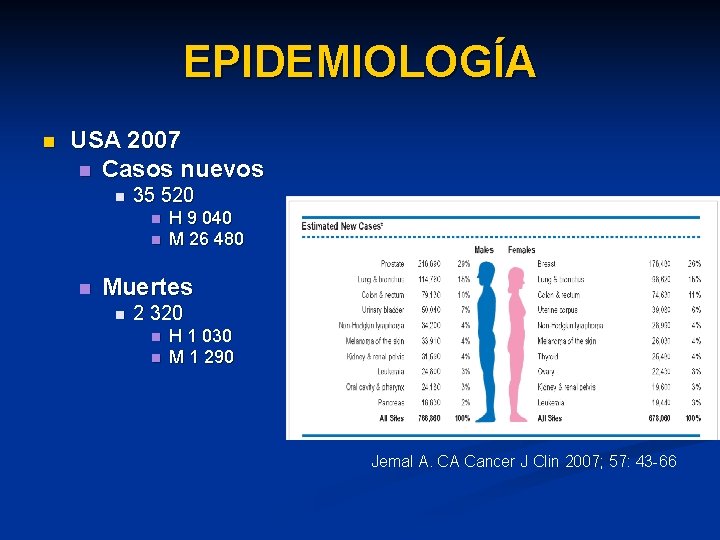
EPIDEMIOLOGÍA n USA 2007 n Casos nuevos n 35 520 n n n H 9 040 M 26 480 Muertes n 2 320 n n H 1 030 M 1 290 Jemal A. CA Cancer J Clin 2007; 57: 43 -66

EPIDEMIOLOGÍA n Relación M: H n n 2 -3: 1 Pico de edad H 65 -69 años n M 50 -54 años n n Riesgo de 1% durante la vida H 0. 3% n M 0. 84% n Moley J. World J Surg 2007; 31: 946 -56

EPIDEMIOLOGÍA n Nódulo tiroideo n Palpables n. M 5% n H 1% n USG n 19 -67% n Autopsia n 50% Nuevos nódulos 0. 1% a 2% por año Rosen J. J Surg Oncol 2006; 94: 649 -661

FACTORES DE RIESGO n Antecedente de radiación n Pacientes con E Hogk. tratados con RT n Aumento de riesgo 36. 4 veces n RR 3 -9 (5. 25) por Gy n Dosis de 20 -29 Gy RR 9. 8 n n SOLO 10% DE LOS CASOS Disminuye con dosis > 30 Gy Niños especialmente vulnerables n Latencia n n 5 -10 años 2. 2% por año Pico 30 años Williams E. J Surg Oncol 2006; 94 -670 -677 Robbins J. Rev Endocr Metabol Dis 2000; 1: 197 -203

FACTORES DE RIESGO Antecedente de radiación n Chernobyl 26 abril 1986 n Liberación n Niños <1 año 10 veces más riesgo n Tumores n n más agresivos Mutaciones RET-PTC n Aumento n de I 131 1990 2000 de 74 veces la incidencia 100 casos/año 1800 casos Williams E. J Surg Oncol 2006; 94 -670 -677 Robbins J. Rev Endocr Metabol Dis 2000; 1: 197 -203

FACTORES DE RIESGO n Deficiencia de I Promueve aumento de TSH n Ingesta mínima 100 mcg/día n n Promedio n en USA 200 -500 mcg/día Controversial Williams E. J Surg Oncol 2006; 94 -670 -677 Robbins J. Rev Endocr Metabol Dis 2000; 1: 197 -203

FACTORES DE RIESGO n Historia familiar n n Bien diferenciados 5% n n Papilar RR 10 n Desarrollan 3 -10% n Cáncer de tiroides familiar no medular n NEM 2 A n Cowden n FAP n n Medular 20% NEM 2 B n n AD Cáncer medular de tiroides Tumores de paratiroides multicéntricos Feocromocitoma (bilateral) n n Cáncer medular de tiroides Feocromocitoma Neuromas de mucosa Habito marfanoide Cáncer medular de tiroides familiar Moore F. J Surg Oncol 2006; 94: 719 -24 Malchoff CD. Cancer Control 2006; 13: 106 -10 n

PATOLOGÍA n Bien diferenciados n n Papilar Folicular n n Células de Hürtle Insular Indiferenciados n n 80% 10% Pobremente diferenciados n n 90% Anaplásico Medular 2 -5% 3 -5% Patel K. Cancer Control 2006; 13: 119 -28

PATOLOGÍA n MICROCARCINOMA n Según la OMS n Tumor < 1 cm de diámetro Autopsias n Tiroidectomías n 30% 24% Slough C. Cancer Control 2006; 13: 99 -105 Am J Otolaryngol 2005; 26: 249 -60

PATOLOGÍA n Carcinoma papilar n Características n Formación de papilas n n n Núcleo (“Orphan Annie eye”) Cuerpos de Psammoma (40 a 50%) Variantes n n n Folicular Esclerosante difuso Células altas Células columnares Insular Peor pronóstico Slough C. Cancer Control 2006; 13: 99 -105 Am J Otolaryngol 2005; 26: 249 -60
PATOLOGÍA n Carcinoma papilar n Extensión extratiroidea n 8 a 32% n n 30 a 40% Diseminación linfática n n 8% 6% 5% Multicéntrico n n Pretiroideos NLR Tráquea SV global 5 a 92% 10 a 89% 20 a 83% 35% clínicos Metástasis n n 1% al diagnóstico Hasta 25% desarrollarán Slough C. Cancer Control 2006; 13: 99 -105 Am J Otolaryngol 2005; 26: 249 -60

PATOLOGÍA n Carcinoma folicular Mayor frecuencia en zonas deficientes de I n Lesiones precursoras n n Adenomas No tiene características citológicas patognomónicas n Criterios de malignidad n n Invasión capsular n Invasión vascular Slough C. Cancer Control 2006; 13: 99 -105 Am J Otolaryngol 2005; 26: 249 -60
PATOLOGÍA n Carcinoma folicular n División n Mínimamente invasivo n n n Ampliamente invasivo n n n Agresivo localmente Tendencia a metástasis Diseminación hematógena más que linfática n n Comportamiento benigno Invasión capsular focal SV global 5 a 85% 10 a 80% 20 a 76% 16% vs 9% Metástasis n Al diagnóstico hasta 15% Slough C. Cancer Control 2006; 13: 99 -105 Am J Otolaryngol 2005; 26: 249 -60

PATOLOGÍA n Carcinoma medular n Tumor neuroendócrino n n n Representa solo el 5 a 10% de las neoplasias malignas del tiroides n n n Origen embriológico en el cuerpo ultimo branquial Distribuidas en la mitad superior de los lóbulos laterales 15% de las muertes por Ca de tiroides No se relaciona con la geografía ni con la disponibilidad de yodo No factor externo predisponente Clayman G. Otolaryngol Clin N Am 2003; 36: 91 -105 Pelizzo M. Eur J Surg Oncol 2006; 1 -5

PATOLOGÍA n Carcinoma anaplásico n n n De las más letales en el hombre Pico 7ª década de la vida Lesiones precursoras ? n n Agresivos localmente Diseminación a distancia temprana n n Bocio multinodular 30% Carcinoma bien diferenciado 23 -90% 20 a 50% al diagnóstico SV media 6 meses Green L. j Surg Oncol 2006; 94: 725 -36 Wiseman S. Head Neck 2003; 25: 662 -70

PATOLOGÍA n Carcinoma epidermoide n n n Raro < 1% Diagnóstico de exclusión Metaplasia? Comportamiento similar al anaplásico Linfoma tiroideo n n Sarcomas n n n Puede confundirse con variante fusiforme del anaplásico Liposarcoma, angiosarcoma, leiomiosarcoma, Lesiones metastásicas n n Riñón Mama Pulmón Útero 33% 16% 9% 7% 6ª década de la vida Hashimoto 80% n n n Riesgo > 70 veces LNH B y MALT Sniezek J. Otolaryngol Clin N Am 2003; 36: 107 -15 Lo C. Am J Surg 199; 177: 337 -39 Rodriguez J. J Am Coll Surg 1998; 187: 503

BIBLIOGRAFIA Farreras Rozman XV edición. Medicina Interna-Harrison 2011. Rev Edocrinol Nutr 2010; 8 (3): 87 -93 Uptodate: Diagnostic approach to and treatment of thyroid nodules.
- Slides: 86