BNG TUN HON CC NGUYN T HO HC
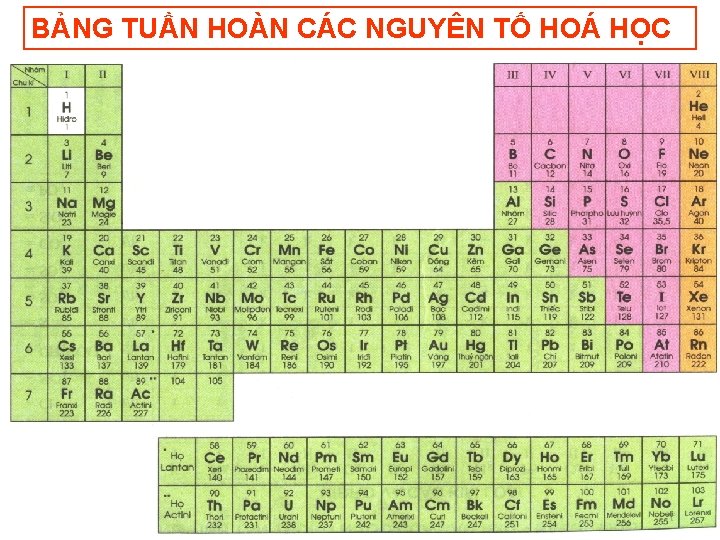
BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HOÁ HỌC

Bài 31 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng hệ thống tuần hoàn: - Các nguyên tố trong bảng hệ thống tuần hoàn được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
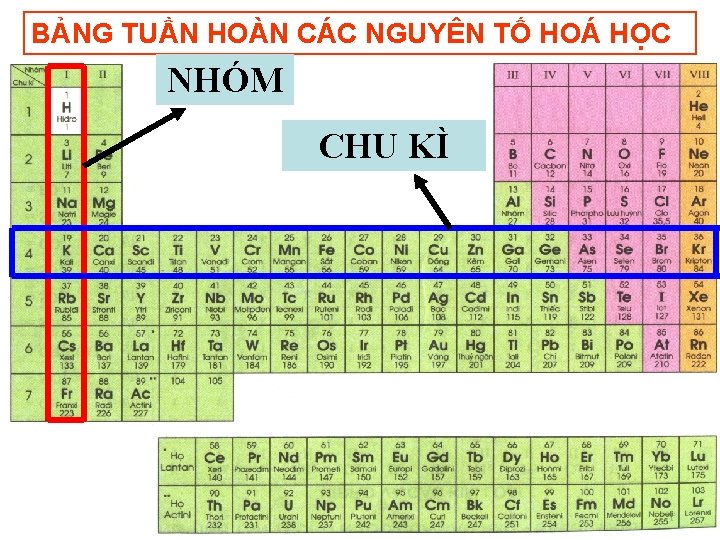
BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HOÁ HỌC NHÓM CHU KÌ

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng hệ thống tuần hoàn: II. Cấu tạo bảng tuần hoàn:

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng hệ thống tuần hoàn: II. Cấu tạo bảng tuần hoàn: - Ô nguyên tố - Chu kì - Nhóm

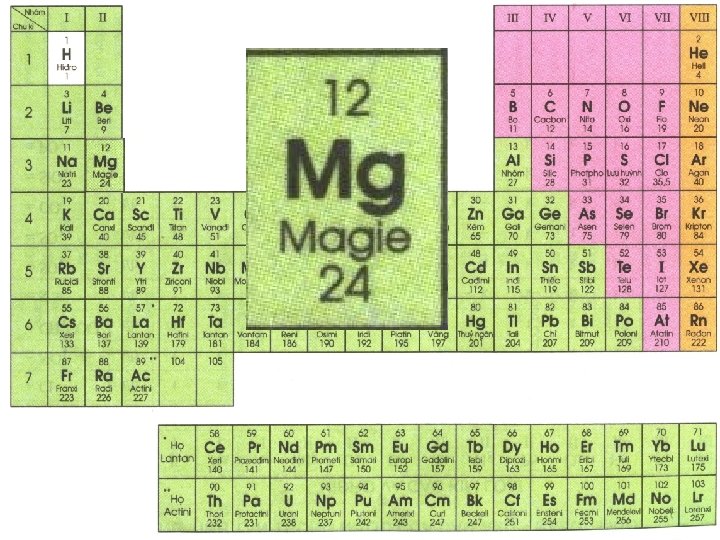
Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng hệ thống tuần hoàn: II. Cấu tạo bảng tuần hoàn: 1. Ô nguyên tố
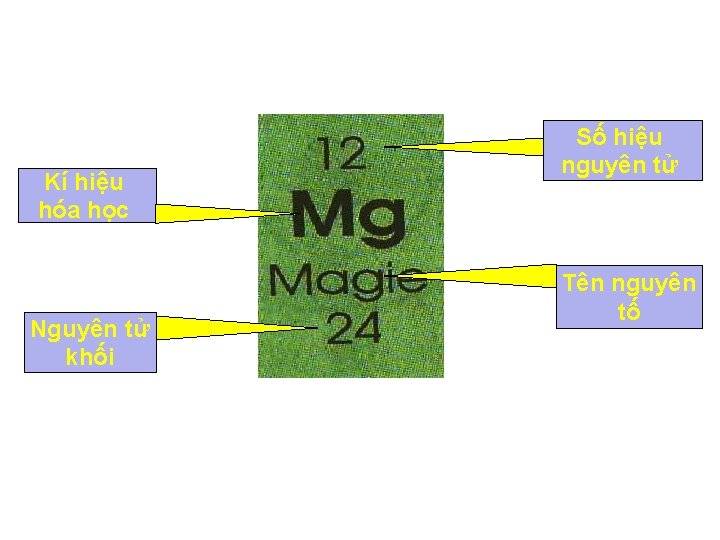
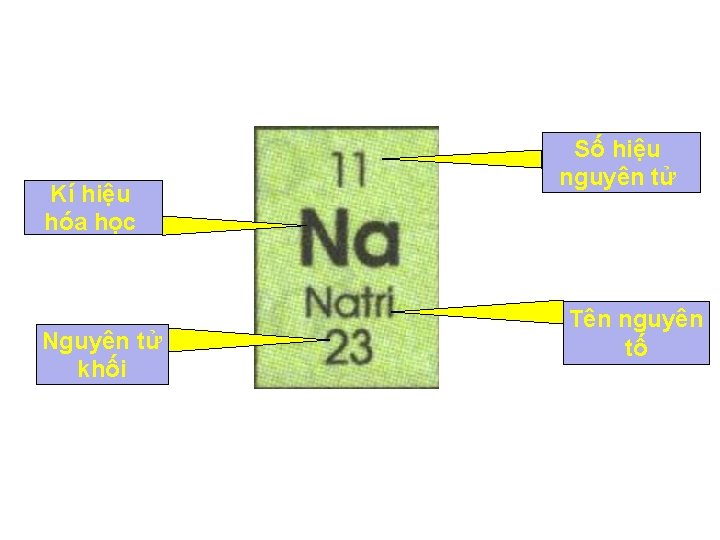
Kí hiệu hóa học Nguyên tử khối Số hiệu nguyên tử Tên nguyên tố
Kí hiệu hóa học Nguyên tử khối Số hiệu nguyên tử Tên nguyên tố

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng hệ thống tuần hoàn: II. Cấu tạo bảng tuần hoàn: 1. Ô nguyên tố cho biết: - Số hiệu nguyên tử - Kí hiệu hoá học - Tên nguyên tố - Nguyên tử khối

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng hệ thống tuần hoàn: II. Cấu tạo bảng tuần hoàn: 1. Ô nguyên tố Số hiệu nguyên tử có trị số bằng: - Số đơn vị điện tích hạt nhân - Số electrong nguyên tử Số hiệu nguyên tử trùng với số thứ tự của nguyên tố trong bảng tuần hoàn
BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HOÁ HỌC CHU KÌ 4

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn II. Cấu tạo bảng tuần hoàn. 1. Ô nguyên tố 2. Chu kì

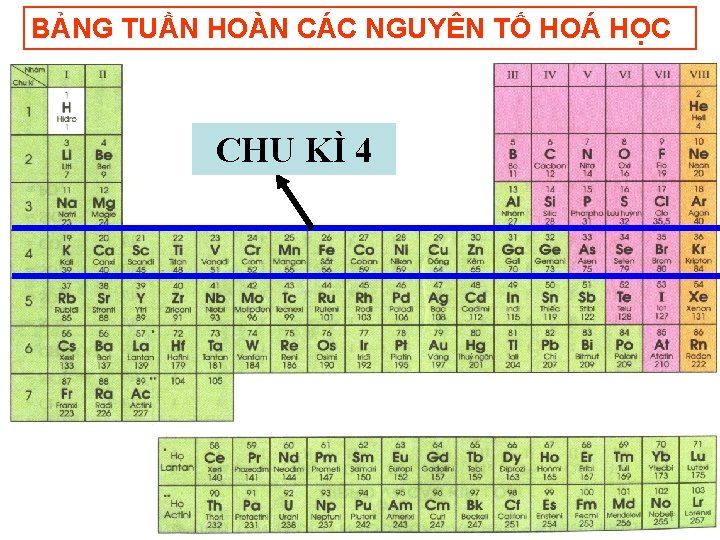
Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn II. Cấu tạo bảng tuần hoàn. 1. Ô nguyên tố 2. Chu kì Bảng tuần hoàn gồm 7 chu kì - 1, 2, 3 được gọi là chu kì nhỏ - 4, 5, 6, 7 được gọi là chu kì lớn (chu kì 7 chưa hoàn chỉnh)

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn II. Cấu tạo bảng tuần hoàn. 1. Ô nguyên tố 2. Chu kì - Chu kì lµ d·y c¸c nguyªn tè được s¾p xÕp theo chiÒu tăng dần của ®iÖn tÝch h¹t nh©n nguyên tử.

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn II. Cấu tạo bảng tuần hoàn. 1. Ô nguyên tố 2. Chu kì 3. Nhóm

Tiết 39 SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC I. Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn. II. Cấu tạo bảng tuần hoàn. 1. Ô nguyên tố 2. Chu kì 3. Nhóm - Nhãm gåm c¸c nguyªn tè có tính chất tương tự nhau, được s¾p xÕp thµnh cét dọc, theo chiÒu tăng cña ®iÖn tÝch h¹t nh©n nguyen tư.
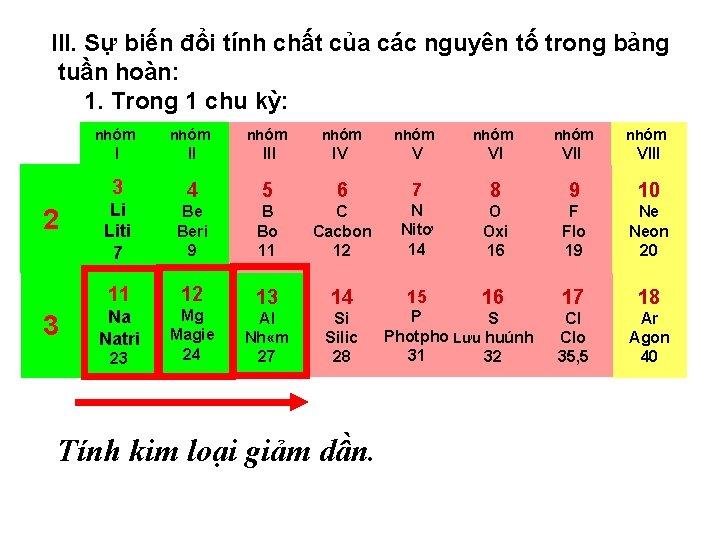
III. Sự biến đổi tính chất của các nguyên tố trong bảng tuần hoàn: 1. Trong 1 chu kỳ: 2 3 nhóm nhóm I II IV V VI VIII 3 Li Liti 7 4 5 6 7 8 9 10 Be Beri 9 B Bo 11 C Cacbon 12 N Nitơ 14 O Oxi 16 F Flo 19 Ne Neon 20 11 12 Mg Magie 24 14 15 Na Natri 13 16 17 18 Al Nh «m 27 Si Silic 28 Cl Clo 35, 5 Ar Agon 40 23 Tính kim loại giảm dần. P S Photpho Lưu huúnh 31 32
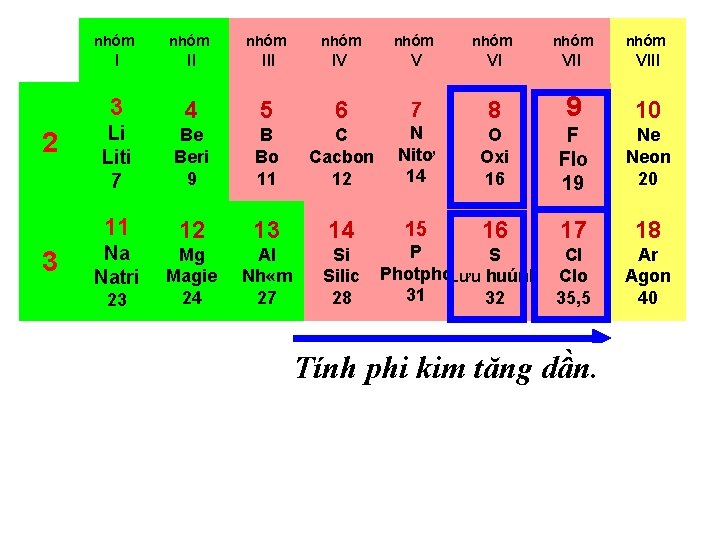
2 3 nhóm nhóm I II IV V VI VIII 3 5 6 7 Li Liti 7 4 9 10 Be Beri 9 B Bo 11 C Cacbon 12 N Nitơ 14 8 O Oxi 16 F Flo 19 Ne Neon 20 11 12 13 14 15 16 17 18 Mg Magie 24 Al Nh «m 27 Si Silic 28 Na Natri 23 P S Cl Photpho. Lưu huúnh Clo 31 32 35, 5 Tính phi kim tăng dần. Ar Agon 40
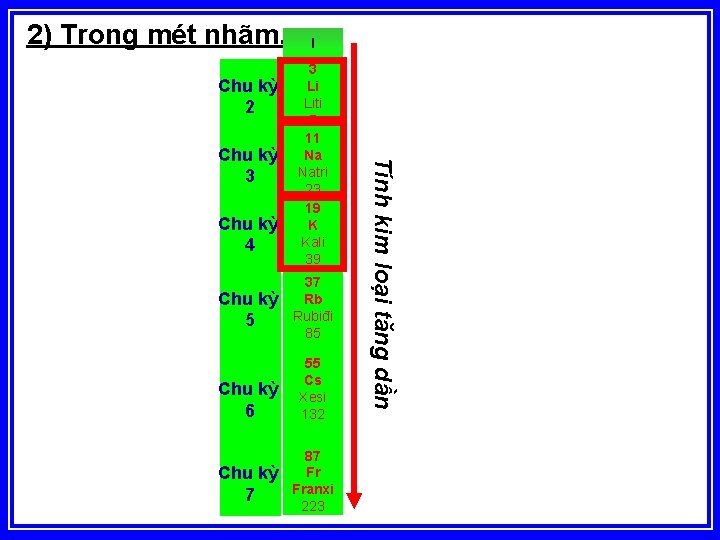
2) Trong mét nhãm. Chu kỳ 2 Chu kỳ 4 Chu kỳ 5 Chu kỳ 6 Chu kỳ 7 3 Li Liti 7 11 Na Natri 23 19 K Kali 39 37 Rb Rubiđi 85 55 Cs Xesi 132 87 Fr Franxi 223 Tính kim loại tăng dần Chu kỳ 3 I
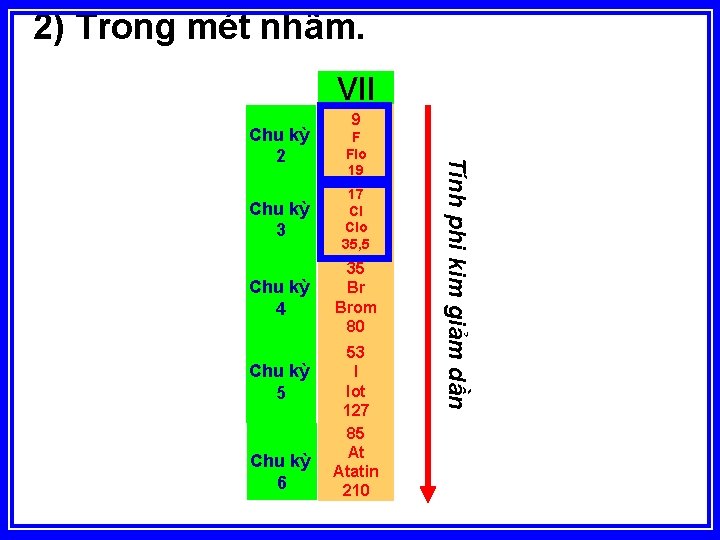
2) Trong mét nhãm. VII F Flo 19 Chu kỳ 3 17 Cl Clo 35, 5 Chu kỳ 4 35 Br Brom 80 Chu kỳ 5 Chu kỳ 6 53 I Iot 127 85 At Atatin 210 Tính phi kim giảm dần Chu kỳ 2 9

IV. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học : 1. Biết vị trí của nguyên tố ta có thể suy đoán cấu tạo nguyên tử và tính chất của nguyên tố. 2 3 4 nhóm nhóm I II IV VI VIII 3 4 5 6 V 7 8 10 B Bo 11 C Cacbon 12 O 9 Be Beri 9 N Nitơ F Flo 19 Ne Neon 20 12 13 14 15 Oxi 16 16 17 18 A Mg Magie 24 Al Nh «m 27 Si Silic 28 Photpho Lưu huúnh 31 19 20 31 32 33 32 34 Ca Canxi 40 Ga Gali 70 Ge Gemani 73 Li Liti 7 11 K kali 39 14 P As Asen 75 S Se Selen 79 Cl Clo 35, 5 35 Br Brom 80 Ar Agon 4 o 36 Kr Kripton 84
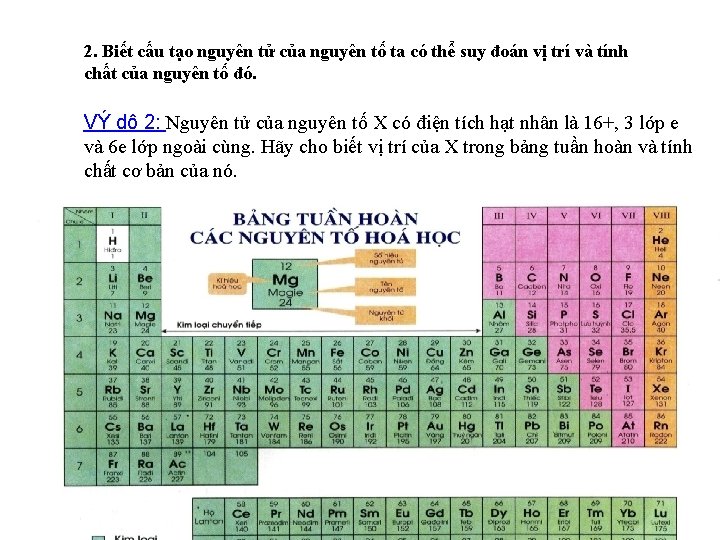
2. Biết cấu tạo nguyên tử của nguyên tố ta có thể suy đoán vị trí và tính chất của nguyên tố đó. VÝ dô 2: Nguyên tử của nguyên tố X có điện tích hạt nhân là 16+, 3 lớp e và 6 e lớp ngoài cùng. Hãy cho biết vị trí của X trong bảng tuần hoàn và tính chất cơ bản của nó.

HƯỚNG DẪN HỌC SINH TỰ HỌC Ở NHÀ: - Học bài - Làm các bài tập 1, 2, 4, 5, 6 SGK tr 101. - Xem lại tính chất hóa học của phi kim, Clo, cacbon và các hợp chất của cacbon, sơ lược bảng tuần hoàn các nguyên tố hóa học để tiết sau luyện tập chương.
- Slides: 26