Bloque f Equipo Cromo Lantanidos l l Grupo

Bloque f Equipo: Cromo

Lantanidos l l Grupo de elementos que forman parte del periodo 6 de la tabla periódica. Estos elementos son llamados tierras raras debido a que se encuentran en forma de óxidos. También se les conoce como elementos de transición interna. El nombre procede del lantano, que suele incluirse dentro de este grupo, dando un total de 15 elementos, desde el de número atómico 57 (lantano) al 71 (lutecio).

el lantano no tiene electrones ocupando ningún orbital f, mientras que los catorce siguientes elementos tienen éste orbital 4 f parcial o totalmente lleno. l Cerio, praseodimio, neodimio, prometio, samario, europio, gadolinio, terbio, disprosio, holmio, erbio, tulio, iterbio, lutecio. l

Características generales Su ultima capa electrónica es la 4 f. l su estado de oxidación más importante es el +3. pero también presentan el estado de oxidación +2 y +4. l
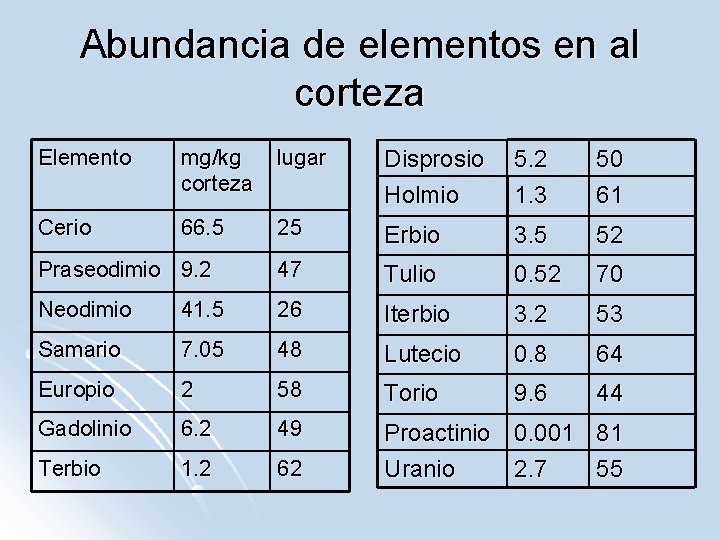
Abundancia de elementos en al corteza Elemento mg/kg corteza lugar Disprosio Holmio 5. 2 1. 3 50 61 Cerio 66. 5 25 Erbio 3. 5 52 Praseodimio 9. 2 47 Tulio 0. 52 70 Neodimio 41. 5 26 Iterbio 3. 2 53 Samario 7. 05 48 Lutecio 0. 8 64 Europio 2 58 Torio 9. 6 44 Gadolinio 6. 2 49 Terbio 1. 2 62 Proactinio 0. 001 81 Uranio 2. 7 55





Cerio El cerio es uno de los 14 elementos químicos que siguen al lantano en la tabla periódica, denominados por ello lantánidos. De color gris metálico similar al hierro, se torna pardo rojizo al exponerlo al aire. Fue descubierto en 1803 por Martin Heinrich Klaproth y Jöns Jacob Berzelius e independientemente por Wilhelm von Hisinger. Tomó su nombre de Ceres, el planeta enano que se había encontrado dos años antes.

Nombre Número atómico Cerio 58 Valencia 3, 4 Estado de oxidación +4 Electronegatividad 1, 1 Radio covalente (Å) Radio iónico (Å) Radio atómico (Å) Configuración electrónica Primer potencial de ionización (e. V ) (e. V) Masa atómica (g/mol ) (g/mol) 1, 65 1, 01 1, 81 [Xe]4 f 15 d 16 s 2 6, 94 140, 12 Densidad (g/ml ) (g/ml) 6, 67 Punto de ebullición (ºC ) (ºC) 3468 Punto de fusión (ºC ) (ºC) Descubridor 795 W. von Hisinger en 1903

Elemento químico, Ce, número atómico 58, peso atómico 140. 12. Es el elemento metálico más abundante del grupo de las tierras raras en la tabla periódica. El elemento natural está constituido de los isótopos 136 Ce, 138 Ce, 140 Ce y 142 Ce. El 142 Ce radiactivo tiene una vida media de 5 x 1015 años. El cerio se encuentra mezclado con otras tierras raras en muchos minerales, en particular en monacita y blastnasita y también se halla entre los productos de la fisión de uranio, torio y plutonio. Aunque la valencia común del cerio es 3, forma también una serie de compuestos tetravalentes y es la única tierra rara que existe como ion tetravalente en solución acuosa. Aunque en alta pureza se le puede separar de las otras tierras raras por métodos de intercambio iónico, por lo general se separa químicamente aprovechando su estado tetravalente. Isótopos En la naturaleza, el cerio tiene tres isótopos estables y uno radiactivo: 136 Ce, 138 -Ce, 140 -Ce y 142 -Ce, siendo el 140 -Ce el más abundante de ellos (un 88, 48%). En total se conocen 27 radioisótopos, siendo el 142 -Ce con 5× 1016 años el de mayor vida media. Este elemento también tiene dos metaestados.

Usos y Aplicaciones Mecheros que sirven para aumentar el brillo de la luz. El sulfato de Cerio se utiliza en la fotografía. El cerio y sus derivados tienen muchas aplicaciones. El dióxido de cerio se emplea en las industrias ópticas para la pulimentación de lentes. Algunas de sus sales se usan en fotografía, cerámica e industrias textiles. Uno de los muchos usos de sus aleaciones es la fabricación de piedras de mechero. Algunos de sus derivados se usan en pirotecnia y como materiales cerámicos. Catalizador en el refinado del petróleo. El cerio raramente se encuentra en la naturaleza, ya que se da en cantidades muy pequeñas. El cerio normalmente se encuentra solamente en dos tipos distintos de minerales: el lantano y el didmio. El uso del cerio sigue aumentando, debido al hecho de que es útil para producir catalizadores y para pulir cristales.

Efecto en la salud El cerio es uno de los elementos químicos raros, que puede ser encontrado en equipos tales como televisiones en color, lámparas fluorescentes y cristales. Todos los compuestos químicos raros tienen propiedades comparables. El cerio raramente se encuentra en la naturaleza, ya que se da en cantidades muy pequeñas. El cerio normalmente se encuentra solamente en dos tipos distintos de minerales. El uso del cerio sigue aumentando, debido al hecho de que es útil para producir catalizadores y para pulir cristales. El cerio es más peligroso en el ambiente de trabajo, debido al hacho de que las humedades y los gases pueden ser inhalados con el aire. Esto puede causar embolias pulmonares, especialmente durante exposiciones a largo plazo. El cerio puede ser una amenaza para el hígado cuando se acumula en el cuerpo humano.

Abundancia La principal mena del cerio es la monacita, Ce. PO 4. Otros minerales importantes son la cerita, H 3(Ca, Fe)Ce 3 Si 3 O 13 , y la bastnaesita, Ce. FCO 3. Se encuentra acompañando a otros metales de las tierras raras en la monacita ((Ce, La, Nd, Pr)PO 4), que se encuentra ampliamente distribuida por el mundo, la bastnaesita, abundante en el sur de California, cerita, con yacimientos importantes en Suecia y alanita, que abunda en Groenlandia. El Cerio es el elemento más abundante de las tierras raras, ocupa el puesto 25 entre los 78 elementos más estables y comunes.

SAMARIO

Propiedades l l l Es un metal sólido, de color blanco grisáceo brillante, duro y quebradizo que conduce bien el calor y la electricidad. Se conocen tres variedades cristalinas con puntos de transición a 734 y 922ºC. Es poco reactivo, se empaña lentamente en el aire húmedo a la temperatura ambiente y arde en el aire a 150ºC. Reacciona lentamente con el agua, dando hidrógeno y se ataca por los ácidos para dar sales generalmente trivalentes de color amarillo pálido. El samario puede obtenerse por reducción de su óxido con lantano.

Valores de las propiedades

Aplicaciones El óxido de samario se utiliza en óptica para absorber la luz infrarroja l Como catalizador en la deshidratación y en la deshidrogenación de etanol. l Fabricación de lámparas de arco voltaico de carbono, usadas en la industria del cine para la iluminación de los estudios y las luces de los proyectores. l

Forma un compuesto con el cobalto (Sm. Co 5) que es un poderoso imán permanente con mayor resistencia a la desmagnetización que cualquier otro material conocido. l Puede ser encontrado en equipos tales como televisiones en color, lámparas fluorescentes y cristales. l

Efectos en la Salud y en el ambiente l El samario es vertido al medio ambiente en muchos lugares diferentes, principalmente por industrias productoras de petróleo. Puede entrar en el medio ambiente cuando se tiran los equipos domésticos. El samario se acumulará gradualmente en los suelos y en el agua de los suelos y esto llevará finalmente a incrementar la concentración en humanos, animales y partículas del suelo. l En los animales acuáticos provoca daños a las membranas celulares, lo que tiene varias influencias negativas en la reproducción y en las funciones del sistema nervioso. l Por inhalación de los vapores pueden producirse embolias pulmonares y daños en el hígado.
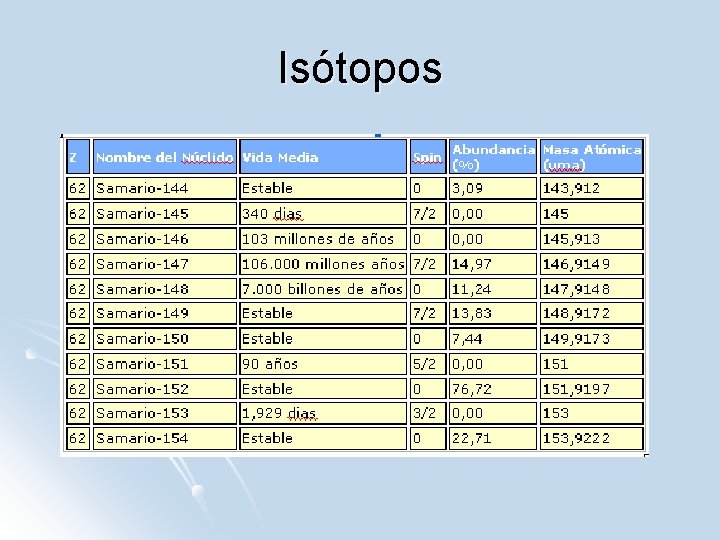
Isótopos
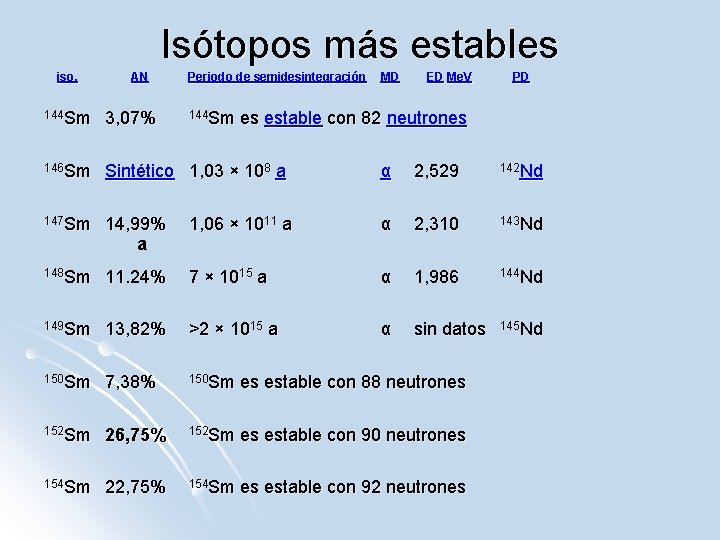
Isótopos más estables iso. AN Periodo de semidesintegración MD ED ED Me. V PD 144 Sm 3, 07% 144 Sm es estable con 82 neutrones 146 Sm Sintético 1, 03 × 108 a α 2, 529 142 Nd 147 Sm 14, 99% a 1, 06 × 1011 a α 2, 310 143 Nd 148 Sm 11. 24% 7 × 1015 a α 1, 986 144 Nd 149 Sm 13, 82% >2 × 1015 a α sin datos 145 Nd 150 Sm 7, 38% 150 Sm es estable con 88 neutrones 152 Sm 26, 75% 152 Sm es estable con 90 neutrones 154 Sm 22, 75% 154 Sm es estable con 92 neutrones

Torio Número atómico: 90 Valencia: 3 Estado de oxidación: +4 Electronegatividad: 1, 3 Radio covalente (Å): 1, 65 Radio iónico (Å): 0, 95 Radio atómico (Å): 1, 82 Configuración electrónica: [Rn]6 d 27 s 2 Primer potencial de ionización (e. V) - Masa atómica (g/mol): 232, 038 Densidad (g/ml): 11, 7 Punto de ebullición (ºC): 3850 Punto de fusión (ºC): 1750

Historia El torio se llamó así en honor a Thor, el dios escandinavo de la guerra. Fue descubierto en Suecia por Jöns Jakob Berzelius en 1828. Setenta años más tarde el matrimonio Pierre Curie y Marie Curie pusieron de manifiesto el carácter radiactivo del elemento.

Es un elemento de la serie de los Actínidos que se encuentra en estado natural en los minerales monazita, torita y troyanita. El torio pertenece a la familia de las substancias radioactivas, lo que significa que su núcleo es inestable y que en un lapso de tiempo más o menos largo se transforma en otro elemento. El torio en estado puro, es un metal blanco-plata que se oxida con mucha lentitud. Si se reduce a un polvo muy fino y se calienta, arde emitiendo una luz blanca deslumbrante.

Serie del Torio Cuando un átomo de torio 232 se desintegra emite una partícula alfa, formada por dos protones y dos neutrones. La emisión de la partícula alfa reduce el número atómico del torio 232 en dos unidades, y el número másico en cuatro, transformándolo en el isótopo 228 de otro elemento, el radio 228. Posteriores desintegraciones forman la cadena natural del torio. Este proceso continúa hasta que se forma finalmente un elemento no radiactivo, y por tanto estable, que es el plomo. Gracias al periodo tan grande de desintegración del torio 232, continuará produciendo elementos de su serie durante miles de millones de años
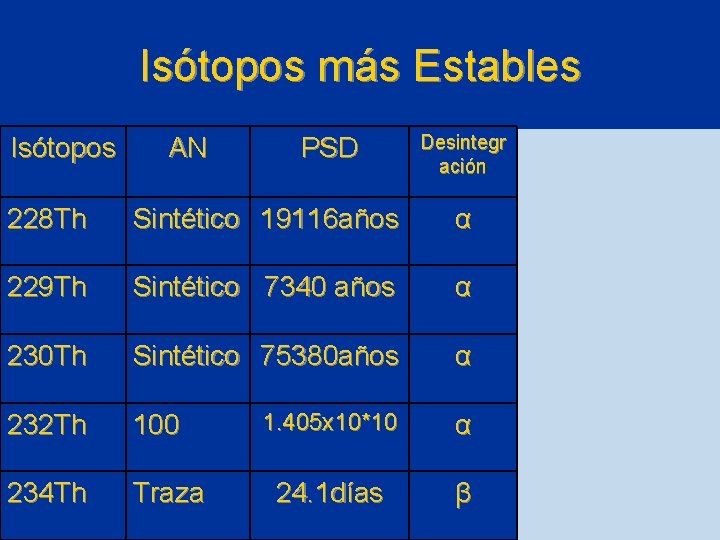
Isótopos más Estables Isótopos AN PSD Desintegr ación 228 Th Sintético 19116 años α 229 Th Sintético 7340 años α 230 Th Sintético 75380 años α 232 Th 100 1. 405 x 10*10 α 234 Th Traza 24. 1 días β

Aplicaciones: Sus principales aplicaciones son en aleaciones con magnesio, utilizado para motores de avión. Tiene un potencial muy grande de poder ser utilizado en el futuro combustible nuclear, pero esa aplicación todavía está en fase de desarrollo. Se incorpora al Tungsteno metálico para fabricar filamentos de lámparas eléctricas. Para fabricar electrodos especiales de soldadura, aleado con Tungsteno (Wolframio) creando la aleación con más alto punto de fusión existente, cerca de los 4000º ,

Los vidrios que contienen óxido de torio el tiene un alto índice de refracción y una baja dispersión por lo que se utilizan en la fabricación de lentes de calidad para cámaras e instrumentos científicos. Se utiliza en la industria electrónica como detector de oxígeno.

Protactinio Símbolo: Pa l Z = 91 l Configuración electrónica: 5 f 2 6 d 7 s 2 l Punto de fusión: 1572°C l Radio atómico: 1. 642 A l Estados de oxidación: +3, +4, +5 l

Su presencia en la corteza terrestre se estima del orden de 0, 00001 ppb. l Se forma por transmutación del torio en la familia radiactiva natural del 235 U, por lo que se encuentra en los minerales de este elemento. l

El protactinio esta presente como 231 Pa en la pechblenda o uraninita (Pech = una forma de alquitrán; blenden = lucir, brillar, cegar) en una cantidad aproximada de 0. 1 ppm l Hay depósitos importantes en Jachymov (República Checa), Kasolo (Zaire) y en Canadá l

Isotopos l Se han caracterizado 29 radioisótopos del protactinio siendo los más estables el 231 Pa, con una vida media de 32. 760 años; el 233 Pa, con una vida media de 26, 967 días; y el 230 Pa con una vida media de 17, 4 días. El resto de isótopos radiactivos tienen vidas medias inferiores a 1, 6 días y la mayoría tienen vidas medias menores de 1, 8 segundos.

Compuestos de protactinio (V) l El pentóxido, Pa 2 O 5, obtenido por calcinación de otros compuestos al aire, posee una estructura cristalina cúbica: al calentarlo al vacío se obtiene una fase subóxido Pa. O 2. 3 color negro, y finalmente, Pa. O 2

El pentafluoruro se obtiene como un sólido blanco por fluoración del Pa. F 4; se sublima al vacío por arriba de 500°. Es muy soluble en HF 1 M, pero la evaporación de las soluciones acuosas solo da mezclas l Los pentahalogenuros se pueden obtener por acción del SOCl 2, Br 2 o I 2, respectivamente, sobre un “carburo”, producido por reducción del Pa 2 O 5 con carbón a 1700° l

Compuestos de protactinio (IV) l El fluoruro Pa. F 4 tiene un punto de fusión elevado y es insoluble en solución de HNO 3 -HF. También es posible obtener el estado de oxidación en solución acuosa por reducción de soluciones de Pa. V con Cr 2+ o amalgama de Zn, pero en las soluciones se oxidan rápidamente al aire

Uranio Descubierto como óxido en 1789 en la pechblenda por el químico alemán Martin Heinrich Klaproth. l En 1841 E. M. Peligot aisló el uranio metalico. l l Las propiedades radioactivas del uranio fueron puestas de manifiesto en 1896 por el físico francés Antoine Henri Becquerel.

Estado Natural l l El uranio nunca se encuentra en estado libre. Se encuentra como óxido o sal compleja en minerales tales como: Pechblenda, óxido mixto de composición entre UO 2 y U 3 O 8 Carnotita, un vanadato de uranilo y potasio ((VO 4 UO 2 K)2 • 3 H 2 O) Uraninita, en las arenas de monacita, en las rocas ígneas y en el lignito.

El origen del uranio l l El uranio es el elemento natural de mayor número atómico. No obstante, es de suponer que ese uranio es un producto de la desintegración de elementos con peso atómico más alto, que pueden haber estado presentes en la tierra o en cualquier otra parte del universo y que se habrían formado en procesos estelares como la explosión de supernovas o el propio big-bang.
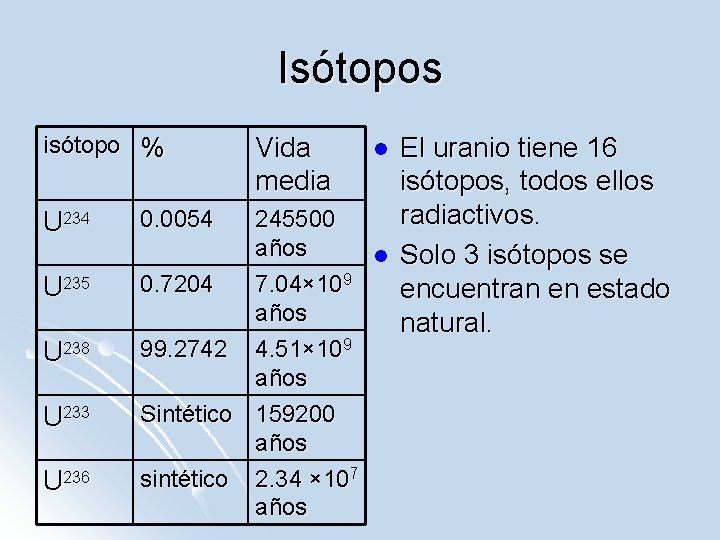
Isótopos isótopo % U 234 U 235 U 238 U 233 U 236 0. 0054 Vida media l 245500 años l 0. 7204 7. 04× 109 años 99. 2742 4. 51× 109 años Sintético 159200 años sintético 2. 34 × 107 años El uranio tiene 16 isótopos, todos ellos radiactivos. Solo 3 isótopos se encuentran en estado natural.
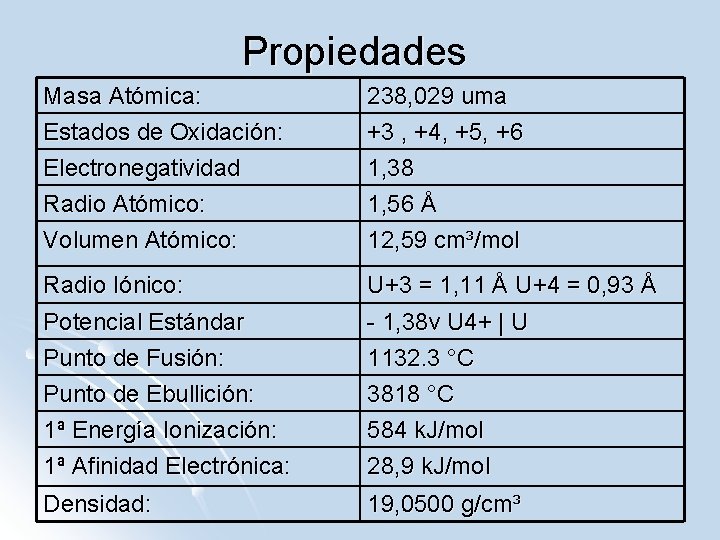
Propiedades Masa Atómica: Estados de Oxidación: Electronegatividad Radio Atómico: 238, 029 uma +3 , +4, +5, +6 1, 38 1, 56 Å Volumen Atómico: 12, 59 cm³/mol Radio Iónico: U+3 = 1, 11 Å U+4 = 0, 93 Å Potencial Estándar Punto de Fusión: Punto de Ebullición: 1ª Energía Ionización: 1ª Afinidad Electrónica: - 1, 38 v U 4+ | U 1132. 3 °C 3818 °C 584 k. J/mol 28, 9 k. J/mol Densidad: 19, 0500 g/cm³

Producción

Extraccion l l La pechblenda triturada y enriquecida por flotación se mezcla con sulfúrico y nítrico. El uranio se disuelve para formar sulfato de uranilo, UO 2 SO 4 y el radio y los otros metales se precipitan como sulfatos. Adición de Na. OH, el uranio precipita como diuranato de sodio, Na 2 U 2 O 7 • 6 H 2 O, conocido también como el óxido amarillo de uranio. Para obtener uranio desde la carnotita, el mineral es finamente triturado y tratado con una solución caliente de sosa cáustica y potasa para disolver el uranio, el radio y el vanadio que posteriormente han de separarse. El uranio extraído se purifica por diversos métodos, principalmente por formación de haluros u óxidos que se reducen con magnesio, calcio, aluminio o carbón a altas temperaturas.

l l El metal también puede ser producido por electrólisis de KUF 5 o UF 4, disueltos en una mezcla fundida de Ca. Cl 2 y Na. Cl. La preparación de uranio de alta pureza se realiza mediante la descomposición térmica de sus haluros sobre un filamento incandescente. Tras cualquiera de los procesos, el uranio se refunde para comercializarlo en lingotes de metal puro o aleado según el uso al que vaya destinado.

Aplicaciones l l Por su alta densidad se usa como contrapeso para el control de aeronaves, veleros y satélites artificiales. El uranio metálico se usa como blanco en las radiografías de rayos X de alta energía, el nitrato se ha utilizado como toner fotográfico y el acetato se usa en química analítica
l l l Material de blindaje vs radiaciones de alta penetración. El uranio empobrecido es usado en la producción de municiones perforantes y blindajes de alta resistencia. Construcción de armamento

l l l Se emplea en los dispositivos inerciales de orientación en giróscopos. Todos los isótopos son importantes en la industria nuclear tanto de armamento como de producción de energía. Los compuestos se usan en la fabricación de vidrios especiales de tonos verdes (Na 2 U 2 O 7. 6 H 2 O) El 238 U, el isótopo de mayor vida media, se ha usado para determinar la edad de las rocas ígneas. Este isótopo puede convertirse en plutonio fisionable según el proceso: 238 U + n + γ 239 U + β 239 Np + β 239 Pu.

l l El uranio natural, ligeramente enriquecido con 235 U en un pequeño porcentaje , se usa para abastecer los reactores nucleares para la producción de energía eléctrica. El torio natural puede irradiarse con neutrones como se indica a continuación para producir el isótopo 233 U: 232 Th + n+ γ 233 Th + β 233 Pa + β 233 U

l Mientras que el torio no es fisionable, el 233 U sí lo es, y puede usarse como combustible nuclear. Un kg de uranio completamente fisionado tiene un poder como combustible equivalente a unas 6. 000 toneladas de carbón. Tras el descubrimiento de la fisión nuclear, el uranio llegó a convertirse en un metal estratégico hasta el punto de que su uso estaba restringido.

l l Sin embargo, a pesar de constituir una poderosa fuente de energía, existe una fuerte controversia social debida a los problemas de seguridad en las plantas y, sobre todo, los del almacenamiento de los residuos radiactivos. El 17% de la electricidad consumida en el planeta es producida en reactores nucleares que utilizan como combustible el uranio.
- Slides: 52