Blkoviny Paed Dr Ivana Tpferov Stedn prmyslov kola

Bílkoviny Paed. Dr. Ivana Töpferová Střední průmyslová škola, Mladá Boleslav, Havlíčkova 456 CZ. 1. 07/1. 5. 00/34. 0861 MODERNIZACE VÝUKY

Anotace: výuková prezentace v prvním ročníku studia Předmět: chemie Ročník: I. ročník SŠ Tematický celek: organická chemie a biochemie Klíčová slova: přírodní látky, bílkoviny, vlastnosti, reakce bílkovin, rozdělení, druhy Forma: vysvětlování, demonstrace Datum vytvoření: 3. 6. 2013

Přírodní látky = organické sloučeniny, které vznikají biochemickými reakcemi v rostlinách a živočiších
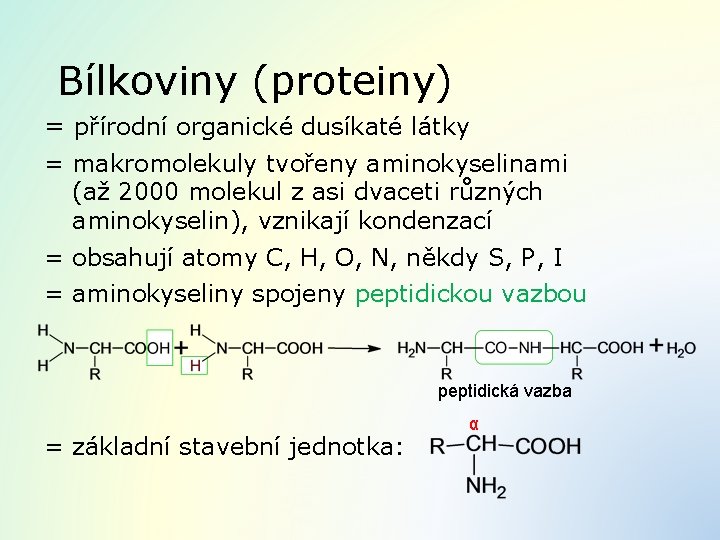
Bílkoviny (proteiny) = přírodní organické dusíkaté látky = makromolekuly tvořeny aminokyselinami (až 2000 molekul z asi dvaceti různých aminokyselin), vznikají kondenzací = obsahují atomy C, H, O, N, někdy S, P, I = aminokyseliny spojeny peptidickou vazbou peptidická vazba = základní stavební jednotka: α

Bílkoviny = vyskytují se v luštěninách, obilovinách, mase, vejcích, mléce a mléčných výrobcích = rostliny si je vyrábí samy z minerálních látek (dusičnanů) = živočichové a člověk přijímá v potravě bílkoviny, získává aminokyseliny, z nich pak vytváří vlastní bílkoviny Obr. 1 Maso Obr. 2 Vejce Obr. 3 Mléčné výrobky

Reakce bílkovin a) Srážecí reakce = denaturace bílkovin = vlivem roztoků kyselin, zásad a solí, ozařováním … = při teplotě kolem 40°C dochází k poškození některých bílkovin, při teplotě 60°C ztrácejí biologické vlastnosti, pozměňuje se struktura Pokus: bílek z vajíčka + 100 ml vody, přefiltrovat 1. zkumavka = bílek + konc. HCl nebo ocet 2. zkumavka = bílek + 10% roztok Na. OH 3. zkumavka = bílek + nasycený roztok Cu. SO 4 4. zkumavka = bílek zahřát

bílek var HNO 3 CUSO 4. 5 H 2 O Obr. 4 Srážecí a xantoproteinová reakce bílkovin

Reakce bílkovin b) Xantoproteinová reakce = působení HNO 3 (nitrace aromatických aminokyselin v bílkovině) Pokus: Do zkumavky s bílkem přidat koncentrovanou HNO 3, opatrně zahřívat k varu a pozorovat vznik sraženiny a změnu zabarvení, přikápnout amoniak nebo Na. OH a pozorovat změnu c) Biuretová reakce = důkaz peptidické vazby Pokus: Do zkumavky s bílkem přidat stejné množství roztoku Na. OH (w% = 10%), ke směsi přikápnout roztok Cu. SO 4. 5 H 2 O (w%= 1%), protřepat a pozorovat změnu zabarvení

Struktura a vlastnosti bílkovin = primární, sekundární, terciární a kvartérní struktura bílkovin – určuje pořadí aminokyselin, prostorový tvar molekuly = tepelně zpracované bílkoviny jsou stravitelnější, teplem se nemění biologická hodnota bílkovin, pozměňuje se struktura = citlivé na teplo = nízkou teplotou k denaturaci nedochází (uchovávání bílkovin v mrazničkách, uchovávání krve a orgánů pro transplantaci) = s vodou tvoří koloidní roztok

Rozdělení bílkovin Podle počtu aminokyselin v řetězci: 2 -10 aminokyselin oligopeptidy více než 10 aminokyselin polypeptidy více než 100 aminokyselin bílkoviny

Rozdělení bílkovin Podle tvaru: ü fibrilární – vláknité (kolagen, keratin, elastin) ü globulární – kuličkové Podle rozpustnosti: ü skleroproteiny – fibrilární, nerozpustné ü sferoproteiny – globulární, rozpustné

Rozdělení bílkovin ü jednoduché – pouze čistá bílkovina ü složené – mají i nebílkovinnou část – lipoproteiny, metaloproteiny (transferin), hemoproteiny (hemoglobin), fosfoproteiny (kasein), glykoproteiny (mucin), nukleoproteiny Obr. 5 Zdroj bílkovin

Funkce bílkovin • stavební – výstavba buněčných struktur a tkání a obnova buněk (kreatin, kolagen) • transportní (hemoglobin, transferin) • zajišťující pohyb (tubulin, myozin, aktin) • ochranná a obranná (imunoglobuliny) • řídící a regulační (hormony) • katalytická – urychlují chemické reakce • zdroj energie – ve stavech nouze • nezbytné k růstu organismu

Seznam obrázků: Obr. 1, 2, 3, 4, 5 foto Ivana Töpferová

Použité zdroje: • ŠIBOR, J. , PLUCKOVÁ, I. , MACH, J. Chemie pro 9. ročník. Úvod do obecné a organické chemie, biochemie a dalších chemických oborů. Brno: NOVÁ ŠKOLA, s. r. o. , 2011. ISBN 978 -80 -7289 -282 -2. • BANÝR, J. , BENEŠ, P. A KOLEKTIV. Chemie pro střední školy. Praha: SPN, a. s. , 1995. ISBN 80 -85937 -11 -5. • ČTRNÁCTOVÁ, H. , KOLÁŘ, K. , SVOBODOVÁ, M. , ZEMÁNEK, F. Přehled chemie pro základní školy. Praha: SPN a. s. , 2006. ISBN 80 -7235 -260 -1. • ŠKODA, J. , DOULÍK, P. Chemie 8 učebnice pro základní školy a víceletá gymnázia. Plzeň: Fraus, 1. vydání, 2006. ISBN 80 -7238 -442 -2.
- Slides: 15