Bitkilerde reme oaltma 1 1 Eeyli generatif oalmaoaltma

Bitkilerde Üreme / Çoğaltma 1

1. Eşeyli / generatif çoğalma/çoğaltma 2. Eşeysiz / vejetatif çoğalma çoğaltma 3. İn vitro çoğaltma 2

Eşeyli Çoğalma/Çoğaltma Tohumlu bitkilerdeki tohum Kara yosunlarındaki sporofit 3
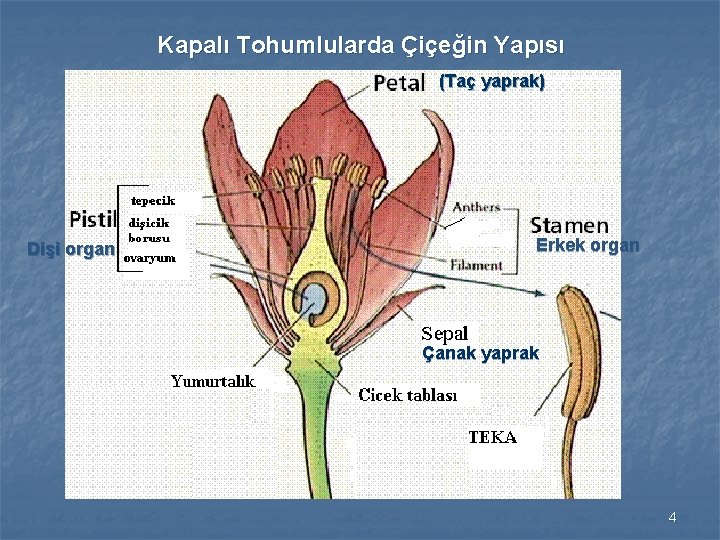
Kapalı Tohumlularda Çiçeğin Yapısı (Taç yaprak) Dişi organ Erkek organ Çanak yaprak 4

Açık Tohumlularda Çiçeğin Yapısı 5

Tanımlamalar 6

1. Tam çiçek: dört organın hepsini içeren çiçek (soya, bezelye, kantaron, vs) 2. Hermafrodit / erselik çiçek: her iki eşey organını içeren çiçek (soya, buğday vs) Kantaron: tam ve hermafradit çiçek Buğday: eksik ancak hermafrodit çiçek 7
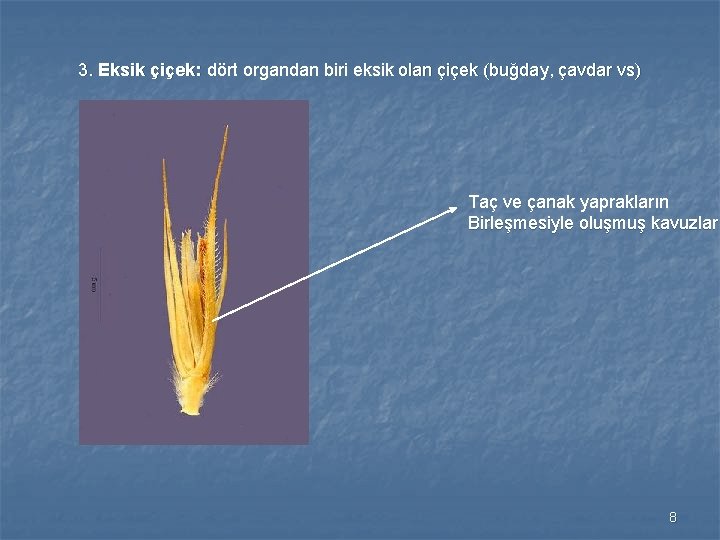
3. Eksik çiçek: dört organdan biri eksik olan çiçek (buğday, çavdar vs) Taç ve çanak yaprakların Birleşmesiyle oluşmuş kavuzlar 8
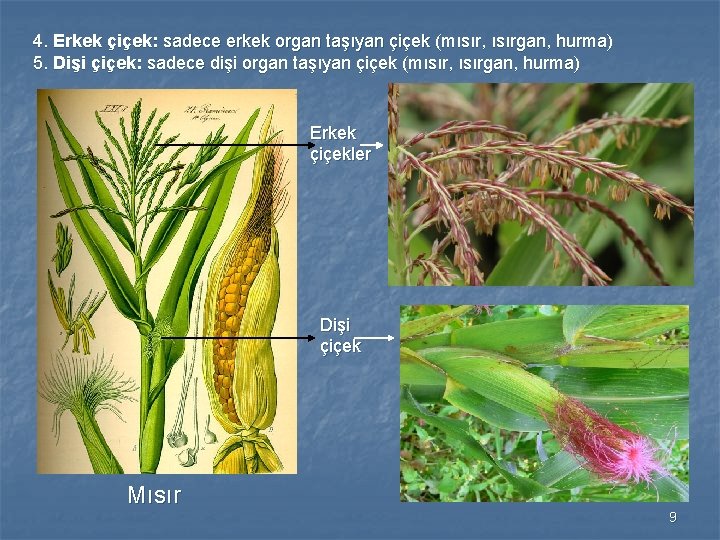
4. Erkek çiçek: sadece erkek organ taşıyan çiçek (mısır, ısırgan, hurma) 5. Dişi çiçek: sadece dişi organ taşıyan çiçek (mısır, ısırgan, hurma) Erkek çiçekler Dişi çiçek Mısır 9

6. Tek evcikli (monoik) bitki: dişi ve erkek çiçekler aynı bitki üzerinde (mısır, sorgum vs. ) Sorgum (Sorghum halepense) 10

7. İki evcikli (dioik) bitki: dişi ve erkek çiçekler farklı bitki üzerinde (ısırgan, hurma, kenevir vs) Kenevirde dişi ve erkek bitkiler 11
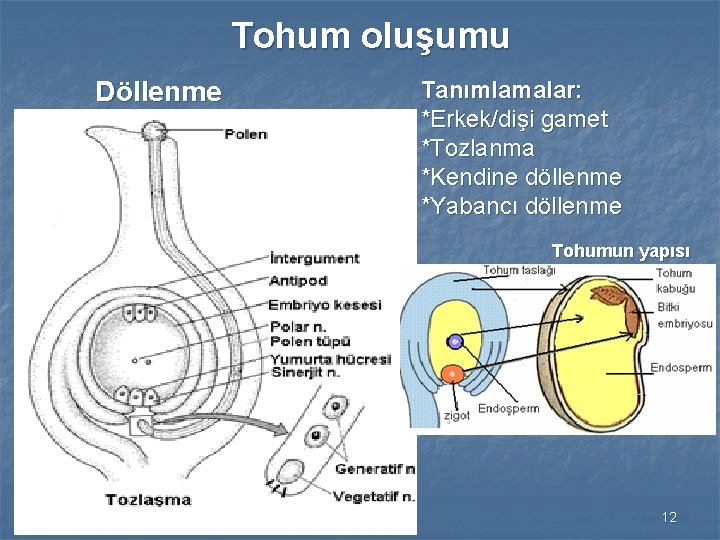
Tohum oluşumu Döllenme Tanımlamalar: *Erkek/dişi gamet *Tozlanma *Kendine döllenme *Yabancı döllenme Tohumun yapısı 12

Çimlenme Aşamaları 1. Suyun emilmesi 2. Enzim faaliyetleri 3. Embriyonun büyümeye başlaması 4. Tohum kabuğunun yırtılması ve çıkış 13
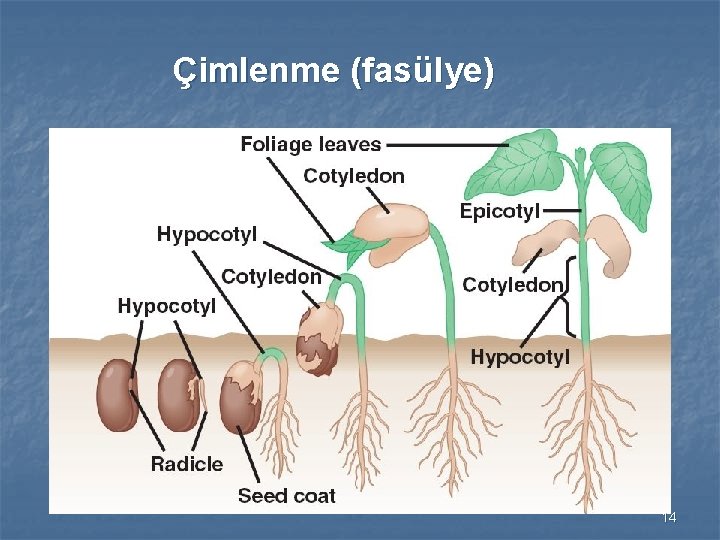
Çimlenme (fasülye) 14

Çimlenme (mısır) Koleoptil 15
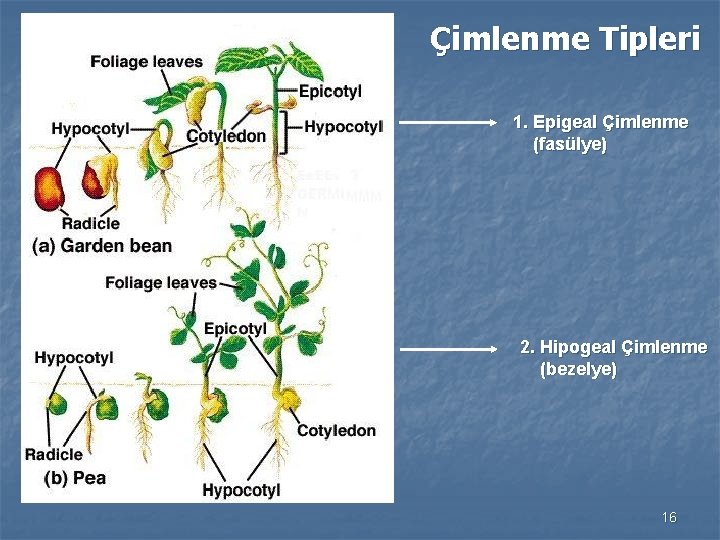
Çimlenme Tipleri 1. Epigeal Çimlenme (fasülye) 2. Hipogeal Çimlenme (bezelye) 16

Çimlenme Faktörleri 1. Su 2. Hava 3. Sıcaklık 4. Işık 17

Tohum Özelliklerinin Çimlenmeye Etkisi *Fizyolojik olgunluk *Tam olgunluk 18

Tohumlarda Dormansi Tanım: Olgun tohumun bütün çimlenme şartlarına sahip ortamda çimlenmemesi Sebepleri: 1. Geçirimsiz tohum kabuğu 2. Embriyo dormansisi a-sıcaklık b-ışık 3. Kimyasal inhibitörler 19

Vejetatif/Eşeysiz Çoğalma/Çoğaltma 20

1. Çelikle Çoğaltma Sürgün, dal, gövde, yaprak ya da yaprak parçalarının, ana bitkiden ayrılarak uygun çevre koşulları yaratılmış ortamlarda köklendirilip ana bitkinin tüm özelliklerini taşıyan yavru ya da yavruların elde edilmesidir. Üretimde kullanılan bitki parçasına ÇELİK, bu işleme de ÇELİKLE ÜRETİM adı verilir. Çelikle üretim, süs bitkilerinin ticari amaçlarla çoğaltılmalarında kullanılan en yaygın yöntemdir. Çelikler, bitkiden kesildikleri bitki bölümüne göre gövde çelikleri, odun çelikleri, otsu çelikler, yaprak çelikleri, kök çelikleri olarak adlandırılırlar. 21

Köklendirme Ortamları n n n Pek çok bitki türünün çelikleri, çok kolay köklendikleri için kullanılacak köklendirme ortamının cinsi önemli değildir. Kışın yaprağını döken bitkilerin odun ve kök çelikleri toprakta yapılır. Kum, talaş, torf, perlit, yanmış ahır gübresi, yaprak ve dal çürüntüsü, kayın yaprağı çürüntüsü, funda ve kestane toprağı ve bunların farklı oranlarda karışımları; bitki türüne ve üretim yapılan bölgeden sağlanabilecek malzeme niteliğine göre belirlenerek kullanılır. Köklendirme ortamından istenen özelliklerin başında süzer ve iyi havalanır olmasıdır. İçerisinde hastalık yapıcı patojenlerin bulunmaması yada sterilize edilmiş olması beklenilen bir özelliktir. Bitki besin maddesi içermeleri koyu renkleri ile (Kış aylarında) ısıyı tutmaları yada yaz aylarında açık renkleri ile yansıtmaları istenebilir. Havalandırılabilen su, pek çok bitki türü için uygun bir üretim ortamıdır. 22

Köklendirmede Çevre Koşulları n n Odun çeliklerinin açık alanda dikimi, bu bitkilerin doğal koşullara uyma zorunluluğunu getirir. Ancak su püskürtme ve örtüleme ile güneşin yakıcı etkisinden çeliklerin korunması yada genç sürgünlerin koruma ve solmalarının önlenmesi getirilecek tedbirlerle sağlanabilir. İşletme masraflarının yüksek oluşu ve ihmallerin büyük kayıplara beden olabileceği kapalı ortam üretiminde; ; kontrollü tutulması kışın ısıtma, yazın havalandırma ile sağlanır. Gece ve gündüz arasındaki ısı farkı 5 -10°C yi geçmemelidir. Çelik köklendirmede gece 16 -21°C, gündüz ise 21 -27°C lik sıcaklık bitki türüne ve mevsime bağlı olarak istenir. Köklendirme tezgahlarında ise 21 -24°C lik toprak sıcaklığı ideal kabul edilir. Çelik köklendirmede, özellikle yeşil çeliklerin köklendirilmesinde güneş ışığı mutlak gereklidir. Bu amaçla gölgeleme yada mist (sisleme) uygulanması ile suyun serinletici ve rutubeti artırıcı etkisinden yararlanılır. Sisleme ile yaprak gübrelemesi ve köklenmeyi uyarıcı maddelerin bitkiye verilmesi de mümkün olacaktır. Nem, çelik köklendirmede vazgeçilmez temel elemandır. Toprak ve hava nispi neminin bitkinin istediği düzeyde olması arzu edilir. 23

Köklenmeyi Uyartıcı Maddeler n n n Çeliklerin uçlarının çizilmesi, yararlanması yada ezilmesi kök oluşturma için gerekli uyarının yapılmasını, kallusun oluşumunun hızlandırıldığı varsayılır. Yaralanmış bu bölümlerin köklenmeyi uyarıcı hormonlarla muamelesi ile etki daha da artırılmış olacaktır. Kullanılabilecek maddelerin çokluğuna rağmen, çeliklerde köklenmeyi uyarıcı kimyasal maddeler, IBA (Indolbütirik asit), IAA (Indolasetik A. ) ve NAA (Naftalenasetikasit) tir. Kullanılan hormon ve kullanım dozu da çeliklerin köklenmesinde etkidir. İndol Butirik asit (IBA) pratikte en yaygın kullanılan hormondur. Ticari uygulamalarda; toz preparatlar (Talk için karıştırılmış olanlar) ve çözeltiler kullanılır. Toz preparatlar standart dozlarda ve ticari işletmenin patentli karışımı olarak tavsiyeler doğrultusunda kullanılır. Eriyik halinde olanlar ise çeliklerin uç kısımlarının kısa süre batırılıp çıkarılması yada seyreltik eriyikte uzun süre bekletilmesi ile istenilen 24 sonuca ulaşmak hedeflenir.

Köklenmiş Çeliklerin Göreceği İşlemler n Köklendirme ortamında 5 -10 mm. boya ulaşan yada çelikler hafifçe çekildiğinde kolayca çıkmadığı görülen çelikler yeterli gelişmeyi göstermiş kabul edilerek sökülürler. Köklerin bozulup kopmadan sökümün sağlanması ortamın hafif ve yumuşaklığına bağlıdır. n Köklü çelikler fincan saksılara yada özel kaplara dikilirler. 10 -15 gün kadar nemli ve rutubetli bir tünel içerisinde adaptasyon için bekletildikten sonra kontrollü olarak açık alana alınır. Burada kap değiştirilerek gelişmesi sağlanır yada toprağa dikilerek toprakta geliştirilir. 25

Çeliklerin Köklenmesi Üzerine Etki Yapan Faktörler n n Çeliklerin alınacağı klon anaçlarının mutlaka sağlıklı olması gerekir. Ayrıca bu anaçlarda düzenli olarak budama, gübreleme, hastalık ve zararlılarla mücadele gibi kültürel işlemlerin yerine getirilmesi zorunludur. Yapılan araştırmalar, genç anaçlardan alınan klonlarda, köklenme oranlarının daha yüksek olduğunu göstermiştir. Çeliklerde köklenme başarısı üzerine çelik alım zamanının çok etkili olduğu belirlenmiştir. Yeşil çeliklerde sürgün boyunun 30 -40 cm olduğu dönem (mayıs sonu - haziran başı), odun çeliklerinde ise yaprak döküm dönemi (ekim sonu-kasım başı) alınan çeliklerde köklenme oranı yüksek olmaktadır. 26

Çay bitkisinde çelikler ve ideal bir çelik 27

Köklendirme ortamları 28

Köklenmiş ve dikime hazır bir çelik 29

2. Aşıyla Üretim 30

31
Açılma ? ? ? 32

33

34

35

a b a) Aşı bıçağı ile kalemden gözün çıkarılması b) Kalemden çıkarılmış aşı gözü c c) Anaç üzerinde aşı bıçağı ile T şeklinde çizik açılması d d) Açılan T’ye gözün yukarıdan aşağıya doğru yerleştirilmesi e f e) Anaca yerleştirilmiş göz f) Aşı yerinin bağlanması. Gülde Aşılama 36

Çayda aşı için kalemler 37

Çayda Kalem aşısı 38

Çayda sürmüş aşı gözleri 39

3. Soğan 40

4. Soğanımsı gövde (corm) Liatris elegans (parlak yıldız) 41

5. Rizom Sarracenia sp. (bir tür süs bitkisi) 42
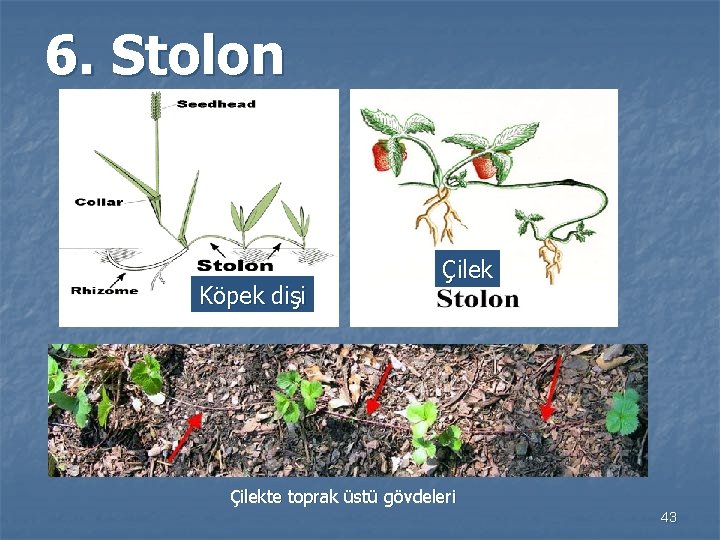
6. Stolon Köpek dişi Çilekte toprak üstü gövdeleri 43

7. Yumru Patates 44
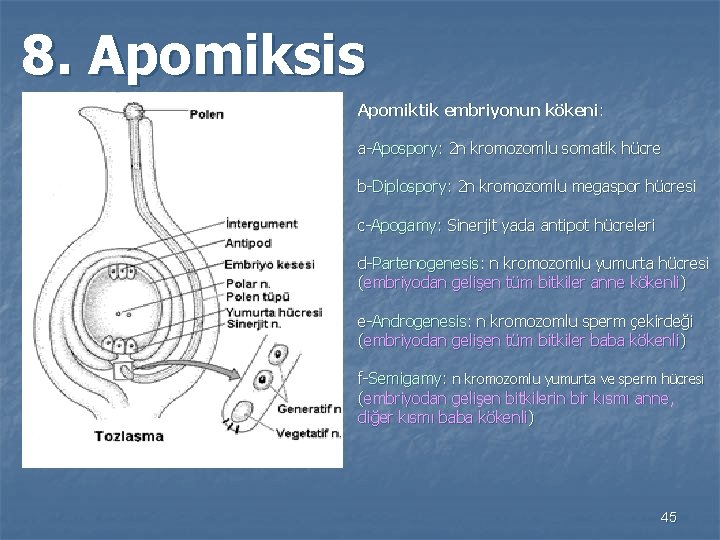
8. Apomiksis Apomiktik embriyonun kökeni: a-Apospory: 2 n kromozomlu somatik hücre b-Diplospory: 2 n kromozomlu megaspor hücresi c-Apogamy: Sinerjit yada antipot hücreleri d-Partenogenesis: n kromozomlu yumurta hücresi (embriyodan gelişen tüm bitkiler anne kökenli) e-Androgenesis: n kromozomlu sperm çekirdeği (embriyodan gelişen tüm bitkiler baba kökenli) f-Semigamy: n kromozomlu yumurta ve sperm hücresi (embriyodan gelişen bitkilerin bir kısmı anne, diğer kısmı baba kökenli) 45

Doku kültürleriyle in vitro çoğaltma 46

Bitki doku kültürü: steril koşullarda yapay besi ortamlarında bir bitkinin hücre, doku veya organ gibi kısımlarından yeni doku, bitki yada bitkisel ürünler (sekonder metabolitler gibi) üretilmesidir. Temel bileşenler: su, agar, şeker, mineral/vitaminler, makro/mikro besinler, büyüme düzenleyicileri Kullanım alanları: 1 -Mikro çoğaltma/in vitro çoğaltma/ klonal çoğaltma (örnek süs bitkileri) 2 -Embriyo kültürü (örnek: dağ elması) 3 -Somatik embriyogenesis (klonal çoğaltma ve sentetik tohum üretimi) (örnek: orman ağaçları ve yağ palmiyesi) 4 -Protoplast kültürü ve somatik melezleme (örnek: patates) 5 -Haploid bitki eldesi (örnek: mısır) 6 -Hastalıksız bitki üretimi (örnek: patateste ve lalede meristem kültürü) 7 -Gen nakli 8 -İn vitro seleksiyon (örnek: birçok bitkide hastalıklara dayanıklı çeşitler) 9 -Somaklonal varyasyon 10 -Sekonder metabolit üretimi (örnek: Ginseng bitkisinde ginsenosid üretimi) 47

Mikro çoğaltma aşamaları 1 - Besi ortamlarının hazırlanması 2 - Eksplant seçimi ve hazırlığı 3 - Sterilizasyon 4 - Kültüre alma 5 - Kallus oluşumu 6 - Sürgün gelişiminin teşviki 7 - Köklendirme 8 - Dış şartlara alıştırma 48

Kantaronda farklı doku kültür uygulamalarıyla mikro çoğaltma çalışması Yüzey sterilizasyonuna tabi tutulan yaprak ve n n n n MS (control) MS + 30 g l-1 sucrose MS + 40 g l-1 sucrose MS + 50 g l-1 sucrose MS+30 g l-1 sucrose+2. 13 μM 2, 4 -D+2. 32 μM kinetin MS+30 g l-1 sucrose+4. 25 μM 2, 4 -D+4. 64 μM kinetin MS+30 g l-1 sucrose+6. 38 μM 2, 4 -D+6. 96 μM kinetin MS+40 g l-1 sucrose+2. 13 μM 2, 4 -D+2. 32 μM kinetin MS+40 g l-1 sucrose+4. 25 μM 2, 4 -D+4. 64 μM kinetin MS+40 g l-1 sucrose+6. 38 μM 2, 4 -D+6. 96 μM kinetin MS+50 g l-1 sucrose+2. 13 μM 2, 4 -D+2. 32 μM kinetin MS+50 g l-1 sucrose+4. 25 μM 2, 4 -D+4. 64 μM kinetin MS+50 g l-1 sucrose+6. 38 μM 2, 4 -D+6. 96 μM kinetin gövde eksplantları kallus oluşturmak üzere farklı sakaroz dozları ve büyüme düzenleyicileri içeren modifiye MS ortamlarına konmuşlardır. Oluşan kalluslar 8 hafta sonra sürgün gelişimi için MS+4. 4 m. M BA+30 g/l sakaroz içeren ortamda alt kültüre alınmışlardır. Bu alt kültürde gelişen sürgünlerin yapılmış bir kısmında kısmı da hypericin kök analizi gelişimi için MS+5. 7 m. M IAA+30 g/l sakaroz içeren ortamda birkez daha alt kültüre alınmışlardır. Köklenen rejenere bitkiler kum+toprak+perlit karışımı içeren kutulara alınarak naylon poşetlerle sağlanan artan nemlilik seviyeleriyle birlikte dış şartlara alıştırılmışlardır. rejenerantlar sera 10 şartlarına gün sonra alınmışlar hayatta kalanların oranı tespit edilmiştir. 49 ve

Bu araştırmanın sonuçlarına göre denenen tüm faktörler kallus oluşum sıklığını önemli derece etkilemiş, en yüksek değer MS+30 g l-1 sucrose+2. 13 μM 2, 4 -D+2. 32 μM kinetin ortamında kültüre alınan yaprak disklerinden elde edilmiştir. Ayrıca artan 2. 4 -D dozları ile birlikte kallus taze ağırlığı gövde segmentlerinden oluşan kalluslarda daha yüksek olmuştur. Kalluslarda görülen kırmızı renk hypericin oluşumuna işaret etmektedir. 50

Bu kalluslar BA içeren ortamda alt kültüre alındıklarında yoğun bir şekilde sürgün oluşturmuşlardır. Kallus başına sürgün sayısı 6 -31 arasında değişmiş olup uygulamalara bağlı olarak önemli derecede farklılık göstermiştir. hypericin kökenli Sürgünlerin içeriği kalluslardan yapraktan rejenere olanlarda hada yüksek olmuştur (ortalama %0. 048). 51

IAA içeren ortamda alt kültüre alınan sürgünler köklenme oranı bakımından önemli bir varyasyon sergilemişlerdir. Köklenme oranı kallus oluşum ortamına bağlı olarak %67 -91 arasında değişmiştir. 52

Köklenen bitkiler in vitro ortamdan çıkarılarak köklerdeki ortam artıkları suyla yıkanmış ve bitkiler toprak+kum+perlit (3 1 1 ) ihtiva eden kutulara konmuşlardır. Seraya konmadan önce üstlerine naylon poşet geçirilerek zaman havalandırılmış ve bu şekilde dış şartlara alıştırılmışlardır. 53

10 gün sonra yapılan sayımda bitkilerin %90’ ı başarılı bir şekilde dış şartlara uymuş ve seraya alınmıştır. 54
- Slides: 54