Biotecnologie in campo medico Il primo farmaco ricavato

Biotecnologie in campo medico

Il primo farmaco ricavato da microrganismi è stata la penicillina (Fleming 1929 da una muffa del genere Penicillium). Ad oggi diversi antibiotici si producono utilizzando muffe e funghi anche geneticamente modificati. Il primo farmaco ottenuto grazie alle tecniche dell’ingegneria genetica (DNA ricombinante) è stata l’insulina ricombinante (1978). In precedenza, veniva ricavata da bovini e suini: risultava efficace, ma dava problemi collaterali di tipo immunitario (allergie). Oltre all’insulina, con batteri ricombinati sono stati prodotti altri ormoni umani (ad es. quello della crescita), fattori per la coagulazione, anticorpi monoclonali, interleuchine (stimolano il sistema immunitario) interferone (antitumorale) e vaccini (epatite B, salmonellosi, erpes simplex, influenza, colera).

Non solo batteri, oggi si utilizzano anche lieviti e piante per produrre farmaci puri come, ad esempio, anticorpi umani utilizzati nella terapia di molte patologie (dalle infezioni virali al cancro). Uno dei vantaggi nell’utilizzo delle piante è che queste hanno sistemi cellulari di sintesi ed elaborazione delle proteine molto più simile a quello umano rispetto ai batteri. Sono state utilizzate, ad esempio, per la produzione di anticorpi monoclonali Un altro esempio di successo è quello della produzione di glucocerebrosidasi, glucocerebrosidasi un enzima utilizzato nella terapia di una rara malattia neurodegenerativa ed epatodegenerativa: la sindrome di Gaucher

Terapie geniche Sono terapie che non fanno ricorso a farmaci, ma sono mirate a «correggere» correggere difetti alla base delle malattie genetiche. Un esempio è quello relativo alla malattia ADASCID, SCID consistente in un grave deficit immunitario (Severe Combined Immuno Deficiencies) dovuto alla carenza dell’enzima adenosina deaminasi (bambini–bolla) La malattia, oggi, può essere risolta inserendo nelle staminali dei globuli bianchi (prelevati dal midollo osseo del paziente) il gene ADA umano utilizzando, come vettori, dei retrovirus Una volta reinserite nel midollo osseo, queste staminali «corrette» producono regolarmente l’enzima ADA, ADA portando alla sconfitta della malattia. Inizialmente, questa tecnica ha avuto un problema: i retrovirus integrano il gene esogeno in un punto qualsiasi di un cromosoma qualsiasi, il che può comportare il blocco di un qualche gene. Tale problema fu superato con l’utilizzo di un cosìdetto virus adeno-associato.

I virus adeno-associati Sono particolari virus a «singola elica di DNA» . DNA Una volta infettate le cellule ospiti, il DNA a singolo filamento si integra in un sito specifico del cromosoma 19. Qui vi rimane in stato di latenza fino a quando la cellula non viene infettata da un virus completo (solitamente l’adenovirus, da cui il loro nome). Data la sua peculiarità viene utilizzato preferendolo ai retrovirus. L’adenovirus Causa una sindrome simile al raffreddore. La sua peculiarità consiste nell’inserire un DNA a doppia elica, ma che rimane in forma plasmidica, senza integrarsi in un cromosoma della cellula ospite. Un successo con tale vettore ingegnerizzato è stato ottenuto nel risolvere la LPLD, LPLD una malattia genetica rara dovuta al deficit di lipoproteina lipasi: lipasi non vengono metabolizzati i chilomicroni presenti nel sangue conseguente infiammazione del pancreas che può essere fatale. Attraverso l’adenovirus è stato inserito nel tessuto muscolare dei pazienti una versione potenziata del gene, che produce una proteina dotata di un’attività enzimatica superiore a quella dell’enzima naturale.

I virus adeno-associati adeno-associat Sono particolari virus a «singola elica di DNA» . DNA Una volta infettate le cellule ospiti, il DNA a singolo filamento si integra in un sito specifico del cromosoma 19. Qui vi rimane in stato di latenza fino a quando la cellula non viene infettata da un virus completo (solitamente l’adenovirus, da cui il loro nome). Data la sua peculiarità viene utilizzato preferendolo ai retrovirus. L’adenovirus Causa una sindrome simile al raffreddore. Inserire nella cellula ospite un DNA a doppia elica in forma plasmidica, senza integrarsi in un cromosoma, ma ugualmente funzionate. Un successo con tale vettore ingegnerizzato è stato ottenuto nel risolvere la LPLD, LPLD una malattia genetica rara dovuta al deficit di lipoproteina lipasi: lipasi non vengono metabolizzati i chilomicroni presenti nel sangue conseguente infiammazione del pancreas che può essere fatale. Attraverso l’adenovirus è stato inserito nel tessuto muscolare dei pazienti una versione potenziata del gene, che produce una proteina dotata di un’attività enzimatica superiore a quella dell’enzima naturale.
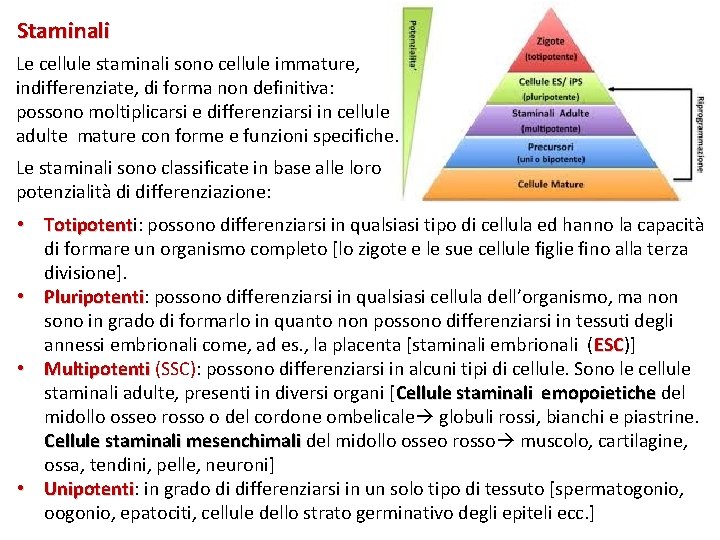
Staminali Le cellule staminali sono cellule immature, indifferenziate, di forma non definitiva: possono moltiplicarsi e differenziarsi in cellule adulte mature con forme e funzioni specifiche. Le staminali sono classificate in base alle loro potenzialità di differenziazione: • Totipotenti: Totipotent possono differenziarsi in qualsiasi tipo di cellula ed hanno la capacità di formare un organismo completo [lo zigote e le sue cellule figlie fino alla terza divisione]. • Pluripotenti: Pluripotenti possono differenziarsi in qualsiasi cellula dell’organismo, ma non sono in grado di formarlo in quanto non possono differenziarsi in tessuti degli annessi embrionali come, ad es. , la placenta [staminali embrionali (ESC)] ESC • Multipotenti (SSC): possono differenziarsi in alcuni tipi di cellule. Sono le cellule staminali adulte, presenti in diversi organi [Cellule staminali emopoietiche del midollo osseo rosso o del cordone ombelicale globuli rossi, bianchi e piastrine. Cellule staminali mesenchimali del midollo osseo rosso muscolo, cartilagine, ossa, tendini, pelle, neuroni] • Unipotenti: Unipotenti in grado di differenziarsi in un solo tipo di tessuto [spermatogonio, oogonio, epatociti, cellule dello strato germinativo degli epiteli ecc. ]
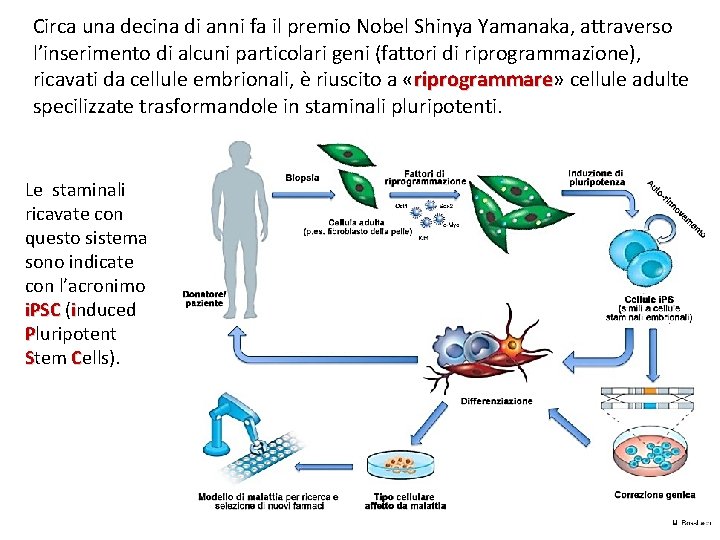
Circa una decina di anni fa il premio Nobel Shinya Yamanaka, attraverso l’inserimento di alcuni particolari geni (fattori di riprogrammazione), ricavati da cellule embrionali, è riuscito a «riprogrammare» riprogrammare cellule adulte specilizzate trasformandole in staminali pluripotenti. Le staminali ricavate con questo sistema sono indicate con l’acronimo i. PSC (induced Pluripotent Stem Cells).

Editing genetico Nato nel 2012, è basato su un processo naturale nei batteri. I batteri, ogni volta che superano una infezione da fagi, conservano frammenti di RNA fagico, detti CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats: brevi ripetizioni palindrome raggruppate e separate a intervalli regolari) in modo da mantenerne la sua memoria In questo modo creano un vero e proprio archivio. Oltre a questo è stato scoperto che, in questo archivio, i frammenti fagici sono intervallati da sequenze nucleotidiche, dette CAS 9 (sequenze CRISPR associate) per la sintesi di enzimi endonucleasi, enzimi, cioè, che tagliano il DNA. Ad una successiva infezione degli stessi fagi, il batterio è in grado di riconoscerli (grazie ad CRISPR complementare) e disattivarlo immediatamente (grazie al CAS 9) Due biologhe, Charpentier (francese) e Doundna (statunitense), hanno pensato bene di sfruttare questo sistema per l’ingegneria genetica: si estrae un CAS 9 e lo si associa ad un frammento di RNA complementare ad un tratto di DNA che si vuole modificare. In questo modo, il materiale genetico viene tagliato con estrema precisione provocando la disattivazione di un gene specifico o, con tecniche di ricombinazione, si può ricostruire un determinato gene con opportune modifiche (editing genetico). Questa tecnica si usa per: • Disattivare (spegnere) geni (al fine di conoscerne la funzione) • Correggere geni difettosi

Knock-out e Knock-in genico Per conoscere il ruolo di un determinato gene (gene target). I biotecnologi usano «spegnerlo» (inattivarlo) oppure inserirlo (esogeno) in embrioni per poi osservarne gli effetti nell’individuo adulto. Una volta conosciuta la sequenza nucleotidica del gene target, si prelevano cellule embrionali (dalla blastocisti di una topina gravida) in cui si inserisce : • uno specifico RNA/CAS 9 che taglierà il gene target (spegnendolo) topi knockout; out oppure • un gene esogeno di cui si vuole conoscere il ruolo (ad es. tramite trasposoni o infezione virale). topi knock-in Le cellule embrionali così trattate vengono inserite nella blastocisti i di un’altra topina accettrice per far sviluppare l’individuo. Gli individui che nascono presentano una o più specifiche anomalie. Con tali tecniche si sono studiate, soprattutto, le malattie geniche.

Attenzione: non tutte le cellule della blastocisti impiantata sono modificate per cui i topi avranno alcuni tessuti modificati, altri no (topi chimerici). Per riconoscere i tessuti modificati, al gene target si associa un gene codificante per una proteina responsabile di un carattere fenotipico facilmente identificabile (es. un pigmento particolare) I gameti di questi topi non saranno tutti uguali (in base all’allele ereditato). Per tal motivo, dagli incroci tra essi, si possono ottenere razze pure: • topi normali, senza alcun tessuto anomalo • geneticamente modificati al 100%, con tutti i tessuti anomali. Il ruolo della miostatina, miostatina una proteina presente nei muscoli, è stato scoperto proprio grazie ai topi knock-out. La miostatina limita lo sviluppo muscolare. In figura il risultato dell’inibizione della proteina in un toro.

Clonazione di interi organismi Per clonazione artificiale si intende la generazione di un intero organismo a partire da una singola cellula non zigotica. Questa tecnica permette di ottenere copie geneticamente identiche dell’organismo di partenza e trova applicazioni nella zootecnia (ad es. per riprodurre animali dalle caratteristiche eccellenti come cavalli da corsa, mucche da latte o tori da riproduzione), ma anche nella conservazione dell’ambiente (per esempio per ripopolare specie animali in via di estinzione che non è possibile fare riprodurre naturalmente in cattività).

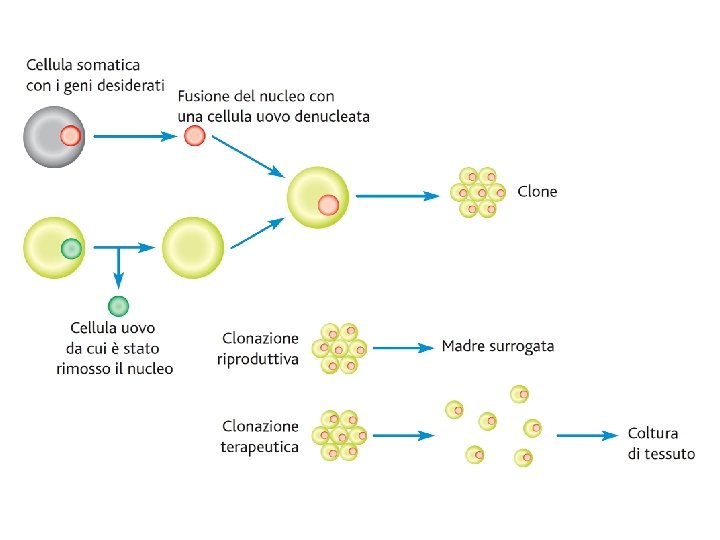
Trasferimento nucleare La tecnica più diffusa è quella del trasferimento nucleare: 1. Il nucleo aploide di una cellula uovo ricevente viene sostituito con il nucleo contenente il genoma diploide di una cellula somatica del donatore; 2. Lo pseudo-zigote (cellula uovo resa diploide non per fecondazione con uno spermatozoo) dà origine a un embrione, anche se il suo genoma deriva da una cellula adulta (cioè differenziata); 3. L’embrione viene trasferito nell’utero di una femmina della specie donatrice (madre surrogata); 4. La prole avrà il genoma identico (clone) a quello della cellula somatica donatrice
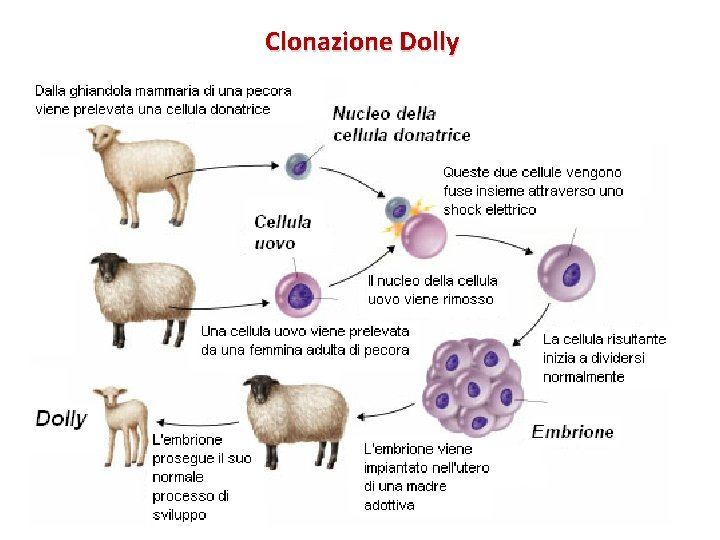
Clonazione Dolly

Per ottenere Dolly (1996), nelle varie sperimentazioni si sono utilizzati 277 oociti di cui solo 29 si sono sviluppati e sono stati impiantati in 13 madri diverse. In seguito sono stati clonati diversi animali: topi, lupi, cavalli, bovini, lupi, scimmie. Dolly visse per sette anni, durante i quali diede alla luce diversi cuccioli; ora è conservata in un museo a Edimburgo.

Biotecnologie e ambiente Le biotecnologie permettono di sviluppare processi produttivi maggiormente eco-compatibili e di rispondere ad esigenze di tutela dell’ambiente. In particolare queste applicazioni si riferiscono a: • produzione di energia da biomasse; • biodegradazione di inquinanti.

Energia dalle biomasse I biocarburanti sono composti combustibili derivati non dalle fonti fossili (carbone, petrolio), ma da biomasse vegetali. I vantaggi sono: • la rinnovabilità della fonte (non si esauriscono come i giacimenti di combustibili fossili); • il bilancio neutro della CO 2 (quella rilasciata dalla combustione è pari a quella sottratta durante la crescita della pianta); • la biocompatibilità (i biocarburanti sono totalmente biodegradabili).

I biocarburanti principali sono : • il bioetanolo prodotto dalla fermentazione di varietà ricche di carboidrati (canna da zucchero, mais, frumento, orzo); • Il biodiesel prodotto da piante oleose (soia, palma, colza); • Il biometano prodotto dalla fermentazione anaerobica di materiale organico; • Il bioidrogeno prodotto dalla fissazione di azoto o fotosintesi da parte di alghe e batteri.

Biorisanamento Per biorisanamento si intende la rimozione, tramite l’utilizzo di microrganismi geneticamente modificati, di inquinanti ambientali difficilmente eliminabili con tecniche chimico-fisiche. Gli inquinanti oggetto di maggiore attenzione sono: • metalli (mercurio, cromo, piombo, arsenico); • idrocarburi e composti organici di origine industriale. Lo scopo del biorisanamento è rendere questi inquinanti biodegradabili da parte di microrganismi modificati.
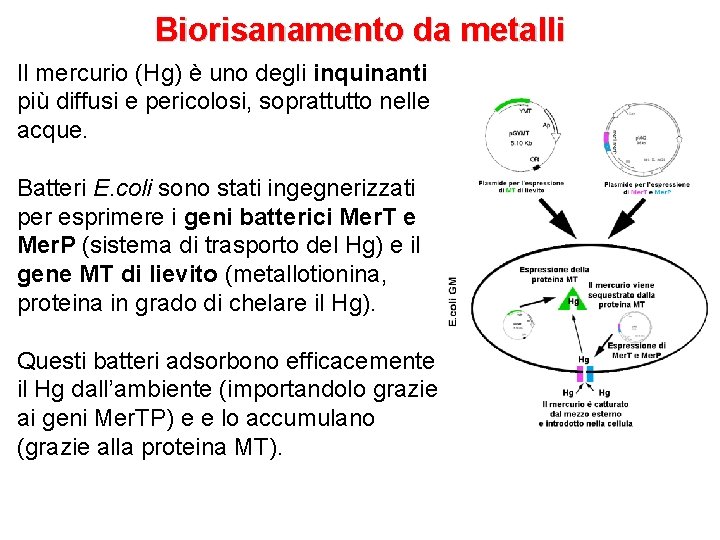
Biorisanamento da metalli Il mercurio (Hg) è uno degli inquinanti più diffusi e pericolosi, soprattutto nelle acque. Batteri E. coli sono stati ingegnerizzati per esprimere i geni batterici Mer. T e Mer. P (sistema di trasporto del Hg) e il gene MT di lievito (metallotionina, proteina in grado di chelare il Hg). Questi batteri adsorbono efficacemente il Hg dall’ambiente (importandolo grazie ai geni Mer. TP) e e lo accumulano (grazie alla proteina MT).
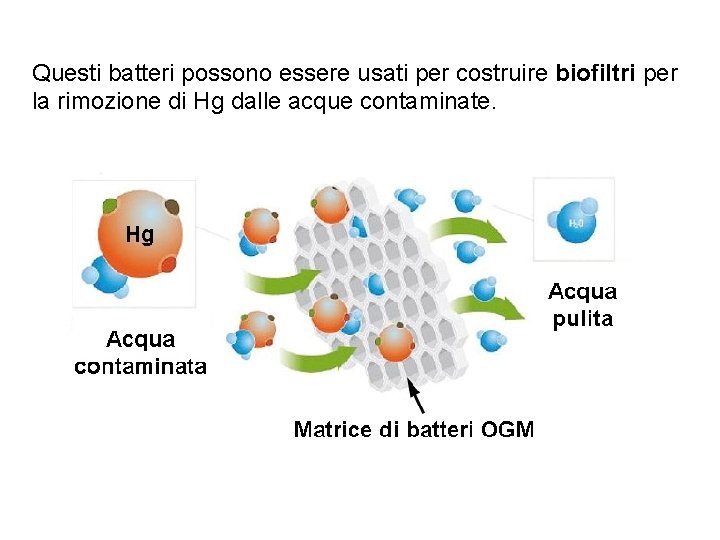
Questi batteri possono essere usati per costruire biofiltri per la rimozione di Hg dalle acque contaminate.
- Slides: 22