Biosynteza kwasw nukleinowych i ich przemiany rdze puryn

Biosynteza kwasów nukleinowych i ich przemiany Ø Ø Ø rdzeń puryn (hipoksantyny), biosynteza nukleotydów purynowych, biosynteza nukleotydów pirymidynowych, biosynteza deoksynukletydów, biosynteza kwasów nukleinowych (DNA i RNA), rozkład kwasów nukleinowych
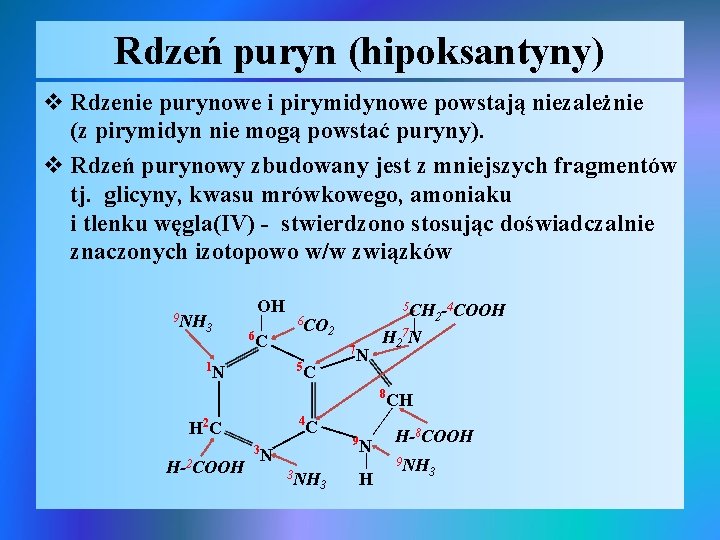
Rdzeń puryn (hipoksantyny) v Rdzenie purynowe i pirymidynowe powstają niezależnie (z pirymidyn nie mogą powstać puryny). v Rdzeń purynowy zbudowany jest z mniejszych fragmentów tj. glicyny, kwasu mrówkowego, amoniaku i tlenku węgla(IV) - stwierdzono stosując doświadczalnie znaczonych izotopowo w/w związków OH | 6 C 3 5 N | 2 7 C H 2 N 8 4 C | H 2 C 9 | 3 H-2 COOH 5 CH | 2 - 4 COOH 7 N | 1 6 CO | 9 NH N 3 NH 3 | N | H CH H-8 COOH 9 NH 3

Biosynteza nukleotydów purynowych v Pochodzenie atomów azotu i węgla w rdzeniu purynowym nukloetydów purynowych: Ø azot – 3, 9 dostarczane są przez grupą amidową glutaminy, a 1 pochodzi i grupy α-aminowej kwasu asparaginowego, Ø węgle formylowe 2 i 8 dostarczane są przez pochodne kwasu tetrahydrofoliowego THFA (koenzym F transferaz przenoszących grupy jednowęglowe w tym formylo-THFA) warunkiem wbudowania reszty kwasu mrówkowego w rdzeń purynowy jest jego aktywacja i przeniesienie na koenzym F – „aktywny mrówczan”. v Enzymatyczna synteza nukleotydów rozpoczyna się od utworzenia analogu o otwartym rdzeniu purynowym: Ø fosforylacja rybozo-5 -fosforanu kosztem ATP i katalizowanej odpowiednią kinazą do formy aktywnej (5 -fosforybolozopirofosforanu)”
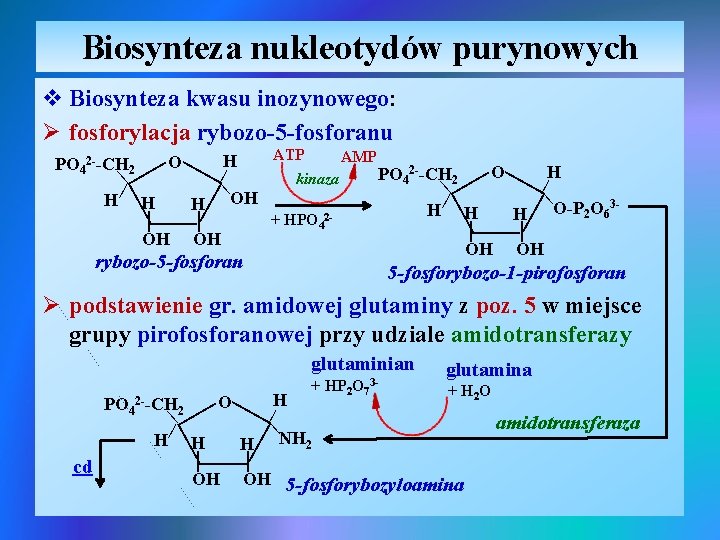
Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego: Ø fosforylacja rybozo-5 -fosforanu | | | | | rybozo-5 -fosforan | | | ATP AMP H O PO 42 --CH 2 | kinaza | | | H H H OH O-P 2 O 63 H H H 2+ HPO 4 | | OH OH 5 -fosforybozo-1 -pirofosforan Ø podstawienie gr. amidowej glutaminy z poz. 5 w miejsce grupy pirofosforanowej przy udziale amidotransferazy glutaminian | | | 2 | | H cd O | PO 4 2 --CH H + HP 2 O 73 - glutamina + H 2 O NH 2 H H OH OH 5 -fosforybozyloamina | | amidotransferaza
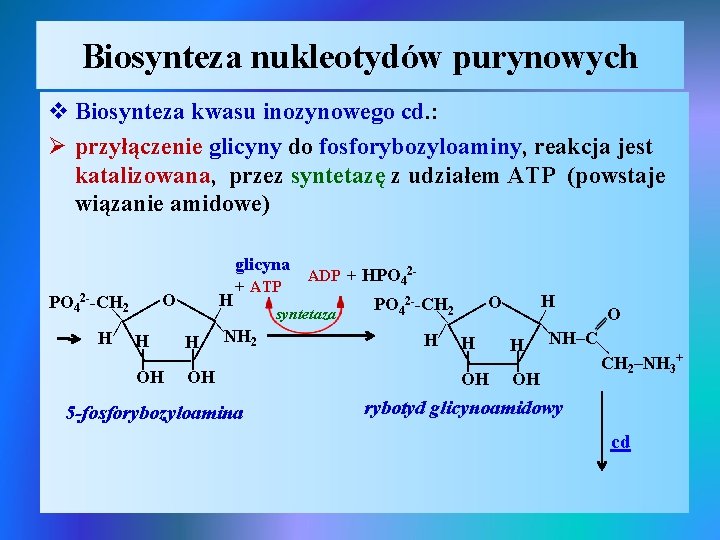
Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego cd. : Ø przyłączenie glicyny do fosforybozyloaminy, reakcja jest katalizowana, przez syntetazę z udziałem ATP (powstaje wiązanie amidowe) | | | | | 5 -fosforybozyloamina | | | glicyna ADP + HPO 42+ ATP O H H PO 42 --CH 2 O PO 42 --CH 2 | syntetaza O | | | H H H NH 2 H NH–C | | CH 2–NH 3+ OH OH rybotyd glicynoamidowy cd
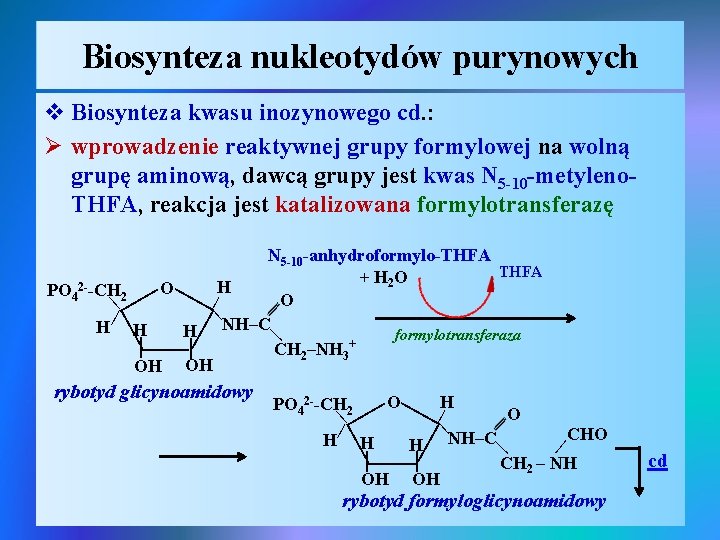
Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego cd. : Ø wprowadzenie reaktywnej grupy formylowej na wolną grupę aminową, dawcą grupy jest kwas N 5 -10 -metyleno. THFA, reakcja jest katalizowana formylotransferazę | | | N 5 -10 -anhydroformylo-THFA + H 2 O 2 H O PO 4 -CH 2 O | | H H H NH–C formylotransferaza + | | CH 2–NH 3 OH OH | | | O H PO 42 --CH 2 O | | H H | CHO H NH–C | | CH 2 – NH OH OH | | | | rybotyd glicynoamidowy rybotyd formyloglicynoamidowy cd
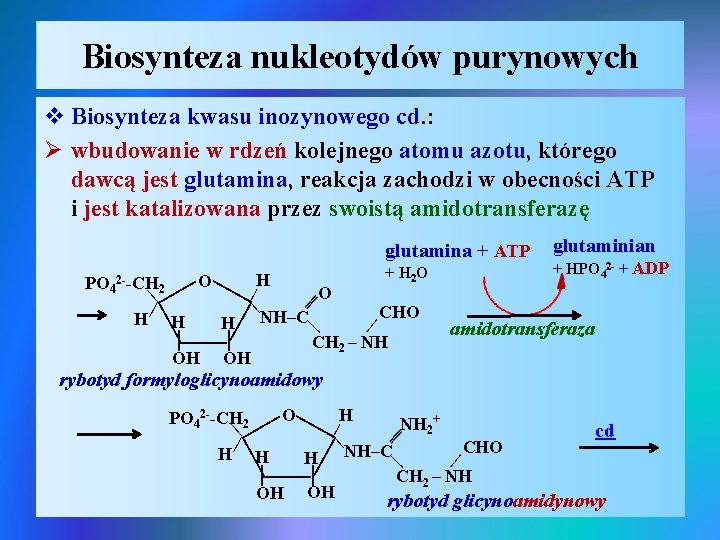
Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego cd. : Ø wbudowanie w rdzeń kolejnego atomu azotu, którego dawcą jest glutamina, reakcja zachodzi w obecności ATP i jest katalizowana przez swoistą amidotransferazę glutamina + ATP | O | | | | H H OH OH | | H + H 2 O O | CHO NH–C | H 2 | PO 4 2 --CH CH 2 – NH glutaminian + HPO 42 - + ADP amidotransferaza rybotyd formyloglicynoamidowy | | | H O PO 42 --CH 2 NH 2+ | cd | H H | CHO H NH–C | | CH 2 – NH OH OH rybotyd glicynoamidynowy | | |
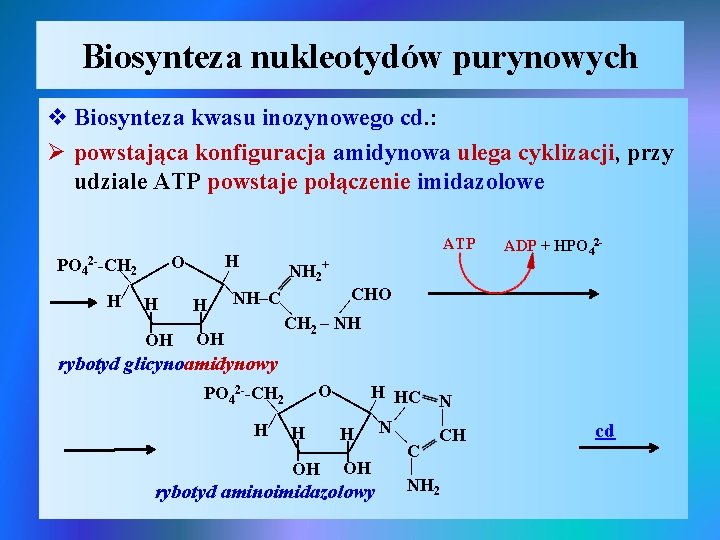
Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego cd. : Ø powstająca konfiguracja amidynowa ulega cyklizacji, przy udziale ATP powstaje połączenie imidazolowe ATP | | | H O PO 42 --CH 2 NH 2+ | | H H | CHO H NH–C | | CH 2 – NH OH OH ADP + HPO 42 - | | | rybotyd glicynoamidynowy | | | O H PO 42 --CH 2 N | HC | | | N H H H CH | | C | OH OH NH 2 rybotyd aminoimidazolowy | | cd | | |
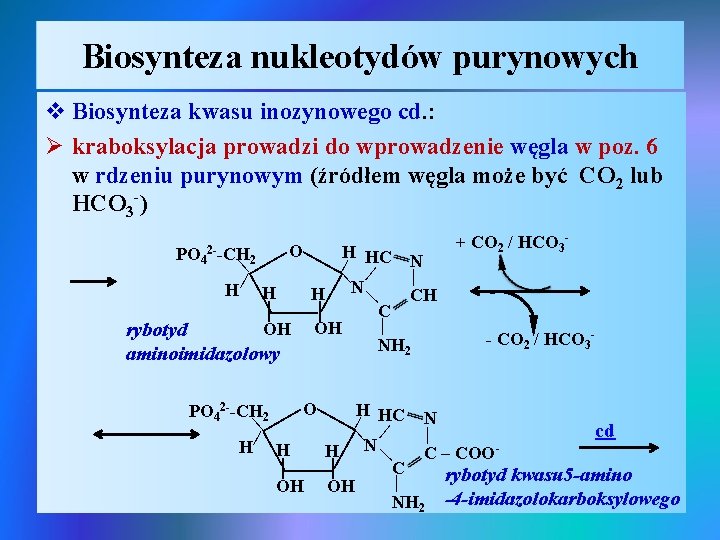
Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego cd. : Ø kraboksylacja prowadzi do wprowadzenie węgla w poz. 6 w rdzeniu purynowym (źródłem węgla może być CO 2 lub HCO 3 -) H | | OH rybotyd aminoimidazolowy | | | H N | HC | | N H CH | C | OH NH 2 | | | O | H 2 + CO 2 / HCO 3 - | PO 4 2 --CH - CO 2 / HCO 3 - | | | O H PO 42 --CH 2 N | HC | cd | | N H H H C – COO | | C rybotyd kwasu 5 -amino | OH OH NH 2 -4 -imidazolokarboksylowego | | |
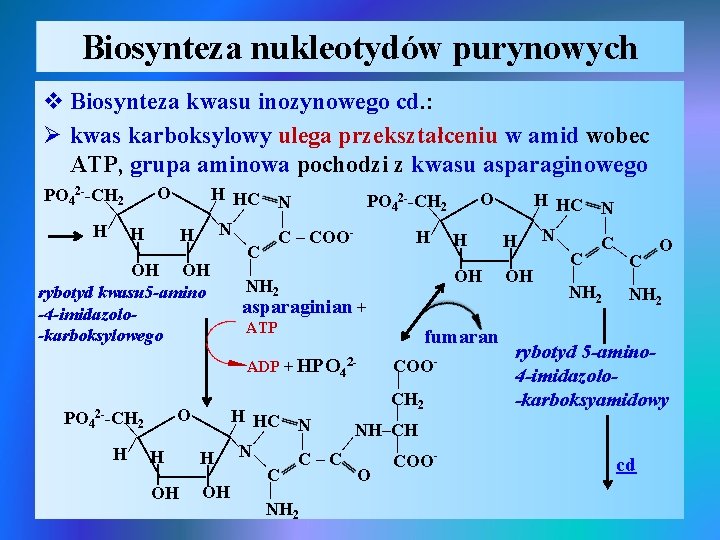
Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego cd. : Ø kwas karboksylowy ulega przekształceniu w amid wobec ATP, grupa aminowa pochodzi z kwasu asparaginowego | | | OH | | | | | H HC N | | NH–CH | | | H N C–C COO| C O | OH NH 2 | O CH 2 | | | | PO 4 2 --CH COO- | | | ADP + HPO 4 2 - | | | O H PO 42 --CH 2 O H HC N PO 42 --CH 2 N | HC | | | | N H H N H C – COO H H H C O | | C C | OH OH | | OH OH NH 2 rybotyd kwasu 5 -amino asparaginian + -4 -imidazolo. ATP -karboksylowego fumaran rybotyd 5 -amino 4 -imidazolo-karboksyamidowy cd
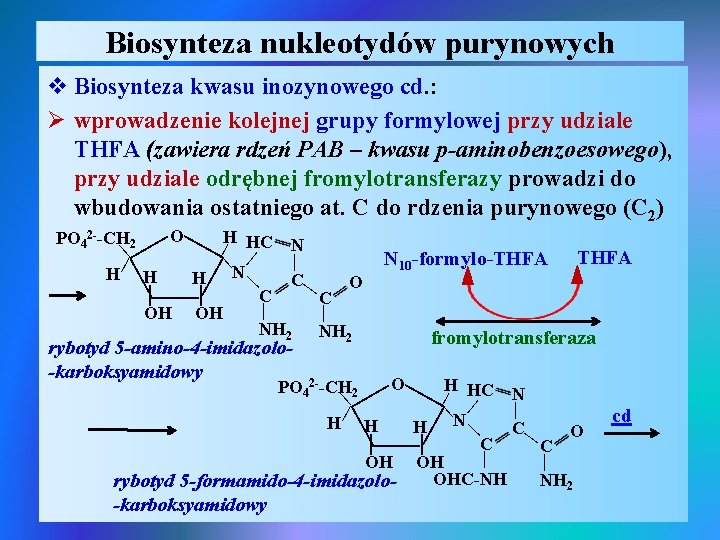
Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego cd. : Ø wprowadzenie kolejnej grupy formylowej przy udziale THFA (zawiera rdzeń PAB – kwasu p-aminobenzoesowego), przy udziale odrębnej fromylotransferazy prowadzi do wbudowania ostatniego at. C do rdzenia purynowego (C 2) | | | O H PO 42 --CH 2 N | HC | | | N H H H C O | | C C | | OH OH NH 2 N 10 -formylo-THFA | | | rybotyd 5 -amino-4 -imidazolo-karboksyamidowy fromylotransferaza | | | -karboksyamidowy | | | O H PO 42 --CH 2 N | HC | | | N H H H C O | | C C | | OH OH OHC-NH NH 2 rybotyd 5 -formamido-4 -imidazolo- cd
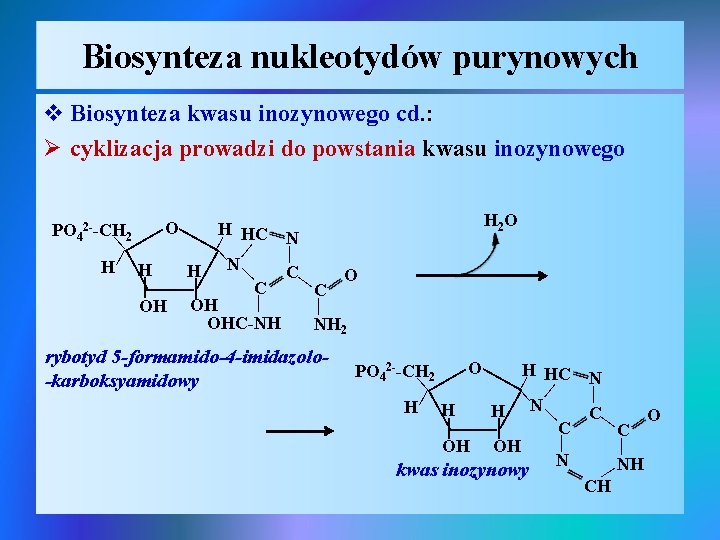
Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego cd. : Ø cyklizacja prowadzi do powstania kwasu inozynowego H 2 O | | | O H PO 42 --CH 2 N | HC | | | N H H H C O | | C C | | OH OH OHC-NH NH 2 | | | C C | NH | | kwas inozynowy N | | O H PO 42 --CH 2 | HC | | H H H N | | C | OH OH N | | rybotyd 5 -formamido-4 -imidazolo-karboksyamidowy CH O
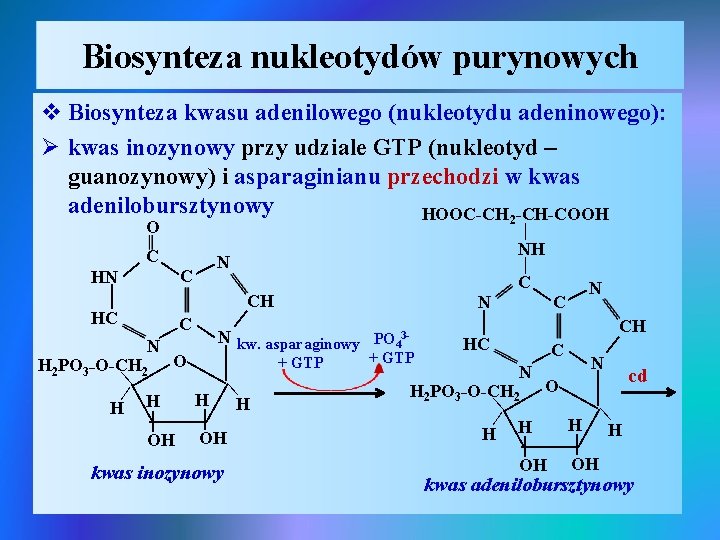
Biosynteza nukleotydów purynowych v Biosynteza kwasu adenilowego (nukleotydu adeninowego): Ø kwas inozynowy przy udziale GTP (nukleotyd – guanozynowy) i asparaginianu przechodzi w kwas adenilobursztynowy HOOC-CH 2 -CH-COOH O | | N O | | | H 2 H H OH OH | | CH N | | | H 2 PO 3 _O-CH | | | kwas inozynowy H C | OH + GTP HC + GTP N | | OH H | | | N kw. asparaginowy PO 43 - | | H N C | | H 2 CH cd | O C | H 2 PO 3 _O-CH N | | HC N | | C | | HN NH | C H kwas adenilobursztynowy
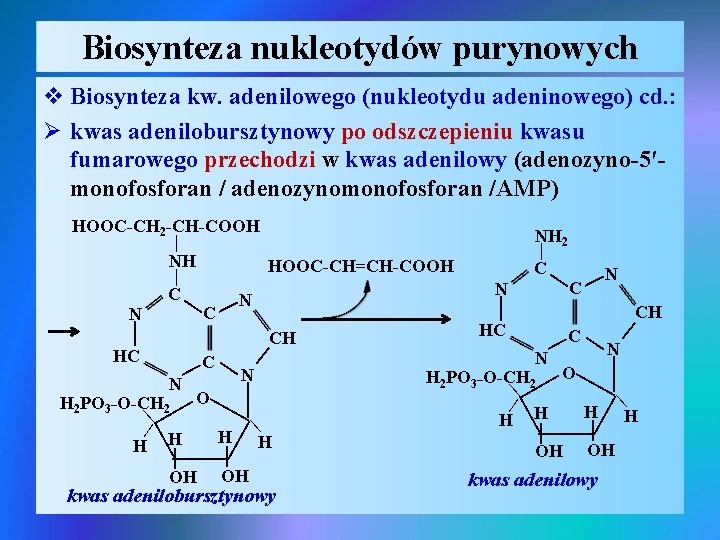
Biosynteza nukleotydów purynowych v Biosynteza kw. adenilowego (nukleotydu adeninowego) cd. : Ø kwas adenilobursztynowy po odszczepieniu kwasu fumarowego przechodzi w kwas adenilowy (adenozyno-5′monofosforan / adenozynomonofosforan /AMP) HOOC-CH 2 -CH-COOH | | kwas adenilobursztynowy | | | | H 2 PO 3_O-CH 2 O | H H H | OH | | | H | CH N N | OH C | | HC OH kwas adenilowy | | H 2 PO 3_O-CH 2 O | H H H OH | CH N | | N | C | HC N C | | N C C | | HOOC-CH=CH-COOH | C | NH NH 2 H
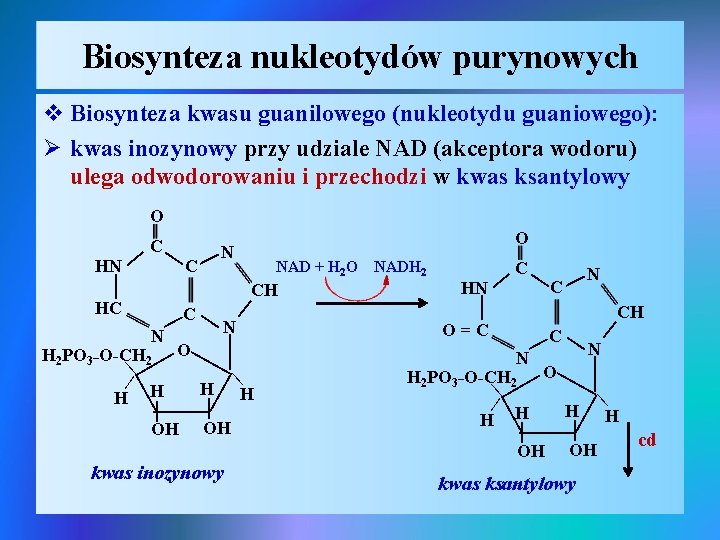
Biosynteza nukleotydów purynowych v Biosynteza kwasu guanilowego (nukleotydu guaniowego): Ø kwas inozynowy przy udziale NAD (akceptora wodoru) ulega odwodorowaniu i przechodzi w kwas ksantylowy O | | | | H 2 PO 3_O-CH 2 O | H H H | OH | | | N N H | OH kwas ksantylowy | C | | | kwas inozynowy O=C CH | OH | C | OH | HN N | H 2 PO 3_O-CH 2 O | H H H C | N | | CH N | C | HC NAD + H 2 O NADH 2 | | C | | HN O N | C H cd
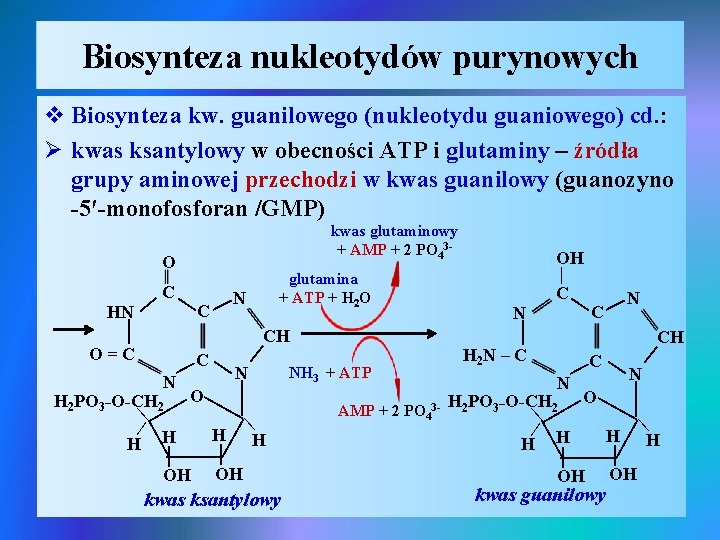
Biosynteza nukleotydów purynowych v Biosynteza kw. guanilowego (nukleotydu guaniowego) cd. : Ø kwas ksantylowy w obecności ATP i glutaminy – źródła grupy aminowej przechodzi w kwas guanilowy (guanozyno -5′-monofosforan /GMP) kwas glutaminowy + AMP + 2 PO 43 - | | | | | kwas ksantylowy | | OH H 2 PO 3_O-CH 2 O | H H H | OH kwas guanilowy | CH N N | | H C | AMP + 2 PO 43 - N OH | NH 3 + ATP H 2 N – C C | H 2 PO 3_O-CH 2 O | H H H N | | CH N | C | O=C | | | C | | HN N | C glutamina + ATP + H 2 O OH | O H |

Biosynteza nukleotydów purynowych v Biosynteza kwasu inozynowego: Ø biosynteza kwasu inozynowgo jest blokowana przez określone inhibitory w określonych etapach biosyntezy: ü związki sulfonamidowe są antagonistami kwasu p-aminobenzoesowego (PAB) i hamują etap wprowadzenia grupy formylowej przy udziale kwasu tetrahydrofoliowego (THFA), ü 6 -diazo-5 -keto-L-norleucyna blokuje etap reakcji z udziałem glutaminy (blokada syntezy ugrupowania amidynowego), Ø antymetabolity powodujące zaburzenia w syntezie kwasów nukleinowych przez blokowanie enzymów w cyklu przemian są wykorzystywane w medycynie do zwalczania drobnoustrojów chorobotwórczych i tkanek nowotworowych.
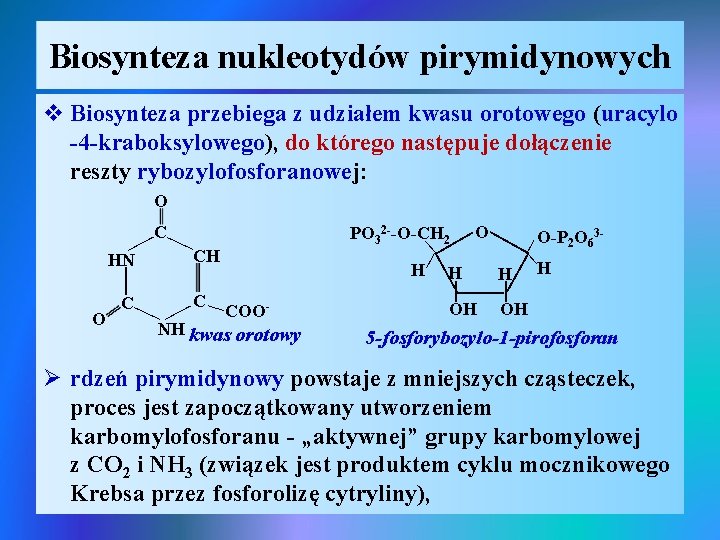
Biosynteza nukleotydów pirymidynowych v Biosynteza przebiega z udziałem kwasu orotowego (uracylo -4 -kraboksylowego), do którego następuje dołączenie reszty rybozylofosforanowej: O 3 PO 32 --O-CH 2 O | O-P 2 O 6 | H H | | COO - NH kwas orotowy | | | C | O C CH | OH | | HN | | C OH 5 -fosforybozylo-1 -pirofosforan Ø rdzeń pirymidynowy powstaje z mniejszych cząsteczek, proces jest zapoczątkowany utworzeniem karbomylofosforanu - „aktywnej” grupy karbomylowej z CO 2 i NH 3 (związek jest produktem cyklu mocznikowego Krebsa przez fosforolizę cytryliny),
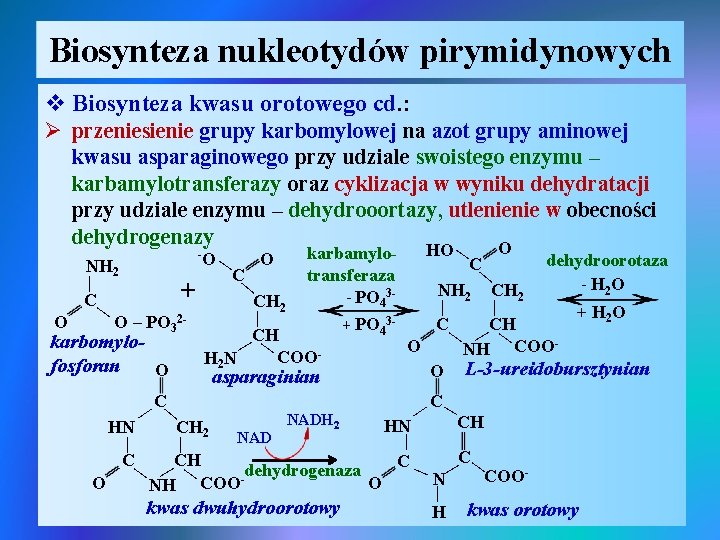
Biosynteza nukleotydów pirymidynowych v Biosynteza kwasu orotowego cd. : Ø przeniesienie grupy karbomylowej na azot grupy aminowej kwasu asparaginowego przy udziale swoistego enzymu – karbamylotransferazy oraz cyklizacja w wyniku dehydratacji przy udziale enzymu – dehydrooortazy, utlenienie w obecności dehydrogenazy O | asparaginian | | | | kwas dwuhydroorotowy | CH | NADH 2 HN CH 2 NAD | | CH C dehydrogenaza O NH COO- C C N | HN | C O NH 2 CH 2 | | + H 2 O C CH O NH COOO L-3 -ureidobursztynian | C + PO 43 - dehydroorotaza - H 2 O C | CH 2 | CH COOH 2 N HO COO- | | | C karbamylotransferaza - PO 43 - | O | karbomylofosforan O O | | NH 2 | + C O O – PO 32 - - kwas orotowy
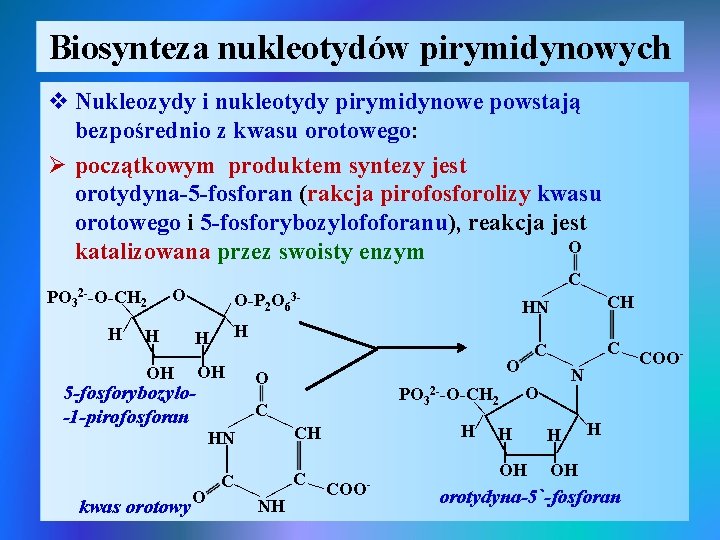
Biosynteza nukleotydów pirymidynowych v Nukleozydy i nukleotydy pirymidynowe powstają bezpośrednio z kwasu orotowego: Ø początkowym produktem syntezy jest orotydyna-5 -fosforan (rakcja pirofosforolizy kwasu orotowego i 5 -fosforybozylofoforanu), reakcja jest O katalizowana przez swoisty enzym | | kwas orotowy C C NH COO - | | | H CH N | O | 2 | | | C HN O PO 3 2 --O-CH | O | 5 -fosforybozylo-1 -pirofosforan OH C C O | OH | | | H H OH OH | CH | | | HN | H 3| O-P 2 O 6 H H | O 2 C | PO 3 2 --O-CH | H orotydyna-5`-fosforan COO-
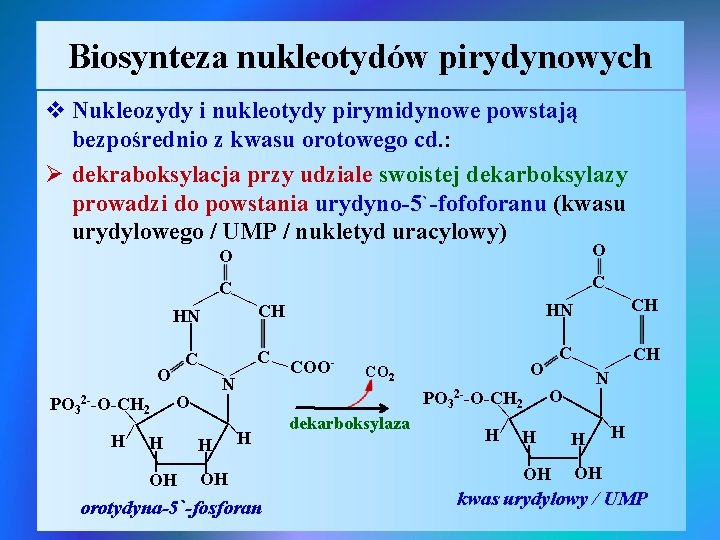
Biosynteza nukleotydów pirydynowych v Nukleozydy i nukleotydy pirymidynowe powstają bezpośrednio z kwasu orotowego cd. : Ø dekraboksylacja przy udziale swoistej dekarboksylazy prowadzi do powstania urydyno-5`-fofoforanu (kwasu urydylowego / UMP / nukletyd uracylowy) O C C OH | | orotydyna-5`-fosforan dekarboksylaza 2 --O-CH | N | O H | 2 | | | CO 2 | | | | OH | | | CH O PO 3 H C | | COO - | N CH | PO 32 --O-CH 2 O | H H H | O C C HN | | | CH | | HN | | O H H OH OH | | H kwas urydylowy / UMP
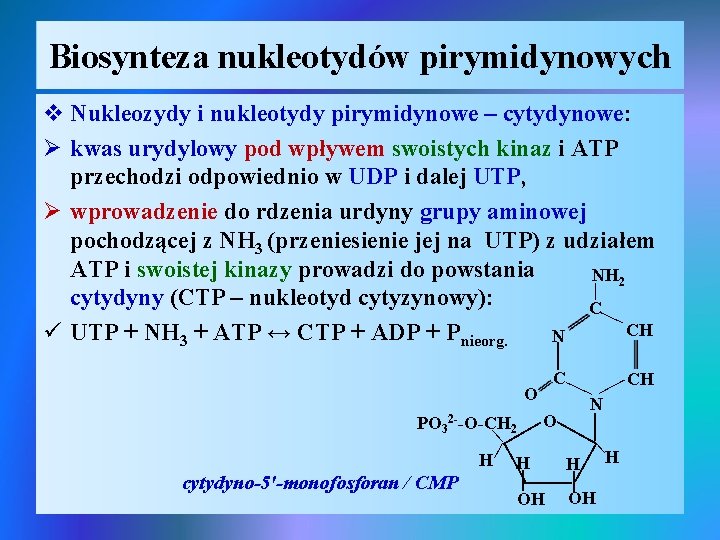
Biosynteza nukleotydów pirymidynowych | v Nukleozydy i nukleotydy pirymidynowe – cytydynowe: Ø kwas urydylowy pod wpływem swoistych kinaz i ATP przechodzi odpowiednio w UDP i dalej UTP, Ø wprowadzenie do rdzenia urdyny grupy aminowej pochodzącej z NH 3 (przeniesienie jej na UTP) z udziałem ATP i swoistej kinazy prowadzi do powstania NH 2 | cytydyny (CTP – nukleotyd cytyzynowy): C CH ü UTP + NH 3 + ATP ↔ CTP + ADP + Pnieorg. N | C | | | | | H cytydyno-5′-monofosforan / CMP N O 2 | PO 3 2 --O-CH CH | O H H OH OH | | H

Biosynteza deoksynukleotydów v Biosynteza deoksyrybonukleotydów (dezoksy-): Ø zamiana rybozy w deoksyrybozę (dezoksyrybozę) przebiega w rybonukleotydach bez naruszenia wiązania między rybozą a zasadą purynową / pirymidynową (odtlenienie na C 2 rybozy przebiega w rybotydach / nukleozydach, nukletydach przy udziale swoistych enzymów), Ø biosynteza nukleotydu tyminowego / TMP (tymidyno-5`-monofosforan): ü „aktywny metyl” / THFA przy udziale enzymu metylotransferazy zostaje przeniesiony na uracyl, produktem jest 5 -metylouracyl / tymina. ü proces może być zablokowany przez antagonistyczny analog koenzymu – aminopterynę.
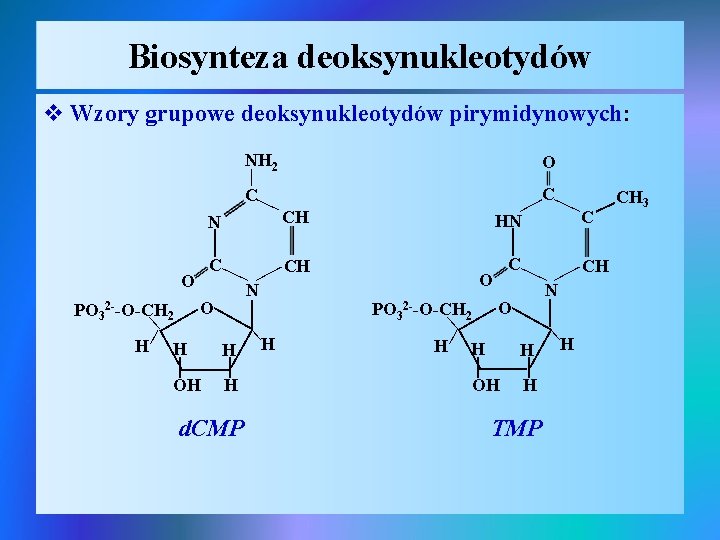
Biosynteza deoksynukleotydów v Wzory grupowe deoksynukleotydów pirymidynowych: NH 2 O C C HN C CH C | N | | | | d. CMP H | OH | PO 32 --O-CH 2 O | H H H | | | CH | OH | | N TMP C | | O | PO 32 --O-CH 2 O | H H H | | | O | CH | N H CH 3 | | |
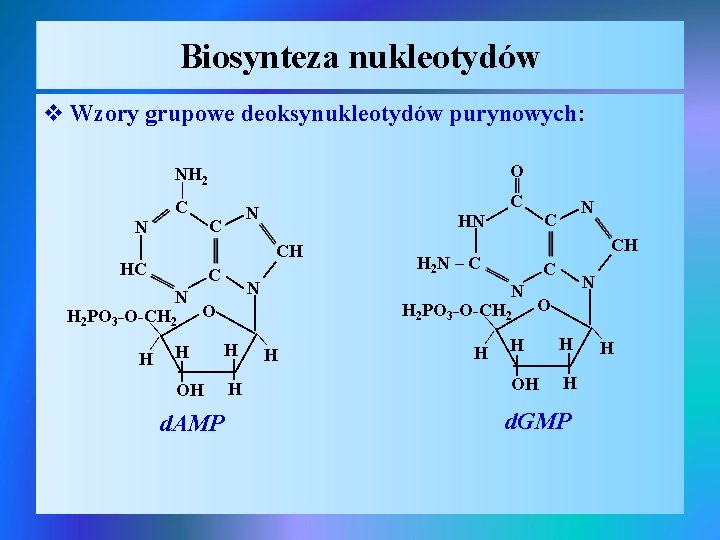
Biosynteza nukleotydów v Wzory grupowe deoksynukleotydów purynowych: O | | | OH | H d. GMP | | | d. AMP H H 2 PO 3_O-CH 2 O | H H H | OH | CH N N | | C | | H 2 PO 3_O-CH 2 O | H H 2 N – C | N | N | C | | HC CH C | | C HN | N C N | C | NH 2 H |

Biosynteza kwasów nukleinowych v Biosynteza DNA: Ø prekursorami dla kwasu DNA są reaktywne nukleotydy – deoksyrybozydo-5`-trifosforany, Ø poszczególne nukleotydy w formie trójfosforanów atakują wiązaniem pirofosforanowym grupę – OH na C 3, która znajduje się na końcu łańcucha polinukleotydowego, Ø odszczepienie się pirofosforanu powoduje wydłużenie łańcucha o jeden element strutkturalny, Ø kolejne przyłączenia nukleotydów wydłuża pojedynczą nić DNA do ok. 10 000 nukleotydów, Ø reakcja musi być zapoczątkowana przez obecny w układzie reagującym DNA (matryca) i w obecności swoistych enzymów grasicy i szpiku, reakcja przebiega z ATP do momentu wyczerpania się nukleotydów.
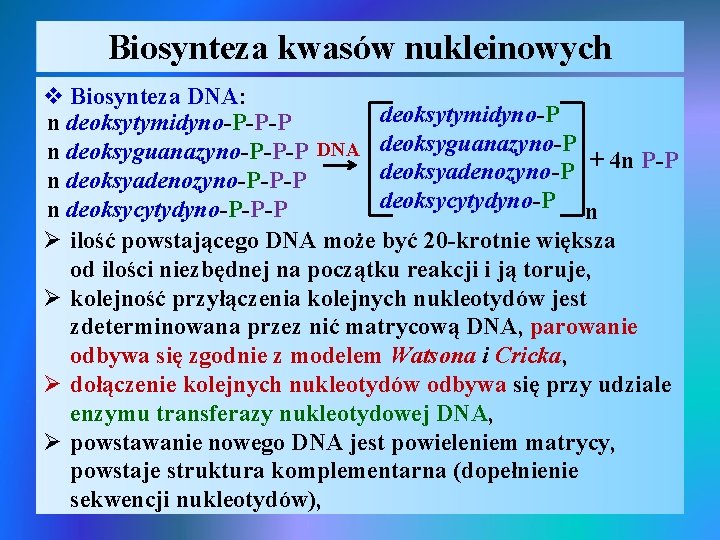
Biosynteza kwasów nukleinowych v Biosynteza DNA: deoksytymidyno-P n deoksytymidyno-P-P-P n deoksyguanazyno-P-P-P DNA deoksyguanazyno-P + 4 n P-P deoksyadenozyno-P n deoksyadenozyno-P-P-P deoksycytydyno-P n n deoksycytydyno-P-P-P Ø ilość powstającego DNA może być 20 -krotnie większa od ilości niezbędnej na początku reakcji i ją toruje, Ø kolejność przyłączenia kolejnych nukleotydów jest zdeterminowana przez nić matrycową DNA, parowanie odbywa się zgodnie z modelem Watsona i Cricka, Ø dołączenie kolejnych nukleotydów odbywa się przy udziale enzymu transferazy nukleotydowej DNA, Ø powstawanie nowego DNA jest powieleniem matrycy, powstaje struktura komplementarna (dopełnienie sekwencji nukleotydów),

Biosynteza kwasów nukleinowych v Wiązanie wodorowe w α-helisie (α-heliksie) DNA: Ø płaskie pierścienie zasad powiązane są za pomocą wiązań wodorowych, które powstają między grupą – NH 2 6 -amionpuryny lub grupą – OH 6 -hydroksypuryny a grupą – OH 6 -hydroksypirymidny lub NH 2 6 -aminopirmidyny, Ø warunki przestrzenne i dobór najtrwalszych wiązań wodorowych między parami zasad purynowych i pirymidynowych warunkuje trwałość sprali (jej nierozkręcalność), Ø kolejność nukleotydów w jednym łańcuchu definiuje ich kolejność w drugim łańcuchu, Ø prawidłowość odgrywa istotną w podziałach chromosomów i procesie dziedziczenia,
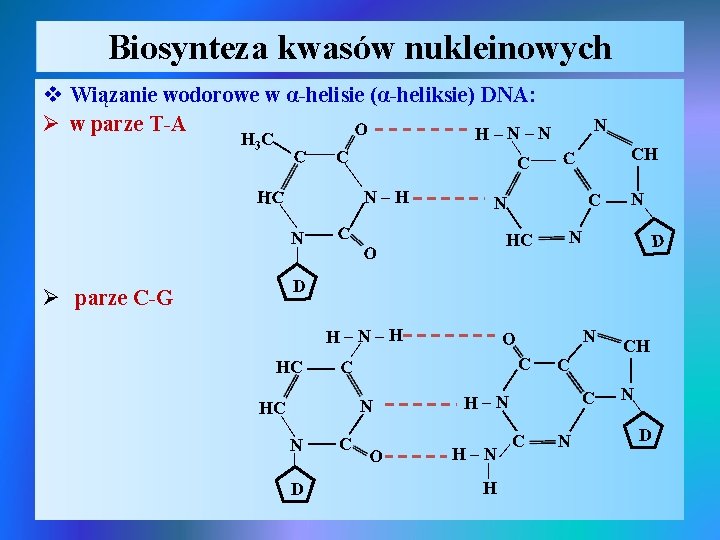
Biosynteza kwasów nukleinowych v Wiązanie wodorowe w α-helisie (α-heliksie) DNA: Ø w parze T-A O H–N–N C | C | N | O N C | | | CH C HC N O | N | C | N | HC | N–H | C | | | H 3 C N | D D H–N–H | D C | N | | C | N O H–N | C | H–N | H CH | C N N | HC C | HC | | Ø parze C-G | D

Biosynteza kwasów nukleinowych v Biosynteza RNA: Ø kwasy rybonukleinowe występują w formie pojedynczych nici, które na określonych odcinkach mogą być zwinięte spiralnie, przyjmuje postać pałeczki o dużej gęstości, Ø w roztworach soli o znacznym stężeniu ulegają rozwinięciu i tworzą chaotyczny zwój, Ø substratem biosyntezy (polikondensacji) nici RNA są difosforany nukleotydowe, przy udziale enzymu transferazy nukleotydowej reszty nukleotydowe są przenoszone na matrycę i jest uwalniany nieorganiczny fosforan, Ø biosynteza odbywa się w jądrze komórkowym i przemieszcza się do cytoplazmy,

Rozkład kwasów nukleinowych v Równoległymi procesami do biosyntezy jest ich rozkład przy udziale swoistych enzymów: Ø deoksyrybonukleaza (dezoksyrybonukleaza) należąca do hydrolaz zrywa niektóre wiązania estrowe między C`3 deoksyrybozy (dezoksyrybozy) z kwasem fosforowym w łańcuchu nukleotydowym, powstaje mieszanina oligonukleotydów, Ø rybonukleaza należąca do transferaz przenosi grupę fosforanową z pozycji C`5 nukleotydu purynowego lub pirymidynowego na pozycję C`2 sąsiadującego nukleotydu pirymidynowego, ü powstaje cykliczny 2`, 3`-dwunukleotyd, który ulega hydrolitycznemu rozpadowi na 3`-nukleotyd, w efekcie powstają oligonukleotydy zakończone nukleotydem pirymidynowym z fosforanem w poz. 3` rybozy,

Rozkład kwasów nukleinowych Ø dalszy rozkład oligonukleotydów przebiega pod wpływem nieswoistych hydrolaz: ü difosfoesterazy odrywają od oligonukleotydów mononukleotydy, ü fosfomonoesterazy rozbijają mononukleotydy na nukleozydy i kwas fosforowy, Ø ogólny schemat rozpadu: ü nukleozyd + fosforan ↔ zasada + rybozo-1 -fosforan ü lub nukleozyd + pirofosforan ↔ zasada + + 5 -fosforybulozopirofosforan, Ø reakcje są odwracalne i mogą powstawać nowe nukleozydy przez wymianę zasad purynowych lub pirymidynowych, dalsze przemiany katabolityczne zachodzą na poziomie nukleozydów (np. reakcje dezaminacji wobec dezaminazy).

Rozkład kwasów nukleinowych kwas inozynowy → inozyna → → → v Drogi rozkładu nukleotydów i nukleozydów purynowych: Ø zależą od właściwości układów enzymatycznych w tkankach zwierzęcych: kwas adenilowy → adenozyna adenina → hipoksantyna → → → kwas ksantylowy → ksantozyna → ksantyna → kwas moczowy kwas guanylowy → guanozyna → guanina Ø końcowym produktem rozkładu tlenowego zasad purynowych w ustroju zwierzęcym jest kwas moczowy, (wydalany z moczem u człowieka – brak enzymu urykazy), u innych saków wydalany jest z moczem w formie allantoiny, u kręgowców (ryby, płazy) wydalany jest w formie mocznika i kwasu glioksalowego.
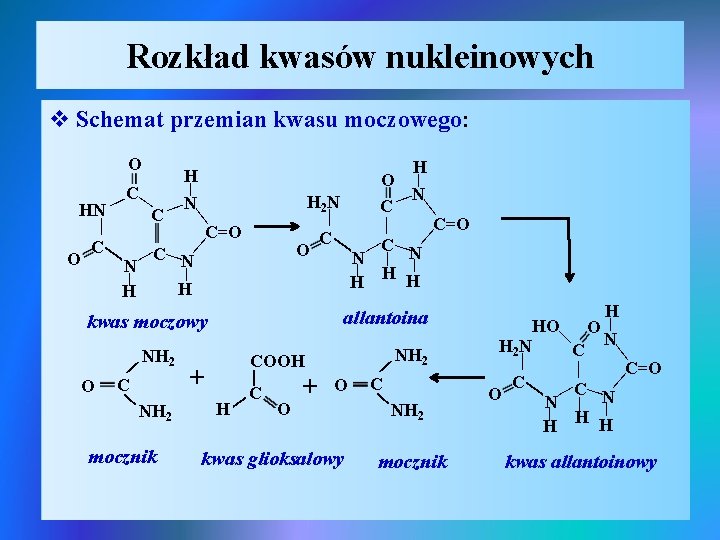
Rozkład kwasów nukleinowych v Schemat przemian kwasu moczowego: | | C N N | | H H C=O | | | O C | | C=O C N | | H H H | | C | | H 2 N | allantoina kwas moczowy H | HO O| N H 2 N C kwas glioksalowy C | | mocznik H | NH 2 mocznik O C | | C=O C N | | H H H | | C NH 2 | O + COOH | + O C O | | NH 2 | O | C | HN H O | N C H | O kwas allantoinowy
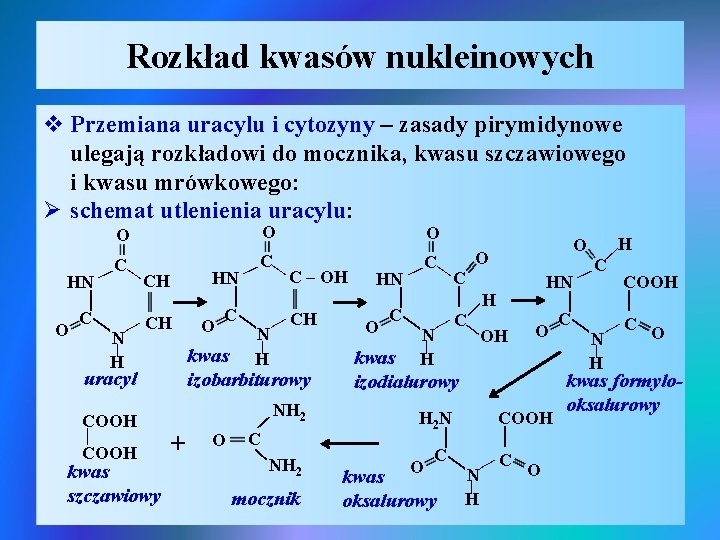
Rozkład kwasów nukleinowych v Przemiana uracylu i cytozyny – zasady pirymidynowe ulegają rozkładowi do mocznika, kwasu szczawiowego i kwasu mrówkowego: Ø schemat utlenienia uracylu: NH 2 C NH 2 mocznik | N | H | OH O kwas izodialurowy H 2 N COOH | | O C kwas oksalurowy N | H C | kwas szczawiowy O C | COOH + | | C | | | H O C COOH N | H C | COOH | uracyl kwas izobarbiturowy O HN C | N | H | | O C | CH HN | C | O | N | H CH | C | O | C – OH H O | | HN CH | C | C | O | HN O O kwas formylooksalurowy
- Slides: 35