Biosimilares y Equivalencia Teraputica Dra Olga Delgado Hospital

Biosimilares y Equivalencia Terapéutica Dra. Olga Delgado Hospital Universitario Son Dureta Palma de Mallorca 8º Curso de Evaluación y Selección de Medicamentos Hospital Universitario Son Dureta Palma de Mallorca, 4 -7 mayo 2010

ü Estudios de equivalencia terapéutica entre dos medicamentos ü Comparador es el medicamento de referencia ü El margen delta aprobado ü La variable reconocida ¿Habría dudas de equivalencia?

¿Qué es un medicamento biotecnológico? Medicamento cuyo principio activo se produce por material de origen biológico (microorganismos, tejidos u órganos, células o fluidos de origen animal o vegeral). Implantación de material genético por la tecnología del DNA recombinante, conviertiéndolos en productores de sustancias que necesitamos. Oligopépticos y proteínas naturales, después mejoradas. Complejas: anticuerpos poli o monoclonales.

Medicamentos biotecnológicos Tipo de molécula Ejemplo Hormonas Insulina, glucacón, GH, tirotropina, hormona folículo estimulante, eritropoyetina Citoquinas Interferón-alfa, factor estimulantes colonias granulocitos, interleukinas Factores coagulación Factor VII, factor VIII, Factor IX Anticuerpos monoclonales Bevacizumab, cetuximab, abciximab, rituximab, infliximab, t ocilizumab, adalimumab, certolizumab, denosumab Enzimas Glucocerebrosidasa, alteplasa, rasburicasa Fragmentos protéicos sinténtico Etanercept Moléculas conjugadas Peg-interferón alfa 2 -a, peg-filgrastim Adaptación. N Engl J Med 2008: 358(8): 843 -9.

Top 10 hospital products in EU (products, molecule and sales) 8 of Top 10 Hospital products are biotech drugs!! IMS data 1 Q 2008


Características Medicamentos biotecnológicos Tamaño molécula Estructura Métodos caracterización Síntesis química Biotecnología Pequeñas Grandes (tridimensionales) Simple Proteínas (glicosiladas) Análisis químicos Ensayos clínicos


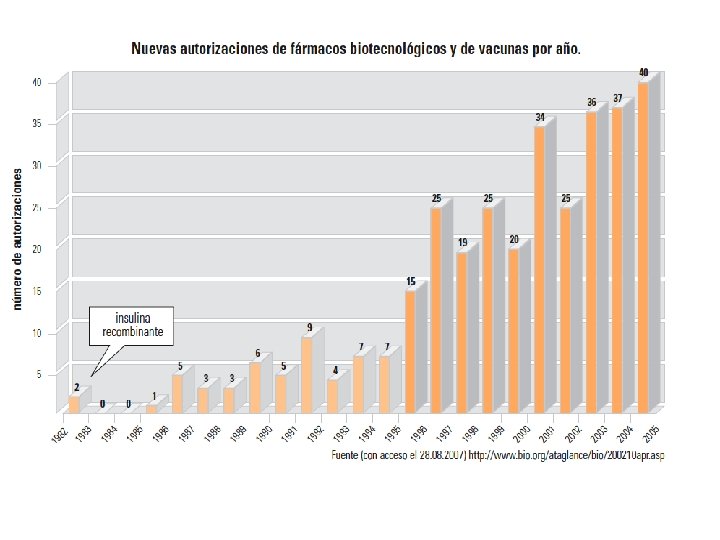
Genéricos y biosimilares Patentes de los primeros medicamentos biotecnológicos empezaron caducaron en el 2004 -2008 en Europa. El mercado se abre a versiones genéricas: Biosimilares (Unión Europea) Follow-on protein products (Estados Unidos) Verificación de la similitud de los biosimilares respecto al innovador ha sido un desafío regulatorio para las agencias, en las que la EMEA ha sido pionera. FDA aún no ha regulado.
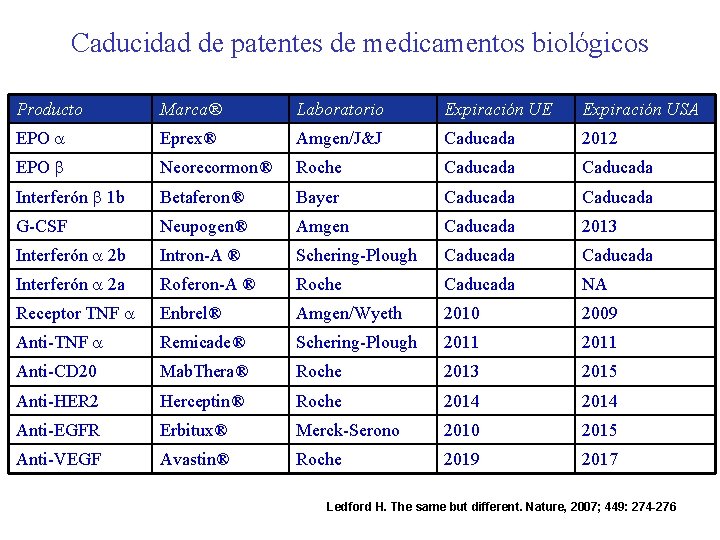
Caducidad de patentes de medicamentos biológicos Producto Marca® Laboratorio Expiración UE Expiración USA EPO Eprex® Amgen/J&J Caducada 2012 EPO Neorecormon® Roche Caducada Interferón 1 b Betaferon® Bayer Caducada G-CSF Neupogen® Amgen Caducada 2013 Interferón 2 b Intron-A ® Schering-Plough Caducada Interferón 2 a Roferon-A ® Roche Caducada NA Receptor TNF Enbrel® Amgen/Wyeth 2010 2009 Anti-TNF Remicade® Schering-Plough 2011 Anti-CD 20 Mab. Thera® Roche 2013 2015 Anti-HER 2 Herceptin® Roche 2014 Anti-EGFR Erbitux® Merck-Serono 2010 2015 Anti-VEGF Avastin® Roche 2019 2017 Ledford H. The same but different. Nature, 2007; 449: 274 -276

¿Qué es un medicamento biosimilar?


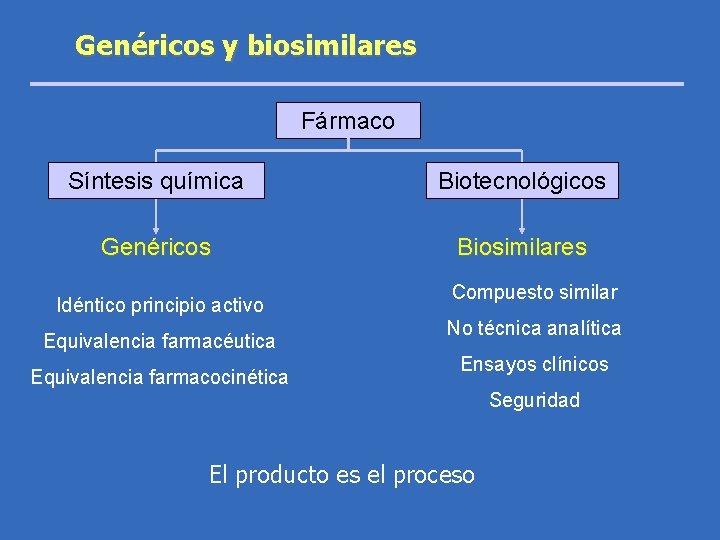
Genéricos y biosimilares Fármaco Síntesis química Biotecnológicos Genéricos Biosimilares Idéntico principio activo Equivalencia farmacéutica Equivalencia farmacocinética Compuesto similar No técnica analítica Ensayos clínicos Seguridad El producto es el proceso

Aspectos diferenciales biosimilares Producción Variabilidad Impacto en la seguridad
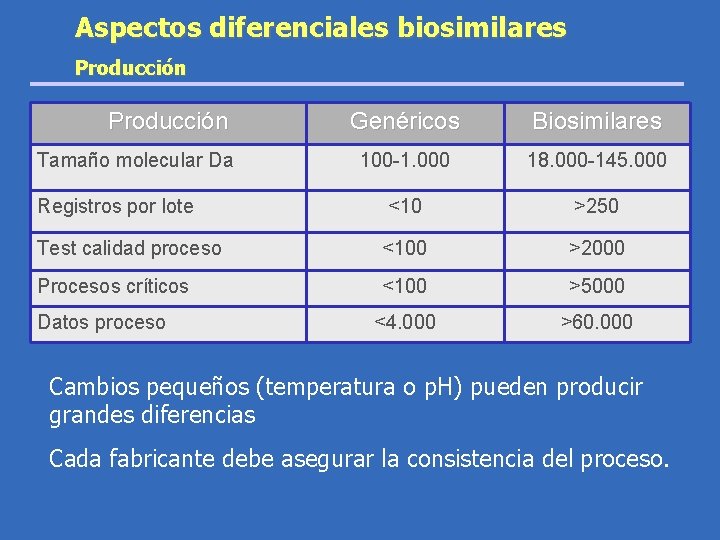
Aspectos diferenciales biosimilares Producción Genéricos Biosimilares Tamaño molecular Da 100 -1. 000 18. 000 -145. 000 Registros por lote <10 >250 Test calidad proceso <100 >2000 Procesos críticos <100 >5000 <4. 000 >60. 000 Datos proceso Cambios pequeños (temperatura o p. H) pueden producir grandes diferencias Cada fabricante debe asegurar la consistencia del proceso.
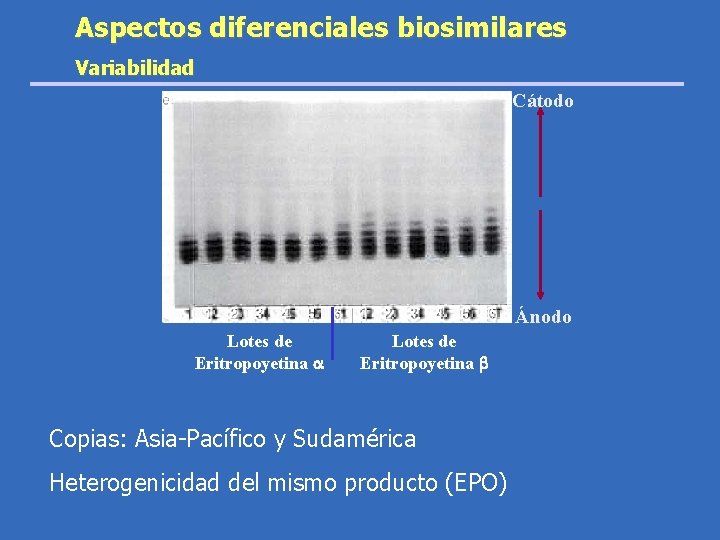
Aspectos diferenciales biosimilares Variabilidad Cátodo Ánodo Lotes de Eritropoyetina Copias: Asia-Pacífico y Sudamérica Heterogenicidad del mismo producto (EPO)

Aspectos diferenciales biosimilares Impacto en la seguridad Potencial inmunogénico, muy diferente entre productos muy similares. Algoritmos informáticos para determinalo, pero es impredecible. Producción de Ac puede ser banal o muy importante


Modification of Eprex formulation outside USA

Garantías Los productos no son exactamente iguales, el proceso de fabricación es el producto y hay que garantizar: -Calidad -Eficacia -Seguridad -Inmunogenicidad

¿Cómo se evalúa un biosimilar? La legislación define qué requisitos debe reuni� r cada producto, para garantizar que es tan seguro y eficaz como el original. La eficacia se mide en variables diferentes para cada enfermedad tratada. Estudios en varias fases: calidad y consistencia del proceso de fabricación, seguidos de estudios de eficiencia y seguridad. Se deben hacer estudios comparativos entre los dos medicamentos.

Estudios en humanos Son el pilar del proceso regulatorio Valorar la eficacia y la seguridad en personas Estudios de farmacovigilancia y postmarketing Variabilidad entre razas, sexo, edad Reacciones derivadas de uso inadecuado, interacciones Requisitos específicos para cada producto en una sola indicación, pero se consigue autorización para todas las indicaciones.

Mundial EMEA: primera en regular CHMP Francia: reglamentación específica Brasil: conciencia y estiman que debe haber estudios de “no inferioridad” frente a los originales América central, Ecuador, Venezuela, Argentina, Chile: se presentan biosimilares sin exigencia de estudios clínicos o de farmacovigilancia.

EMEA Proceso regulatorio se inició en 2001 y en 2006 se establecen las guías para la aprobación de productos. Se establece el procedimiento para mostrar comparabilidad del biosimilar con el producto original en cuanto a calidad, seguridad y eficacia. 2006: primeras aprobaciones de SOMATROPINA (Omnitrope y Valtropin). FDA Hay 2 productos aprobados: Omnitrope y Cangene. Los mismos principios que la EMEA.
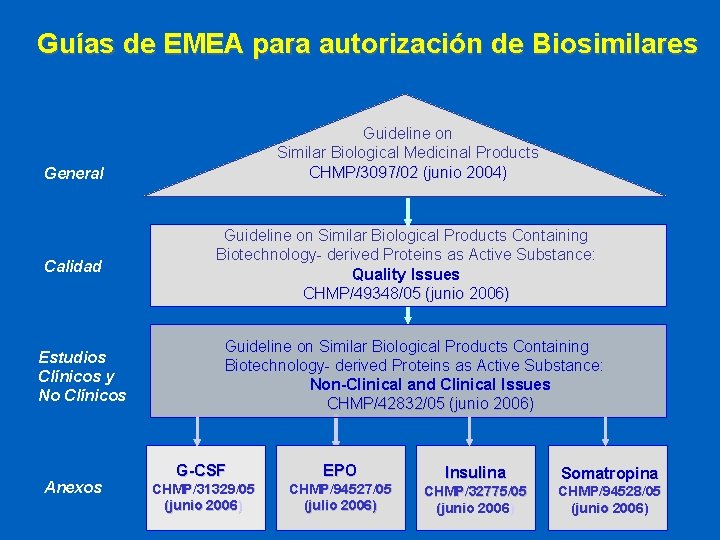
Guías de EMEA para autorización de Biosimilares Guideline on Similar Biological Medicinal Products CHMP/3097/02 (junio 2004) General Calidad Estudios Clínicos y No Clínicos Anexos Guideline on Similar Biological Products Containing Biotechnology- derived Proteins as Active Substance: Quality Issues CHMP/49348/05 (junio 2006) Guideline on Similar Biological Products Containing Biotechnology- derived Proteins as Active Substance: Non-Clinical and Clinical Issues CHMP/42832/05 (junio 2006) G-CSF EPO CHMP/31329/05 (junio 2006) CHMP/94527/05 (julio 2006) Insulina Somatropina CHMP/32775/05 (junio 2006) CHMP/94528/05 (junio 2006)

Otros documentos EMEA de Biosimilares Conceptos Interferon-alfa Conceptos: Fin consulta 1 august 2006 Reflection paper Aspectos no clínicos y clínicos: efectivo April 2006 HPBM Fin consulta 30 april 2007 Guidelines no-clinical and clinical: efectiva octubre 2009 EPO Revisión Guideline no-clinical and clinical será efectiva en septiembre 2010 Anticuerpos monoclonales Inmunogenicidad: Fin consulta: junio 2009 Guidelines: Fin consulta enero 2010 Hormona Folículo Estimulante (FSH) Conceptos: Fin consulta Junio 2010

Farmacovigilacia Postcomercialización Inmunogenicidad impredecible Farmacovigilancia para monitorizar inmunogenicidad

Para una mejor farmacovigilancia, la EMEA definió una guía para la gestión de riesgos aplicable a todo medicamento de uso humano cuya solicitud de autorización sea a través de la EMEA , incluídos los biosimilares. Esta guía está vigente desde Noviembre 2005.
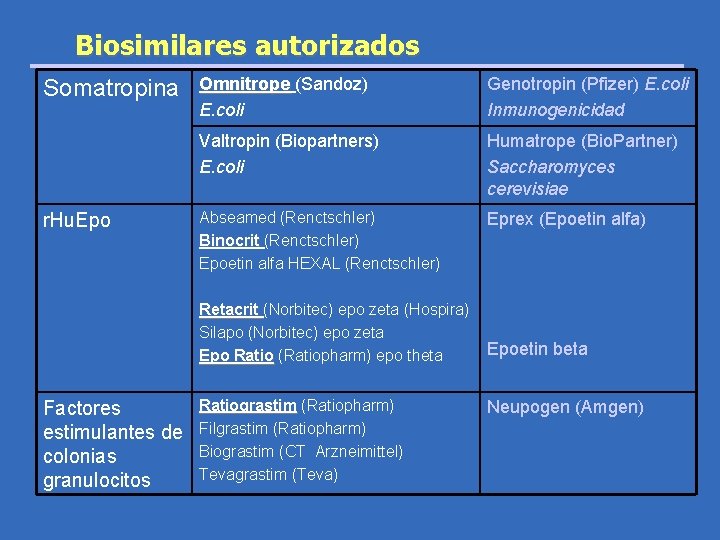
Biosimilares autorizados Somatropina r. Hu. Epo Omnitrope (Sandoz) E. coli Genotropin (Pfizer) E. coli Inmunogenicidad Valtropin (Biopartners) E. coli Humatrope (Bio. Partner) Saccharomyces cerevisiae Abseamed (Renctschler) Binocrit (Renctschler) Epoetin alfa HEXAL (Renctschler) Eprex (Epoetin alfa) Retacrit (Norbitec) epo zeta (Hospira) Silapo (Norbitec) epo zeta Epo Ratio (Ratiopharm) epo theta Ratio Factores estimulantes de colonias granulocitos Ratiograstim (Ratiopharm) Ratiograstim Filgrastim (Ratiopharm) Biograstim (CT Arzneimittel) Tevagrastim (Teva) Epoetin beta Neupogen (Amgen)

Biosimilares no autorizados Interferon alfa-2 Alpheon Roferon-A (Pfizer) Datos insuficientes

Ensayos eficacia clínica biosimilares Somatropina biosimilar (Omnitrope, Sandoz 2006) Somatropina Omnitrope (Sandoz) E. coli Genotropin (Pfizer) E. coli EC: 89 niños + 51 Inmunogenicidad EC Fase III Somatropin con Genotropin (9 meses) y extensión 6 meses Pacientes naïve déficit Hormona Crecimiento <-1 SD 1º Talla y talla estandarizada edad y sexo mes 6, velocidad mes 0 y 9. 2º: niveles séricos meses 1, 3, 6 y 9. Estudio inicial de superioridad rediseñado posteriormente para mostrar similitud.
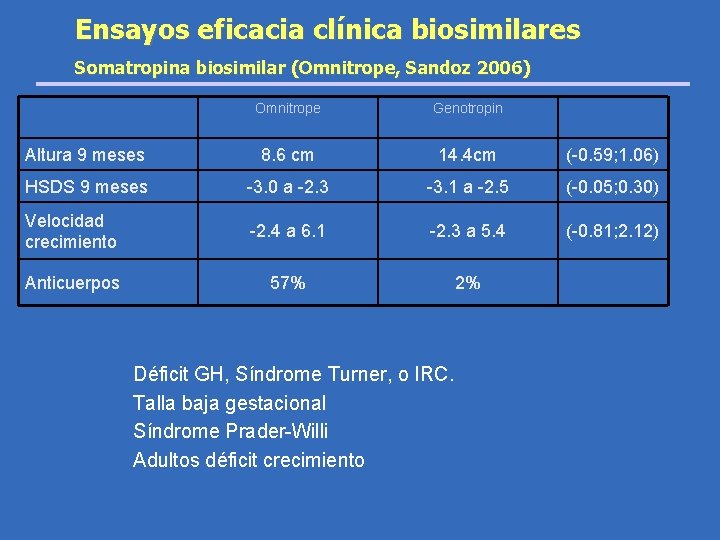
Ensayos eficacia clínica biosimilares Somatropina biosimilar (Omnitrope, Sandoz 2006) Omnitrope Genotropin Altura 9 meses 8. 6 cm 14. 4 cm (-0. 59; 1. 06) HSDS 9 meses -3. 0 a -2. 3 -3. 1 a -2. 5 (-0. 05; 0. 30) Velocidad crecimiento -2. 4 a 6. 1 -2. 3 a 5. 4 (-0. 81; 2. 12) Anticuerpos 57% 2% Déficit GH, Síndrome Turner, o IRC. Talla baja gestacional Síndrome Prader-Willi Adultos déficit crecimiento

Ensayos eficacia clínica biosimilares Epoteina theta (Eporatio, Ratiopharm 2009) r. Hu. Epo Ratio (Ratiopharm) epo theta Epoetin beta 6 ensayos clínicos en IRC (2 EC doble ciego, aleatorizados) No inferioridad comparado con Epoetin beta 2 vías de administración Variables: cambio nivel Hg final tratamiento Tratamiento previo EPO-beta Delta <1. 0 g/d. L

Ensayos eficacia clínica biosimilares Epoteina theta (Eporatio, Ratiopharm 2009) Anemia sintomática asociada IRC Anemia sintomática en pacientes con cáncer con quimioterapia con enfermedad no mieloide Nota: no autorizado en autodonación en programa de donación de sangre autóloga

Valoración de biosimilares Aspectos de Calidad y eficacia Aspectos de seguridad Comparador es el de referencia Una indicación y se extiende a las demás Menor número de pacientes Inmunogenicidad Consecuencia impredecible Detección sistema inmune y causas Plan de farmacovigilancia y gestión riesgos Intercambiabilidad Aspectos del Coste- Cada vez más importancia Impacto sanitario y económico global eficacia

Dispensación Trazabilidad Programas de farmacovigilancia y gestión de riesgos No pueden ser sustituidos

Puntos a debate Nomenclatura Ampliación de indicaciones Capacidad inmunogénica impredecible Intercambio terapéutico

Denominación (International Nonproprietary Name)

Puntos a debate Nomenclatura Ampliación de indicaciones Capacidad inmunogénica impredecible Intercambio terapéutico

Introducción de biosimilares de EPO (Alemania) 23. 4% 21. 6% 19. 6% 16. 3% 17. 3% 14. 4% 13. 5% 10. 6% 8. 2% 5. 6% 0. 7% 0. 4% 3. 2% 2. 0% 3. 5% 5. 0% 9. 9% 8. 2% 6. 5% 10. 6% 11. 8% 13. 1%

Introducción del biosimilar de Filgrastim (Alemania) Diciembre 2008 – Febrero 2009 35% Diciembre 2008 Enero 2009 Febrero 2009

2009 2010
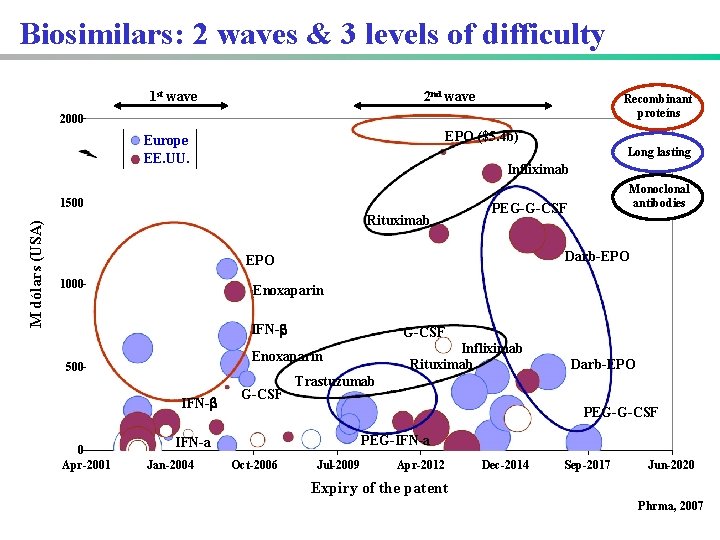
Biosimilars: 2 waves & 3 levels of difficulty 1 st wave 2 nd wave Recombinant proteíns 2000 EPO ($5. 4 b) Europe EE. UU. Long lasting Infliximab M dólars (USA) 1500 Rituximab PEG-G-CSF Darb-EPO 1000 Enoxaparin IFN- G-CSF Infliximab Rituximab Enoxaparin 500 IFN- 0 Apr-2001 Monoclonal antibodies G-CSF Trastuzumab PEG-G-CSF PEG-IFN-a Jan-2004 Darb-EPO Oct-2006 Jul-2009 Apr-2012 Dec-2014 Sep-2017 Jun-2020 Expiry of the patent Phrma, 2007

Conclusión § Biosimilares estarán cada día más presentes en los hospitales § Las repercusiones económica de su aparición y selección son muy importantes § Los procesos de evaluación y aprobación son propios, y específicos de cada molécula. Suficientes garantías regulatorias. § Evaluados en los hospitales en términos económicos, se seguridad y de intercambiabilidad.
- Slides: 46