Bioqumica de los Acidos Nucleicos CA Garca Seplveda

Bioquímica de los Acidos Nucleicos CA García Sepúlveda MD Ph. D Laboratorio de Genómica Viral y Humana Facultad de Medicina, Universidad Autónoma de San Luis Potosí 1

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA es una molécula bicatenaria (duplex), antiparalela y complementaria. 2

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA es una molécula BICATENARIA (duplex), antiparalela y complementaria. Cadena #1 Cadena #2 3
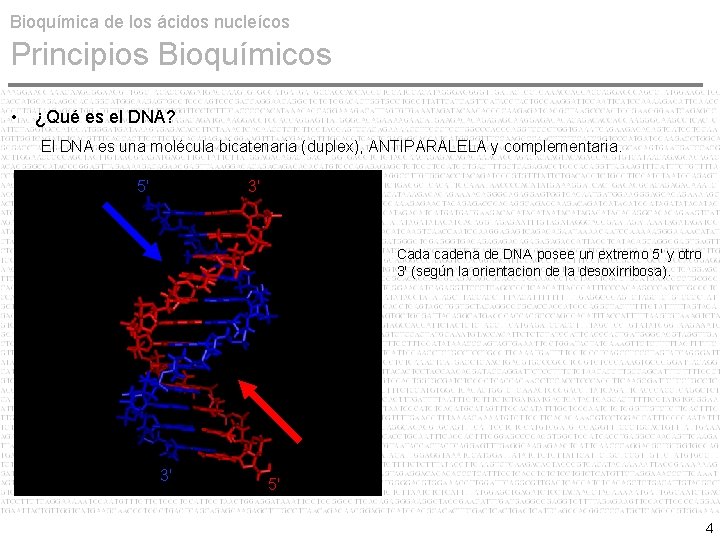
Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA es una molécula bicatenaria (duplex), ANTIPARALELA y complementaria. 5' 3' Cada cadena de DNA posee un extremo 5' y otro 3' (según la orientacion de la desoxirribosa). 3' 5' 4

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA es una molécula bicatenaria (duplex), antiparalela y COMPLEMENTARIA. A T T G C C G A T G C A Cuando no se encuentran formando parte de un duplex las cadenas aisladas de DNA se denominan A T ss. DNA. A C G T A T G C C G 5
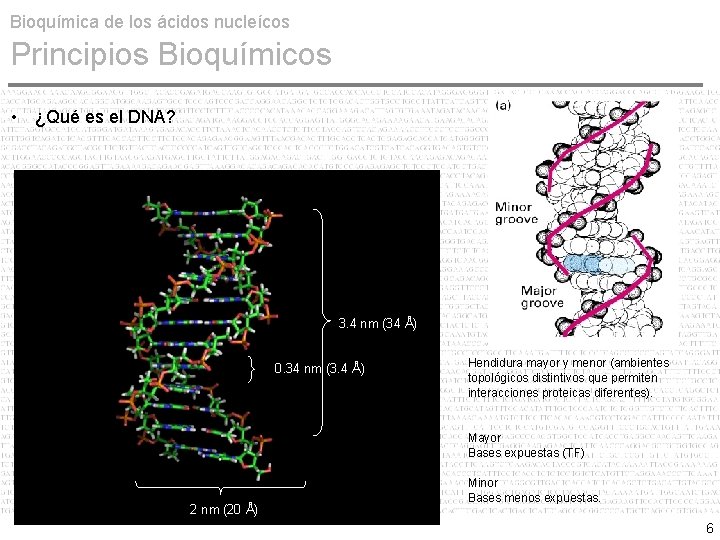
Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? 3. 4 nm (34 Å) 0. 34 nm (3. 4 Å) Hendidura mayor y menor (ambientes topológicos distintivos que permiten interacciones proteicas diferentes). Mayor Bases expuestas (TF) 2 nm (20 Å) Minor Bases menos expuestas. 6
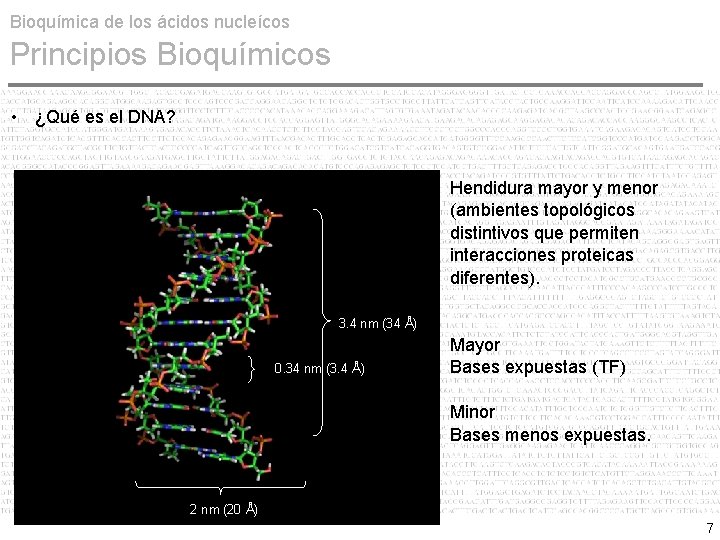
Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? Hendidura mayor y menor (ambientes topológicos distintivos que permiten interacciones proteicas diferentes). 3. 4 nm (34 Å) 0. 34 nm (3. 4 Å) Mayor Bases expuestas (TF) Minor Bases menos expuestas. 2 nm (20 Å) 7

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 8

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 9

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 10

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 11

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 12

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 13

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 14

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 15

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 16

Bioquímica de los ácidos nucleícos Principios Bioquímicos • ¿Qué es el DNA? El DNA (al igual que el RNA) es un polímero biológico. 17
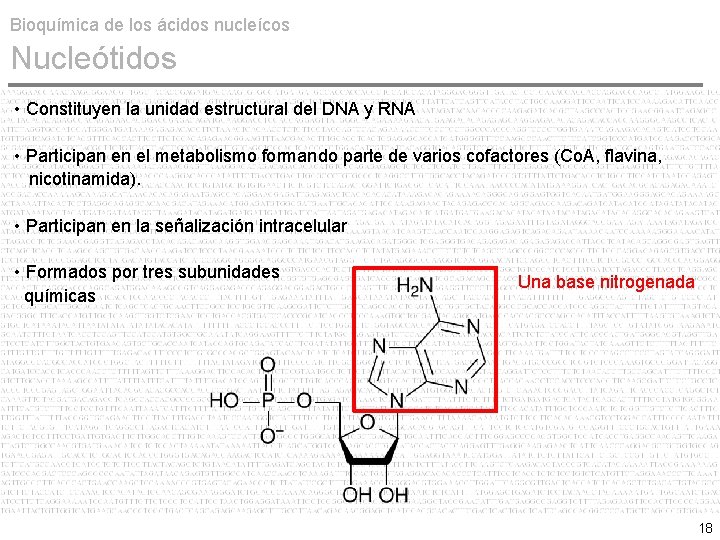
Bioquímica de los ácidos nucleícos Nucleótidos • Constituyen la unidad estructural del DNA y RNA • Participan en el metabolismo formando parte de varios cofactores (Co. A, flavina, nicotinamida). • Participan en la señalización intracelular • Formados por tres subunidades químicas Una base nitrogenada 18
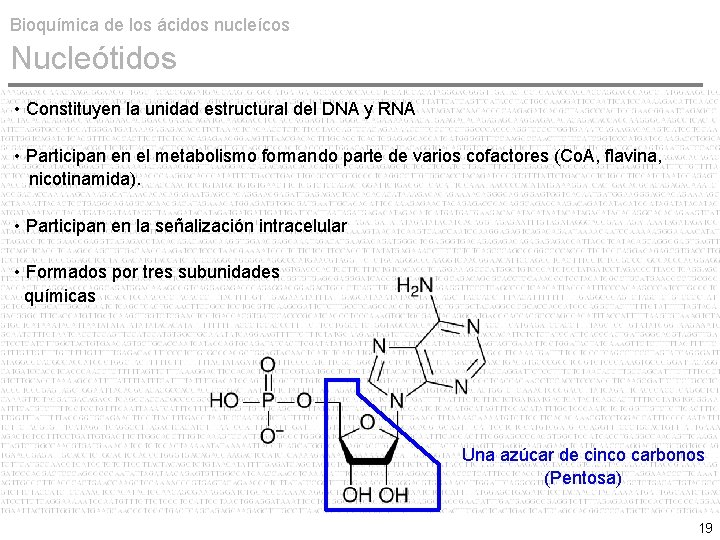
Bioquímica de los ácidos nucleícos Nucleótidos • Constituyen la unidad estructural del DNA y RNA • Participan en el metabolismo formando parte de varios cofactores (Co. A, flavina, nicotinamida). • Participan en la señalización intracelular • Formados por tres subunidades químicas Una azúcar de cinco carbonos (Pentosa) 19
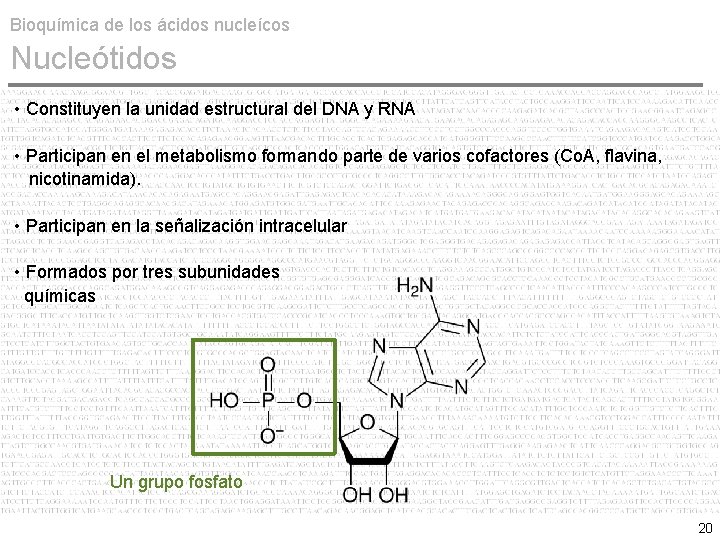
Bioquímica de los ácidos nucleícos Nucleótidos • Constituyen la unidad estructural del DNA y RNA • Participan en el metabolismo formando parte de varios cofactores (Co. A, flavina, nicotinamida). • Participan en la señalización intracelular • Formados por tres subunidades químicas Un grupo fosfato 20
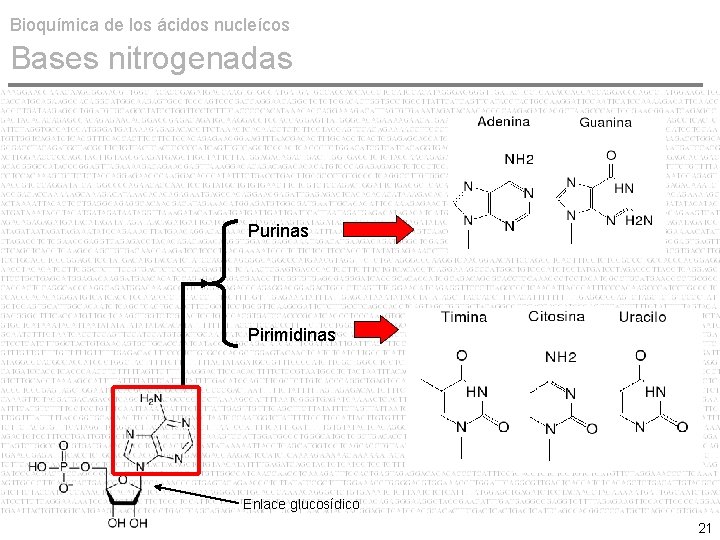
Bioquímica de los ácidos nucleícos Bases nitrogenadas Purinas Pirimidinas Enlace glucosídico 21
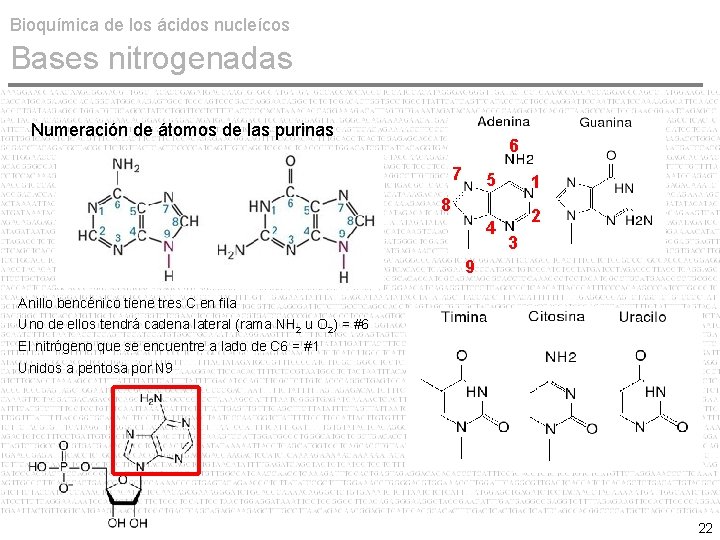
Bioquímica de los ácidos nucleícos Bases nitrogenadas Numeración de átomos de las purinas 6 7 5 1 8 4 2 3 9 Anillo bencénico tiene tres C en fila Uno de ellos tendrá cadena lateral (rama NH 2 u O 2) = #6 El nitrógeno que se encuentre a lado de C 6 = #1 Unidos a pentosa por N 9 22
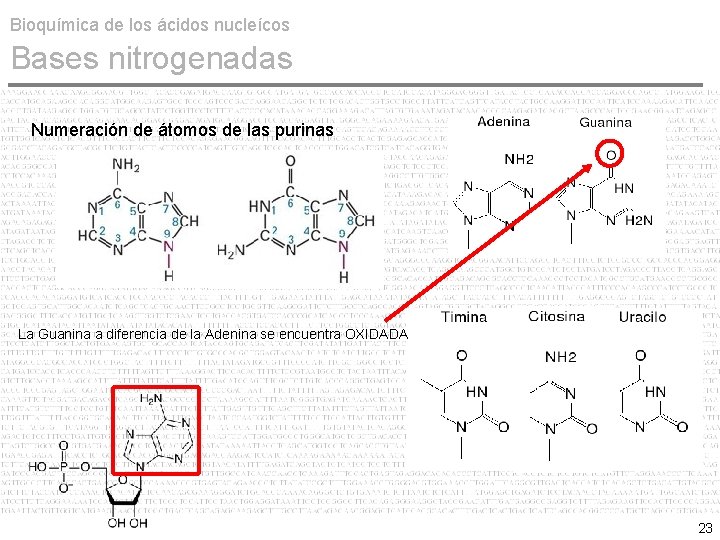
Bioquímica de los ácidos nucleícos Bases nitrogenadas Numeración de átomos de las purinas La Guanina a diferencia de la Adenina se encuentra OXIDADA 23
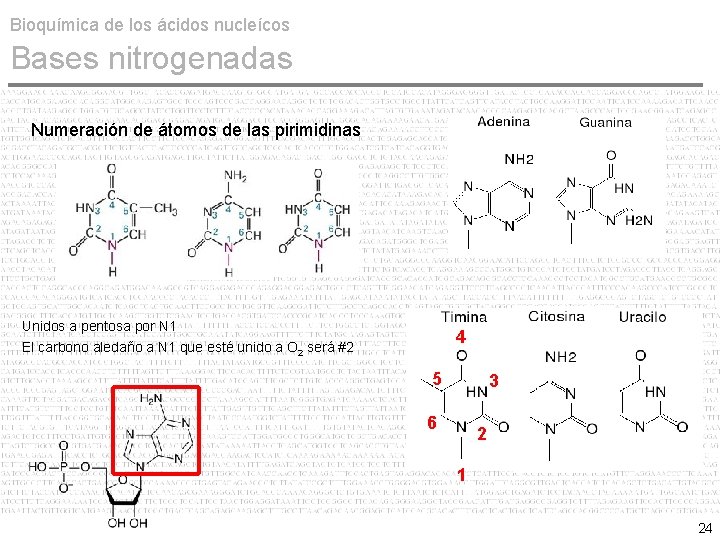
Bioquímica de los ácidos nucleícos Bases nitrogenadas Numeración de átomos de las pirimidinas Unidos a pentosa por N 1 El carbono aledaño a N 1 que esté unido a O 2 será #2 4 5 3 6 2 1 24
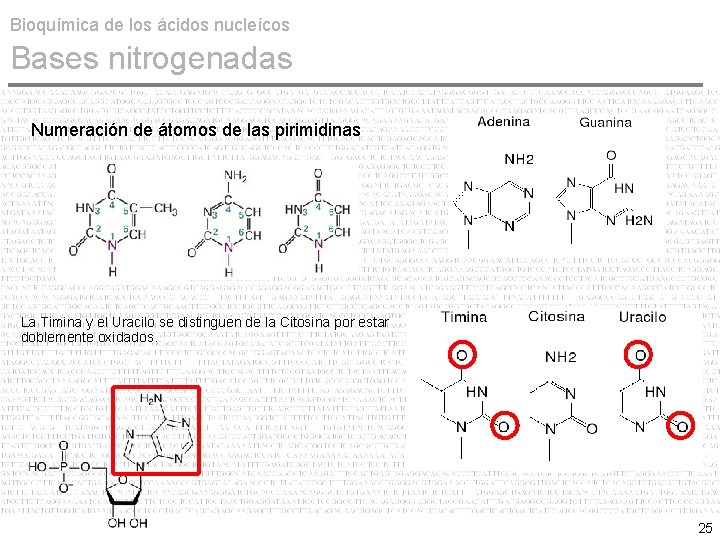
Bioquímica de los ácidos nucleícos Bases nitrogenadas Numeración de átomos de las pirimidinas La Timina y el Uracilo se distinguen de la Citosina por estar doblemente oxidados. 25

Bioquímica de los ácidos nucleícos Bases nitrogenadas Numeración de átomos de las pirimidinas La Timina se encuentra Metilada mientras que el urcailo no. 26
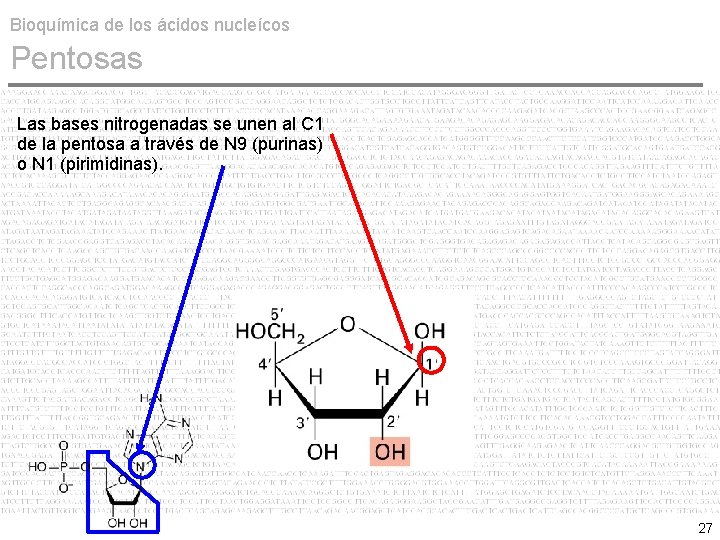
Bioquímica de los ácidos nucleícos Pentosas Las bases nitrogenadas se unen al C 1 de la pentosa a través de N 9 (purinas) o N 1 (pirimidinas). 27
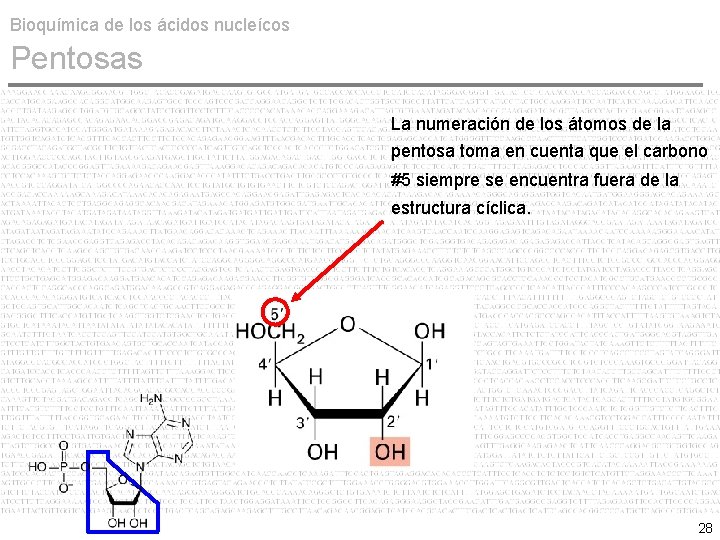
Bioquímica de los ácidos nucleícos Pentosas La numeración de los átomos de la pentosa toma en cuenta que el carbono #5 siempre se encuentra fuera de la estructura cíclica. 28
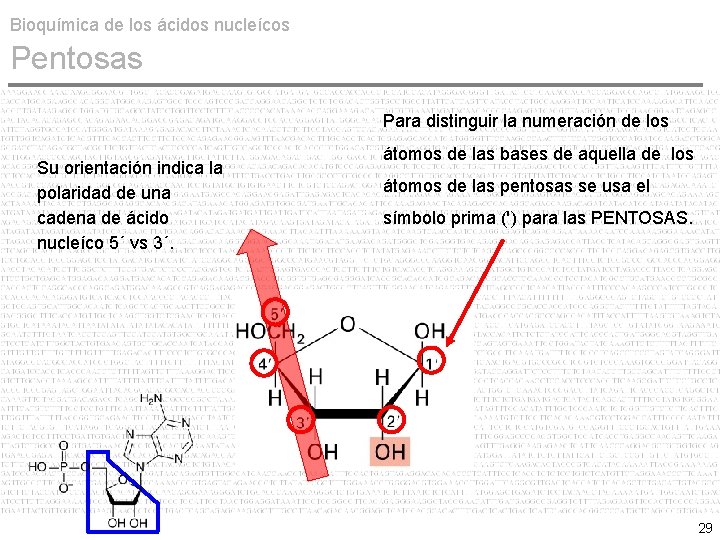
Bioquímica de los ácidos nucleícos Pentosas Para distinguir la numeración de los Su orientación indica la polaridad de una cadena de ácido nucleíco 5´ vs 3´. átomos de las bases de aquella de los átomos de las pentosas se usa el símbolo prima (') para las PENTOSAS. 29
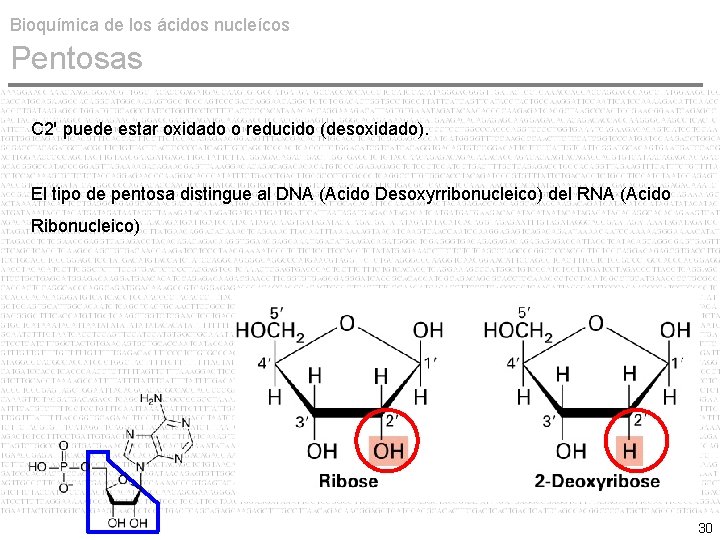
Bioquímica de los ácidos nucleícos Pentosas C 2' puede estar oxidado o reducido (desoxidado). El tipo de pentosa distingue al DNA (Acido Desoxyrribonucleico) del RNA (Acido Ribonucleico) 30
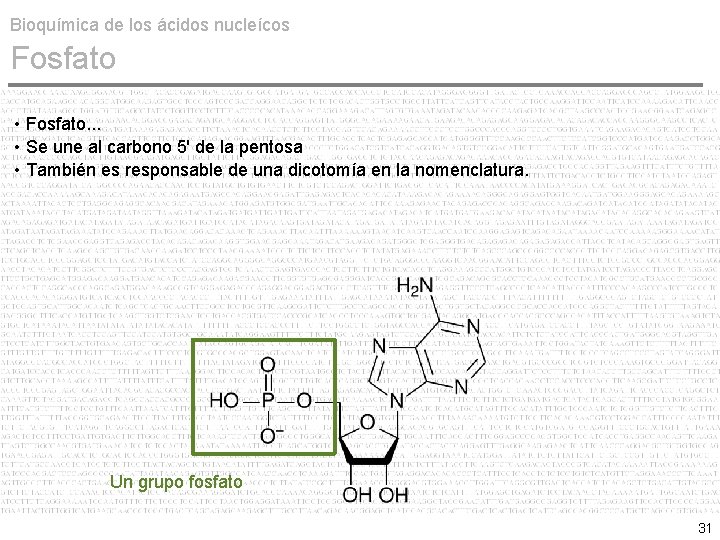
Bioquímica de los ácidos nucleícos Fosfato • Fosfato. . . • Se une al carbono 5' de la pentosa • También es responsable de una dicotomía en la nomenclatura. Un grupo fosfato 31
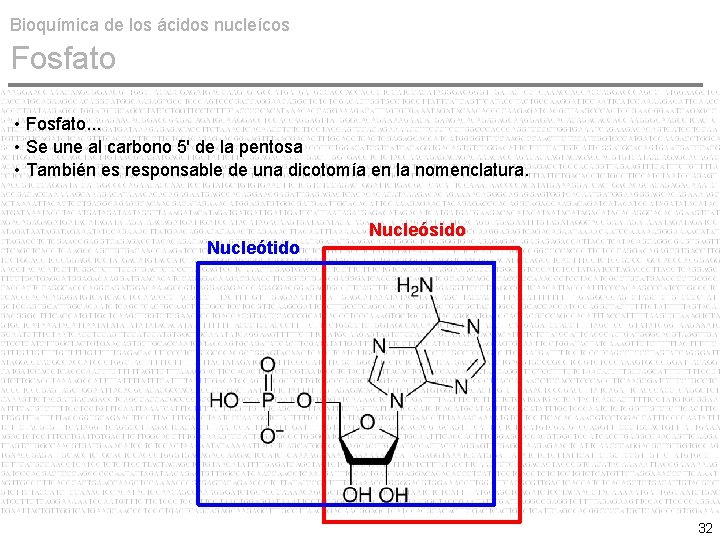
Bioquímica de los ácidos nucleícos Fosfato • Fosfato. . . • Se une al carbono 5' de la pentosa • También es responsable de una dicotomía en la nomenclatura. Nucleótido Nucleósido 32
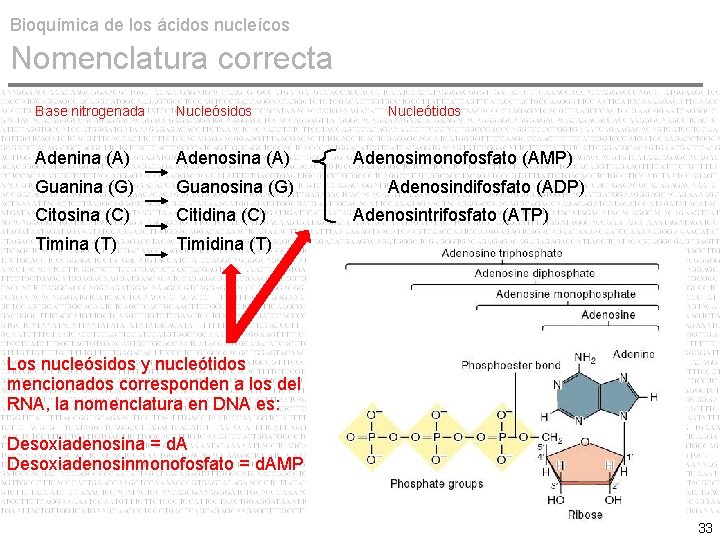
Bioquímica de los ácidos nucleícos Nomenclatura correcta Base nitrogenada Nucleósidos Adenina (A) Adenosina (A) Guanina (G) Guanosina (G) Citosina (C) Citidina (C) Timina (T) Timidina (T) Nucleótidos Adenosimonofosfato (AMP) Adenosindifosfato (ADP) Adenosintrifosfato (ATP) Los nucleósidos y nucleótidos mencionados corresponden a los del RNA, la nomenclatura en DNA es: Desoxiadenosina = d. A Desoxiadenosinmonofosfato = d. AMP 33
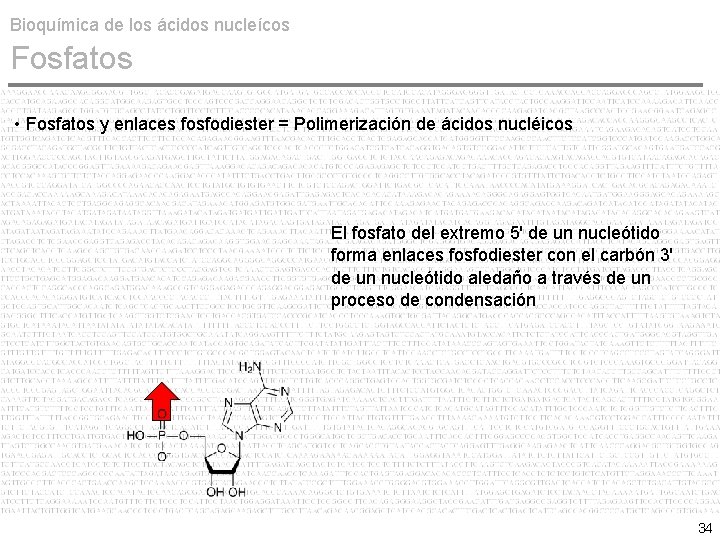
Bioquímica de los ácidos nucleícos Fosfatos • Fosfatos y enlaces fosfodiester = Polimerización de ácidos nucléicos El fosfato del extremo 5' de un nucleótido forma enlaces fosfodiester con el carbón 3' de un nucleótido aledaño a través de un proceso de condensación 34
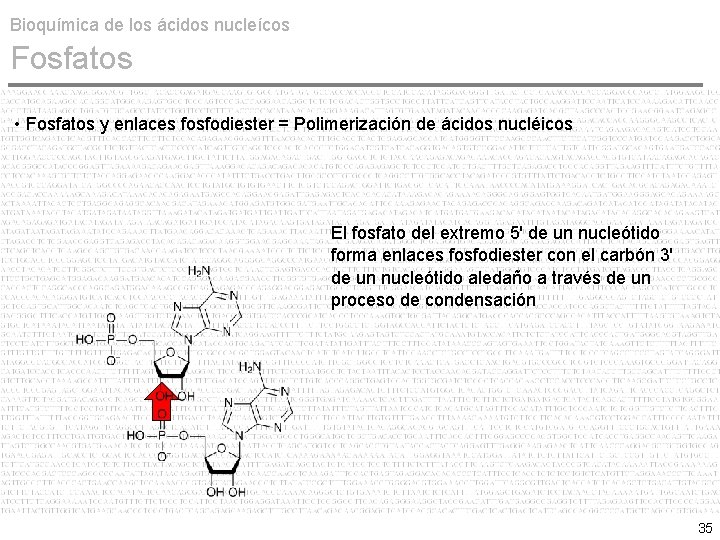
Bioquímica de los ácidos nucleícos Fosfatos • Fosfatos y enlaces fosfodiester = Polimerización de ácidos nucléicos El fosfato del extremo 5' de un nucleótido forma enlaces fosfodiester con el carbón 3' de un nucleótido aledaño a través de un proceso de condensación 35
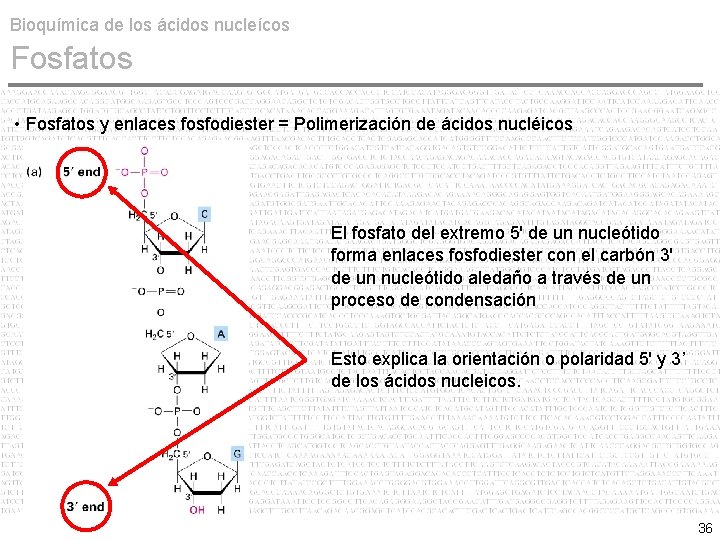
Bioquímica de los ácidos nucleícos Fosfatos • Fosfatos y enlaces fosfodiester = Polimerización de ácidos nucléicos El fosfato del extremo 5' de un nucleótido forma enlaces fosfodiester con el carbón 3' de un nucleótido aledaño a través de un proceso de condensación Esto explica la orientación o polaridad 5' y 3’ de los ácidos nucleicos. 36
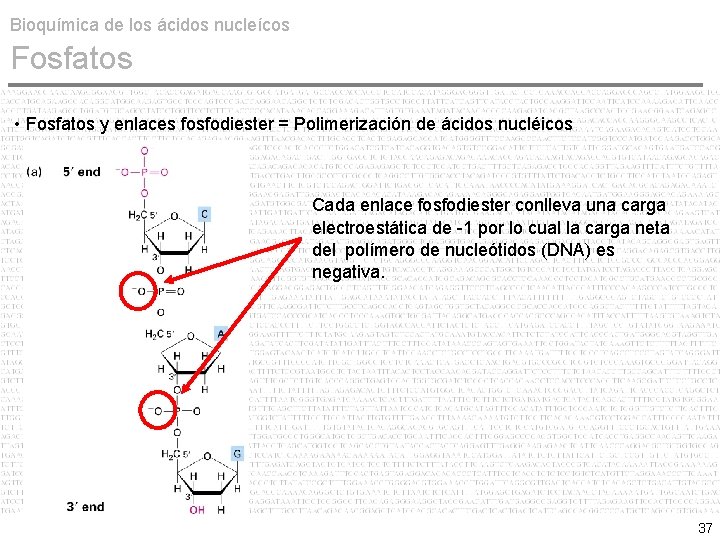
Bioquímica de los ácidos nucleícos Fosfatos • Fosfatos y enlaces fosfodiester = Polimerización de ácidos nucléicos Cada enlace fosfodiester conlleva una carga electroestática de -1 por lo cual la carga neta del polímero de nucleótidos (DNA) es negativa. 37
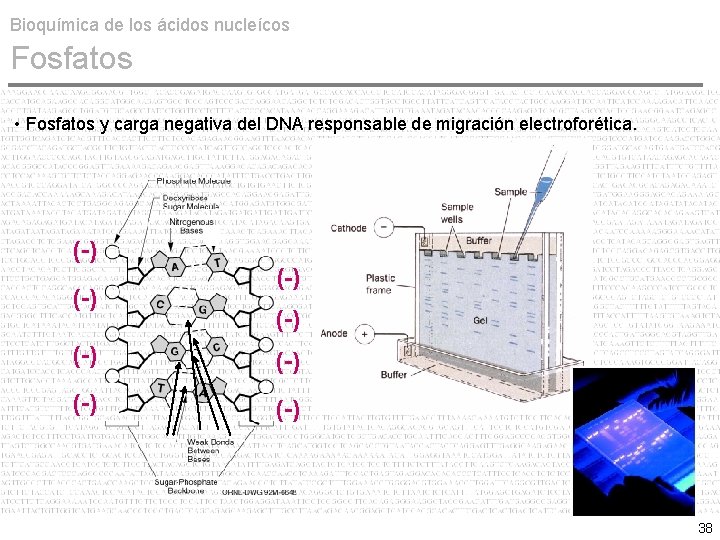
Bioquímica de los ácidos nucleícos Fosfatos • Fosfatos y carga negativa del DNA responsable de migración electroforética. (-) (-) 38
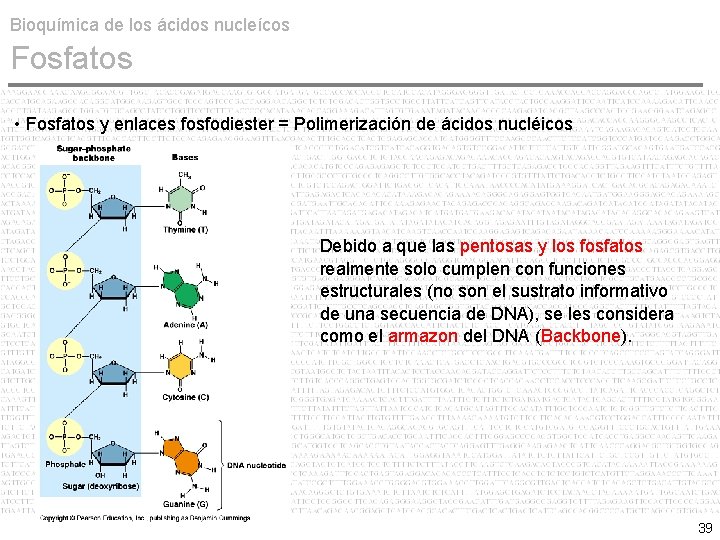
Bioquímica de los ácidos nucleícos Fosfatos • Fosfatos y enlaces fosfodiester = Polimerización de ácidos nucléicos Debido a que las pentosas y los fosfatos realmente solo cumplen con funciones estructurales (no son el sustrato informativo de una secuencia de DNA), se les considera como el armazon del DNA (Backbone). 39
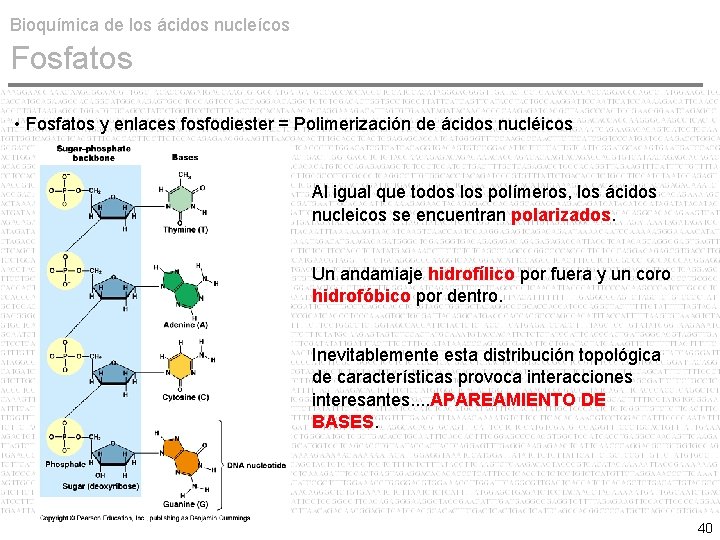
Bioquímica de los ácidos nucleícos Fosfatos • Fosfatos y enlaces fosfodiester = Polimerización de ácidos nucléicos Al igual que todos los polímeros, los ácidos nucleicos se encuentran polarizados. Un andamiaje hidrofílico por fuera y un coro hidrofóbico por dentro. Inevitablemente esta distribución topológica de características provoca interacciones interesantes. . APAREAMIENTO DE BASES. 40
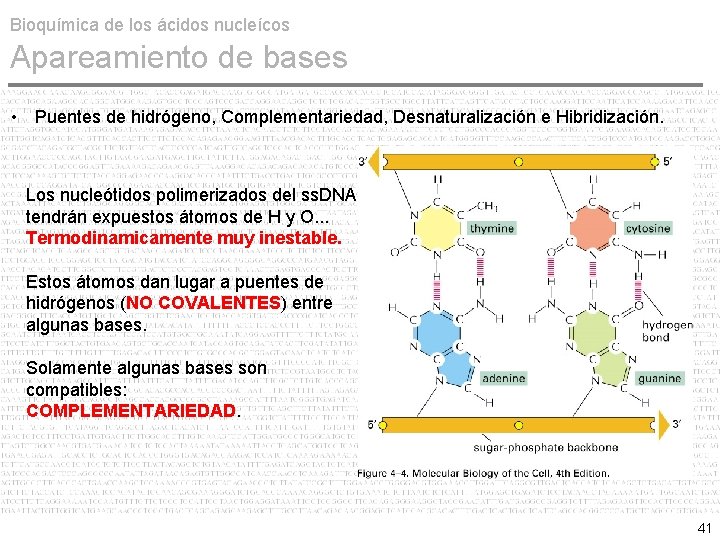
Bioquímica de los ácidos nucleícos Apareamiento de bases • Puentes de hidrógeno, Complementariedad, Desnaturalización e Hibridización. Los nucleótidos polimerizados del ss. DNA tendrán expuestos átomos de H y O. . . Termodinamicamente muy inestable. Estos átomos dan lugar a puentes de hidrógenos (NO COVALENTES) entre algunas bases. Solamente algunas bases son compatibles: COMPLEMENTARIEDAD. 41
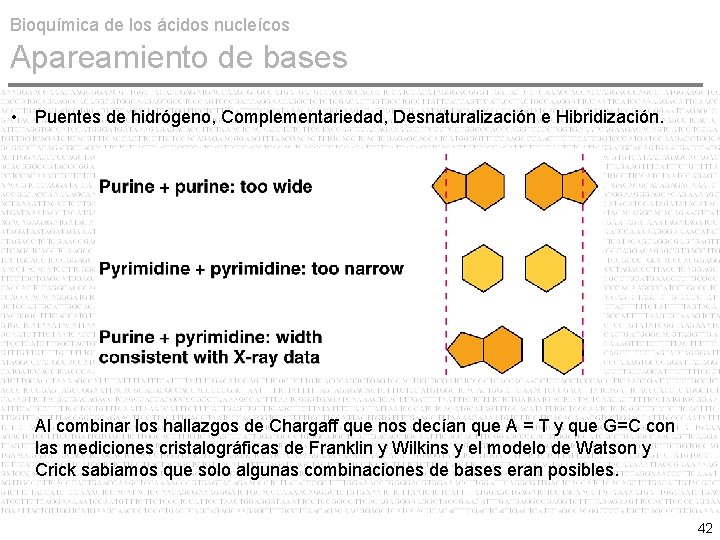
Bioquímica de los ácidos nucleícos Apareamiento de bases • Puentes de hidrógeno, Complementariedad, Desnaturalización e Hibridización. Al combinar los hallazgos de Chargaff que nos decían que A = T y que G=C con las mediciones cristalográficas de Franklin y Wilkins y el modelo de Watson y Crick sabiamos que solo algunas combinaciones de bases eran posibles. 42
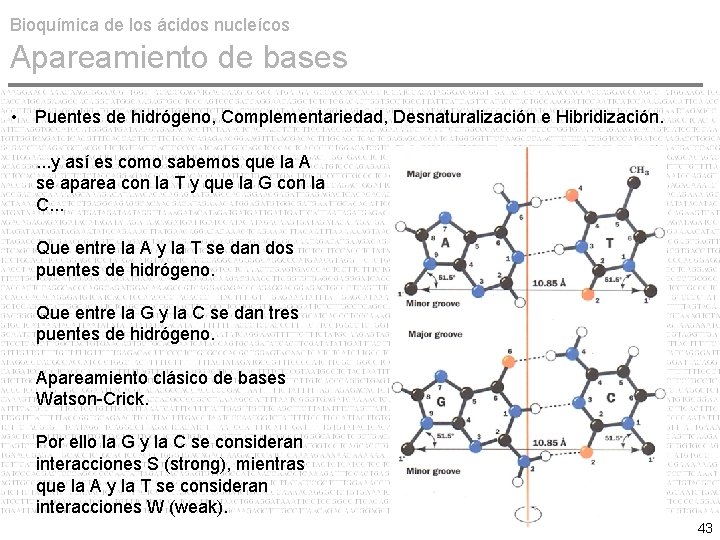
Bioquímica de los ácidos nucleícos Apareamiento de bases • Puentes de hidrógeno, Complementariedad, Desnaturalización e Hibridización. . y así es como sabemos que la A se aparea con la T y que la G con la C. . . Que entre la A y la T se dan dos puentes de hidrógeno. Que entre la G y la C se dan tres puentes de hidrógeno. Apareamiento clásico de bases Watson-Crick. Por ello la G y la C se consideran interacciones S (strong), mientras que la A y la T se consideran interacciones W (weak). 43
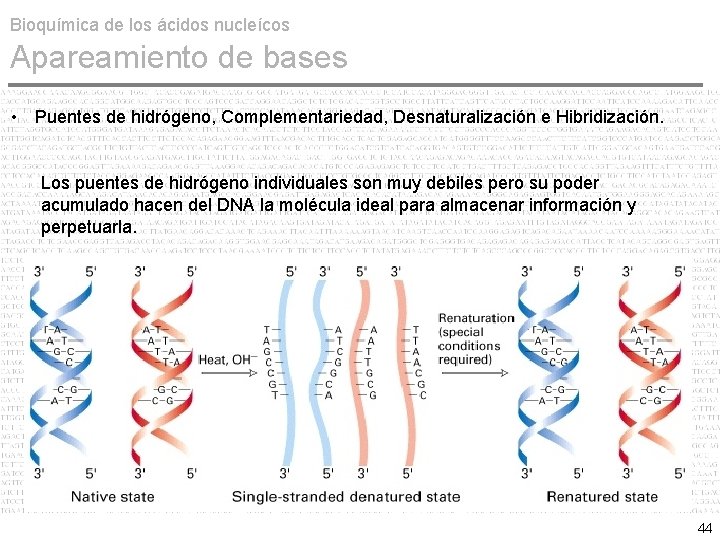
Bioquímica de los ácidos nucleícos Apareamiento de bases • Puentes de hidrógeno, Complementariedad, Desnaturalización e Hibridización. Los puentes de hidrógeno individuales son muy debiles pero su poder acumulado hacen del DNA la molécula ideal para almacenar información y perpetuarla. 44

Bioquímica de los ácidos nucleícos Enlaces no-covalentes: Puentes de hidrógeno • Breviario cultural Four Main Types of Noncovalent Interactions in Cells: Hydrogen Bond (H-Bonds): Specialized polar interaction where the positive hydrogen (H) atom is partially shared by two negative atoms. Hydrogen (H) is a proton that is partially dissociated from the donor atom so it can be shared with a second acceptor atom: H bonds: Properties and Characteristics: individual H-bonds are very weak ~ 1/20 th the strength of covalent bond multiple H-bonds together are strong highly directional; strongest when atoms are arranged in a straight-line. Water weakens H-bonds by forming competing H-bonds. 45

Bioquímica de los ácidos nucleícos Enlaces no-covalentes: Iónicos • Breviario cultural Four Main Types of Noncovalent Interactions in Cells: Ionic bonds: Electrostatic interactions between atoms of opposite charge (+) and (- ); Ionic bonds are formed by atoms that can fill outer shell by transferring electrons from another atom, instead of sharing electrons. Water molecules “cluster” to orient around fully charged ions and polar groups that contain permanent dipoles, this reduces the attraction between oppositely charged ions or polar groups: Water significantly decreases ionic interactions. 46

Bioquímica de los ácidos nucleícos Enlaces no-covalentes: Atracciones Vd. W • Breviario cultural Four Main Types of Noncovalent Interactions in Cells: (3) Van der Waals attractions: Fluctuation of the electron cloud around any nonpolar atom forms a transient dipole that induces an opposite transient dipole in a nearby atom, causing a very weak attraction between the atoms. Two macromolecules with complementary molecular surfaces can bind together very tightly as a result of multiple, weak noncovalent interactions, which together have a very large effect(s). (Van der Waals forces are not weakened by water). Fig 2 -16 Macromolecules bind together very tightly if they have matching complementary surfaces that interact through multiple noncovalent bonds. This is critical for biological interactions between proteins! In the figure, the plus (+) and minus (-) signs mark chemical groups that can attract each other if opposite charges are aligned in pairs (+) (- ) in close proximity. 47

Bioquímica de los ácidos nucleícos Enlaces no-covalentes: Attracción Hidrófoba • Breviario cultural Four Main Types of Noncovalent Interactions in Cells: (4) Hydrophobic forces: Water lattice: Water molecules join together transiently via Hbonds; even at 37 C (98 F) ~15% of water molecules are joined to four other water molecules in an H-bonded water network (lattice). This causes water molecules to have a cohesive property resulting in high surface tension, etc. Water forces hydrophobic groups together because clustering the hydrophobic groups reduces the disruptive effects on H-bonded water network (lattice). Repulsion from water results in attraction between hydrophobic groups called hydrophobic bonds. 48

Bioquímica de los ácidos nucleícos Enlaces covalentes: Fosfodiester Enlace covalente: se forma cuando dos átomos se aproximan lo suficiente como para compartir electrones. Single bond: one electron from each of the two atoms is shared Double bond: four electrons are shared Hydrogen bonds are NOT COVALENT Why is this biologically important? Fig 2 -8 Covalent bonds have a defined spatial arrangement of atoms. Fig 2 -9 Covalent double bonds restrict rotation around bonds between atoms. 49
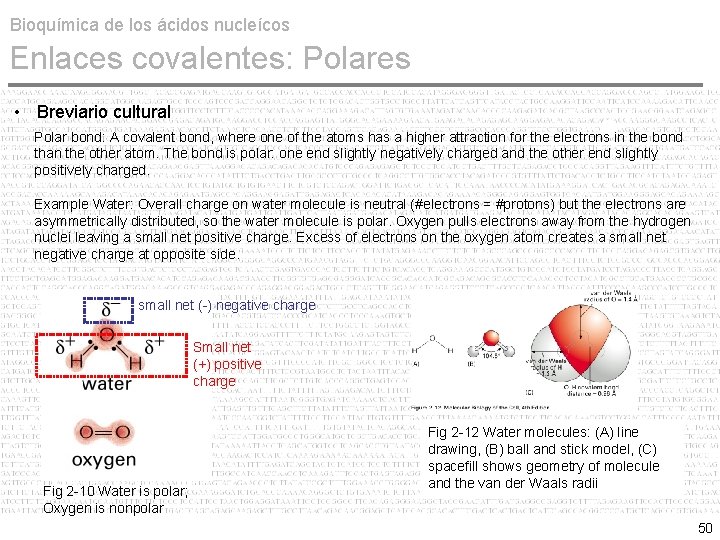
Bioquímica de los ácidos nucleícos Enlaces covalentes: Polares • Breviario cultural Polar bond: A covalent bond, where one of the atoms has a higher attraction for the electrons in the bond than the other atom. The bond is polar: one end slightly negatively charged and the other end slightly positively charged. Example Water: Overall charge on water molecule is neutral (#electrons = #protons) but the electrons are asymmetrically distributed, so the water molecule is polar. Oxygen pulls electrons away from the hydrogen nuclei leaving a small net positive charge. Excess of electrons on the oxygen atom creates a small net negative charge at opposite side. small net (-) negative charge Small net (+) positive charge Fig 2 -10 Water is polar; Oxygen is nonpolar Fig 2 -12 Water molecules: (A) line drawing, (B) ball and stick model, (C) spacefill shows geometry of molecule and the van der Waals radii 50
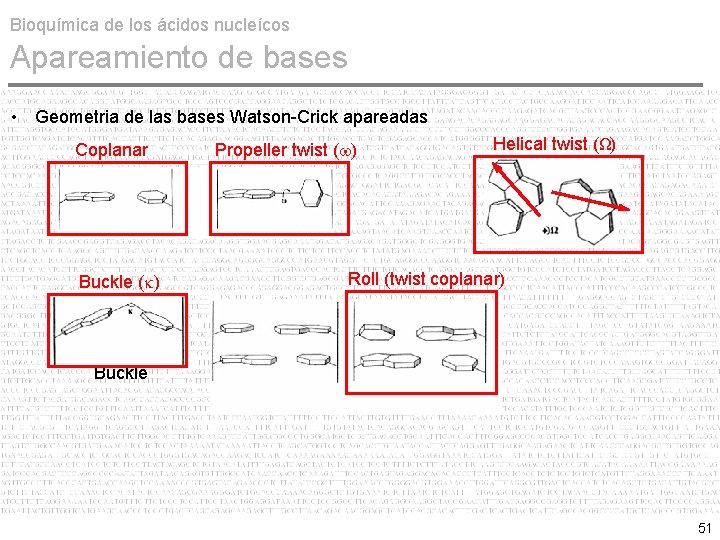
Bioquímica de los ácidos nucleícos Apareamiento de bases • Geometria de las bases Watson-Crick apareadas Coplanar Buckle (k) Propeller twist (w) Helical twist (Ω) Roll (twist coplanar) Buckle 51
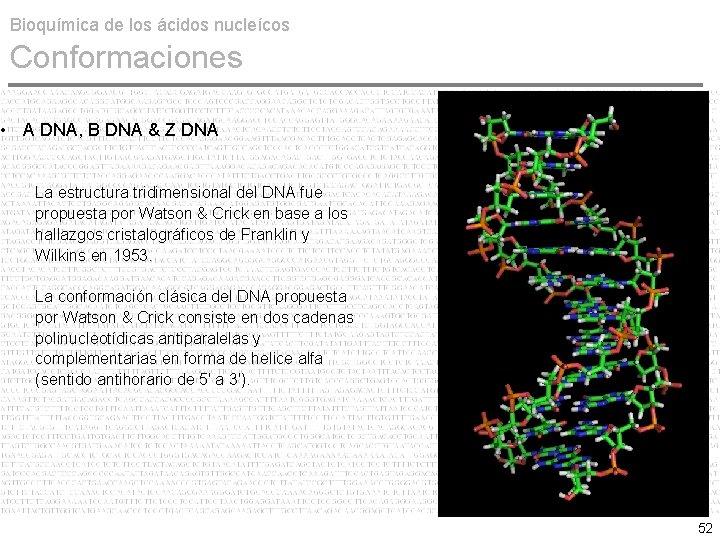
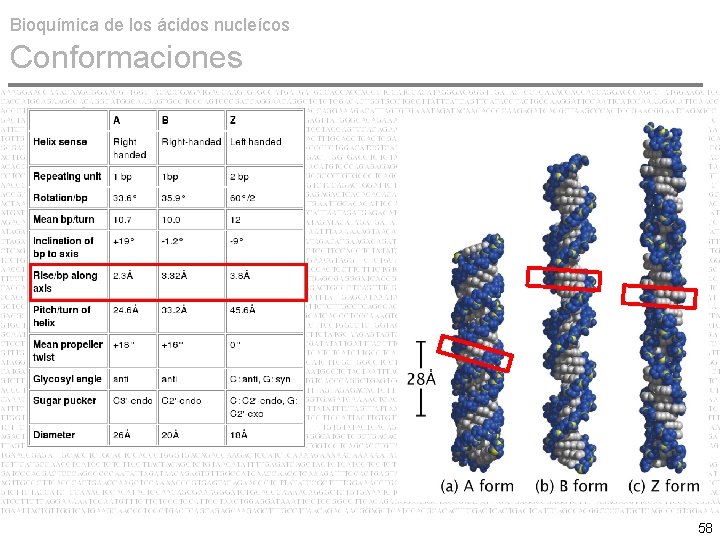
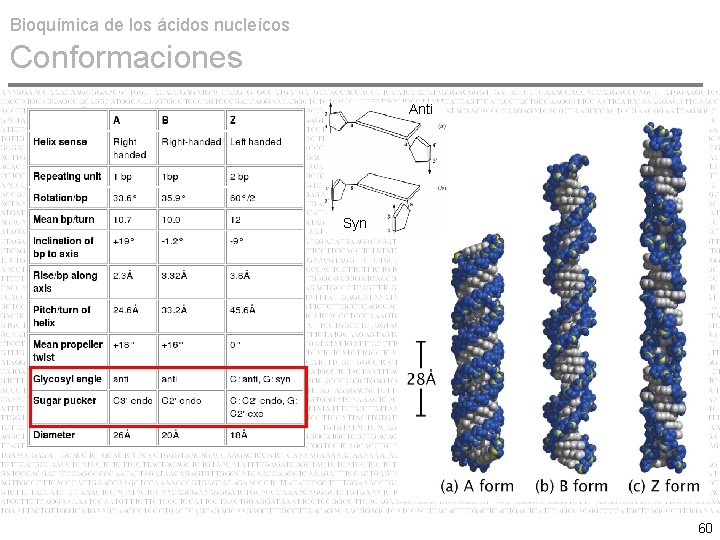
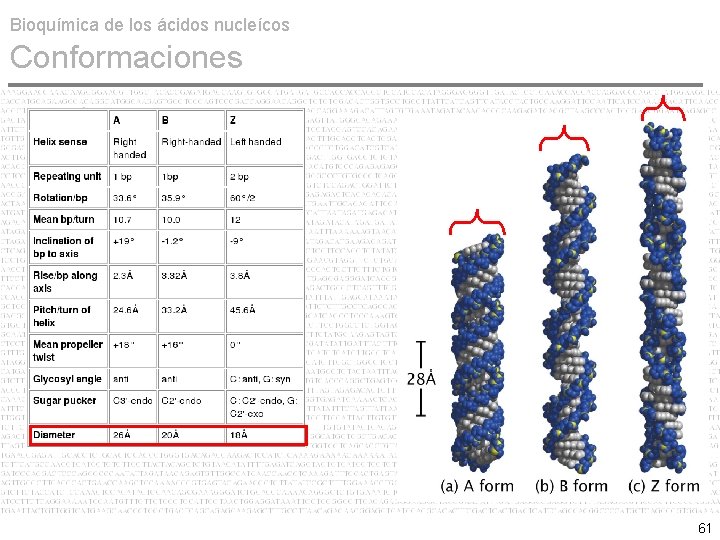
Bioquímica de los ácidos nucleícos Conformaciones • A DNA, B DNA & Z DNA La estructura tridimensional del DNA fue propuesta por Watson & Crick en base a los hallazgos cristalográficos de Franklin y Wilkins en 1953. La conformación clásica del DNA propuesta por Watson & Crick consiste en dos cadenas polinucleotídicas antiparalelas y complementarias en forma de helice alfa (sentido antihorario de 5' a 3'). 52
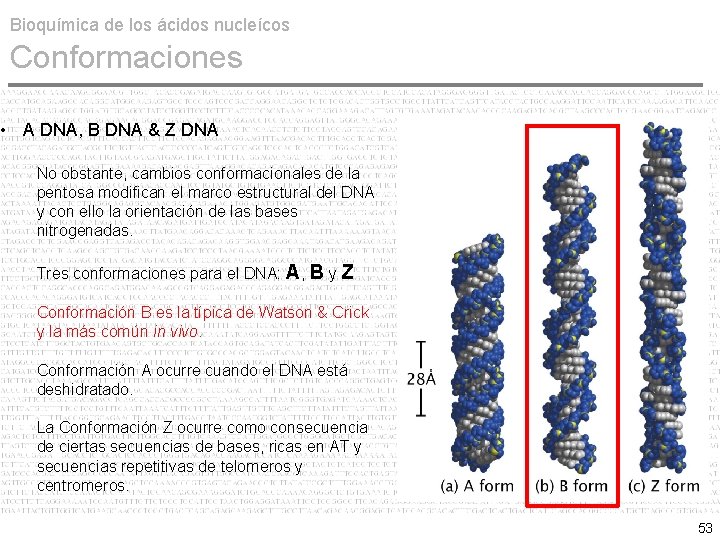
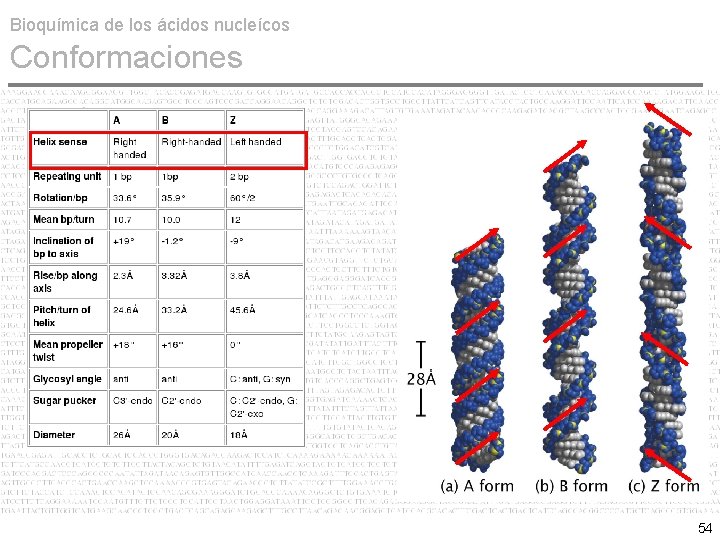
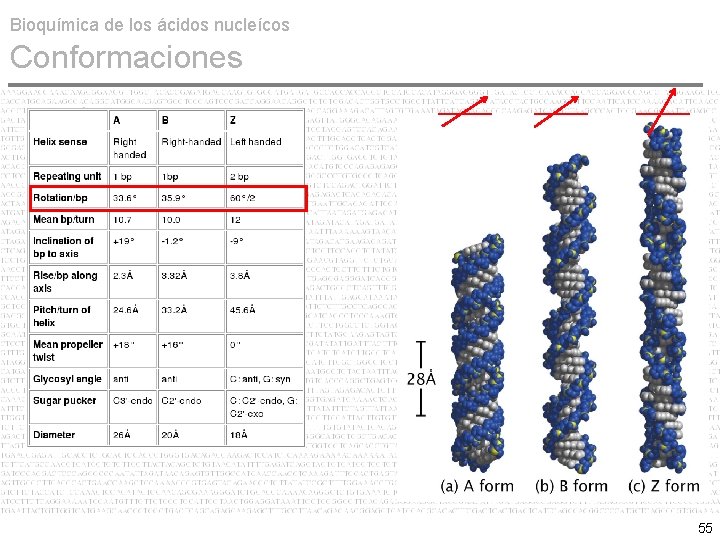
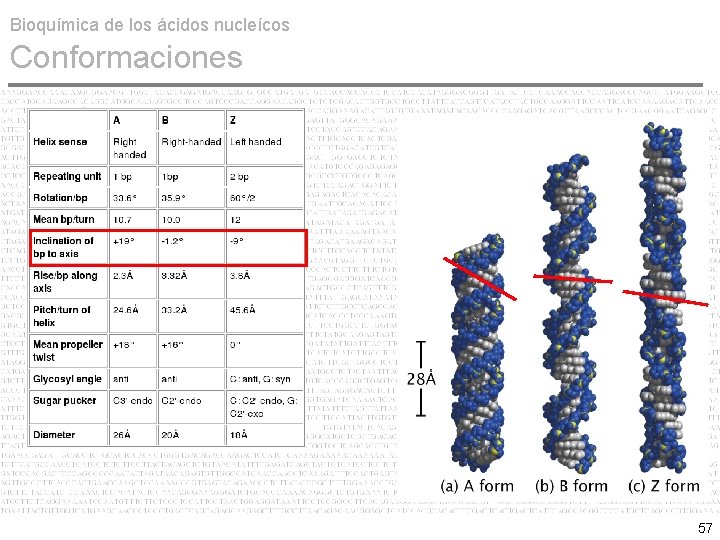
Bioquímica de los ácidos nucleícos Conformaciones • A DNA, B DNA & Z DNA No obstante, cambios conformacionales de la pentosa modifican el marco estructural del DNA y con ello la orientación de las bases nitrogenadas. Tres conformaciones para el DNA: A, B y Z Conformación B es la típica de Watson & Crick y la más común in vivo. Conformación A ocurre cuando el DNA está deshidratado. La Conformación Z ocurre como consecuencia de ciertas secuencias de bases, ricas en AT y secuencias repetitivas de telomeros y centromeros. 53
Bioquímica de los ácidos nucleícos Conformaciones 54
Bioquímica de los ácidos nucleícos Conformaciones 55

Bioquímica de los ácidos nucleícos Conformaciones 56
Bioquímica de los ácidos nucleícos Conformaciones 57
Bioquímica de los ácidos nucleícos Conformaciones 58

Bioquímica de los ácidos nucleícos Conformaciones Propeller twist (w) 59
Bioquímica de los ácidos nucleícos Conformaciones Anti Syn 60
Bioquímica de los ácidos nucleícos Conformaciones 61
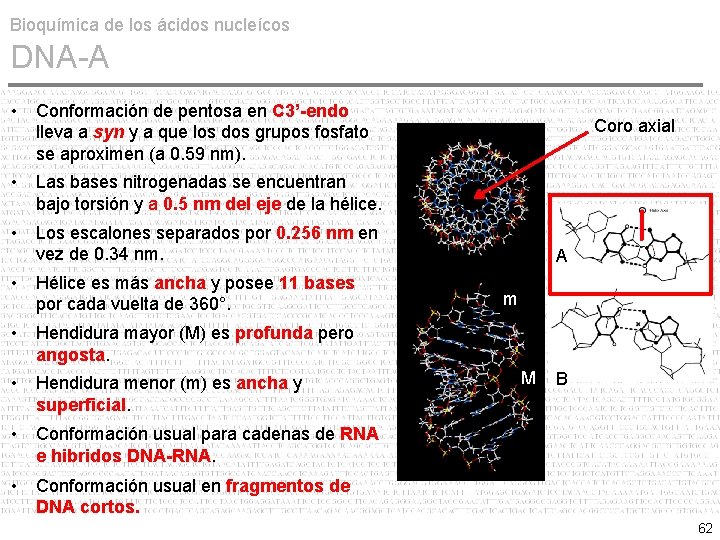
Bioquímica de los ácidos nucleícos DNA-A • Conformación de pentosa en C 3’-endo lleva a syn y a que los dos grupos fosfato se aproximen (a 0. 59 nm). Coro axial • Las bases nitrogenadas se encuentran bajo torsión y a 0. 5 nm del eje de la hélice. • Los escalones separados por 0. 256 nm en vez de 0. 34 nm. • Hélice es más ancha y posee 11 bases por cada vuelta de 360°. A m • Hendidura mayor (M) es profunda pero angosta. • Hendidura menor (m) es ancha y superficial. M B • Conformación usual para cadenas de RNA e hibridos DNA-RNA. • Conformación usual en fragmentos de DNA cortos. 62

Bioquímica de los ácidos nucleícos DNA-B • Estructura cristalográfica de Franklin & Wilkins. • Conformación de pentosa en C 2'-endo lleva a que las bases nitrogenadas se encuentren más relajadas y pucker en anti. • Grupos fosfato lejos uno del otro (0. 7 nm). • 10. 4 o 10. 5 bases por giro de 360°. • Rotación hacia la derecha en sentido 5’ - 3'. • Escalones de bases separados por 0. 34 nm. • Hendiduras M y m más accesibles a proteinas. • Bases no torsionadas y perpendiculares al eje molecular. • Permite libertad de flexión de 15° (muy util si uno quiere compactar el DNA). • Conformación fisiologica de DNA m M A B 63
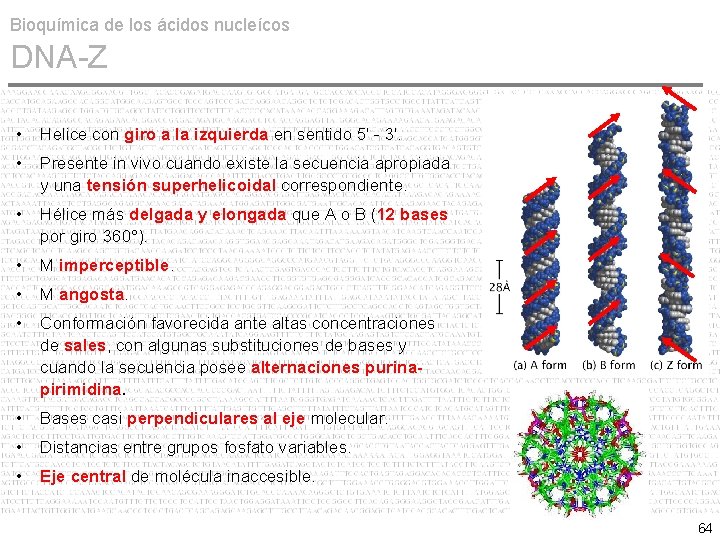
Bioquímica de los ácidos nucleícos DNA-Z • Helice con giro a la izquierda en sentido 5' - 3'. • Presente in vivo cuando existe la secuencia apropiada y una tensión superhelicoidal correspondiente. • Hélice más delgada y elongada que A o B (12 bases por giro 360°). • M imperceptible. • M angosta. • Conformación favorecida ante altas concentraciones de sales, con algunas substituciones de bases y cuando la secuencia posee alternaciones purinapirimidina. • Bases casi perpendiculares al eje molecular. • Distancias entre grupos fosfato variables. • Eje central de molécula inaccesible. 64
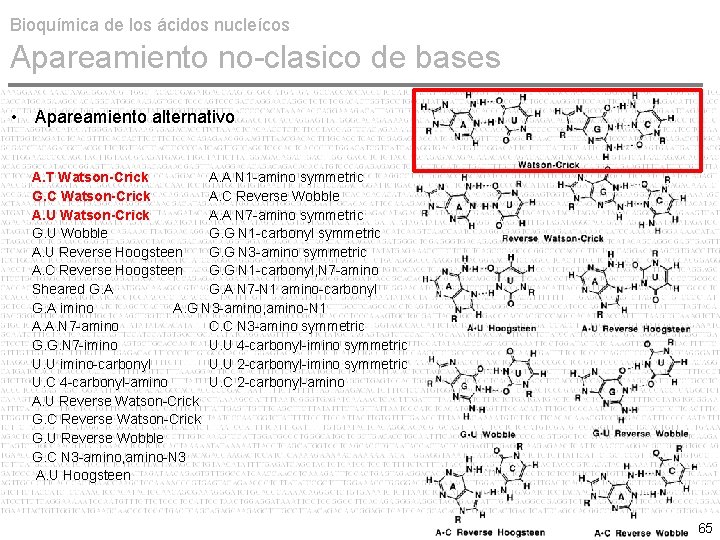
Bioquímica de los ácidos nucleícos Apareamiento no-clasico de bases • Apareamiento alternativo A. T Watson-Crick A. A N 1 -amino symmetric G. C Watson-Crick A. C Reverse Wobble A. U Watson-Crick A. A N 7 -amino symmetric G. U Wobble G. G N 1 -carbonyl symmetric A. U Reverse Hoogsteen G. G N 3 -amino symmetric A. C Reverse Hoogsteen G. G N 1 -carbonyl, N 7 -amino Sheared G. A N 7 -N 1 amino-carbonyl G. A imino A. G N 3 -amino, amino-N 1 A. A. N 7 -amino C. C N 3 -amino symmetric G. G. N 7 -imino U. U 4 -carbonyl-imino symmetric U. U imino-carbonyl U. U 2 -carbonyl-imino symmetric U. C 4 -carbonyl-amino U. C 2 -carbonyl-amino A. U Reverse Watson-Crick G. C Reverse Watson-Crick G. U Reverse Wobble G. C N 3 -amino, amino-N 3 A. U Hoogsteen 65
Bioquímica de los ácidos nucleícos Tetradas y Quadraplex • Otras conformaciones del DNA (Tetra/Quadruplex) • DNA del 5 to Elemento. 66
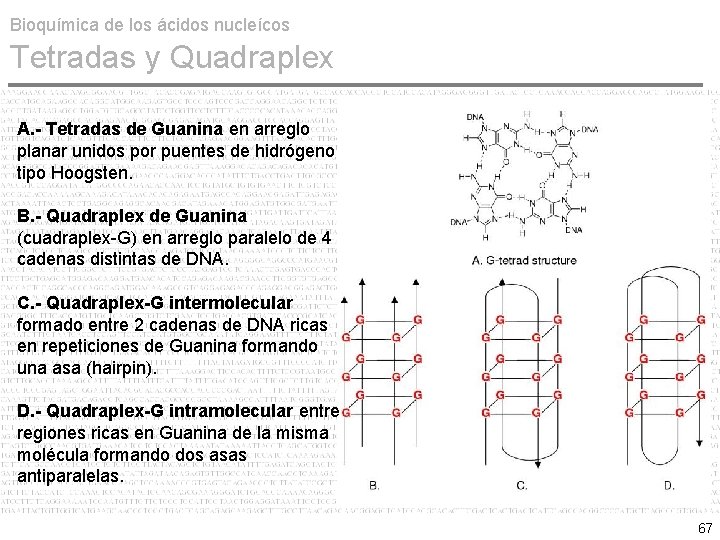
Bioquímica de los ácidos nucleícos Tetradas y Quadraplex A. - Tetradas de Guanina en arreglo planar unidos por puentes de hidrógeno tipo Hoogsten. B. - Quadraplex de Guanina (cuadraplex-G) en arreglo paralelo de 4 cadenas distintas de DNA. C. - Quadraplex-G intermolecular formado entre 2 cadenas de DNA ricas en repeticiones de Guanina formando una asa (hairpin). D. - Quadraplex-G intramolecular entre regiones ricas en Guanina de la misma molécula formando dos asas antiparalelas. 67
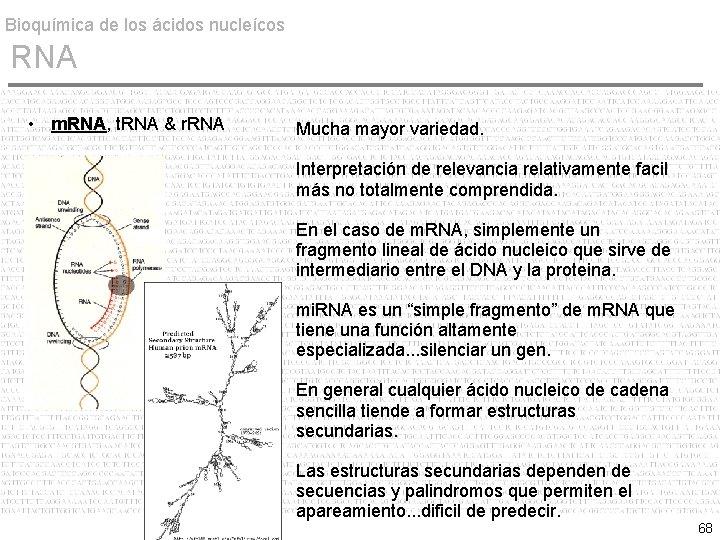
Bioquímica de los ácidos nucleícos RNA • m. RNA, t. RNA & r. RNA Mucha mayor variedad. Interpretación de relevancia relativamente facil más no totalmente comprendida. En el caso de m. RNA, simplemente un fragmento lineal de ácido nucleico que sirve de intermediario entre el DNA y la proteina. mi. RNA es un “simple fragmento” de m. RNA que tiene una función altamente especializada. . . silenciar un gen. En general cualquier ácido nucleico de cadena sencilla tiende a formar estructuras secundarias. Las estructuras secundarias dependen de secuencias y palindromos que permiten el apareamiento. . . dificil de predecir. 68
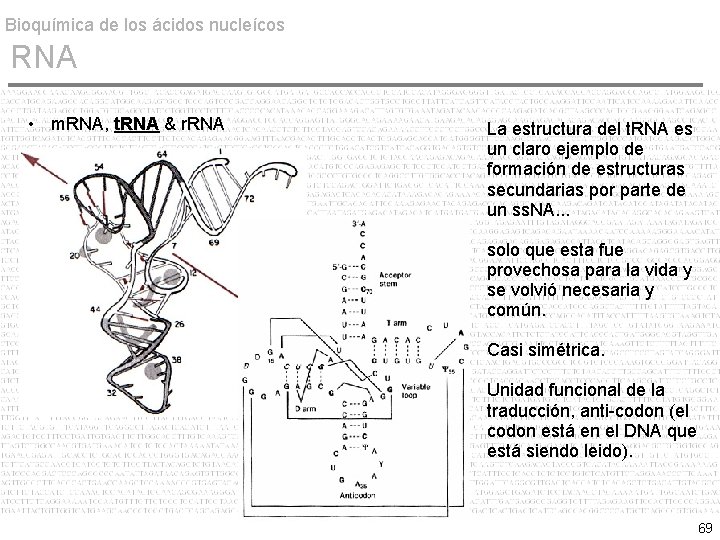
Bioquímica de los ácidos nucleícos RNA • m. RNA, t. RNA & r. RNA La estructura del t. RNA es un claro ejemplo de formación de estructuras secundarias por parte de un ss. NA. . . solo que esta fue provechosa para la vida y se volvió necesaria y común. Casi simétrica. Unidad funcional de la traducción, anti-codon (el codon está en el DNA que está siendo leido). 69
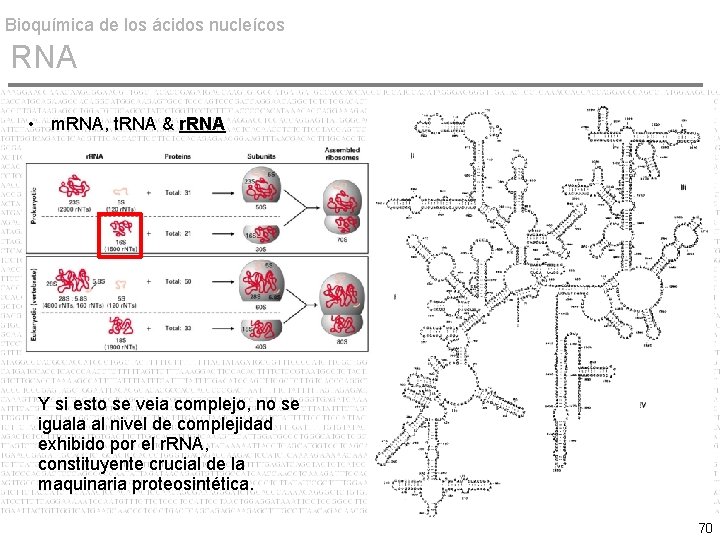
Bioquímica de los ácidos nucleícos RNA • m. RNA, t. RNA & r. RNA Y si esto se veia complejo, no se iguala al nivel de complejidad exhibido por el r. RNA, constituyente crucial de la maquinaria proteosintética. 70
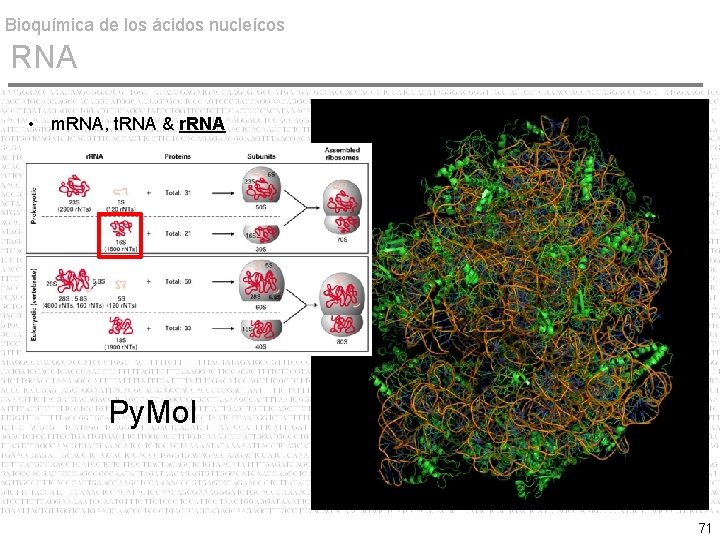
Bioquímica de los ácidos nucleícos RNA • m. RNA, t. RNA & r. RNA Py. Mol 71
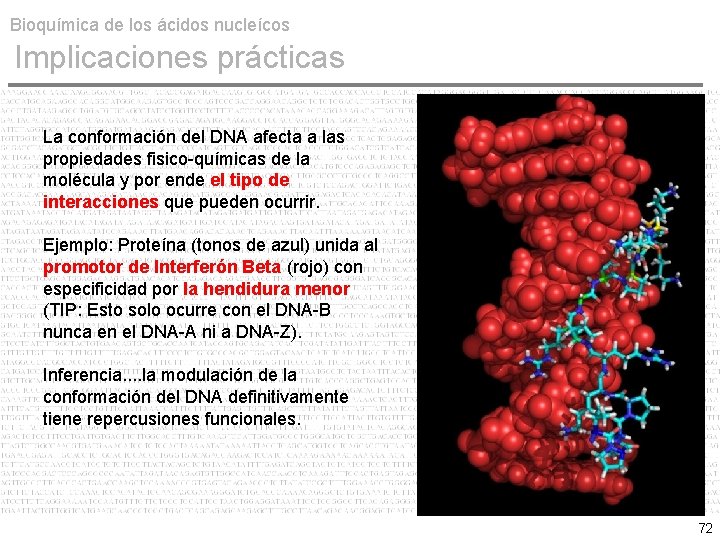
Bioquímica de los ácidos nucleícos Implicaciones prácticas La conformación del DNA afecta a las propiedades fisico-químicas de la molécula y por ende el tipo de interacciones que pueden ocurrir. Ejemplo: Proteína (tonos de azul) unida al promotor de Interferón Beta (rojo) con especificidad por la hendidura menor (TIP: Esto solo ocurre con el DNA-B nunca en el DNA-A ni a DNA-Z). Inferencia. . la modulación de la conformación del DNA definitivamente tiene repercusiones funcionales. 72
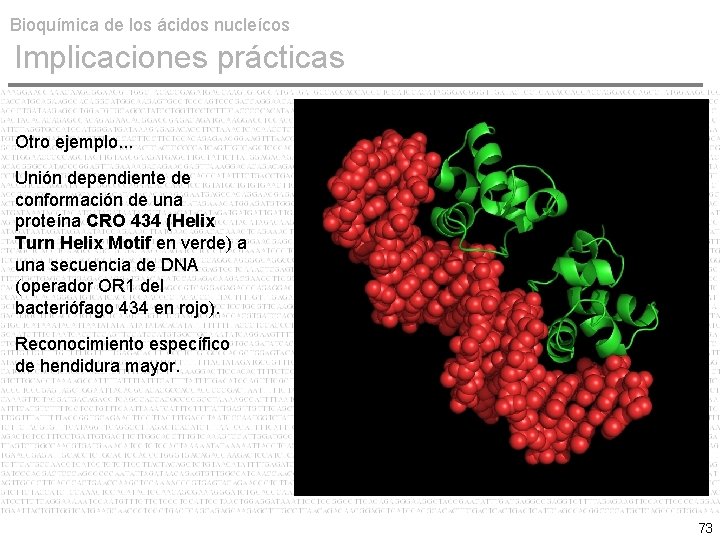
Bioquímica de los ácidos nucleícos Implicaciones prácticas Otro ejemplo. . . Unión dependiente de conformación de una proteína CRO 434 (Helix Turn Helix Motif en verde) a una secuencia de DNA (operador OR 1 del bacteriófago 434 en rojo). Reconocimiento específico de hendidura mayor. 73
Bioquímica de los ácidos nucleícos Resúmen • Resúmen Ir a Py. Mol 74
- Slides: 74