BIOQUIMICA ENZIMAS ENZIMOLOGA CLNICA 2012 Tema 7 Lic

BIOQUIMICA ENZIMAS ENZIMOLOGÍA CLÍNICA 2012 Tema: 7 Lic. Mariana Ferramola Dra. Silvia Varas bioquimica. enfermeria. unsl@gmail. com

Propiedades Generales de las Enzimas: n n n n Presentan un sitio activo Eficiencia catalítica (mayor velocidad de reacción) Condiciones de reacción (tº, p. H y presión) compatible con la vida Especificidad Grupos prostéticos Regulación de su actividad Localización celular
![Sitio Activo E + S ES] E + P Sitio Activo E + S ES] E + P](http://slidetodoc.com/presentation_image/497635403dd8b18c9eebe62456ec0adf/image-3.jpg)
Sitio Activo E + S ES] E + P
![S E E [E-S] P E S E E [E-S] P E](http://slidetodoc.com/presentation_image/497635403dd8b18c9eebe62456ec0adf/image-4.jpg)
S E E [E-S] P E

Propiedades Generales de las Enzimas: n n n n Presentan un sitio activo Eficiencia catalítica (mayor velocidad de reacción) Condiciones de reacción (tº, p. H y presión) compatible con la vida Especificidad Grupos prostéticos Regulación de su actividad Localización celular

Propiedades Generales de las Enzimas: n n n n Presentan un sitio activo Eficiencia catalítica (mayor velocidad de reacción) Condiciones de reacción (tº, p. H y presión) compatible con la vida Especificidad Grupos prostéticos Regulación de su actividad Localización celular

Grupos Prosteticos: Cofactores y Coenzimas Apoenzima (inactiva) + Grupo Prostético n Holoenzima (activa) Grupo prostético: cofactores (ión metálico) o coenzima unido covalentemente a la enzima. Son de características no proteicas
![S E E [E-S] P E S E E [E-S] P E](http://slidetodoc.com/presentation_image/497635403dd8b18c9eebe62456ec0adf/image-8.jpg)
S E E [E-S] P E
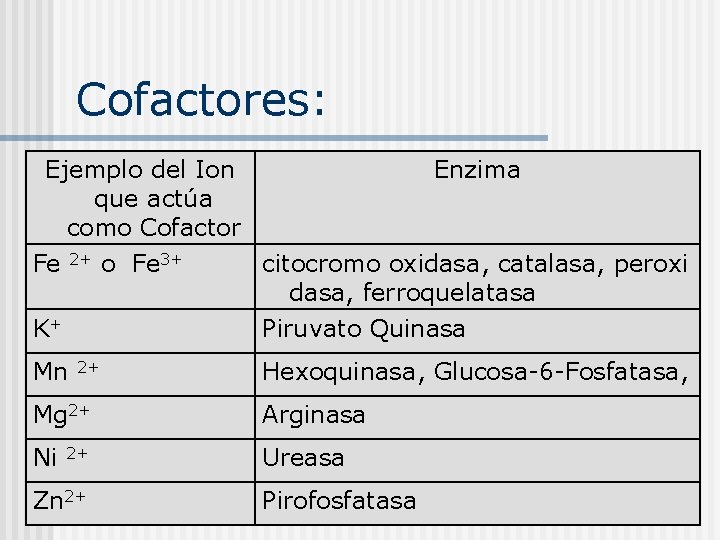
Cofactores: Ejemplo del Ion que actúa como Cofactor Fe 2+ o Fe 3+ Enzima K+ citocromo oxidasa, catalasa, peroxi dasa, ferroquelatasa Piruvato Quinasa Mn 2+ Hexoquinasa, Glucosa-6 -Fosfatasa, Mg 2+ Arginasa Ni 2+ Ureasa Zn 2+ Pirofosfatasa
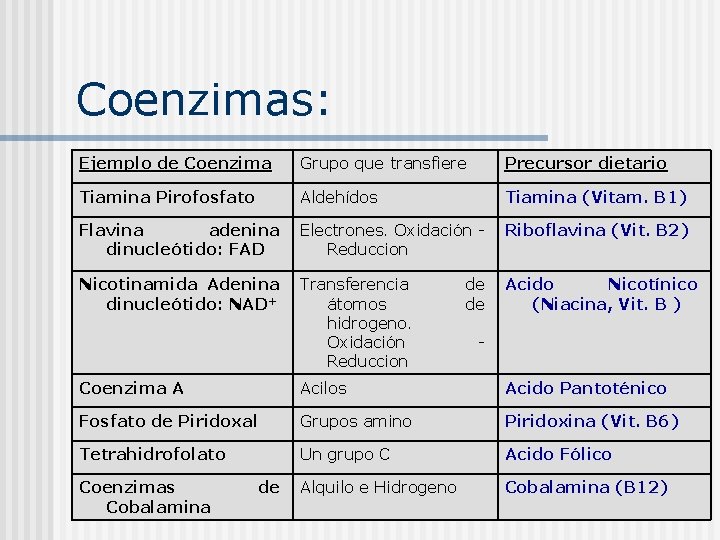
Coenzimas: Ejemplo de Coenzima Grupo que transfiere Precursor dietario Tiamina Pirofosfato Aldehídos Tiamina (Vitam. B 1) Flavina adenina Electrones. Oxidación - Riboflavina (Vit. B 2) dinucleótido: FAD Reduccion Nicotinamida Adenina Transferencia dinucleótido: NAD+ átomos hidrogeno. Oxidación Reduccion de Acido Nicotínico de (Niacina, Vit. B ) - Coenzima A Acilos Acido Pantoténico Fosfato de Piridoxal Grupos amino Piridoxina (Vit. B 6) Tetrahidrofolato Un grupo C Acido Fólico Coenzimas Cobalamina de Alquilo e Hidrogeno Cobalamina (B 12)

Propiedades Generales de las Enzimas: n n n n Presentan un sitio activo Eficiencia catalítica (mayor velocidad de reacción) Condiciones de reacción (tº, p. H y presión) compatible con la vida Especificidad Grupos prostéticos Regulación de su actividad Localización celular

Propiedades Generales de las Enzimas: n n n n Presentan un sitio activo Eficiencia catalítica (mayor velocidad de reacción) Condiciones de reacción (tº, p. H y presión) compatible con la vida Especificidad Grupos prostéticos Regulación de su actividad Localización celular
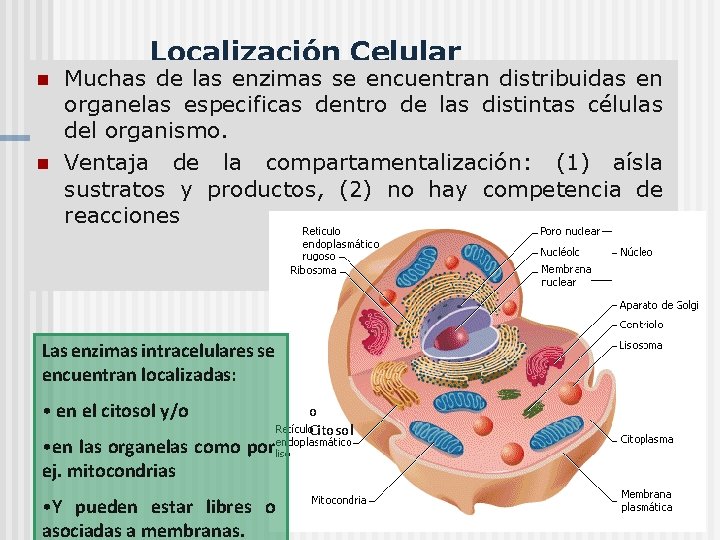
Localización Celular n n Muchas de las enzimas se encuentran distribuidas en organelas especificas dentro de las distintas células del organismo. Ventaja de la compartamentalización: (1) aísla sustratos y productos, (2) no hay competencia de reacciones Las enzimas intracelulares se encuentran localizadas: • en el citosol y/o • en las organelas como por ej. mitocondrias • Y pueden estar libres o asociadas a membranas. o Citosol

Enzimas intracelulares más frecuentemente analizadas n n n Citosólicas: LDH (láctico deshidrogenasa) y ALAT (alanina amino transferasa). Mitocondriales: GIDH (glutamato deshidrogenasa). Mitocondriales y citosólicas: ASAT (aspartato amino transferasa) y MDH (malato deshidrogenasa).

ISOENZIMAS n Las isoenzimas son proteínas que difieren en la secuencia de aminoácidos pero que catalizan la misma reacción, estando presentes en la misma especie. n Estas enzimas pueden poseer diferentes: Propiedades físicas y químicas determinadas genéticamente (punto isoeléctrico, especificidad de sustrato y cofactor, etc), Mostrar diferentes parámetros cinéticos (por ej. diferentes valores de Km), o Propiedades de regulación diferentes. n n n

Nomenclatura de las enzimas n Las enzimas se denominan por el agregado del sufijo –asa al nombre del sustrato o a la reacción que cataliza

Ejemplos: n n n n deshidrogenasas oxidasas. aminotransferasas o transaminasas. fosfatasa peptidasas fosfoglucomutasa racemasas o epimerasas ligasas o sintetasas

ENZIMAS DE IMPORTANCIA CLÍNICA n Las enzimas son empleadas en los laboratorios clínicos y en las investigaciones biomédicas como reactivos biológicos para la determinación de analitos, y la medición de sus niveles de actividad en el suero u otras muestras biológicas constituyen herramientas eficaces en el diagnóstico y pronóstico de una enfermedad

Las enzimas para ser herramientas eficaces en el diagnóstico y pronóstico de Distribución tisular de las enzimas: El conocimiento de la una enfermedad se debe tener distribución tisular de las enzimas es necesario para en cuenta: establecer una correlación clínica ante el aumento de una determinada enzima en plasma. Localización Intracelular: El conocimiento de ello permite entender el tipo y grado de daño que ha sufrido una célula. Tiempo de vida media de la enzima estudiada: El conocimiento de este parámetro nos permite interpretar los tiempos de desaparición de las actividades enzimáticas aumentadas.
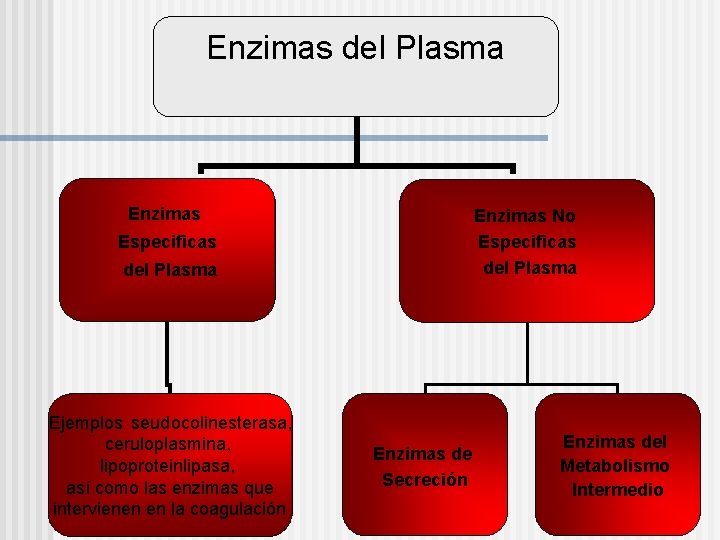
Enzimas del Plasma Enzimas No Especificas del Plasma Ejemplos: seudocolinesterasa, ceruloplasmina, lipoproteinlipasa, así como las enzimas que intervienen en la coagulación Enzimas de Secreción Enzimas del Metabolismo Intermedio

Enzimas del plasma específicas n n Son componentes funcionales de la sangre. Están por lo común allí y en un nivel de actividad superior al de los tejidos, siendo mantenido su nivel constante por secreción activa de uno o más órganos. A este grupo pertenecen la seudocolinesterasa, ceruloplasmina, lipoproteinlipasa, así como las enzimas que intervienen en la coagulación sanguínea. La actividad de estas enzimas tiene interés clínico en le evaluación tanto de la función propia de la enzima en el estudio como de la función del tejido que la sintetiza.

Las enzimas del plasma no específicas n No desempeñan función biológica en el plasma; no son, por tanto, constituyentes funcionales plasmáticos y sólo se aprecia una muy pequeña actividad en condiciones normales, debido a la renovación celular natural o pequeños traumatismos espontáneos n Su presencia en plasma en niveles más altos de lo normal sugiere un aumento en la velocidad de destrucción o recambio celular y tisular. La determinación de estos niveles de enzimas plasmáticas puede proveer información valiosa para diagnóstico y pronóstico n

Las enzimas del plasma no específicas: (1) Enzimas de Secreción n Ejercen su actividad fuera de las células que las originaron, por ejemplo se producen en glándulas exócrinas, como páncreas (enzimas o fermentos digestivos) y próstata, así como en tejidos como mucosa gástrica y hueso. n En condiciones fisiológicas: durante el embarazo o en en niños en crecimiento donde hay aumento de actividad de FAL por osteoblastos. n En adenocarcinoma y osteosarcoma se observa un aumento importante de la actividad plasmática de las fosfatasas ácida y alcalina.

Las enzimas del plasma no específicas: (2) Enzimas del Metabolismo Intermedio n Son las que se ubican en los distintos componentes celulares y cuya salida se produce cuando una causa determinada altera la estructura de la célula. n La concentración en los tejidos de estas enzimas es miles de veces más alta que en el plasma. n Un daño puede conducir a un aumento en la permeabilidad de la membrana plasmática con su consecuente liberación a la circulación general.

Ejemplos: n aspartato amino transferasa (AST) o glutámicooxalacético transaminasa (GOT), n alanina amino transferasa (ALT) o glutámico pirúvico transaminasa (GPT), n lactato deshidrogenasa (LDH), n creatín quinasa (CK), n -amilasa, n γ-glutamiltranspeptidasa (γ-GT), n 5´nucleotidasa y aldolasa (ALS).

ENZIMAS CELULARES DEL METABOLISMO INTERMEDIO: MECANISMOS DE LIBERACIÓN AL PLASMA SANGUINEO Hipoxia Presencia de microorganismos (bacterias, parásitos y virus) Agentes químicos, físicos y farmacológicos. Mecanismos inmunitarios. Trastornos nutricionales.
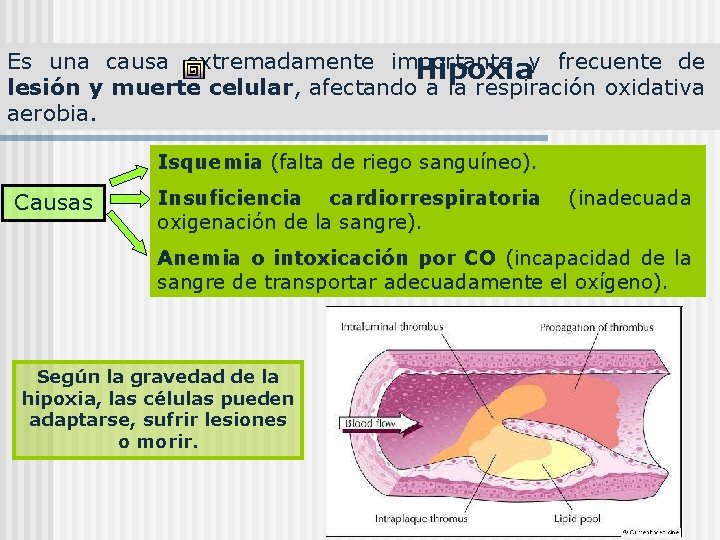
Es una causa extremadamente importante y frecuente de Hipoxia lesión y muerte celular, afectando a la respiración oxidativa aerobia. Isquemia (falta de riego sanguíneo). Causas Insuficiencia cardiorrespiratoria oxigenación de la sangre). (inadecuada Anemia o intoxicación por CO (incapacidad de la sangre de transportar adecuadamente el oxígeno). Según la gravedad de la hipoxia, las células pueden adaptarse, sufrir lesiones o morir.

Agentes microbiológicos, químicos, físicos y farmacológicos Infección por microorganismos tales como bacterias, virus, hongos, así como también con parásitos. Hay ataque directo de ellos sobre las membranas celulares promoverá también la salida de enzimas intracelulares a la circulación sanguínea. La contaminación ambiental es fuente de agentes químicos que dañan las células, tal como los metales pesados, etc. Otra fuente importante de agentes químicos es el alcohol y el tabaco. En el alcoholismo se observa la inducción enzimática de γGT (Gama Glutamil Transferasa), con aumento de sus niveles séricos. Los fármacos pueden producir: liberación de enzimas desde membranas (imipramina), inducción o represión de la síntesis enzimática y modificaciones del flujo biliar (fenobarbital).
Trastornos Nutricionales Mecanismos Inmunitarios Anafilaxis (reacción alérgica grave). Los mecanismos que pueden generar daño tisular son: Formación de complejos inmunes en exceso (puede ocurrir por la presencia de gran cantidad de antígeno en el organismo). Citotoxicidad (el sistema inmune es capaz de eliminar células infectadas). En deficiencias vitamínicas y/o minerales. También se observa en la malnutrición proteico-calórica. Un ejemplo es la deficiencia de hierro, que al producir anemia genera hipoxia, dañando consecuentemente los tejidos.

FACTORES QUE DETERMINAN LA CONCENTRACION Y ACTIVIDAD ENZIMATICA EN PLASMA: n Depende de la localización intracelular de las enzimas n Depende de las características del órgano o tejido dañado n Depende del proceso de clarificación de las enzimas que llegan al torrente circulatorio

FACTORES QUE DETERMINAN LA CONCENTRACION Y ACTIVIDAD ENZIMATICA EN SUERO n Depende de la localización intracelular de las enzimas: Enzimas citosolicas daño de membrana Enzimas mitocondriales mayor año y necrosis celular n Depende de las características del órgano o tejido dañado Hígado órgano muy vascularizado, con capilares muy permeables, pasa rápido a suero Músculo esquelético capilares menos permeables, pasa a linfa

FACTORES QUE DETERMINAN LA CONCENTRACION Y ACTIVIDAD ENZIMATICA EN SUERO n Depende del proceso de clarificación de las enzimas que llegan al torrente circulatorio a- Eliminación renal: se cumple para aquellas de bajo peso molecular. Ej: amilasa y algunas fosfatasas b- Inactivación sérica: existen inactivadores o inhibidores para varias enzimas: Ej: tripsina, quimiotripsina. Luego son eliminadas rápidamente, con la participación del sistema retículo endotelial en un proceso de endocitosis mediado por macrófagos. c- Para algunas enzimas existe recaptación por parte de los tejidos convalecientes, al restablecerse anatómica y fisiológicamente. Esta pequeñísima parte de las enzimas previamente liberadas sería utilizada, no para su función primitiva, sino como integrante de un “pool” (reservorio) de aminoácidos.
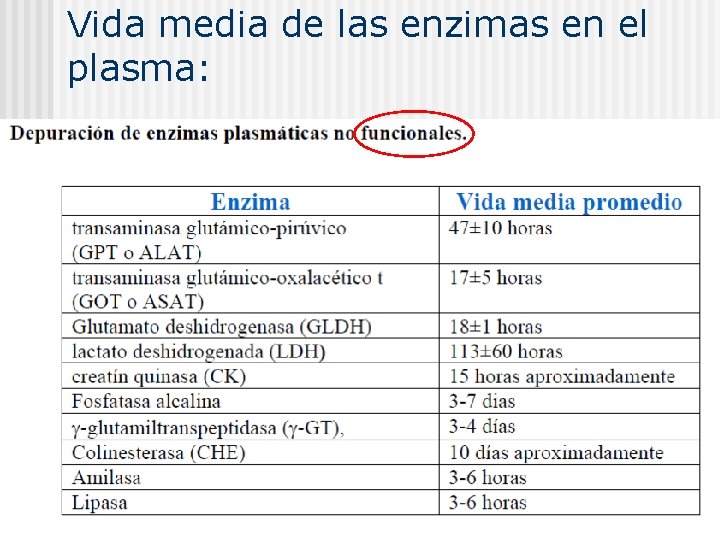
Vida media de las enzimas en el plasma:

ENZIMAS FRECUENTEMENTE ANALIZADAS: n n n n Transaminasas hepáticas (ALT o GPT y AST o GOT) alfa−Amilasa Creatín fosfoquinasa (CPK) Fosfatasa ácida (Ac. P) Fosfatasa alcalina (ALP) Gama glutamil transpeptidasa (GGT) Láctico deshidrogenasa (LDH) 5’-nucleotidasa (NTP)

ENZIMOLOGÍA DE LAS ENFERMEDADES DEL CORAZÓN, HÍGADO Y PÁNCREAS Corazón: IAM n Hígado: Infección VHA n Páncreas: Pancreatitis Aguda n 1°, la biliar, por obstrucción del colédoco por cálculos biliares. Y la 2° se debe principalmente al abuso del consumo del alcohol.
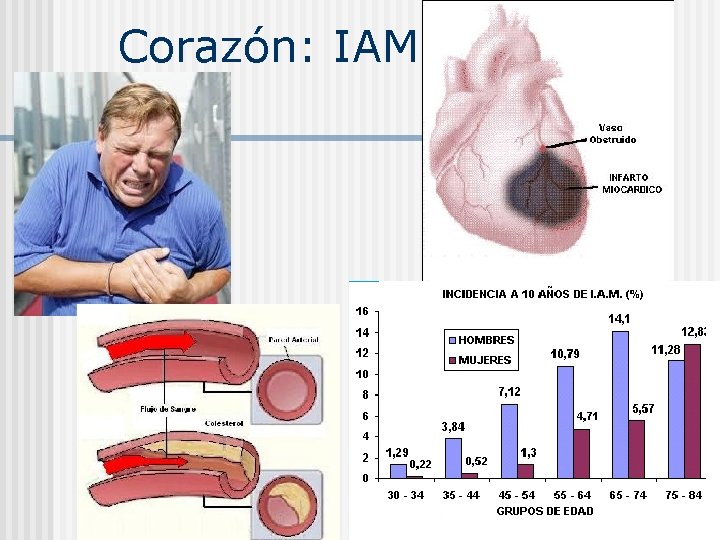
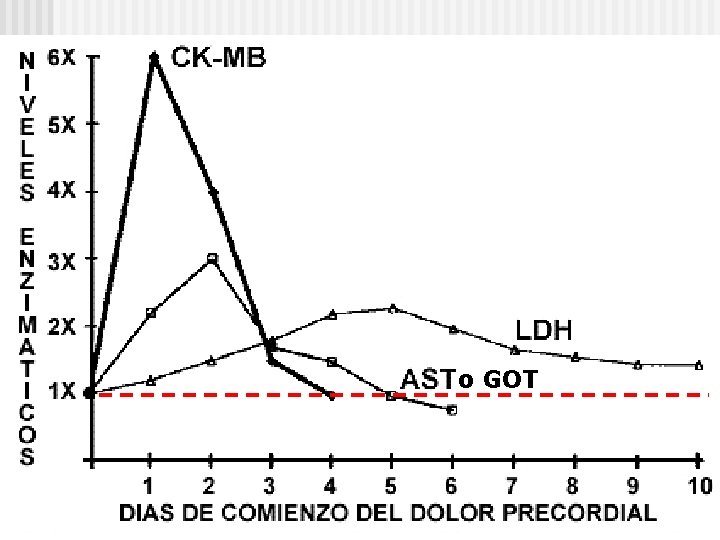
Corazón: IAM
o GOT
Lactato deshidrogenasa (LDH) LDH es una enzima tetramérica, formada por la combinación de dos tipos de cadenas diferentes: H y M. La combinación de ellas da lugar a 5 isoenzimas diferentes. Las isoenzimas LDH 1 y LDH 2 están presentes en miocardio. Condiciones normales: Niveles bajos de LDH en plasma. Concentraciones plasmáticas de LDH 1 < LDH 2. Infarto de miocardio: Primeramente, la concentración plasmática de LDH 1 aumenta, llegando incluso a superar la de LDH 2 (es decir se invierte la relación). Posteriormente, los valores de LDH total aumentan por encima de su valor normal en plasma. Retornan a la normalidad luego de 814 días.

Creatina Fosfoquinasa (CK) La CK es un diméro, formada por monómeros que pueden ser de dos tipos: M y B. La CK presenta 3 isoenzimas: CK-MM, de localización muscular. CK-MB, de localización cardíaca. CK-BB, de localización cerebral. En un infarto de miocardio, la actividad de CK aumenta en plasma, debido a un incremento de la concentración de CK-MB en el mismo. El incremento comienza entre las 6 -8 hs post-infarto, y los niveles se normalizan luego de 3 -4 días.

Aspartato-amino transferasa(GOT) En un infarto agudo de miocardio (IAM), los valores elevados de GOT pueden persistir hasta 5 días y puede ser útil cuando no se conoce el tiempo de instalación de los síntomas o cuando el paciente fue ingresado tardíamente. Los aumentos de GOT son de 4 -5 veces los valores normales. Si los aumentos son de 10 -15 veces, se asocian con IAM de peor pronóstico.

Hígado: Infección VHA El hígado contiene una gran cantidad de enzimas, las de mayor interés clínico son : § Transaminasas (GOT y GPT) § § Fosfatasa alcalina (FAL) Gamaglutamiltransferasa (γGT) La elevación de las enzimas hepáticas en plasma puede reflejar daño hepático o alteración del flujo biliar.
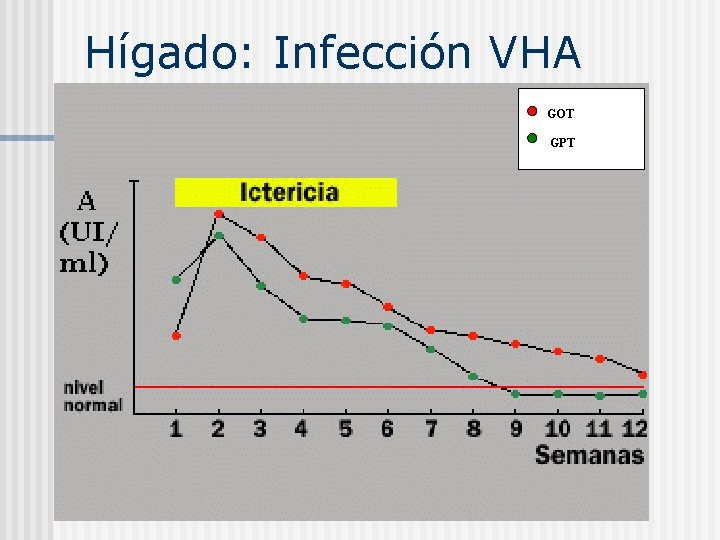
Hígado: Infección VHA GOT GPT

Enzimas plasmáticas usadas como marcadores de inflamación: Transaminasas (GOT y GPT) Las transaminasas son enzimas que participan en el metabolismo de los aminoácidos. Estas enzimas no son específicas del hígado, encontrándose también en músculo, corazón, páncreas y cerebro. Todas aquellas enfermedades hepáticas que cursan con necrosis celular dan lugar a hipertransaminemia. Lesiones agudas Lesiones crónicas ↑↑↑ Transaminemia (500 -1000 UI/ml) ↑ Transaminemia
Enzimas plasmáticas usadas como marcadores de colestasis: FAL y GGT La FAL sérica tiene varios orígenes, aunque las fuentes más importantes son: hígado, huesos e intestino ↑ FAL de origen hepático Es típico de obstrucción biliar intra o extrahepática, entre otros procesos. La colestasis aumenta la síntesis y liberación de FAL. Su vida media en la circulación es de aproximadamente una semana. Gamaglutamiltransferasa (γGT) Participa del metabolismo de las proteínas. No es específica del hígado, siendo el riñón el órgano más rico en esta enzima. ↑↑↑ γGT Se observan en procesos obstructivos o neoplásicos
Pancreatitis Aguda

Enzimas relacionadas con daño pancreático: -Amilasa n Lipasa Tripsinógeno n n No existe una relación directa entre la duración y la magnitud de los aumentos de actividad enzimática en plasma con la gravedad y el pronóstico de la pancreatitis.

- Amilasa Además del páncreas, esta enzima puede aumentar en plasma por procesos inflamatorios originados en otros órganos. Determinación de la fracción P 3 de la amilasa, isoenzima de origen exclusivamente pancreático. El aumento de esta enzima se ha observado en forma casi constante en las pancreatitis agudas. La amilasa también puede aparecer en orina. Su determinación contribuye al diagnóstico y seguimiento de la evolución de una pancreatitis.
Lipasa Es la segunda determinación más frecuente para el diagnóstico de la pancreatitis aguda. Es más específica que la amilasa. Un aumento de lipasa plasmática solo puede deberse a afecciones del páncreas.

Enzimuria Se define como enzimuria la presencia de enzimas en orina. Las enzimas presentes en orina pueden tener diferentes orígenes. Pueden ser usados como marcadores de: Destrucción celular renal. n Rechazo a transplante renal. Marcadores de evolución de enfermedad renal. n n

Mañana: n GRAN CONSULTA 2° PARCIAL!
- Slides: 50