Biophysique des solutions Gnralits sur les solutions Diffusion

Biophysique des solutions Généralités sur les solutions Diffusion en phase liquide Propriétés générales des solutions micromoléculaires Les solutions macromoléculaires et les colloïdes

Ch 2 GENERALITES SUR LES SOLUTIONS

SOLUTION BINAIRE n. Une solution binaire est un mélange homogène en phase condensée ( liquide ou solide) de deux corps différents.

SOLUTION BINAIRE § Une seule phase : Solvant (Grande proportion) + Soluté

TITRE m = masse du soluté m 0 = masse du solvant

CONCENTRATION PONDERALE m = masse du soluté V = volume de la solution V dépend de la température

CONCENTRATION MOLAIRE OU MOLARITE

EXEMPLE 1 Solution de glucose (M = 180 g) à 18 g/l Molarité ? m = 18 / 180 = 0. 1 : Solution DECIMOLAIRE Solution MOLAIRE = M =1 mole / l = N molécules/l

MOLALITE Solution aqueuse et diluée : Molalité = Molarité

UNITES MOLARITE MOLE = M = 1 (mole /l ) MILLIMOLE = m. M = 10 -3 (mole /l ) MICROMOLE= M = 10 -6 (mole /l ) NANOMOLE =n. M = 10 -9 (mole /l )

REMARQUES n. Concentrations pondérales non additives n Molarités additives

FRACTION MOLAIRE n 1 = nombre de moles de soluté n 0 = nombre de moles du solvant

EXEMPLE 2 Solution aqueuse de glucose à 36 g/l n 1 = 36 / 180=0, 2 ; n 0=(1000 -36)/18= 53, 55 FSOLUTE=0, 2/ (0, 2+53, 55)=0, 0037 FSOLVANT =53, 55/(0, 2+53, 55)=0, 9962 F soluté + Fsolvant = 1

QCM 1 On mélange 1 dl d’une solution aqueuse de Na. Cl à 58 g. l-1 avec 0. 9 l d’eau. Quelle est la concentration pondérale de la solution résultante ? A. 58 g. l-1 B. 5, 8 g. l-1 C. 580 g. l-1 D. 5, 8 kg. m-3 E. 58 kg. m-3

Réponses QCM 1 A. 58 -1 g. l 5, 8 -1 C. 580 g. l -3 D. 5, 8 kg. m -3 E. 58 kg. m B. -1 g. l

QCM 2 Quelle est la concentration molaire résultant du mélange de la question précédente? A. 580 g. m-3 B. 100 mol. m-3 C. 5, 8 g. l-1 D. 0, 1 mol. l-1 E. 5, 8 mol. l-1

Réponses QCM 2 A. B. C. D. E. -3 g. m 580 100 mol. m-3 5, 8 g. l-1 0, 1 mol. l-1 5, 8 mol. l-1

QCM 3 Une solution d’albumine à 70 g/l a une masse volumique de 1, 03 g/ml. Le plasma peut être assimilé à une solution d’albumine. [Na+]plasma= 142 mmol/l A. Un litre de plasma contient 55, 56 moles d’eau B. Un litre de plasma contient 53, 33 moles d’eau C. Cela correspond à un volume d’eau pure de 960 ml D. La masse de sodium par litre de plasma est de 3, 27 g E. La molalité en sodium est de 142 mmol/kg d’eau

QCM 3 1 litre de plasma = 1030 g Masse d’eau/litre plasma =1030 – 70 =960 g Nombre de moles d’eau / litre de plasma = 960 / 18 = 53, 33 Eau : 1 kg/litre = 1 g /ml Donc 960 g d’eau = 960 ml Masse Na+ /litre plasma = 142 10 -3 23 = 3, 266 g Molalité Na+ = 142 mmol / 0, 96 = 147, 96 mmol/kg d’eau

Réponses QCM 3 A. Un litre de plasma contient 55, 56 moles d’eau B. Un litre de plasma contient 53, 33 moles d’eau C. Cela correspond à un volume d’eau pure de 960 ml D. La masse de sodium par litre de plasma est de 3, 27 g E. La molalité en sodium est de 142 mmol/kg d’eau

Le Faraday Si une molécule gramme donne après dissociation un anion et un cation ( Na+, Cl- par exemple) ----> 6, 02. 1023 x 1, 6. 10 -19 = 96 500 coulombs à l’anode et à la cathode 1 Eq = 96500 coulombs = 1 Faraday ( F)

Concentration équivalente n. Molécules avec ions monovalents : Concentration équivalente = Concentration molaire n. Molécules avec ions bivalents : Concentration équivalente = Concentration molaire x 2 n. Molécule non ionisée : Ceq = 0

NOTION D’EQUIVALENT Solutions ioniques ou électrolytiques CONDUCTRICES D’ELECTRICITE ( Cation = + , Anion = -) 1 ion gramme de Na+ = 1 Equivalent 1 ion gramme de Ca++, = 2 Equivalents 1 ion gramme de Al+++ = 3 Equivalents

Exemple 3 Soit 14, 2 g de cristaux de Na 2 SO 4 ( M =142 g ) dissous dans 500 ml d’eau Na 2 SO 4 --- 2 Na + + SO 4 2Ø Ø Ø n(Na 2 SO 4 ) = 14, 2 / 142 = 0, 1 mole Molarité de la solution : m = 0, 1/0, 5 =0, 2 mole/l [Na+] = 2 x 0, 2 = 0, 4 mole/l, Valence z+=1 [SO 4 2 -] = 1 x 0, 2 = 0, 2 mole/l, z-=-2 Ceq ( Na+) = 0, 4 x 1 = 0, 4 Eq/l Ceq (SO 4 2 -) = 0, 2 x 2 = 0, 4 Eq/l Ø Concentration équivalente solution : Ceq = 0, 8 Eq/l

MASSE D’UN EQUIVALENT

n Na+ EXEMPLE 4 : Poids atomique : Valence : 1 Masse d’un équivalent = g n Ca++ : Poids atomique Valence : 2 Masse d’un équivalent = 23 23/1 = 23 : 40; 40 / 2

CONCENTRATION EQUIVALENTE D’UNE SOLUTION n Concentrations équivalentes n Concentration totale en Eq ADDITIVES = Ceq anioniques cationiques + Ceq

ELECTRONEUTRALITE Ceq anionique = Ceq cationique Ceq = m. n-. Z- = m. n+. Z+

EXEMPLE 5 Plasma : par litre 155 m. Eq anioniques 155 m. Eq cationiques Total de 310 m. Eq q Solution glucose : Ceq=0 q

NOMBRE DE m. EQ 1 m. Eq = -3 10 Eq

EXEMPLE 6 Sérum sanguin normal Na+ = 3, 25 g/l = 142 m. Eq/l K+=0, 20 g/l = 5 m. Eq/l Ca++ = 0, 100 g/l = 5 m. Eq/l Cl- = 3, 60 g/l = 103 m. Eq/l CO 3 H- = 1, 65 g/l = 27 m. Eq/l

FORCE IONIQUE

EXEMPLE 6 Solution de molarité 2 M (NH 4)2 SO 4, (NH 4)2 SO 4 2(NH 4)+ + SO 42 - C 1 = C(NH 4)+= 4 M C 2 = C(SO 42 -) = 2 M ; ; v 1 = 1 v 2 = 2 de
![QCM 4 On considère une solution contenant des ions à la concentration : [Na+] QCM 4 On considère une solution contenant des ions à la concentration : [Na+]](http://slidetodoc.com/presentation_image_h/a23f403b42e1c283361c5b82d98ce595/image-34.jpg)
QCM 4 On considère une solution contenant des ions à la concentration : [Na+] = 150 mmol. L-1, [K+] = 5 mmol. L-1, [Ca 2+] = 2, 5 mmol. L-1, [Mg 2+] =1, 5 mmol. L-1. A. La concentration pondérale en sodium est de 3, 45 g. L 1. B. La molalité en magnésium est de 3, 0 mmol. kg 1. C. La concentration équivalente en calcium est de 2, 5 m. Eq. L-1. D. La concentration équivalente de la solution est de 163 m. Eq. L-1. E. La fraction molaire en potassium est de 3, 1
![QCM 4 [Na+] = 150. 10 -3. 23 = 3, 45 g. L-1 [K+] QCM 4 [Na+] = 150. 10 -3. 23 = 3, 45 g. L-1 [K+]](http://slidetodoc.com/presentation_image_h/a23f403b42e1c283361c5b82d98ce595/image-35.jpg)
QCM 4 [Na+] = 150. 10 -3. 23 = 3, 45 g. L-1 [K+] = 5. 10 -3. 39 = 0, 95 g. L-1 [Ca 2+] = 2, 5. 10 -3. 40 = 0, 1 g. L-1 [Mg 2+] = 1, 5. 10 -3. 24 = 0, 036 g. L-1 [H 2 O] = 1000 – (3, 45 + 0, 95 + 0, 1 + 0, 036) = 995, 46 g. L-1 = 55, 30 mol. L-1 F K+ = 5 / (150 + 5 + 2, 5 + 1, 5 + 55300) = 5/55304 = 0, 009 %

Réponses QCM 4 A. La concentration pondérale en sodium est de 3, 45 g. L 1. B. La molalité en magnésium est de 3, 0 mmol. kg 1. C. La concentration équivalente en calcium est de 2, 5 m. Eq. L-1. D. La concentration équivalente de la solution est de 163 m. Eq. L-1. E. La fraction molaire en potassium est de 3, 1 %.

QCM 5 Un volume V=500 m. L d’une solution est obtenu par dissolution de : 3, 73 g de KCl; 5, 55 g de Ca. Cl 2; 7, 10 g de Na 2 SO 4 ; 4, 50 g de glucose; 0, 15 g d’urée. KCl = 74, 6; Ca. Cl 2 =111; Na 2 SO 4=142 ; Glucose = 180; Urée = 60. A. La concentration en Cl- est égale à 200 mmol/L B. La concentration en Na+ est égale à 100 mmol/L C. La concentration éq en urée est 2, 5 m. Eq/L D. Céq de la solution est de 1 Eq/L
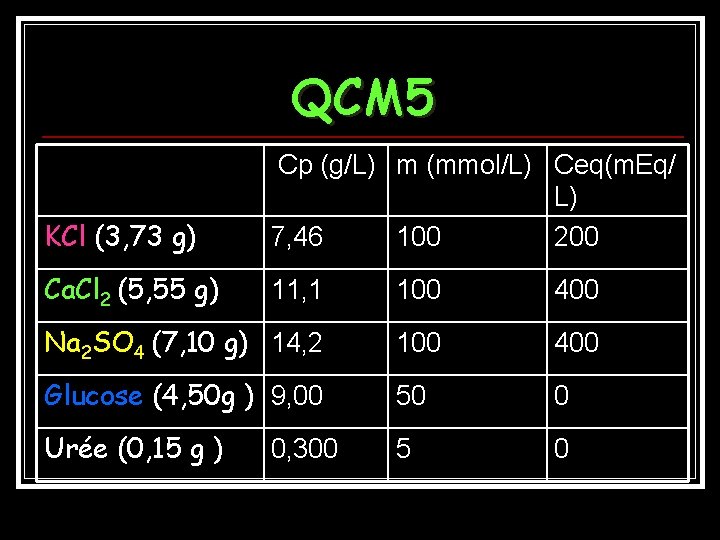
QCM 5 KCl (3, 73 g) Cp (g/L) m (mmol/L) Ceq(m. Eq/ L) 7, 46 100 200 Ca. Cl 2 (5, 55 g) 11, 1 100 400 Na 2 SO 4 (7, 10 g) 14, 2 100 400 Glucose (4, 50 g ) 9, 00 50 0 Urée (0, 15 g ) 5 0 0, 300

Réponses QCM 5 A. La concentration en Cl- est égale à 200 mmol/L B. La concentration en Na+ est égale à 100 mmol/L C. La concentration éq en urée est 2, 5 m. Eq/L D. Céq de la solution est de 1 Eq/L E. La molarité de la solution est de 355 mmol/L

QCM 6 On a dosé dans le sang d’un patient l’ensemble des cations, le glucose et l’urée. [Na+] = 145 mmol. L-1, [K+] = 5 mmol. L-1, [Ca 2+] = 2, 5 mmol. L-1, [Mg 2+] =1, 5 mmol. L-1, Glucose=1 g. L-1 et urée = 1, 81 g. L-1. La concentration éq totale du sérum de ce patient est : A. 313 m. Eq. L-1 B. 158 m. Eq. L-1 C. 156 m. Eq. L-1 D. 323 m. Eq. L-1 E. 316 m. Eq. L-1

Réponses QCM 6 A. 313 m. Eq. L-1 B. 158 m. Eq. L-1 C. 156 m. Eq. L-1 D. 323 m. Eq. L-1 E. 316 m. Eq. L-1

OSMOLE Important pour les phénomènes NON ELECTRIQUES (Diffusion, osmose etc. …). C’est toute particule : Molécules ou ions d’une solution

EXEMPLE 7 Glucose 0, 1 mol. L-1 0, 1 Osmol. L-1 Na. Cl 0, 1 mol. L-1 0, 2 Osmol. L-1 PO 4 Na 3 0, 015 mol. L-1 0, 06 Osmol. L-1 Ca. Cl 2 0, 1 mol. L-1 0, 3 Osmol. L-1

OSMOLARITE ou Concentration molaire particulaire = Nombre d’OSMOLES par unité de volume de solution ( Osm. L-1 ou -1 m. Osmol. L )

EXEMPLE 9 Solution de molarité m de chlorure de calcium de coefficient de dissociation Ca. Cl 2 2 Cl- + Ca++ 2 m ions-g ou osmoles de Cl- par litre m ions-g ou osmoles de Ca++ par litre m(1 - ) moles non dissociées = m(1 - )+ m + 2 m =m(1+2 ) Pour m= 0, 1 mol. L-1 et =0, 6 : = 0, 1 ( 1+1, 2) = 0, 1. 2, 2 = 0, 22 Osmol. L-1 Ceq= 4 m = 4. 0, 1. 0. 6 = 0, 24 m. Eq. L-1

QCM 7 On mélange une solution de Na. Cl d’osmolarité 300 osmol. m-3 avec une solution de KCl d’osmolarité 300 osmol. m-3. Quelle est la molarité de la solution résultante ? A. 600 mol. m-3 B. 300 mol. m-3 C. 0, 6 mol. l-1 D. 150 mol. m-3 E. 300 mmol. l-1

Réponses QCM 7 A. 600 mol. m-3 B. 300 mol. m-3 C. 0, 6 mol. l-1 D. 150 mol. m-3 E. 300 mmol. l-1

QCM 8 Une solution contenant 1 mole de Ca. Cl 2 par litre d’eau a : A. une molarité égale à 1 mole/m 3 B. une molalité égale à 1 mole/kg C. une osmolarité égale à 3000 Osmol/ m 3 si le coefficient de dissociation est égal à 1 D. une osmolalité égale à 3 moles/kg si le coefficient de dissociation est égal à 1 E. une osmolarité égale à 0 si le coefficient de dissociation est égal à 0

Réponses QCM 8 A. une molarité égale à 1 mole/m 3 B. une molalité égale à 1 mole/kg C. une osmolarité égale à 3000 Osmol/ m 3 si le coefficient de dissociation est égal à 1 D. une osmolalité égale à 3 moles/kg si le coefficient de dissociation est égal à 1 E. une osmolarité égale à 0 si le coefficient de dissociation est égal à 0

QCM 9 La sensation de soif provient d’une hyperosmolarité plasmatique et se traduit pour les cellules par: A. une hyperhydratation B. une augmentation de volume C. une déshydratation D. une lyse E. une diminution de volume

Réponses QCM 9 A. une hyperhydratation B. une augmentation de volume C. une déshydratation D. une lyse E. une diminution de volume

A RETENIR n Osmolarité plasma normal = 300 m. Osmoles /L n Concentration normale uréique sanguine = 0, 25 -0, 30 g/L n Concentration normale du glucose dans le sang = 1 g/L

Electrolytes forts Tout électrolyte qui se dissocie totalement dans l’eau ( Na. Cl, Na. OH, KOH, HCl) Dans la solution on ne trouve que des ions majoritaires ( dissociation du cristal ou de la molécule) et les molécules du solvant.

Electrolytes faibles L’ionisation du soluté est partielle. La solution contient donc les ions du soluté, des molécules du soluté et celles du solvant.

TAUX DE DISSOCIATION
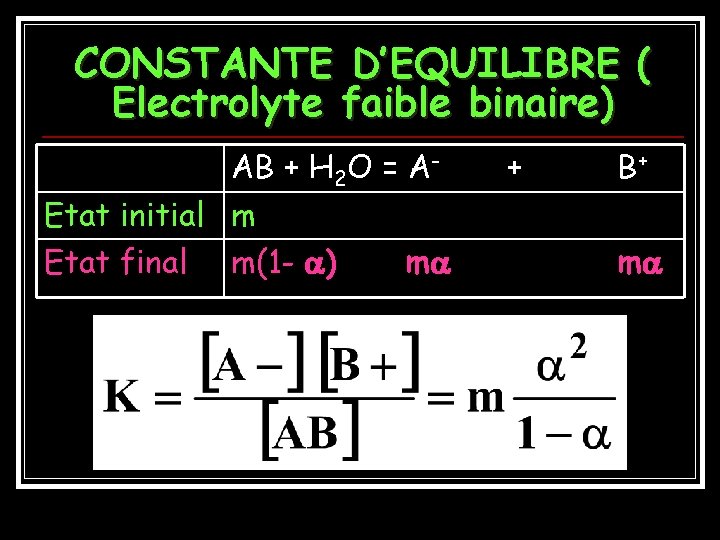
CONSTANTE D’EQUILIBRE ( Electrolyte faible binaire) AB + H 2 O = A- Etat initial m Etat final m(1 - ) m + B+ m

Remarques La constante d’équilibre K : 1. dépend du soluté 2. dépend de la nature du solvant 3. Augmente avec la température 4. ne dépend pas de ou de m

EXEMPLE 10 On dissout 0, 1 mol d’acide faible, noté AH dans un volume V=1 L d’eau. Le coeff de dissociation de cet acide est = 0, 08. Constante K et de la solution ? AH + H 2 O = A- + H 3 O + Øm= 0, 1 mol. L-1 , K = 0, 1. ( (0, 08)2 / (10, 08) = 6, 96. 10 -4; Ø = m(1 - ) +m + m = m(1+ ) =0, 1 x (1+0, 08) =0, 108 osmol. L-1 = 108 mosm. L-1

Détermination du taux de dissociation

Electrolyte du type BA 2 m(1 - ) = B 2+ m + 2 A 2 m
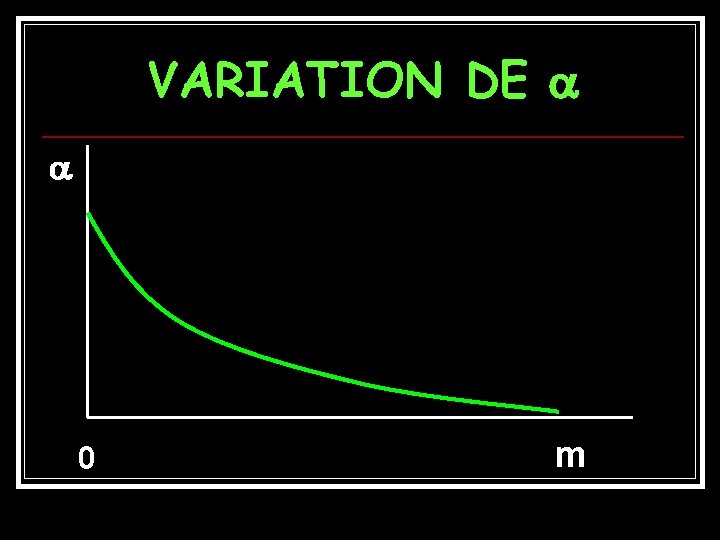
VARIATION DE 0 m

COEFF. D’ IONISATION

EXPRESSION DU COEFF. IONISATION m : molarité électrolyte Ni: Nb d’ions / molécule dissociée = Nb particules neutres + Nb ions = m(1 - ) + m . Ni = m[1+ (Ni – 1)]

Exemple 11 CH 3 COOH = CH 3 COO- + H+ α = 0, 1 i = 1 + 0, 1(2 -1)= 1, 1 Solution 2 M ; = 2, 2 Osm. l-1

EXEMPLE 12 Solution aqueuse 3, 28 g/l de PO 4 Na 3 3 PO 4 Na 3 ↔ PO 4 + 3 Na+ m = 3, 28/164 = 20 mmol. l-1 i = 4. 20 = 80 m. Osm. l-1 C- = 1. 20 = 20 mmol. l-1= 1, 9 g. l-1 C+ = 3. 20 = 60 mmol. l-1 = 1, 38 g. l-1 CEq-=20. 3=60 m. Eq CEq=120 m. Eq

LOI de DILUTION D’OSTWALD Øm 0 (Solution infiniment diluée), 1: A dilution infinie un électrolyte faible est totalement dissocié ( Electrolyte fort) Øm , 0 : A l’état pur un électrolyte faible ne se dissocie pas.

QCM 3 Une solution de Na. Cl isotonique au plasma a une osmolarité de : A. O, 3 mosmol. l-1 B. 300 mosmol. l-1 C. 300 osmol. m-3 D. 3 mosmol. l-1 E. 3 osmol. m-3

Réponses QCM 3 Une solution de Na. Cl isotonique au plasma a une osmolarité de : A. 300 mosmol. l-1 C. 300 osmol. m-3 B. D. E.

QCM 4 Cette solution correspond à une molarité de Na. Cl de : A. 600 mol. m-3 B. 0, 6 mol. l-1 C. 0, 15 mol. l-1 D. 150 mmol. l-1 E. 6 mol. l-1

Réponses QCM 4 Cette solution correspond à une molarité de Na. Cl de : A. B. C. D. E. 150 mmol. l-1

QCM 5 La sensation de soif provient d’une hyperosmolarité plasmatique et se traduit pour les cellules par: A. une hyperhydratation B. une augmentation de volume C. une déshydratation D. une lyse E. une diminution de volume
- Slides: 71