Biomolculas Toda la materia viviente y no viviente

Biomoléculas • Toda la materia, viviente y no viviente se compone de sustancias químicas -4000 x 106 años hasta llegar a células interacciones entre moléculas para finalmente “evolucionr” Niveles de organización: propiedades emergentes

Átomos Electrones: 9 x 10 -28 g Protones: masa de 1 protón= 1 Dalton (1, 7 x 10 -24 g) Neutrones= 1 Dalton Orbitales (cada uno 2 electrones), niveles energéticos Número atómico: número de protones Número másico: (masa atómica o peso atómico) protones + neutrones (es un promedio de todos los isótopos) difieren en la cantidad de neutrones (pesados, radioactivos, utilidad en Biología) Elemento: es una sustancia pura que contiene un solo tipo de átomo, cada elemento se identifica por el número de protones (C = 6 protones, H = 1 protón, O = 8 protones) El 98% de la masa de un organismo vivo sólo 6 elementos: C, H, O, N, P, S

Átomos interaccionan con otros átomos a través de enlaces químicos moléculas El comportamiento de los electrones determina el tipo de enlace químico, cómo reccionan unos con otros Capas electrónicas 1 ra tiene 1 orbital : s 2 da P, tiene 4 orbitrales: 1 s y 3 p Etc La capa más externa determina cómo se combina con otros átomos, los más estables poseen 4 orbitales o sea 8 electrones en su última capa (He, Ne, Ar) Los átomos de elementos reactivos (cuyas capan externas tienen orbitales sin completar) buscan tener 8 electrones en su última capa Ganan, pierden o comparten

Covalentes: los electrones se comparten, entre átomos con electronegatividad parecida Ejemplos: H 2, , CO 2, metano (CH 4) Enlaces fuertes, la diferencia de electronegatividad entre los átomos determina la polaridad del enlace Covalentes No polares: CO 2, O 2 Covalentes Polares: agua Puentes de hidrógeno: enlaces débiles entre moléculas, atracción entre densidades de carga – y + de otra molécula

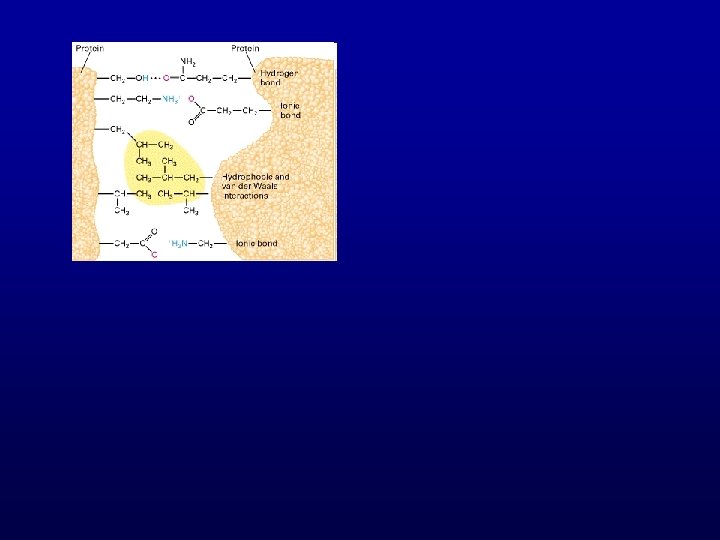
Enlaces iónicos: entre átomos de electronegatividades muy diferentes, Los electrones se ganan o se pierden. El enlace se forma por atracción eléctrica entre los átomos. Iones: partículas cargadas, aniones, cationes Polar-polar No polar-no polar Molécula anfipática

Agua: La sustancia más abundante en la célula. La polaridad de la molécula le permite establecer puentes de hidrógeno. Estos son responsables de las propiedades características como: • Tensión superficial • Adhesión • cohesión • Alto calor específico, alta capacidad calórica del agua líquida • Alto calor de vaporización • Solvente polar • El hielo flota p. H: Qué es? Ácido? Base? fuertes y débiles Agua pura? Concentración de H+ y HO- (10 -7 moles por litro)

Buffer: qué es? Ácido débil + su correspondiente base H 2 CO 3 HCO 3 - + H+ Por qué funciona como buffer? Principales moléculas orgánicas Cadenas carbonadas con grupos funcionales que le brindan propiedades específicas a las moléculas Ejemplos?
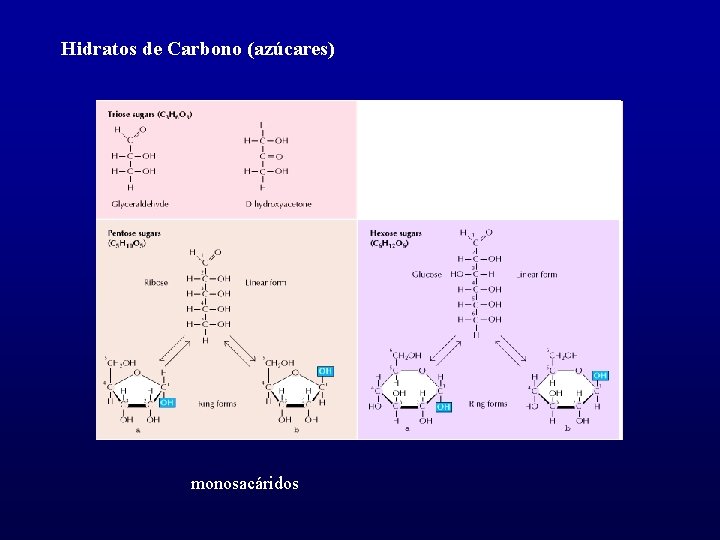
Hidratos de Carbono (azúcares) monosacáridos
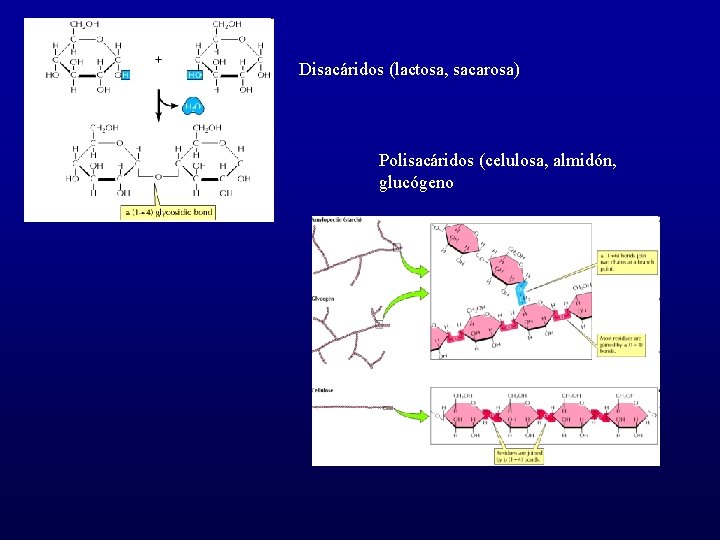
Disacáridos (lactosa, sacarosa) Polisacáridos (celulosa, almidón, glucógeno
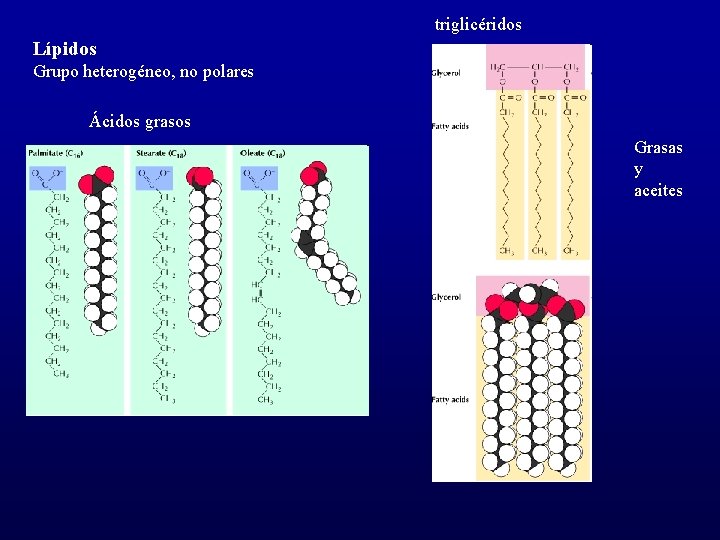
triglicéridos Lípidos Grupo heterogéneo, no polares Ácidos grasos Grasas y aceites
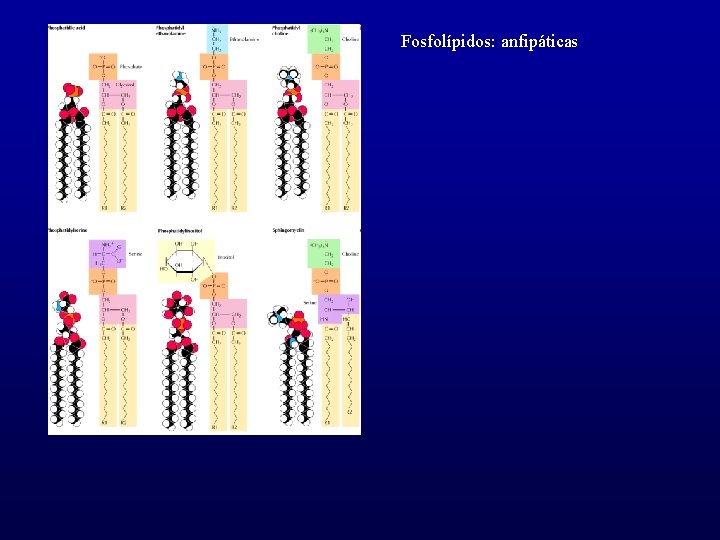
Fosfolípidos: anfipáticas
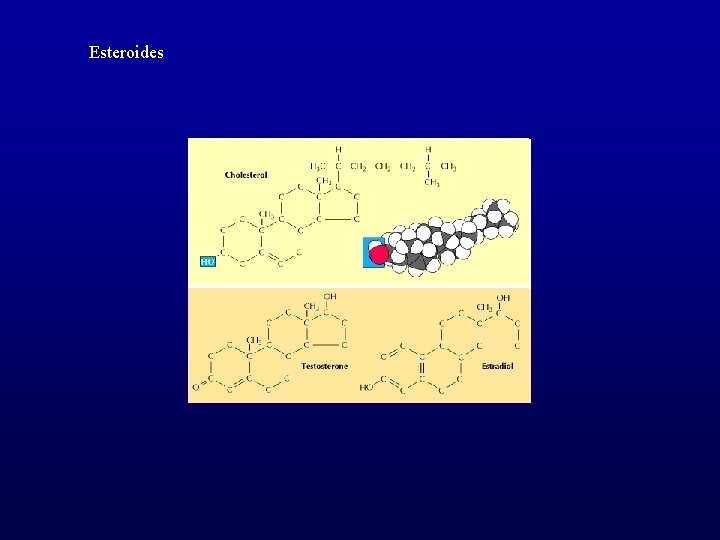
Esteroides
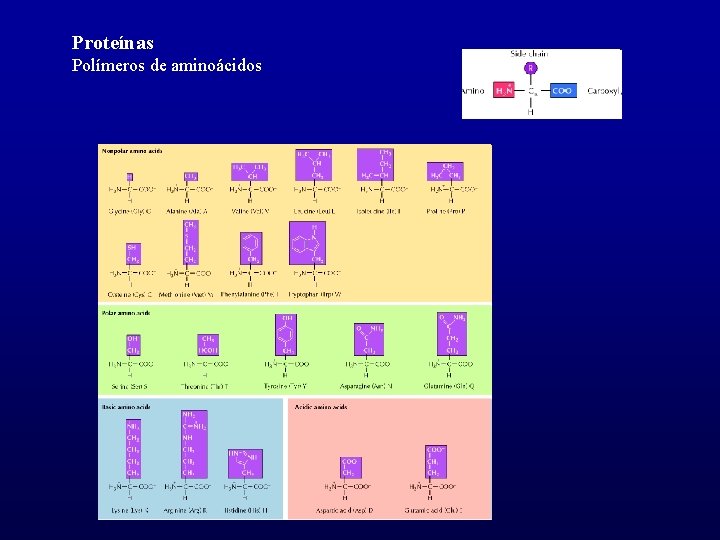
Proteínas Polímeros de aminoácidos
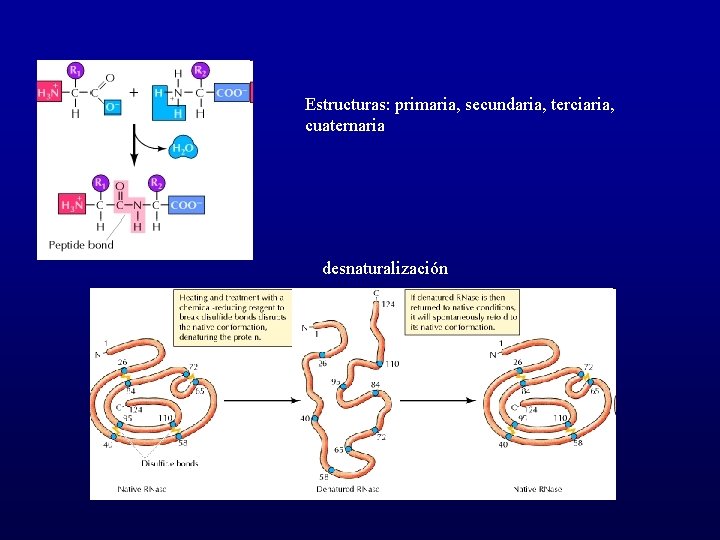
Estructuras: primaria, secundaria, terciaria, cuaternaria desnaturalización

Estructura secundaria Patrones regulares y repetidos en diferentes regiones de una cadena polipeptídica Se genera por puentes de hidrógeno entre el H del NH y el O del C=O de otro aa.
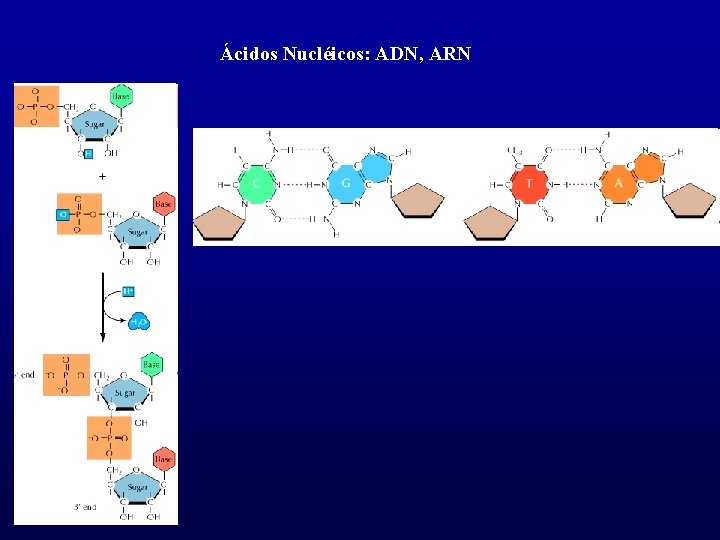
Ácidos Nucléicos: ADN, ARN

- Slides: 19