Biomolculas Professor Sstenes Pereira Biomolculas Estruturas e Funes

Biomoléculas Professor: Sóstenes Pereira

Biomoléculas �Estruturas e Funções das Biomoléculas • Carboidratos • Lipídios • Aminoácidos e Proteínas

Aminoácidos e Proteínas

� Cadeia Proteínas formada por aminoácidos � Apenas 20 aminoácidos (2, 4 x 1018 moléculas)

Proteínas � Constituintes � celulares mais abundantes Grande diversidade estrutural e funcional üFunções Estruturais § Componentes do esqueleto celular e de estruturas de sustentação (colágeno e elastina) üFunções Dinâmicas § Processos biológicos (enzimas) § Transporte de moléculas (mioglobina, hemoglobina) § Mecanismo de defesa (imunoglobulinas) § Controle metabólico (hormônios) § Mecanismos contráteis (actina e miosina) § Controle da expressão gênica

Classificação quanto a forma Ø Proteínas fibrosas üForma alongada üInsolúveis üFunções estruturais üÚnico tipo de estrutura secundária repetitiva vα-queratina o Cabelo, unha, epiderme, lã v. Colágeno Ø Proteínas Globulares üForma final esférica üSolúveis üFunções dinâmicas v. Albuminas v. Globulinas
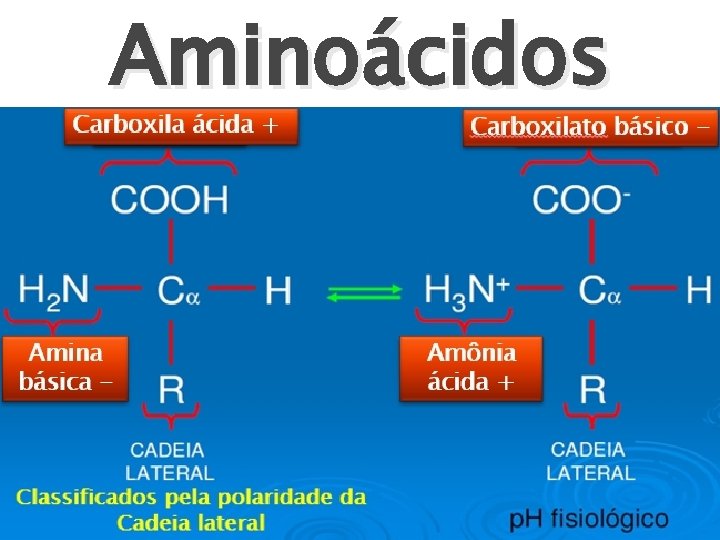
Aminoácidos
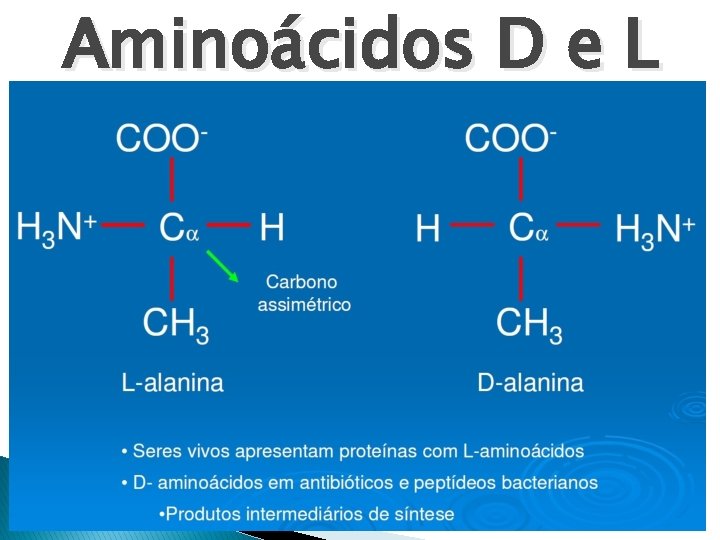
Aminoácidos D e L
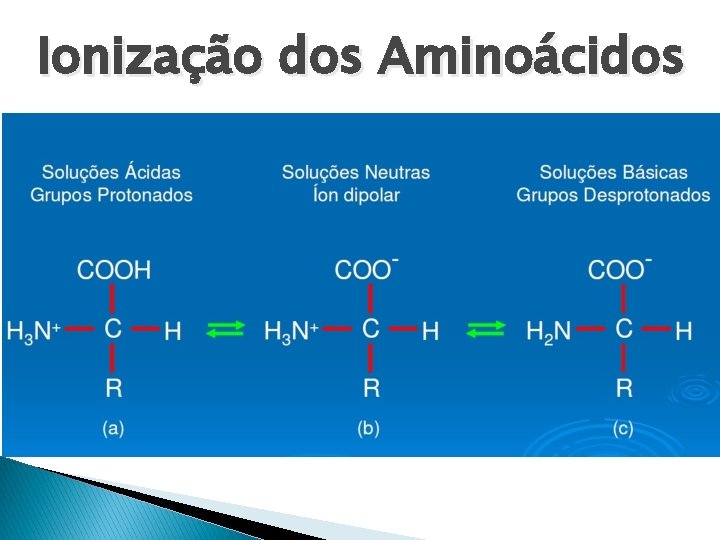
Ionização dos Aminoácidos

� Polímero Proteínas de aminoácidos üDipeptídeos – Tripeptídeos - Tetrapeptídeos üOligopeptídeos ou peptídeos – até 30 aminoácidos üPolipeptídeos – mais que 30 aminoácidos

Estruturas Proteicas

Estruturas Proteicas � Sequência de aminoácidos � Disposição dos aminoácidos entre si üCargas das cadeias üPolaridade: aminoácidos tem carga üPresença ou não de cadeias interligadas Grau de complexidade 1. 2. 3. 4. Primária Secundária Terciária Quaternária
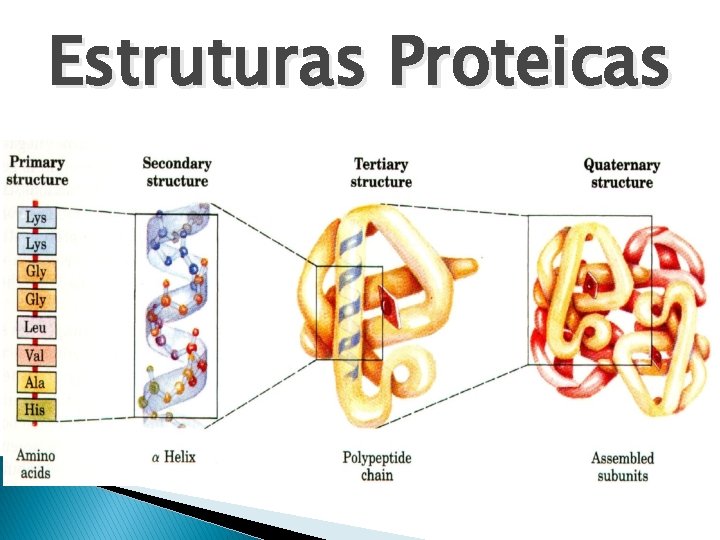
Estruturas Proteicas

Estrutura Primária � Dada pela sequência de aminoácidos üN-terminal C-terminal üGly – Ala – Val ou G – A – V

Estrutura Secundária �

Estrutura Secundária Alfa Hélice Beta Folha
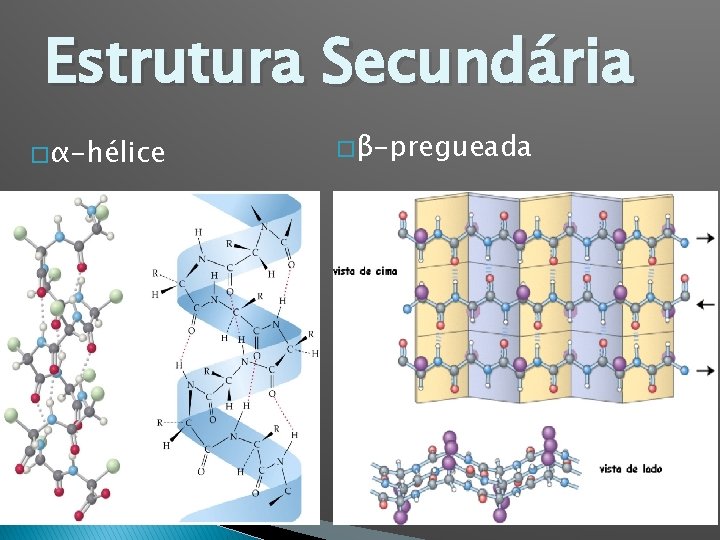
Estrutura Secundária � α-hélice � β-pregueada

Estrutura Terciária üDescreve a estrutura tridimensional dos segmentos da cadeia polipeptídica ü Combinação entre alfa hélices e beta folhas isoladas ou juntas ü Interações covalentes: pontes dissulfetos ü Interações não covalentes: hidrogênio, hidrofóbica e eletrostáticas.

� Estrutura Terciária Tipos de interação entre os grupos R dos aminoácidos üPontes dissulfeto üLigações de hidrogênio § Entre os grupos R de aminoácidos polares üInterações Hidrofóbicas § Entre cadeias laterais apolares § Mais importantes para manutenção da conformação protéica üInterações eletrostáticas § Interações entre grupos R de cargas opostas § Importantes para o dobramento da cadeia quando ocorrem na região apolar (menor frequência) § Maior frequência na superfície proteica interagindo com a água
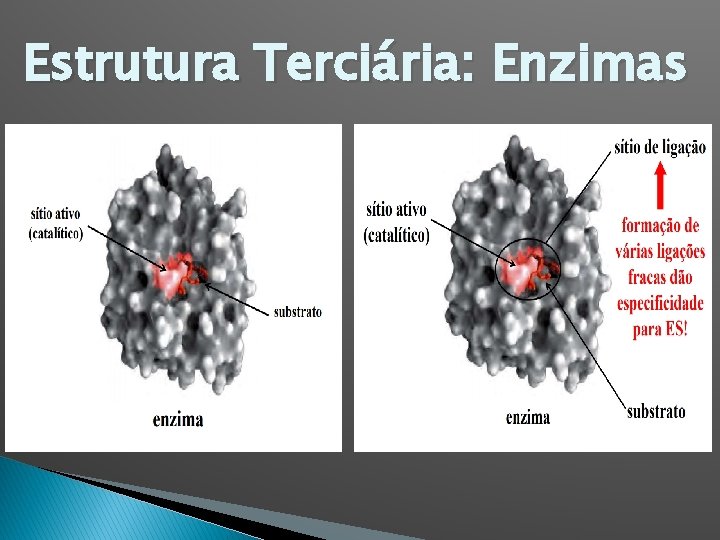
Estrutura Terciária: Enzimas

Estrutura Quaternária � Interação entre 2 ou mais subunidades � Composição de uma proteína oligomérica � Ligações não covalentes como na estrutura terciária � Subunidades semelhantes ou não üHemoglobina (4 subunidades iguais 2 a 2) § 2 subunidades α e 2 subunidades β associadas principalmente por interações hidrofóbicas
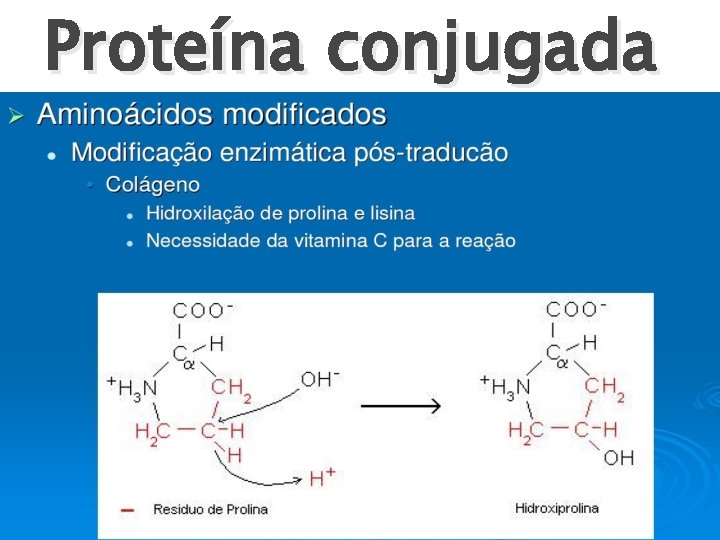
Proteína conjugada

Proteína Conjugada � Grupos prostéticos üMoléculas orgânicas não proteicas üLigação covalente ou não covalente üGrupo heme na mioglobina � Carboidrato – Glicoproteína üMucina, Imunoglobulinas � Lipídio - lipoproteína üEstruturais da membrana üProteínas de Transporte

Desnaturação das Proteínas No aquecimento, a albumina da clara do ovo sofre desnaturação proteica, ficando branca

Desnaturação das Proteínas � Quebra das ligações não covalentes � Manutenção da ligação peptídica primária � Maneiras de provocar desnaturação üAumentar temperatura – abaixo de 100°C üForça iônica – aumentar ou diminuir p. H üSolventes orgânicos – diminui [K] dielétrica üUreia – formação de pontes de hidrogênio üDetergentes e sabões § Cadeia hidrofóbica (apolar) ligada a grupo carregado § Ligação com radicais apolares da proteína § Rompimento interações hidrofóbicas
- Slides: 25