BIOMEDICAMENTS 2010 Enjeux et propositions pour favoriser lattractivit

BIOMEDICAMENTS 2010 Enjeux et propositions pour favoriser l'attractivité de la France Mardi 16 novembre 2004

BIOMEDICAMENTS 2010 Jean Derégnaucourt : Directeur du Département bioingénierie, Direction de la Technologie, Ministère délégué à la Recherche représentant François d'Aubert, Ministre délégué à la Recherche

Comité Biotechnologies du Leem : objectifs et missions Marc de Garidel Président du Comité Biotechnologies

La mission du Comité : Contribuer à ce que la France joue un rôle majeur dans les biotechnologies Fédérer et mobiliser les différents acteurs du secteur 4 Etre force de propositions pour inciter au développement du secteur

4 objectifs majeurs ● Faciliter les échanges entre acteurs et coordonner les opérations, études et formations correspondantes ● Permettre un travail commun approfondi de tous les acteurs sur les réponses aux contraintes techniques spécifiques, liées à l’activité ● Permettre un travail similaire sur les contraintes liées au cadre réglementaire français et proposer des optimisations à partir des opportunités offertes par le cadre européen ● Faire connaître et valoriser dans le paysage français les biotechnologies appliquées au médicament 5

Biomédicaments : une nouvelle frontière pour la santé

Objectifs de l’étude « Bioproduction » Bernard Lemoine Vice-Président délégué du Leem

L’environnement de l’industrie du médicament est en pleine mutation ● Un changement de paradigme scientifique offrant des perspectives thérapeutiques nouvelles… ● … s’accompagnant d’une transformation du modèle économique de l’Innovation : du « blockbuster » aux blockbuster « multibusters » … ● … dans un contexte d’internationalisation des marchés imposant aux entreprises une compétitivité accrue à tous les niveaux Quelle place pour la France au plan européen et international ? 8
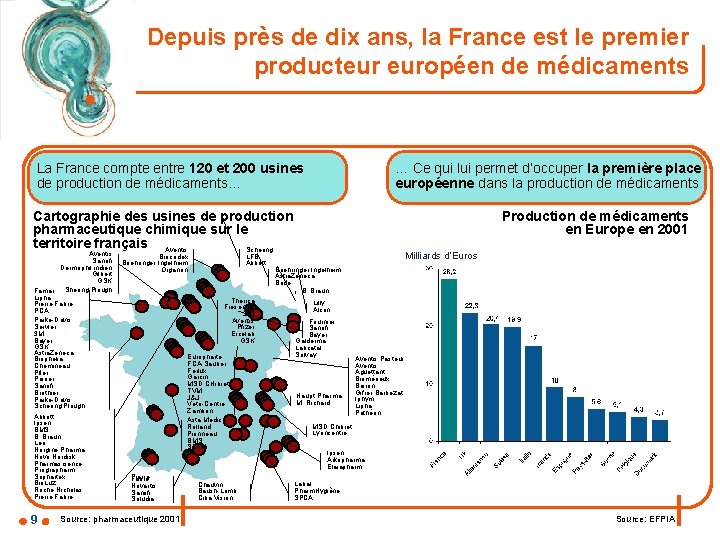
Depuis près de dix ans, la France est le premier producteur européen de médicaments La France compte entre 120 et 200 usines de production de médicaments. . . … Ce qui lui permet d’occuper la première place européenne dans la production de médicaments Production de médicaments en Europe en 2001 Cartographie des usines de production pharmaceutique chimique sur le territoire français Aventis Schering Aventis Sanofi Dermophil indien Gilbert GSK Famar Shering Plough Lipha Pierre Fabre PCA Parke-Davis Servier 3 M Bayer GSK Astra. Zeneca Biophelia Chemineau Pfier Poirier Sanofi Brothier Parke-Davis Schering Plough Abbott Ipsen BMS B. Braun Leo Norgine Pharma Novo Nordisk Pharmascience Prographarm Sophartex Bio. Luz Roche Nicholas Pierre Fabre 9 Biocodex Boehringer Ingelheim Organon LFB Abbott Therica Fresenius J&J Aventis Pfizer Ercelab GSK Europharte FCA-Sauber Ferlux Garcin MSD CHibret TVM J&J Veto-Centre Zambon Asta Medica Rolland Pionneau BMS Sanofi Pierre Fabre Novartis Sanofi Soludia Source: pharmaceutique 2001 Chauvin Baush-Lomb Ciba Vision Milliards d’Euros Boehringer Ingelheim Astra. Zeneca Bride B. Braun Lilly Alcon Fournier Sanofi Bayer Galderma Labcatal Solvay Haupt Pharma M. Richard Aventis Pasteur Aventis Aguettant Biomérieux Boiron Gifrer Barbezat Iphym Lipha Pathéon MSD Chibret Lyoncentre Ipsen Arkopharma Elaiapharm Labal Pharm. Hygiène SPCA Source: EFPIA

Et dispose d’atouts majeurs… ● Une expertise scientifique internationalement reconnue ● Des avantages compétitifs en terme d’essais cliniques ● Une politique conventionnelle et des spécificités facilitant l’accès au marché ● Un marché large et solvable : – le 4ème marché mondial – 2ème marché pharmaceutique européen ● 3ème exportateur mondial 10

… mais des faiblesses de plus en plus handicapantes ● Des délais d’accès au marché longs et préjudiciables aux patients ● Un niveau de taxation parmi les plus élevés ● Des signaux négatifs en matière de compétitivité des études cliniques ● Des niveaux de prix européens, encore inférieurs à ceux du Royaume-Uni et de l’Allemagne ● Une compétitivité en perte de vitesse sur le terrain de la production : ● Face à l’émergence des pays à faible coût de main-d’œuvre pour les produits « installés » sur le marché 11 ● Face aux pays ayant fortement développé leur avantage compétitif sur l’innovation

Améliorer l’attractivité de la France dans le secteur stratégique du médicament s’appuyer sur nos atouts, conquérir de nouveaux territoires 12

France : conquérir le nouveau territoire des biomédicaments ● Le virage des biotechnologies abordé avec retard… ● Un tissu immature d’entreprises émergentes ● Des modalités d’attractivité insuffisantes pour les entreprises du médicament développant une compétence ou des traitements issus des biotechnologies ● Une compétition naissante dans le domaine de la Bioproduction ● … entraînant un risque de délocalisation de tous les maillons de la chaîne d’innovation 13
France : conquérir le nouveau territoire des biomédicaments ● A la clé, de véritables enjeux : ● de santé publique ● sociétaux ● industriels d’où cette mobilisation du Comité Biotechnologies du Leem 14

Une mobilisation du Comité Biotechnologies du Leem ● Objectifs de l’étude : ● Analyser les enjeux et les opportunités pour la France en termes de développement de la bioproduction ● Déterminer les facteurs clés d’implantation de nouvelles unités de production ● Élaborer des propositions pour attirer de nouveaux acteurs en France 15

Médicaments : perspectives et enjeux de la bioproduction Dr Annick Schwebig Vice-Présidente du Comité Biotechnologies du Leem

Médicaments : perspectives et enjeux de la bioproduction ● Le Comité Biotechnologies du Leem a fait appel à Arthur D. Little pour répondre aux questions-clés suivantes : ● Quels sont les enjeux et opportunités pour la France ? ● Quel est le positionnement de la France sur les facteurs clés d’implantation ? 17

Le marché mondial des biomédicaments et ses perspectives
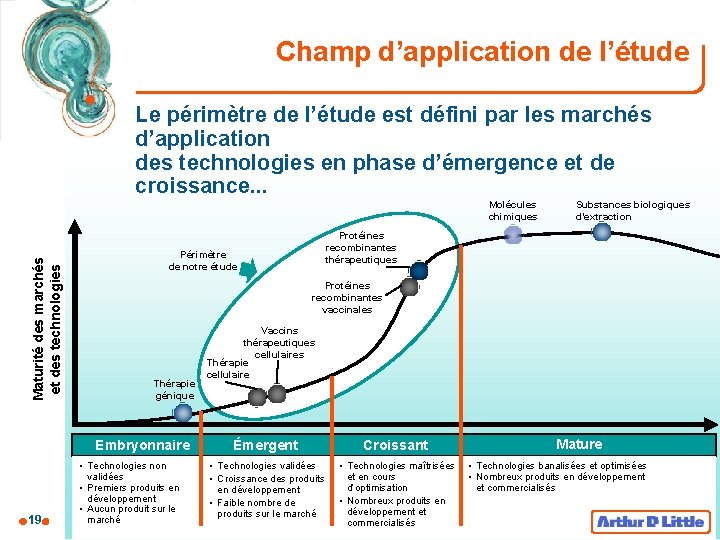
Champ d’application de l’étude Le périmètre de l’étude est défini par les marchés d’application des technologies en phase d’émergence et de croissance. . . Maturité des marchés et des technologies Molécules chimiques Protéines recombinantes thérapeutiques Périmètre de notre étude Protéines recombinantes vaccinales Thérapie génique Embryonnaire 19 Substances biologiques d’extraction • Technologies non validées • Premiers produits en développement • Aucun produit sur le marché Vaccins thérapeutiques cellulaires Thérapie cellulaire Émergent Croissant • Technologies validées • Croissance des produits en développement • Faible nombre de produits sur le marché • Technologies maîtrisées et en cours d’optimisation • Nombreux produits en développement et commercialisés Mature • Technologies banalisées et optimisées • Nombreux produits en développement et commercialisés
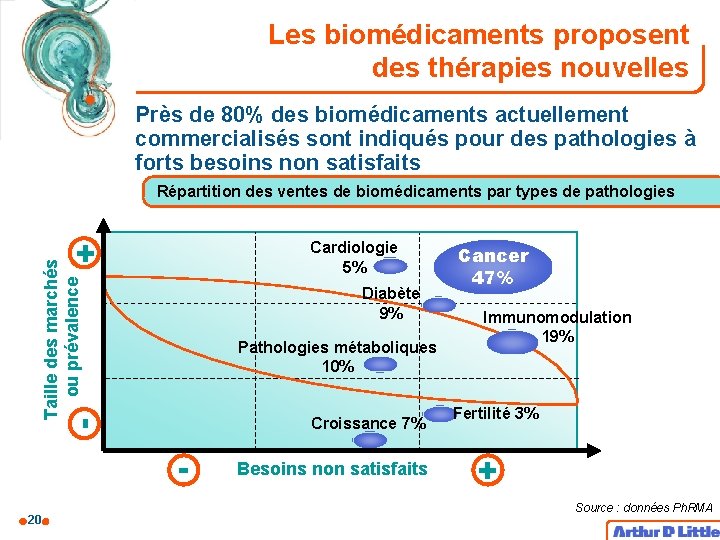
Les biomédicaments proposent des thérapies nouvelles Près de 80% des biomédicaments actuellement commercialisés sont indiqués pour des pathologies à forts besoins non satisfaits Répartition des ventes de biomédicaments par types de pathologies Taille des marchés ou prévalence + Cardiologie 5% Diabète 9% Pathologies métaboliques 10% - Croissance 7% 20 Besoins non satisfaits Cancer 47% Immunomodulation 19% Fertilité 3% + Source : données Ph. RMA

Une part croissante dans les portefeuilles et les pipelines Les produits biologiques prennent une part croissante au sein des nouveaux médicaments commercialisés et des nouvelles molécules en développement Part des molécules biothérapeutiques parmi les nouvelles entités moléculaires (NME) approuvées par la FDA* NME part des biomédicaments En 2003, plus de 40% des nouvelles molécules mises sur le marché étaient d’origine biologique 21 *: Federal Drug Administration Source : Ph. RMA
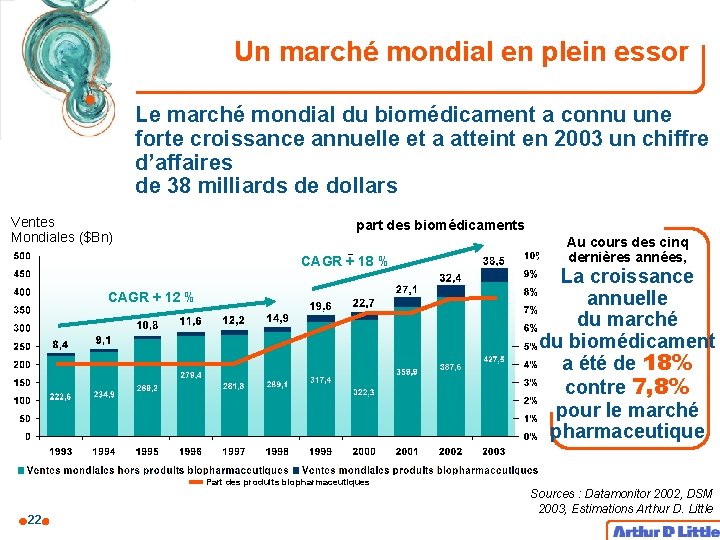
Un marché mondial en plein essor Le marché mondial du biomédicament a connu une forte croissance annuelle et a atteint en 2003 un chiffre d’affaires de 38 milliards de dollars Ventes Mondiales ($Bn) part des biomédicaments CAGR + 18 % CAGR + 12 % Au cours des cinq dernières années, La croissance annuelle du marché du biomédicament a été de 18% contre 7, 8% pour le marché pharmaceutique Part des produits biopharmaceutiques 22 Sources : Datamonitor 2002, DSM 2003, Estimations Arthur D. Little
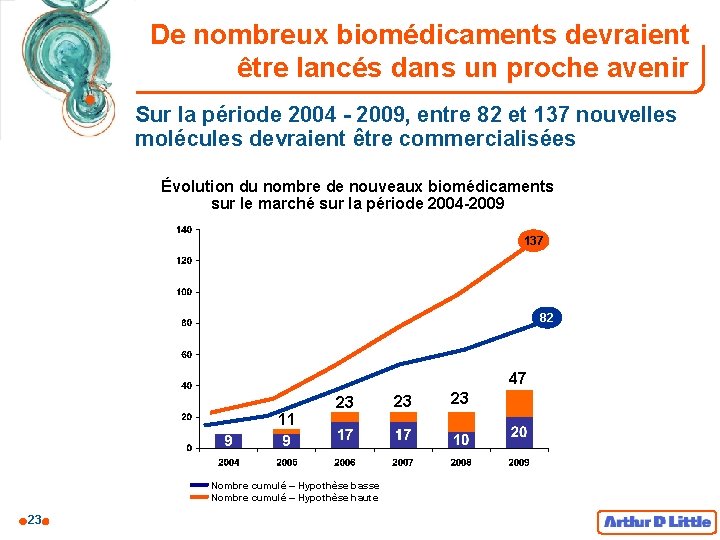
De nombreux biomédicaments devraient être lancés dans un proche avenir Sur la période 2004 - 2009, entre 82 et 137 nouvelles molécules devraient être commercialisées Évolution du nombre de nouveaux biomédicaments sur le marché sur la période 2004 -2009 137 82 47 11 23 Nombre cumulé – Hypothèse basse Nombre cumulé – Hypothèse haute 23 23 23
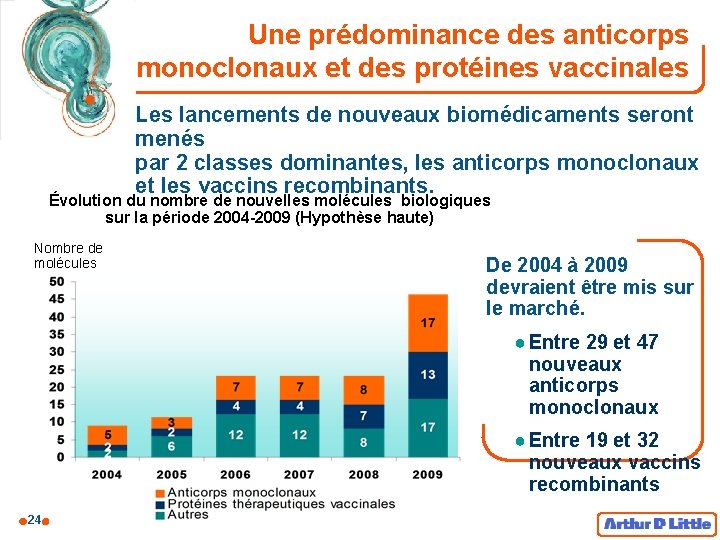
Une prédominance des anticorps monoclonaux et des protéines vaccinales Les lancements de nouveaux biomédicaments seront menés par 2 classes dominantes, les anticorps monoclonaux et les vaccins recombinants. Évolution du nombre de nouvelles molécules biologiques sur la période 2004 -2009 (Hypothèse haute) Nombre de molécules De 2004 à 2009 devraient être mis sur le marché. ● Entre 29 et 47 nouveaux anticorps monoclonaux ● Entre 19 et 32 nouveaux vaccins recombinants 24

Des perspectives économiques en progression continue Le marché du biomédicament devrait atteindre plus de 100 milliards de dollars en 2010 et représenter 12% du marché mondial du médicament part des biomédicaments Ventes ($Bn) CAGR + 14, 6 % Source : Analyse Arthur D. Little, données Exane BNP Paribas, Datamonitor, IMS pour les prévisions de ventes des produits déjà sur le marché en 2003 Part des biomédicaments ● Au cours des six prochaines années, la croissance annuelle du marché du biomédicament devrait atteindre 14, 6% 25
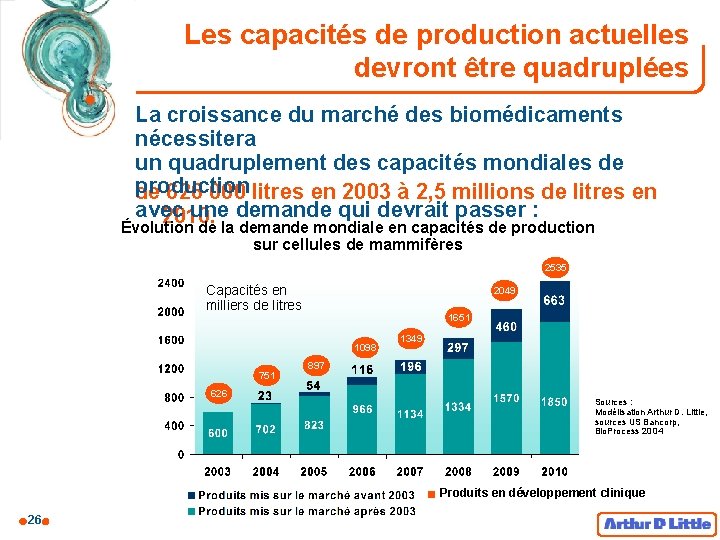
Les capacités de production actuelles devront être quadruplées La croissance du marché des biomédicaments nécessitera un quadruplement des capacités mondiales de production de 626 000 litres en 2003 à 2, 5 millions de litres en avec une demande qui devrait passer : 2010. Évolution de la demande mondiale en capacités de production sur cellules de mammifères 2535 Capacités en milliers de litres 2049 1651 1098 751 626 1349 897 Sources : Modélisation Arthur D. Little, sources US Bancorp, Bio. Process 2004 Produits en développement clinique 26

Enjeux de la production biologique pour les entreprises du médicament

Des investissements considérables Le déploiement d’une unité de production de 50 000 litres nécessite un investissement minimum compris entre 250 et 300 millions de dollars sur 4 à 5 ans ● Le fonctionnement d’une unité représente des frais opérationnels compris entre 80 et 120 Millions de dollars et requiert plus de 250 emplois 28 Répartition des coûts de déploiement d’une unité de production biologique en millions de dollars

Implantation d’unités de production : une opportunité de création d’emplois L’implantation d’une unité de 50 000 litres de capacité pourrait créer plus de 3500 « emplois » en équivalent temps plein. Nombre d’équivalents emplois créés par an pour une unité de production 1 : Emplois maintenus pendant une période de cinq ans, correspondant à la construction de bâtiments et la mise en route de l’unité de production 2 : Emplois correspondant à l’exploitation de l’unité de production, à partir de la cinquième année 29 ► Des emplois directs liés à la construction puis au fonctionnement de l’usine ► Des emplois indirects liés à l’environnement du site ► Des emplois induits qui correspondent à l’effet de levier de l’injection dans l’économie des investissements réalisés ► Une forte proportion d’emplois hautement qualifiés
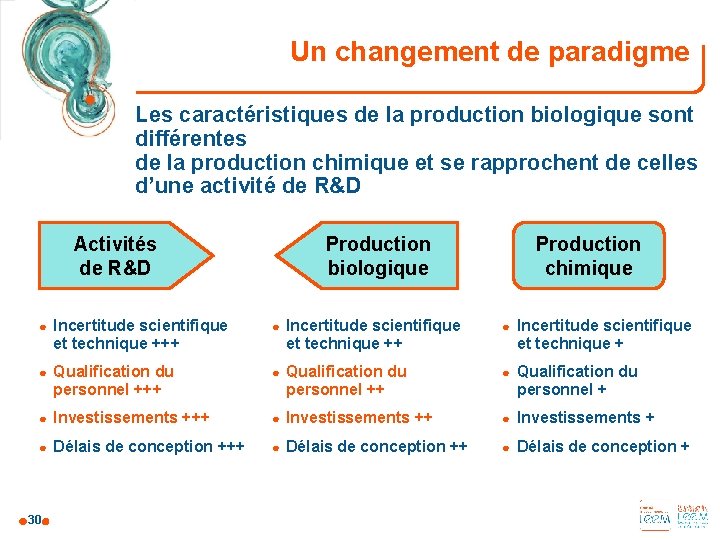
Un changement de paradigme Les caractéristiques de la production biologique sont différentes de la production chimique et se rapprochent de celles d’une activité de R&D Production biologique Activités de R&D Production chimique ● Incertitude scientifique et technique +++ ● Incertitude scientifique et technique + ● Qualification du personnel ++ ● Qualification du personnel + ● Investissements ++ ● Investissements + ● Délais de conception ++ ● Délais de conception + 30

Des unités de bioproduction principalement situées à l’étranger ● La majorité des unités de bioproduction est localisée en Amérique et en Europe du Nord ● La Caroline du Nord, la Californie, l’Irlande et la Suisse disposent des plus fortes capacités de production de protéines recombinantes 31
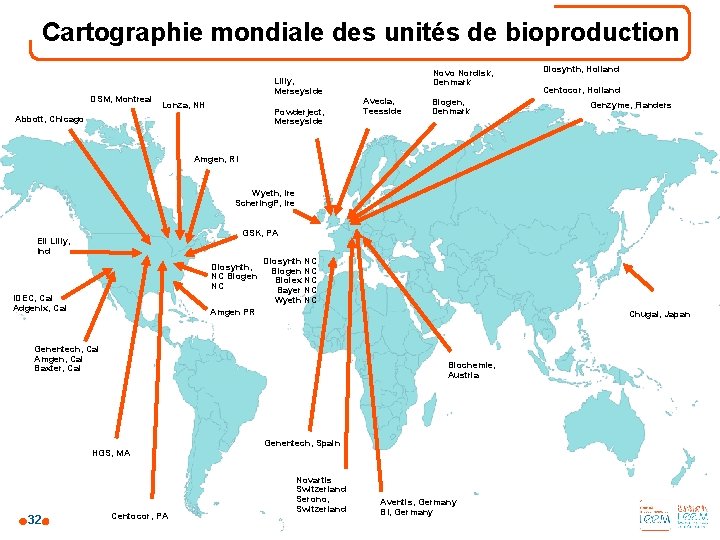
Cartographie mondiale des unités de bioproduction DSM, Montreal Lilly, Merseyside Lonza, NH Powderject, Merseyside Abbott, Chicago Novo Nordisk, Denmark Avecia, Teesside Biogen, Denmark Diosynth, Holland Centocor, Holland Genzyme, Flanders Amgen, RI Wyeth, Ire Schering. P, Ire GSK, PA Eli Lilly, Ind Diosynth, NC Biogen NC IDEC, Cal Adgenix, Cal Diosynth NC Biogen NC Biolex NC Bayer NC Wyeth NC Amgen PR Chugai, Japan Genentech, Cal Amgen, Cal Baxter, Cal Biochemie, Austria HGS, MA 32 Centocor, PA Genentech, Spain Novartis Switzerland Serono, Switzerland Aventis, Germany BI, Germany

Les spécificités industrielles des biomédicaments : table ronde Marc de Garidel Dr Alain Clergeot Pr Félix Reyes Dr Annick Schwebig Dr philippe Pouletty Pierre-Noël lirsac

Biothérapies : des perspectives nouvelles pour les malades

Bioproduction : Un facteur clé du développement des entreprises émergentes

Investir : Les critères de choix des industriels en bioproduction

Bioproduction : Une place spécifique au sein des pôles de compétitivité ?

L’engagement de la France dans les biotechnologies Dr Pierre Le Sourd Président du Leem

L’incontournable évolution du progrès thérapeutique… ● Biomédicaments aujourd’hui : déjà 40 % des innovations mises à la disposition des patients ● Le marché du biomédicament à horizon 2010… ● Une accélération du développement : ► entre 82 et 137 nouveaux biomédicaments ● Des solutions nouvelles à des pathologies graves : ► 80% des biomédicaments commercialisés pour des pathologies sans solution thérapeutique satisfaisante ● Des perspectives économiques très prometteuses : ► 100 milliards $ (12% du marché mondial) ● … nécessitant un quadruplement des capacités 39 mondiales

… et la place de la R&D dans les activités de production ● La production de biomédicaments présente les caractéristiques d’une activité de R&D… ● Mais, au delà, produire les biomédicaments de demain, c’est préserver l’ensemble de la chaîne de valeur du progrès thérapeutique : - Recherche fondamentale / Recherche médicale / Recherche clinique - Recherche industrielle (process & production) / Fabrication - Accès aux soins ● Dans les phases de développement, l’accès stratégique à 40 des capacités de production pour des lots d’essais

La France menacée sur le front de l’innovation et de la production ● Sur le front de l’innovation : ● Biotechnologies : une industrie encore peu structurée ● Centres de recherche et pôles d’innovation : risque de délocalisation et de dépendance ● Compétitivité des essais cliniques : des signaux négatifs récents ● Sur le front de la production : ● Depuis près de 10 ans, un leadership français en Europe : ● … mais une position compétitive qui se dégrade ● … et une situation qui risque encore de s’accentuer si la France ne comble pas son retard en bioproduction 41
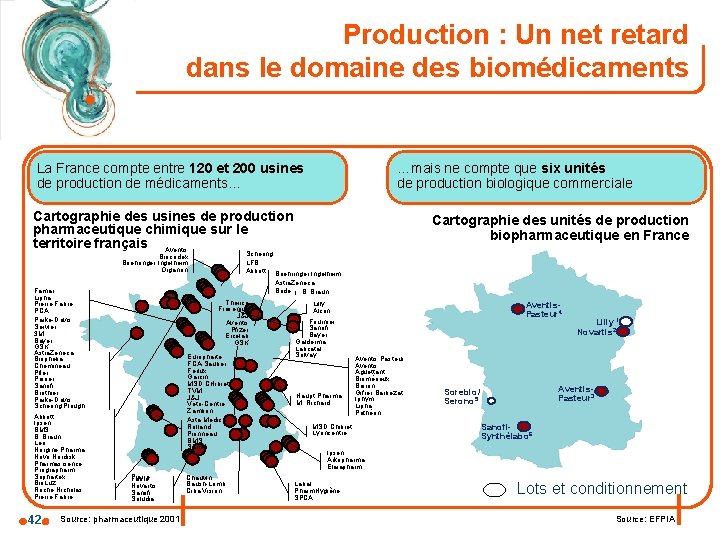
Production : Un net retard dans le domaine des biomédicaments La France compte entre 120 et 200 usines de production de médicaments. . . …mais ne compte que six unités de production biologique commerciale Cartographie des usines de production pharmaceutique chimique sur le territoire français Aventis Schering LFB Abbott Boehringer Ingelheim Biocodex Boehringer Ingelheim Organon Famar Lipha Pierre Fabre PCA Parke-Davis Servier 3 M Bayer GSK Astra. Zeneca Biophelia Chemineau Pfier Poirier Sanofi Brothier Parke-Davis Schering Plough Abbott Ipsen BMS B. Braun Leo Norgine Pharma Novo Nordisk Pharmascience Prographarm Sophartex Bio. Luz Roche Nicholas Pierre Fabre 42 Cartographie des unités de production biopharmaceutique en France Astra. Zeneca Bride B. Braun Therica Fresenius J&J Aventis Pfizer Ercelab GSK Europharte FCA-Sauber Ferlux Garcin MSD CHibret TVM J&J Veto-Centre Zambon Asta Medica Rolland Pionneau BMS Sanofi Pierre Fabre Novartis Sanofi Soludia Source: pharmaceutique 2001 Chauvin Baush-Lomb Ciba Vision Aventis. Pasteur 4 Lilly Alcon Fournier Sanofi Bayer Galderma Labcatal Solvay Haupt Pharma M. Richard Aventis Pasteur Aventis Aguettant Biomérieux Boiron Gifrer Barbezat Iphym Lipha Pathéon MSD Chibret Lyoncentre Lilly 1 Novartis 2 Aventis. Pasteur 3 Sorebio/ Serono 5 Sanofi. Synthélabo 6 Ipsen Arkopharma Elaiapharm Labal Pharm. Hygiène SPCA Lots et conditionnement Source: EFPIA
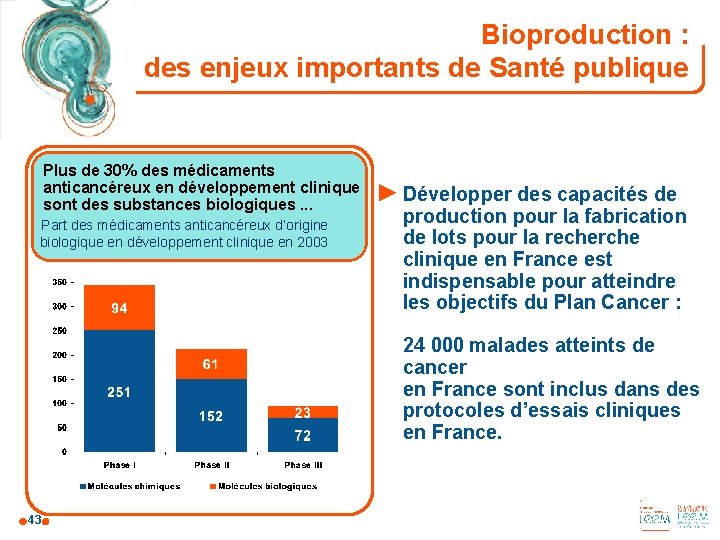
Bioproduction : des enjeux importants de Santé publique Plus de 30% des médicaments anticancéreux en développement clinique sont des substances biologiques. . . Part des médicaments anticancéreux d’origine biologique en développement clinique en 2003 ► Développer des capacités de production pour la fabrication de lots pour la recherche clinique en France est indispensable pour atteindre les objectifs du Plan Cancer : 24 000 malades atteints de cancer en France sont inclus dans des protocoles d’essais cliniques en France. 43

5 propositions du Leem Pour accélérer l’engagement de la France dans les biotechnologies

Proposition 1 Labelliser 2 à 3 pôles de compétitivité spécialisés en biotechnologies 45

Proposition 2 Reconnaître la dimension « Recherche » propre à la production des biomédicaments 46

Proposition 3 Créer un fonds de soutien pour faciliter la production de lots d’essais cliniques pour les premières phases de la recherche clinique 47

Proposition 4 Mettre en place des dispositifs financiers adaptés aux investissements requis par la production biologique 48

Proposition 5 Développer un plan stratégique national pour l’emploi et la formation 49

Biomédicaments : des perspectives enthousiasmantes ● Une opportunité de créer des dizaines de milliers d’emplois à haute valeur ajoutée ● Un renforcement de la chaîne du Progrès thérapeutique ● Une place émérite pour la France dans la nouvelle cartographie européenne des soins ● Une étape supplémentaire vers le développement d’une économie innovante 50

Philipe Douste-Blasy Ministre de la Santé et de la Protection Sociale

BIOMEDICAMENTS 2010 Enjeux et propositions pour favoriser l'attractivité de la France
- Slides: 52