Biomdecine quantitative Dveloppement dun mdicament Etudes Cliniques Exemple

Biomédecine quantitative Développement d’un médicament Etudes Cliniques Exemple des anti-cancéreux Pr Alain Duhamel : Biostatistique – Méthodologie Dr Nicolas Penel : Oncologie Médicale Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Plan Schéma général du développement d’un médicament Phase préclinique Etudes de phase I Méthodologie statistique générale Etudes de phase II – Méthodologie statistique Etudes de phase II – problématique et exemples cliniques Etudes de phase III – Méthodologie statistique Etudes de phase III – problématique et exemples cliniques Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
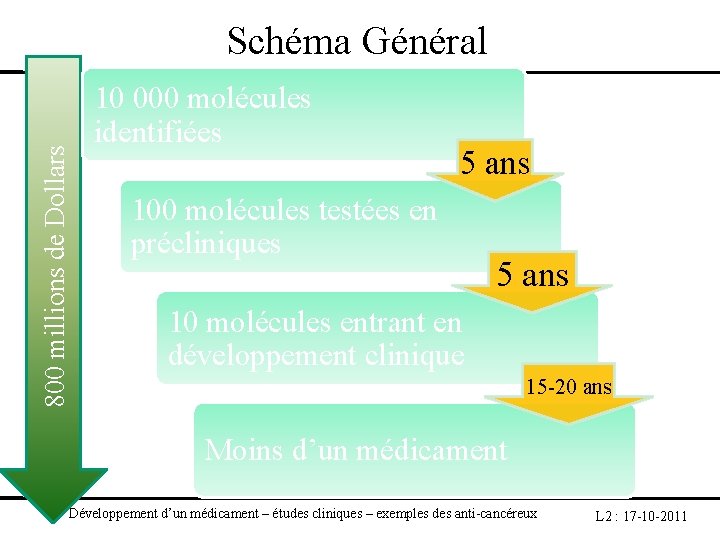
800 millions de Dollars Schéma Général 10 000 molécules identifiées 5 ans 100 molécules testées en précliniques 5 ans 10 molécules entrant en développement clinique 15 -20 ans Moins d’un médicament Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Schéma Général Phases Objectifs – Points-clés Les phases précliniques: In vitro puis in vivo Puis 4 phases cliniques 1 2 3 4 Définir la dose maximale tolérée & la dose recommandée pour les phases II (≈30 -40 pts) Déterminer l’activité et la tolérance d’un nouveau traitement sur une population clairement définie (≈40 -50 pts) Essais comparatifs - (randomisation) - Evaluation comparative des profils de tolérance et d’efficacité (≈100 -4000 pts) Evaluation post-marketing pour préciser le profil de toxicité/efficacité dans certaines populations particulières ou pour confirmer le bénéfice clinique Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Biomédecine quantitative Phase pré-clinique Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
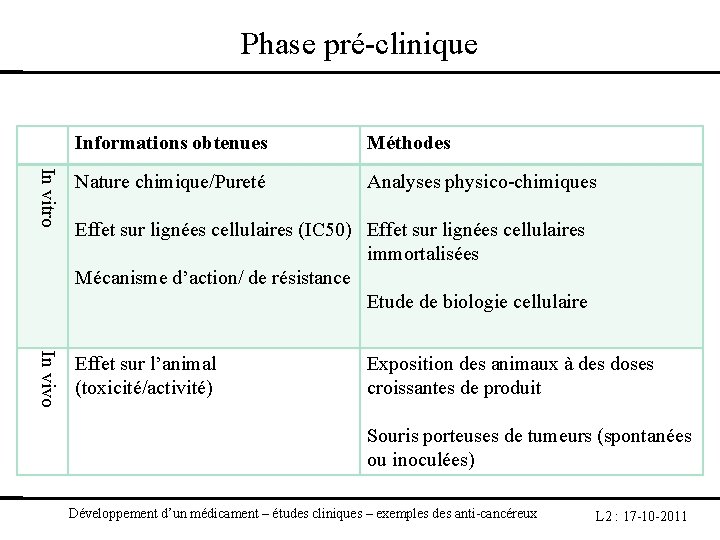
Phase pré-clinique Informations obtenues Méthodes In vitro Nature chimique/Pureté Analyses physico-chimiques In vivo Effet sur l’animal (toxicité/activité) Effet sur lignées cellulaires (IC 50) Effet sur lignées cellulaires immortalisées Mécanisme d’action/ de résistance Etude de biologie cellulaire Exposition des animaux à des doses croissantes de produit Souris porteuses de tumeurs (spontanées ou inoculées) Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
Phase pré-clinique Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
Poissons du fuseau: exemple • 4 familles • • Vinca-alcaloïdes Taxanes Epipodophyllotoxines Colchicine Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
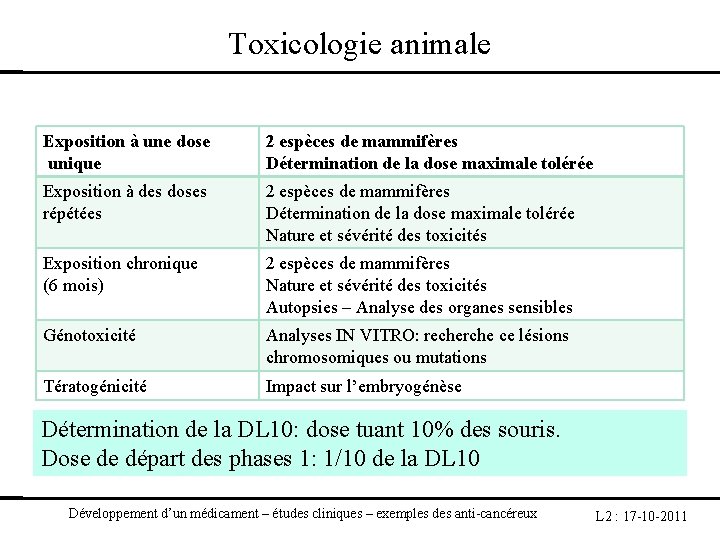
Toxicologie animale Exposition à une dose unique 2 espèces de mammifères Détermination de la dose maximale tolérée Exposition à des doses répétées 2 espèces de mammifères Détermination de la dose maximale tolérée Nature et sévérité des toxicités Exposition chronique (6 mois) 2 espèces de mammifères Nature et sévérité des toxicités Autopsies – Analyse des organes sensibles Génotoxicité Analyses IN VITRO: recherche ce lésions chromosomiques ou mutations Tératogénicité Impact sur l’embryogénèse Détermination de la DL 10: dose tuant 10% des souris. Dose de départ des phases 1: 1/10 de la DL 10 Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Biomédecine quantitative Etudes de Phase I Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Etudes de phases I: Pré-requis • La drogue – Caractérisation physico-chimique – Lignées cellulaires – Toxicologie animale • Les patients – Cancer en impasse thérapeutique – Bon état général – Constantes biologiques correctes Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase I : Méthodologie/mise en oeuvre • Quel est l’objectif principal d’une étude de phase I ? • ►Schéma recommandé pour les phases II • • • Quels sont les objectifs secondaires ? ► Caractériser et quantifier les toxicités ► Déterminer la dose maximale tolérée (DMT) ►Données Pharmacocinétiques ( A, D, M, E) ► Signe d’activité Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
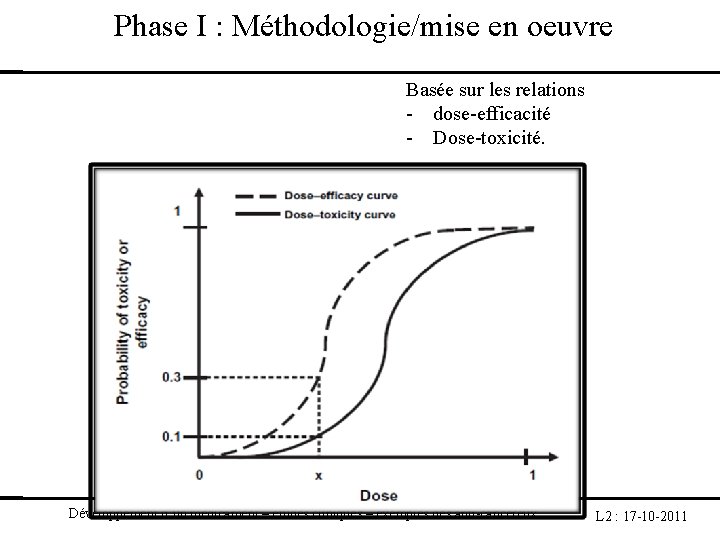
Phase I : Méthodologie/mise en oeuvre Basée sur les relations - dose-efficacité - Dose-toxicité. Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase I : Méthodologie/mise en oeuvre • Cohortes successives de patients (3) à des doses croissantes de produits jusqu’à atteindre un niveau pré-établi de toxicité définissant la Dose Maximale Tolérée (2 pts/3 ou 3/6 avec Dose-limiting toxicity DLT) • DLT définie en terme – Nature d’événement (ex. Neutropénie) – Sévérité (ex. grade 4) – +/-Durée (ex. de plus de 72 heures) Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase I : Méthodologie/mise en oeuvre Pt 1 Pt 2 Pt 3 Pt 4 Pt 5 Pt 6 X X X DLT X X X Passage au palier suivant X X DLT - - DMT DLT - Passage au palier suivant DMT ± Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase I : Méthodologie/mise en oeuvre Palier 1 Dose 1 RAS RAS Palier 2 Dose 1. 5 RAS RAS Palier 3 Dose 2 RAS RAS Palier 4 Dose 2. 3 RAS RAS ► Dose recommandée Palier 5 Dose 2. 6 DLT RAS DLT ► Dose maximale tolérée ± Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase I : Rapport bénéfice-Risque • Pourcentage de décès toxique: moins de 0, 5% • Toxicité sévère: ≈ 1 patient sur 6 • Stabilisation tumorale à 4 mois: 25 -30% Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase I : Attention ! • Pour les anticancéreux: études de phase 1 chez des patients atteints de cancer en situation d’impasse thérapeutique • Pour d’autres traitements: volontaires sains – exposition à des doses faibles et/ou pour des durées courtes (pharmacocinétique) Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Biomédecine quantitative Méthodologie Statistique Générale Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Etude clinique : nécessité de rédiger un protocole de recherche Le protocole est rédigé avant l’étude et il précise : Le rationnel : la question scientifique principale non résolue Les objectifs de l’étude • UN objectif principal : évaluer l’effet d’un traitement • UN critère de jugement principal : comment on mesure l’effet • Il peut exister des objectifs secondaires (phase III) Les critères d’inclusion et de non inclusion des patients dans l’étude Exemple : • Objectif principal : Phase I, détermination de la DMT pour un anti cancéreux. • Critère de jugement principal : taux d’évènements indésirables • Inclusion : Patient souffrant du cancer de la prostate en impasse thérapeutique • Non inclusion : patients cirrhotiques / présence d’un autre cancer … Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Etude clinique : nécessité de rédiger un protocole de recherche Le(s) groupe(s) de patients qui seront recrutés (plan expérimental) • Plan expérimental pour répondre de manière optimale à la question scientifique • Dépend de l’objectif principal • Exemple précédent : cohortes successives de 3 patients provenant de la même population statistique (impasse thérapeutique) Le nombre de sujets à recruter • Exemple précédent : cohortes successives de 3 patients jusqu’à arrêt par détermination de la DMT • Dans certains cas, le nombre de sujets à recruter peut se calculer a priori (phases II et III) Les « mesures » (prélèvements sanguins, IRM, . . ) effectuées chez les patients Les analyses statistiques qui seront effectuées Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Etude clinique : nécessité de rédiger un protocole de recherche Obligation médico-réglementaire : autorisation délivrée par le CPP (Comité de Protection des Personnes) Obligation méthodologique : définir les règles a priori pour minimiser les biais Etude sur des patients car variabilité inter individuelle Utilisation d’outils statistiques Utilisation du test statistique en phase II et III Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Le test statistique Un essai clinique est donc bâti pour répondre à une question Phase II : arrêter précocement le développement du médicament si effet insuffisant ou si mal toléré Phase III : preuve de l’efficacité En phase II et III, la conclusion est fondée sur un test statistique Principe du test statistique Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

PRINCIPE DU TEST STATISTIQUE TROIS PRINCIPES Outil pour répondre à une question : aide à la décision • Le nouveau traitement est-il meilleur que le traitement habituel ? Preuve expérimentale • Nécessité de prendre un « risque » (on dispose de mesures sur des groupes limités de patients) Test d’hypothèse (H 0 / H 1) • Les hypothèses sont déduites de la question Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
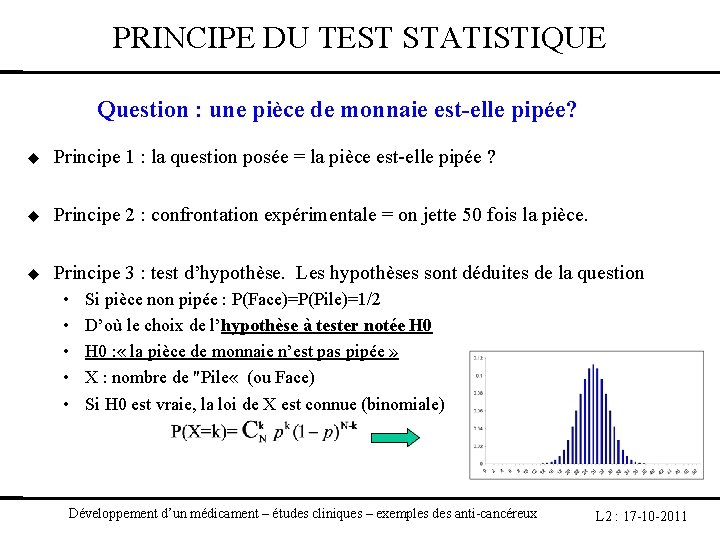
PRINCIPE DU TEST STATISTIQUE Question : une pièce de monnaie est-elle pipée? Principe 1 : la question posée = la pièce est-elle pipée ? Principe 2 : confrontation expérimentale = on jette 50 fois la pièce. Principe 3 : test d’hypothèse. Les hypothèses sont déduites de la question • • • Si pièce non pipée : P(Face)=P(Pile)=1/2 D’où le choix de l’hypothèse à tester notée H 0 : « la pièce de monnaie n’est pas pipée » X : nombre de "Pile « (ou Face) Si H 0 est vraie, la loi de X est connue (binomiale) Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Principe du test statistique : Notion de risque Si H 0 vraie, toutes les configurations sont possibles P(0 P)=(0, 5)50 Il faut décider : on choisit un risque raisonnable = 5% On partage l’ensemble des possibilités en 2 zones, selon le risque 5% : 18 P 25 P 32 P 0 P 50 P Compatible H 0 = 95% Très improbable sous H 0 = 5% de chance =REJET DE H 0 Limites de la zone compatible avec H 0 se déterminent grâce au calcul des probabilités. Ici 18 - 32 Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Principe du test statistique : Règle de décision Zone compatible avec H 0 = probabilité de 95% de se produire si H 0 vraie Zone de rejet de H 0 = probabilité de 5% de se produire si H 0 est vraie !!! (risque) Règle de décision : on fixe a priori la règle suivante : - Si le résultat de l’expérience se trouve dans la zone compatible avec H 0 (exemple 22 P), on ne décide rien ( « non significatif » ) - Si il se situe dans le zone « rejet de H 0» on déclare H 0 FAUSSE, donc on déclare H 1 vraie, mais au risque 5%. - Exemple : 15 P, on décide que la pièce est truquée RISQUE DE PREMIERE ESPECE = Probabilité de rejeter H 0 A TORT = 5% Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Principe du test statistique : résumé AVANT l’étude = on recrute des patients, on mesure le critère de jugement suivant le protocole Une question Choix de H 0 = permet de faire des prévisions Observations Si H 0 vraie : prévisions Confrontation aux prévisions Décision : Règle de décision -Rejet de H 0 : on décide H 1 avec un risque -Non rejet de H 0: observations compatibles avec H 0 Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Puissance d’un test = Proba (décider H 1 / H 0 est vraie) = risque de première espèce = Proba ( décider « compatible avec H 0 » / H 1 est vraie) = risque de deuxième espèce Puissance = 1 - = Proba ( décider H 1 / H 1 est vraie) Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Puissance d’un test Risque : Risque de conclure qu’il existe une différence alors qu’il n’y en a pas en réalité Risque : Risque de conclure à une absence de différence alors qu’il en existe une réellement. Puissance = 1 - : Probabilité de conclure à une différence si elle existe réellement. Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
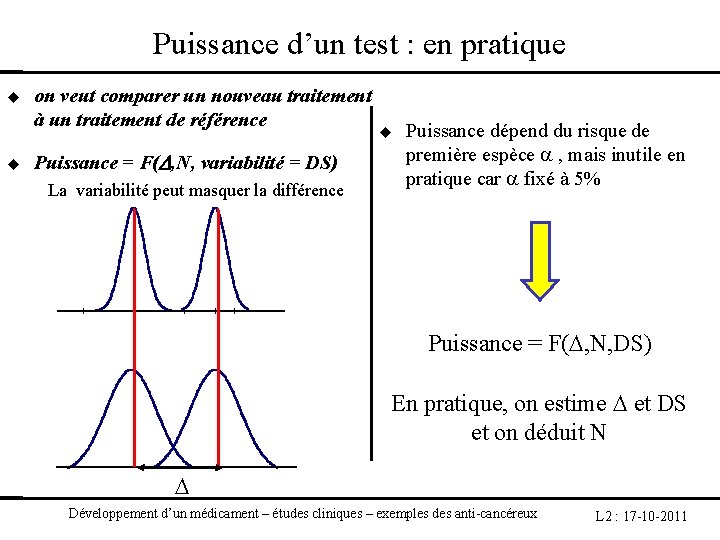
Puissance d’un test : en pratique on veut comparer un nouveau traitement à un traitement de référence Puissance = F( , N, variabilité = DS) La variabilité peut masquer la différence Puissance dépend du risque de première espèce , mais inutile en pratique car fixé à 5% Puissance = F( , N, DS) En pratique, on estime et DS et on déduit N Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Puissance d’un test : en pratique Les deux risques sont antagonistes = 0 =1 et = 0 = 1 Calcul du nombre de sujets à recruter : • on fixe =5% • on se donne sur critères cliniques (il faut des données : littérature, étude précédente) • on estime DS (il faut des données : littérature, étude précédente) • on a donc « la main » que sur N : • on calcule N pour assurer = 10% ou 20% (puissance > 80%) Formules, tables, logiciels Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Biomédecine quantitative Etudes de phase II – Méthodologie Statistique Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phases II : Principes Généraux La question : première étude d’efficacité du traitement Objectif : déterminer si un nouveau traitement est suffisamment efficace pour passer en Phase III Un seul groupe de patients sélectionnés (exemple patients en échec thérapeutique) Critère de jugement binaire (efficacité selon des critères normalisés) • Exemple : taux de réponse au traitement (RECIST) Hypothèse : p <= p 0 versus p >= p 1 • p : efficacité observée du traitement évalué: inefficacité m • p 0 : en dessous de p 0, le traitement n’est pas assez efficace (efficacité miminale) • p 1 : efficacité attendue • p 1 – p 0 analogue de et permet de calculer le nombre de sujets pour et donnés Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phases II : principes généraux Option 1 : on recrute n patients et on fait l’analyse en fin d’essai. On en conclue alors p>p 0 ou p<p 0. Option 2 : on divise les n patients et on réalise l’étude en plusieurs étapes. On parle alors d’essai séquentiel. Intérêt des essais séquentiels • Arrêt précoce en cas de forte efficacité ou forte inefficacité. • Avantages éthiques, économiques et gain de temps Règles d’arrêt ? Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase II - Essai séquentiel : Principe général Pour un nombre d’étapes données (souvent 2 ou 3), pour , , p 0 et p 1 donnés, on peut calculer un nombre total de sujets potentiellement nécessaires On inclut n 1 sujets dans l’étape 1 et selon le nombre de réponses r 1, on ajoute ou non une seconde étape avec n 2 sujets, etc jusqu’au nombre total calculé A chaque étape k , on compare le nombre de succès observés rk aux nombres de succès attendus sous les hypothèses p 0 et p 1 (ak et bk). • Si rk > bk on stoppe pour efficacité • Si rk<ak, on stoppe pour inefficacité • Si rk entre ak et bk, on continue en incluant n 2 sujets Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase II : Les principaux plans séquentiels Plan de Gehan (1961) : 2 étapes Arrêt précoce si longue série d’échec Plan de Fleming (1982) : k étapes (k<5) Arrêt précoce pour des valeurs extrêmes de p (inefficacité ou efficacité) Plans de Simon (1989) : 2 étapes Arrêt précoce si produit inefficace Plan de Ensign (1994) : 3 étapes Arrêt précoce si longue série d’échec et si produit inefficace …. Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Biomédecine quantitative Etudes de phase II – problématique et exemples cliniques Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Etude de Phase II: Principe général Arrêter précocément le développement d’un traitement non efficace ou non faisable Si positive: phase III Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Etude de phase II : Principe général • Basée sur un critère rapidement obtenu, standardisé, mesurant de manière non ambigue l’effet du traitement: exemple réduction du volume tumoral (RECIST) • Sur une population très sélectionnée • A la dose définie dans la phase 1 Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
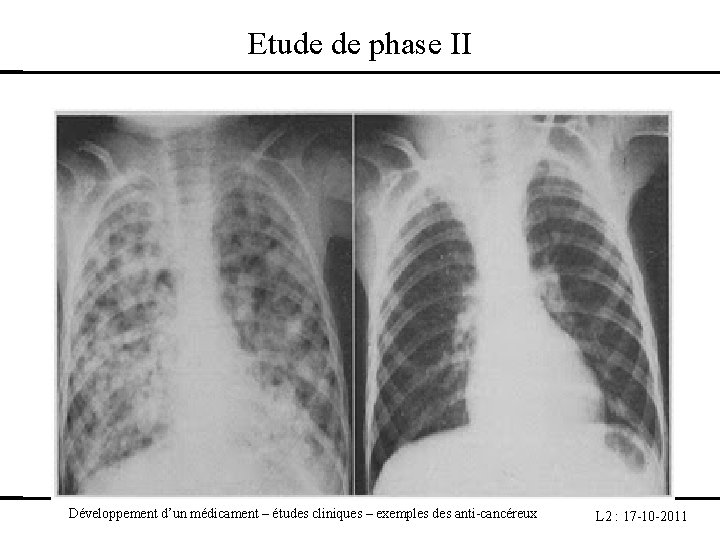
Etude de phase II Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
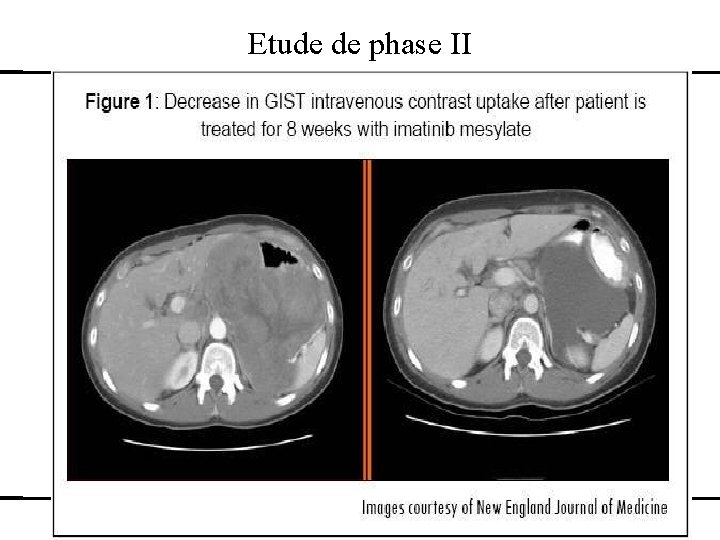
Etude de phase II Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Etude de phase II Il n’y a pas de traitement efficace connu dans cette situation On considère qu’un traitement donnant moins de 10% de réponse objective serait décevant. P 1=15% et p 0=10% Risque Alpha de 5% et risque Béta de 10%. Nombre de sujets nécessaires 50 Plan en une étape Un traitement inefficace est rejeté si ≥ 7/50 Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
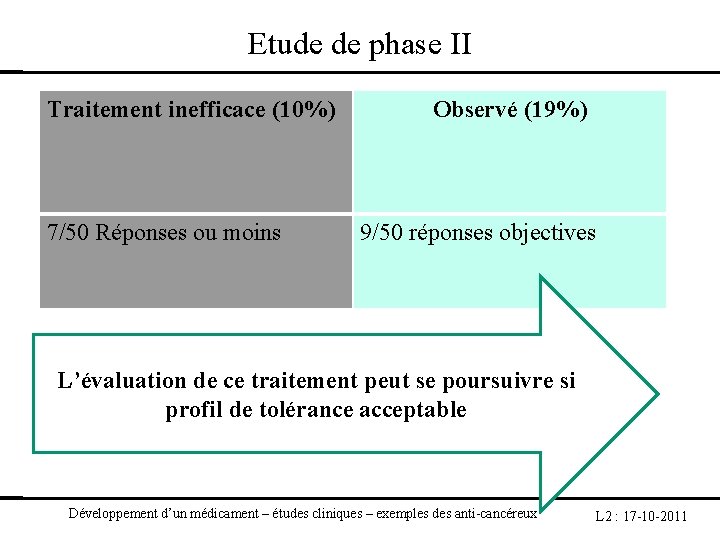
Etude de phase II Traitement inefficace (10%) 7/50 Réponses ou moins Observé (19%) 9/50 réponses objectives L’évaluation de ce traitement peut se poursuivre si profil de tolérance acceptable Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Biomédecine quantitative Etudes de phase III – Méthodologie Statistique Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase III : Principes Généraux La question : preuve de l’effet du traitement Pourquoi une étude comparative? • Evolution spontanée de la maladie • Effet placebo Souvent 2 groupes : un groupe reçoit le traitement à tester et un groupe reçoit le traitement de référence (ou un placebo) Plan d’expérience • Constitution de 2 groupes par tirage au sort (randomisation : voir application clinique) Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase III : Principes Généraux Critère de jugement divers : • Binaire • Numérique • Survie Objectif principal: cher à démontrer qu’un nouveau traitement T est meilleur qu’un traitement de référence R sur le critère de jugement. On réalise un test statistique Hypothèse H 0 : T=R et on cherche à rejeter l’hypothèse Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase III : Nombre de sujets à inclure dans l’étude On a déterminé le problème clinique On a déterminé le(s) critère(s) de jugement On a défini le plan d’expérience adapté Il faut calculer le nombre de patients à inclure pour répondre correctement à l’hypothèse posée (se garantir une « puissance » suffisante ) Il existe des formules et des logiciels Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011

Phase III : Nombre de sujets à inclure dans l’étude Comparaison de deux antihypertenseurs avec : : 5 mm de mercure • Ecart-type (DS): 10 mm • Risque de première espèce ( ): 5% 1 - = 0. 9 N 1=N 2=86 L’étude a été réalisée sans calcul de puissance préalable sur 2 groupes de 30 sujets. Puissance = 1 - = 0. 48 Ne pas confondre : Conditions d’application du test et Puissance du test Développement d’un médicament – études cliniques – exemples des anti-cancéreux L 2 : 17 -10 -2011
- Slides: 49