Biologia do desenvolvimento 20132014 Actina e o Desenvolvimento
Biologia do desenvolvimento 2013/2014 Actina e o Desenvolvimento Docente: Paulo de Oliveira Discentes : Maria João nº 30440 Marisa Ribeiro nº 30792

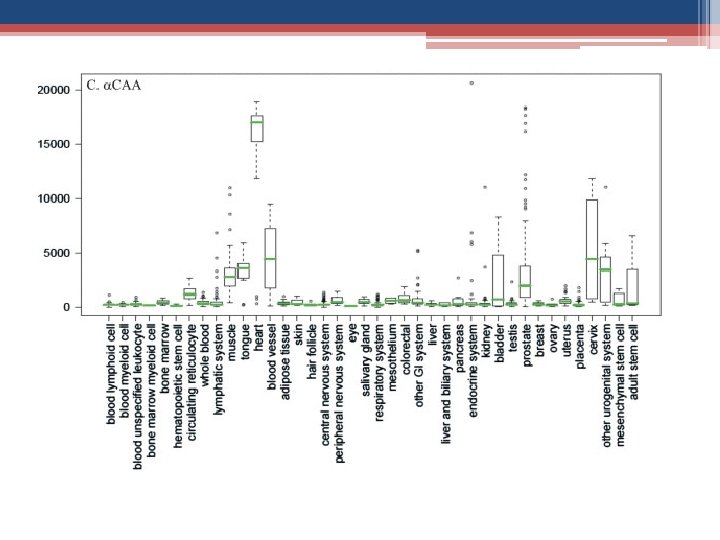
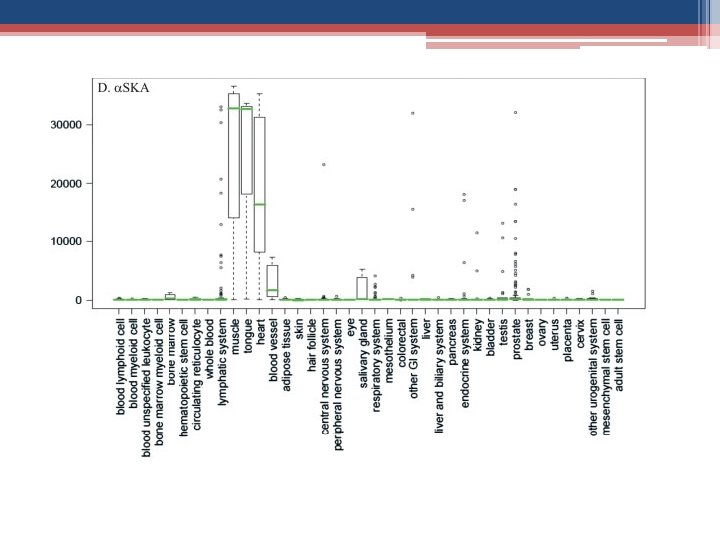
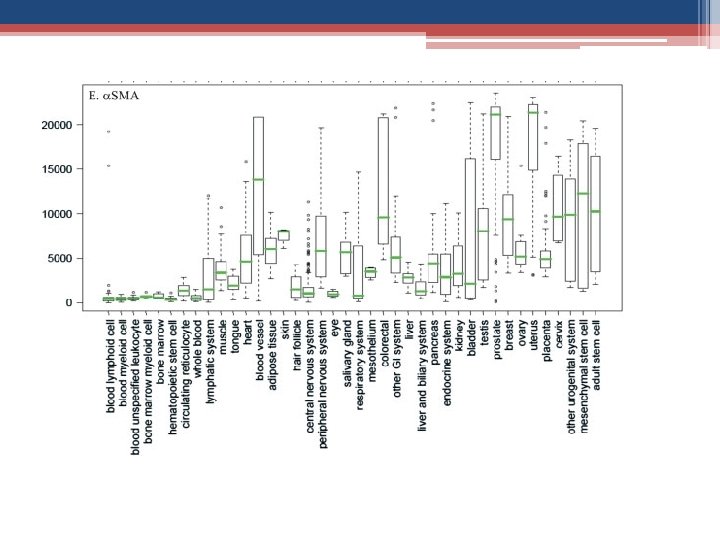
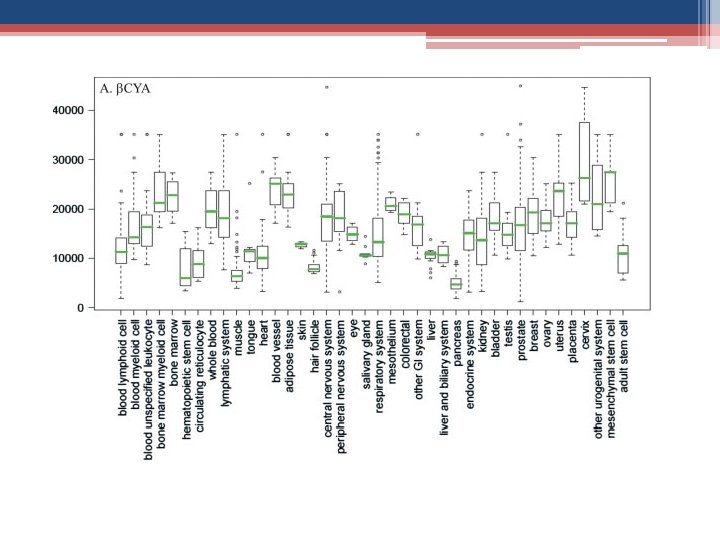
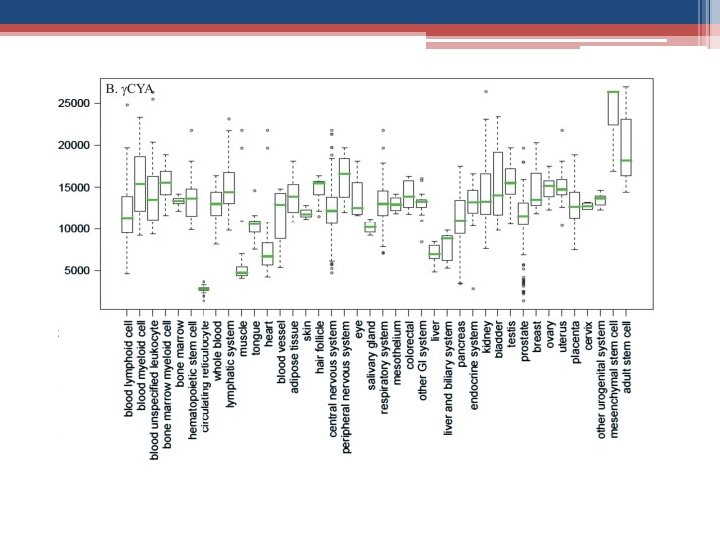
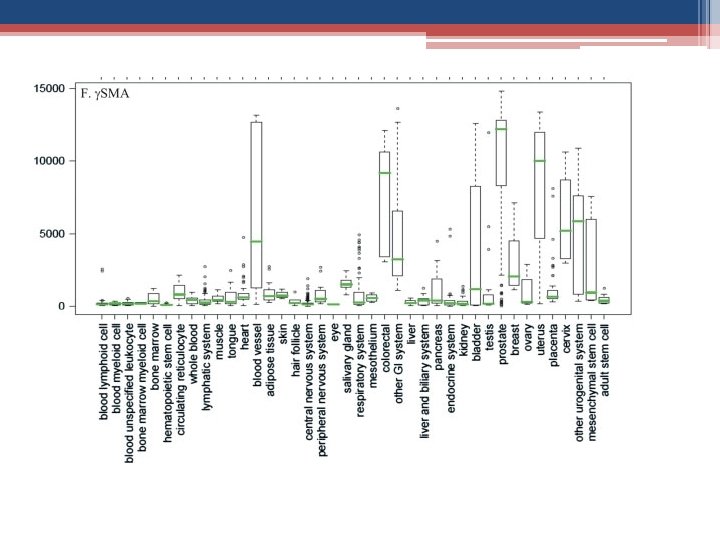
A actina é uma proteína que, em conjunto com a miosina e moléculas de ATP, gera movimentos celulares e musculares. A actina polimerizada forma os microfilamentos de actina importantes na composição do citoesqueleto. Nos seres humanos existem 6 isoformas de actina: • αCAA – α actina do músculo cardíaco • αSKA – α actina do músculo esquelético • αSMA – α actina do musculo liso • βCYA – β actina citoplasmática • γCYA – γ actina citoplasmática • γSMA – γ actina do musculo liso
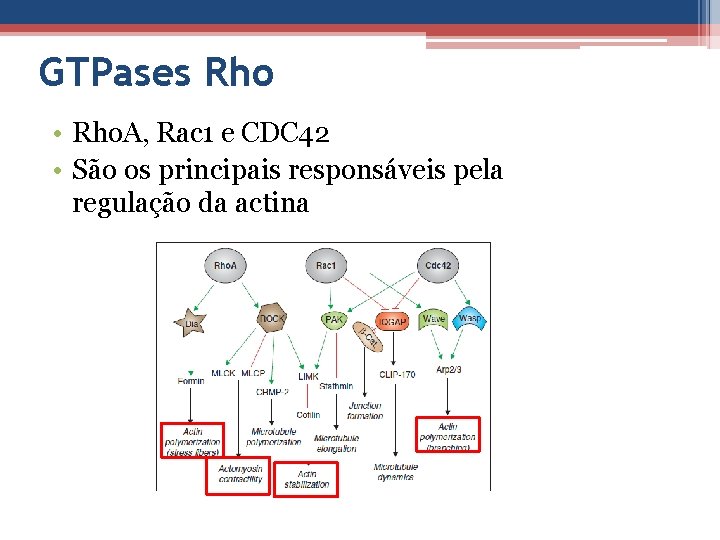
GTPases Rho • Rho. A, Rac 1 e CDC 42 • São os principais responsáveis pela regulação da actina
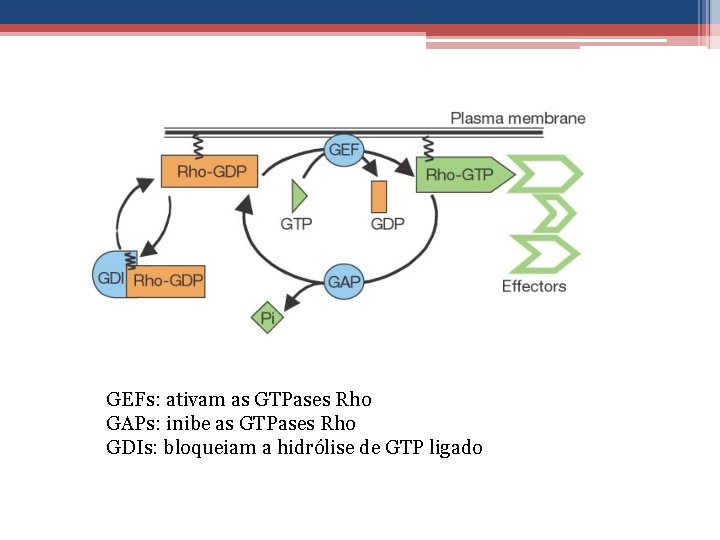
GEFs: ativam as GTPases Rho GAPs: inibe as GTPases Rho GDIs: bloqueiam a hidrólise de GTP ligado

Actina-F • A actina-F em conjunto com a miosina II geram forças corticais que influenciam: § as propriedades hidrodinâmicas do citoplasma; § formas das saliências da membrana celular; § diferenciação de stem cells • A contração da actina-F é um mecanismo importante para a constrição apical das camadas epiteliais.

Profilinas • São proteínas que estão presentes nos animais, incluindo nos seres humanos; • Reguladores da polimerização de actina; • Núcleos interfásicos, por todo o citoplasma e perto do córtex das células em diferentes estádios de maturação do oócito, na fertilização e no desenvolvimento embrionário. • É detectada na fase de blastocisto, onde a profilina localiza a massa celular interna;

• Os anticorpos anti-profilina inibem desenvolvimento normal do embrião; o

Tipos de Profilina: Profilina I • Todas as fazes embrionárias; • Quase todos os tipos de células; • Quase todos os tecidos. Profilina II • Sistema nervoso. Profilina III • Testículos.

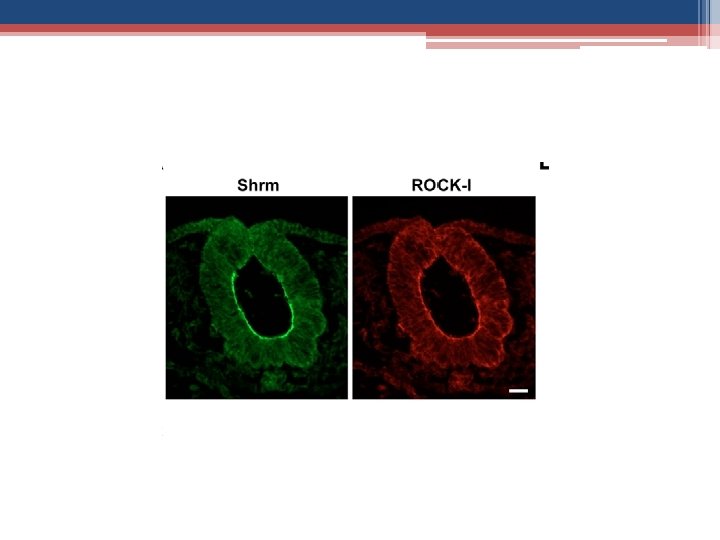
Invaginação do tubo neural • Shroom 3, uma proteína de ligação de actina, é responsável pela constrição apical epitelial juntamente com o aumento da acumulação de miosina 2. • Esta proteína está localizada no complexo das junções apicais do tubo neural e sua ausencia provoca defeitos de encerramento do tubo neural. • Shroom 3 recruta ROCK para as junções apicais. • A ativação de Rho 1 e ROCK na junção da célula, leva à invaginação da camada mesodérmica.

β actina no desenvolvimento da crista neural • A formação da crista neural é induzida pela interação de sinalizações vindas da placa neural e do tecido ectodérmico não neuronal. • A β actina é fundamental para a sobrevivência da células da crista neural, na fase inicial de desenvolvimento. • A β actina promove a expressão da caderina, que é fundamental para a adesão das células pré-migratórias e regula a sinalização de Rho.
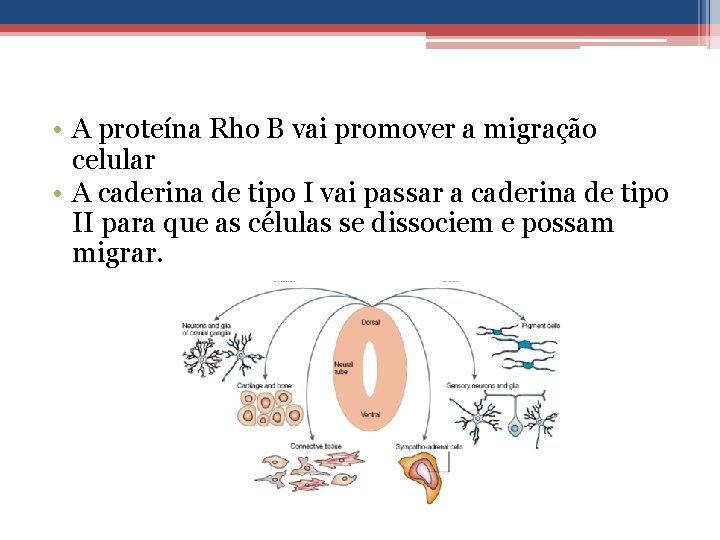
• A proteína Rho B vai promover a migração celular • A caderina de tipo I vai passar a caderina de tipo II para que as células se dissociem e possam migrar.
Desenvolvimento dos neuronios • Durante o desenvolvimento, a maioria dos neurónios do SNC polarizam para elaborar um axónio e múltiplos dendritos. • GTPases Rho, surgiram como integradores chave de estímulos ambientais para regular os citoesqueletos do axónio e dendrites. Células multipolares rapidamente Neurites Axónio Dias mais tarde Dendrites

Desenvolvimento neuronal • Ativação localizada da GTPase Rac 1 contribui para o rápido alongamento do axónio. Esta é regulada através de GEFs Rac – específicas: Ø Tiam – 1 e um Tiam related protein-1: afeta polarização neuronal através da reorganização da actina Ø STEF: remodelação da actina para promover a elongação do futuro axônio. • A ativação de uma sinalização Rac controla a remodelação da actina contribui para o desenvolvimento do axônio. • DOCK 7 (Rac específico – GEF) regula a atividade Rac para inativar microtúbulos, desestabilizar proteína stathmin/Op 18 e promover a formação de axônio.

Cancro • Alteração na actina do citoesqueleto causa mudanças na adesão celular, migração e invasão, resultando em metástase, neoangiogénese e infiltração de células imunes. • O aumento da expressão de ROCK e Rho está associada a estágios avançados de cancro humano, incluindo a invasão e metástase, mas não afeta iniciação do tumor e o desenvolvimento.

Rho no cancro • Rho A está associada a estágios avançados de cancro humano, incluindo a invasão e metástase de células germinativas • Rho. C está associada a um fenótipo móvel e invasivo de células de cancro da mama, sugerindo um papel significativo para Rho. C na progressão, mas não de iniciação de cancro. • Rho. B tem sido demonstrado que têm efeitos inibitórios sobre a migração, invasão e metástase de células de cancro humano através da supressão da via Ras/PI 3 quinase / Akt.

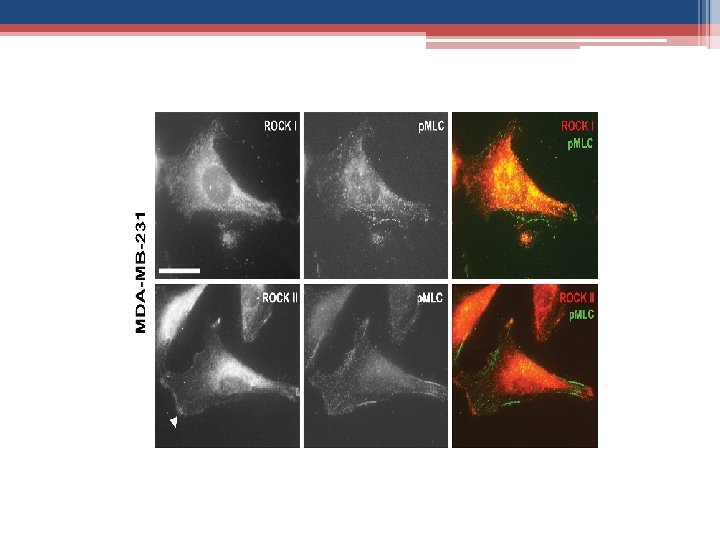
ROCK no cancro Mutações no gene ROCK I : • Interrupção prematura da tradução em Y 405 e S 1126 no cancro da mama • Substituição de prolina 1193 para uma serina em cancro do pulmão Mutações em ROCK II: • Interrupção prematura da tradução Y 1174 e S 1194 P no cancro do estomago • Interrupção prematura da tradução em W 138 em cancro do pulmão O aumento da expressão de ROCK II vai provocar o aumento da rigidez do ECM , através da deposição de colagénio e ROCK I vai aumentar a densidade do ECM.

Referências: • Chen Jian, Guerriero Emily, Sado Yoshikazu, Sundar. Raj Nirmala (Agosto 2009); “Rho-Mediated Regulation of TGF-1– and FGF-2–Induced Activation of Corneal Stromal Keratocytes” • Tondeleir Davina et al (2009); “Actin Isoform Expression Patterns During Mammalian Development and in Pathology: Insights From Mouse Models” • Shaheen Ranad et al (Agosto 2011); “Recessive Mutations in DOCK 6, Encoding the Guanidine Nucleotide Exchange Factor DOCK 6, Lead to Abnormal Actin Cytoskeleton Organization and Adams-Oliver Syndrome” • Tondeleir Davina, Rivka Noelanders, Karima Bakkali, Christophe Ampe (Janeiro 2014), “Beta-Actin Is Required for Proper Mouse Neural Crest Ontogeny” • Nishimura Tamako, Takeichi Masatoshi (Fevereiro 2008); “Shroom 3 -mediated recruitment of Rho kinases to the apical cell junctions regulates epithelial and neuroepithelial planar remodeling” • Diensthuber Ralph P. et al (26 Julho 2013); “Distinct Functional Interactions between Actin Isoforms and Nonsarcomeric Myosins” • Govek Eve-Ellen, Newey Sarah E. , Aelst Linda Van (2005), “The role of the Rho GTPases in neuronal development” • Morgan-Fisher Marie, Wewer Ulla M. , Yoneda Atsuko (2012); “Journal of Histochemistry & Cytochemistry” • Röper Katja (2013); “Supracellular actomyosin assemblies during development”

• Ramachandran C. , Patil R. V. , Combrink K. , Sharif N. A. , Srinivas S. P. , (2011); “Rho-Rho kinase pathway in the actomyosin contraction and cellmatrix adhesion in immortalized human trabecular meshwork cells” • Rawe Vanessa Y. , Payne Christopher, Shatten Gerald, ( 20 Janeiro 2006); “Profilin and actin-related proteins regulate microfilament dynamics during early mammalian embryogenesis” • Samuel Michael S et al (Junho 2011); “Actomyosin-mediated cellular tension drives increased tissue stiffness and β-catenin activation to induce interfollicular epidermal hyperplasia and tumor growth” • Wiggan O’Neil (Março 2012); “ADF/Cofilin regulates actomyosin assembly through competitive inhibition of myosin II binding to F-actin” • Lessey Elizabeth C. et al (setembro 2012), “From mechanical force to Rho. A activation” • Baranwal Somesh ( 24 Julho 2012), “Nonredundant roles of cytoplasmic β- and γ-actin • isoforms in regulation of epithelial apical junctions” • Sato Akira et al (2006); “Profilin is an effector for Daam 1 in non-canonical Wnt signaling and is required for vertebrate gastrulation” • Shindo Asako, Wallingford John B. , (7 Fevereiro 2014); “PCP and Septins Compartmentalize Cortical Actomyosin to Direct Collective Cell Movement” • Simões Sérgio de Matos, Mainieri Avantika, Zallen Jennifer A. (17 Fevereiro 2014); “Rho GTPase and Shroom direct planar polarized actomyosin contractility during convergent extension” • Perrin Benjamim J, Ervasti James M. (30 Julho 2010); “The Actin Gene Family: Function Follows Isoform”
- Slides: 26