BIOLOGA MOLECULAR EN HEMOGLOBINOPATAS RICARDO MOLINA GASSET HOSPITAL

BIOLOGÍA MOLECULAR EN HEMOGLOBINOPATÍAS RICARDO MOLINA GASSET HOSPITAL VIRGEN DE LOS LIRIOS MAYO 2019

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS HEMOGLOBINA ØProteína globular de 6, 4 nm diámetro ØEstructura: Ø 4 cadenas polipeptidicas de globina (2 alfa y 2 Beta) Ø 4 grupos Hemo unidos por interacciones hidrofóbicas Concentración: 13 – 18 g/dl en el hombre y 12 – 16 g/dl en la mujer. ØCaracterísticas: o. Transporte Oxígeno/CO 2 o. Capacidad de “captar” y “ceder “ oxígeno o. Capacidad amortiguadora por captación de H+ o. Gran solubilidad ØEstados de la Hb en los globulos rojos: o. Oxihemoglobina (oxidada): rojo intenso o. Dexosihemoglobina (reducida): rojo oscuro *sangre arterial *sangre venosa
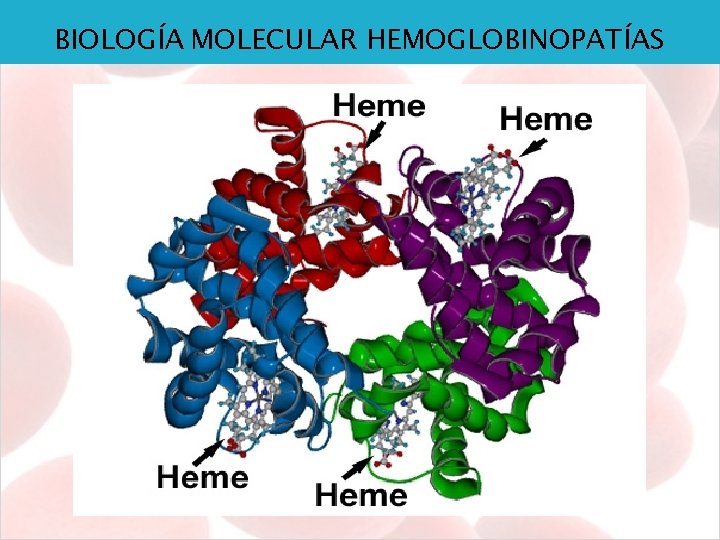
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
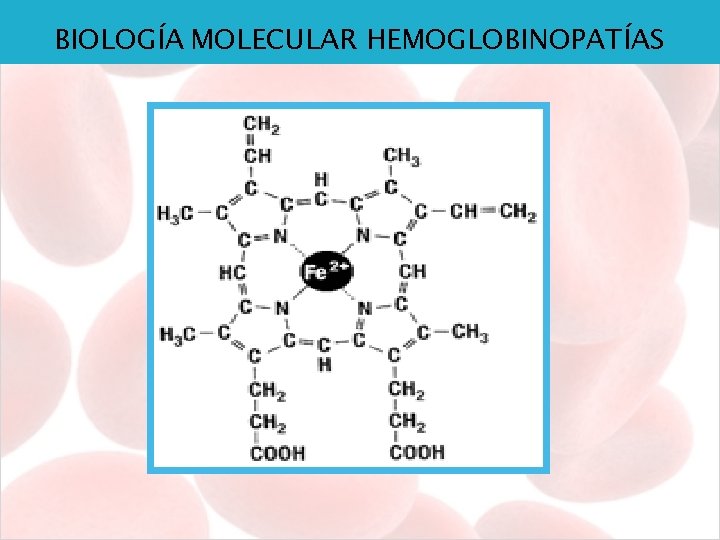
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
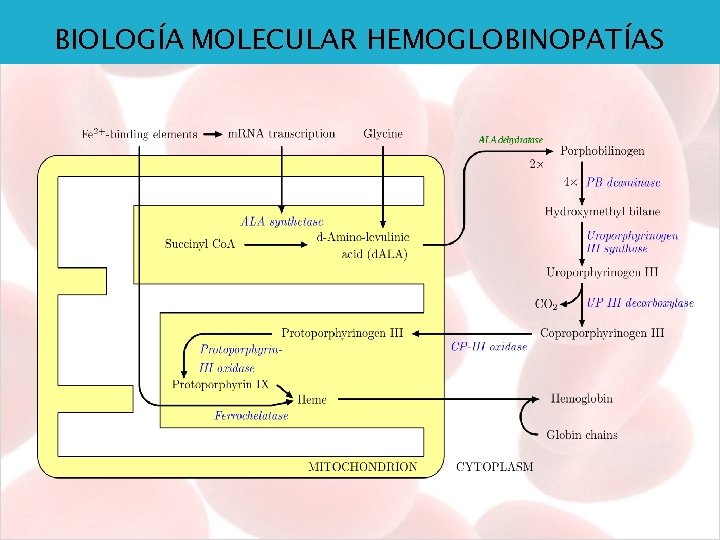
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
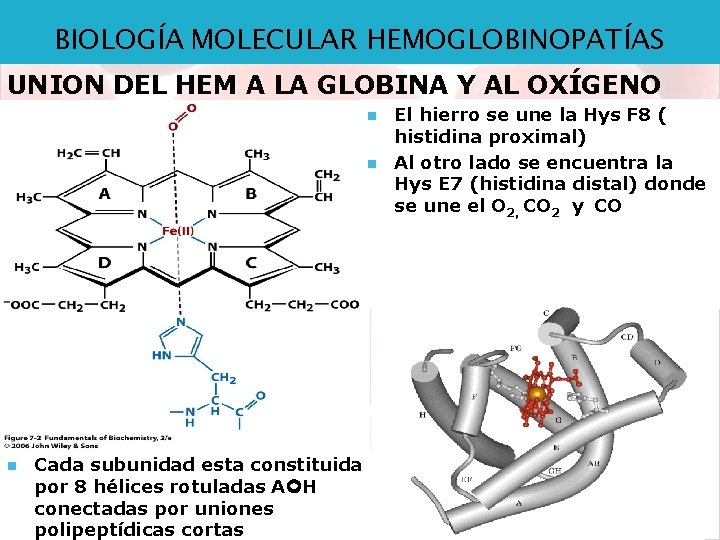
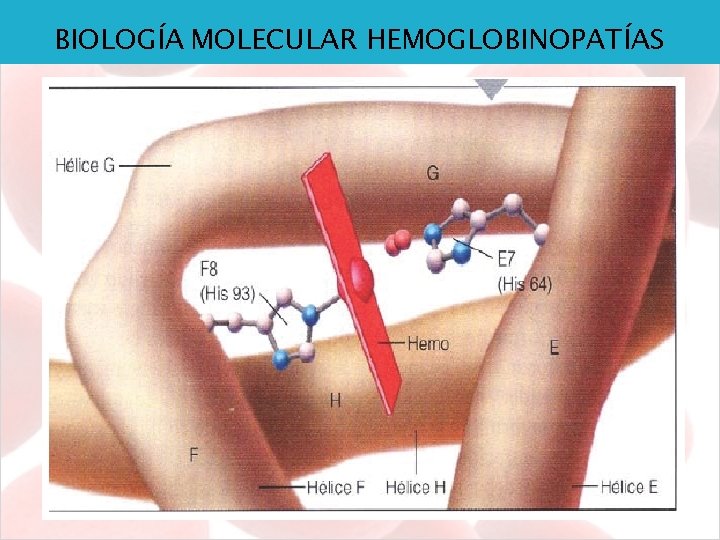
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS UNION DEL HEM A LA GLOBINA Y AL OXÍGENO n n n Cada subunidad esta constituida por 8 hélices rotuladas A H conectadas por uniones polipeptídicas cortas El hierro se une la Hys F 8 ( histidina proximal) Al otro lado se encuentra la Hys E 7 (histidina distal) donde se une el O 2, CO 2 y CO
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
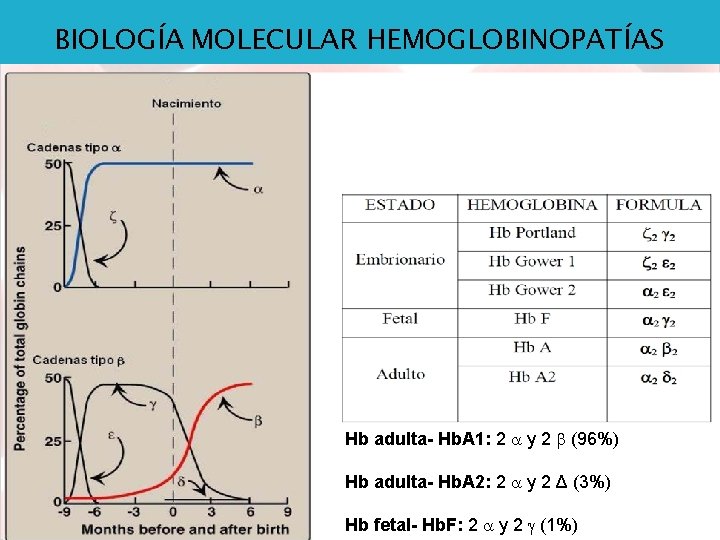
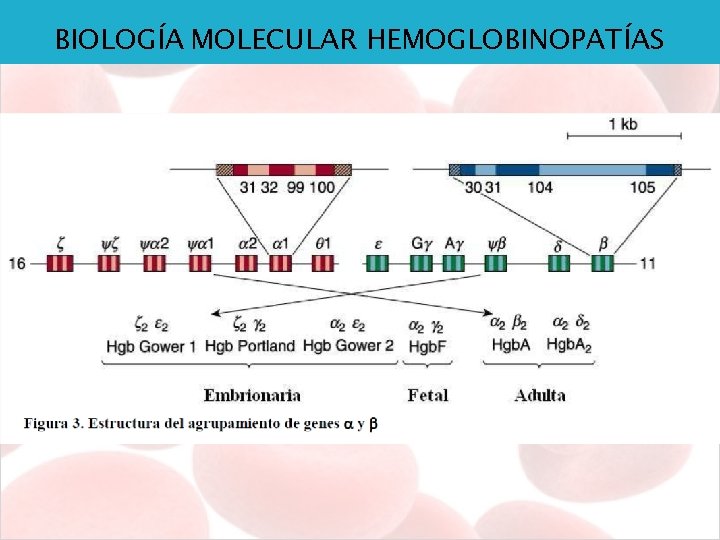
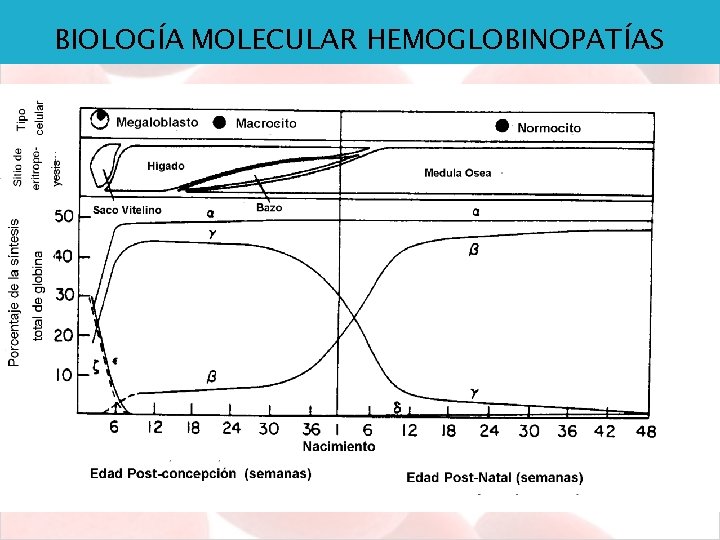
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Hb adulta- Hb. A 1: 2 y 2 (96%) Hb adulta- Hb. A 2: 2 y 2 Δ (3%) Hb fetal- Hb. F: 2 y 2 (1%)

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS ALTERACIONES CUALITATIVAS Hemoglobinopatías estructurales ALTERACIONES CUANTITATIVAS Síndromes Talasémicos Caracteristicas: ØFormas sintomatología, leves y formas graves como los síndromes talasémicos y enfermedad células falciformes ØEnfermedades ØAutosómicas, hederitarias monogénicas mas comunes en el mundo mayoritariamente recesivas ØProblema de salud púbica en: Sudeste asiático, oriente medio, mediterraneo, subcontinente indio, Africa y Caribe Ø 250 millones personas hemoglobina patológica potencialmente portadores de una
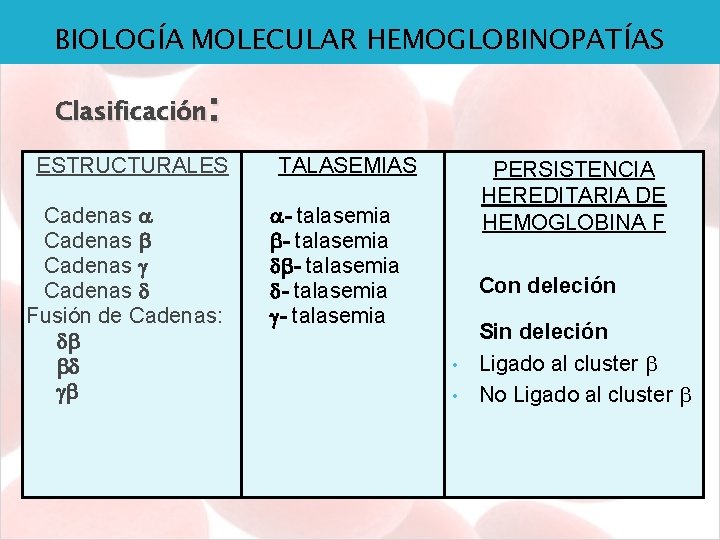
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS : Clasificación ESTRUCTURALES Cadenas Fusión de Cadenas: TALASEMIAS PERSISTENCIA HEREDITARIA DE HEMOGLOBINA F - talasemia - talasemia Con deleción • • Sin deleción Ligado al cluster No Ligado al cluster

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Clasificación según patología molecular: Ø Sustituciones de una única base. Hb. S, HBC, Hb E Ø Variantes de cadena de hemoglobina elongadas (cadenas alargadas). Hb CS Ø Cadenas de globinas truncadas (deleción de fragmentos). Hb Leiden, Gun Hill Ø Hemoglobinas de fusión (hibridización anómala). Hb Lepore Ø Talasemias
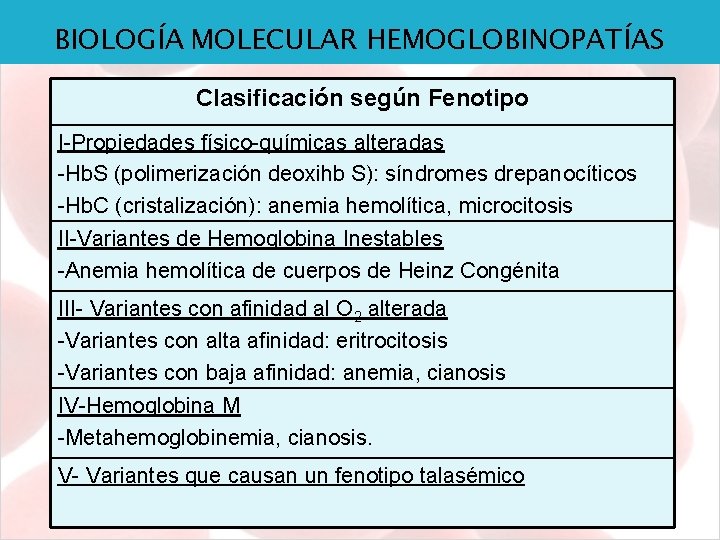
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Clasificación según Fenotipo I-Propiedades físico-químicas alteradas -Hb. S (polimerización deoxihb S): síndromes drepanocíticos -Hb. C (cristalización): anemia hemolítica, microcitosis II-Variantes de Hemoglobina Inestables -Anemia hemolítica de cuerpos de Heinz Congénita III- Variantes con afinidad al O 2 alterada -Variantes con alta afinidad: eritrocitosis -Variantes con baja afinidad: anemia, cianosis IV-Hemoglobina M -Metahemoglobinemia, cianosis. V- Variantes que causan un fenotipo talasémico

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS I-Propiedades físico-químicas alteradas Ø Defecto de carácter hereditario Ø Tiene como consecuencia una estructura anormal en una de las cadenas de las globina Ø Simple cambio de un aminoácido en una de las cadenas de globina Ø Se han descrito mas de 1300 variantes Ø Mayoría variantes asintomáticas Ø Afectación de la cadena beta (gen HBB) son más frecuentes y con mayor significado clínico
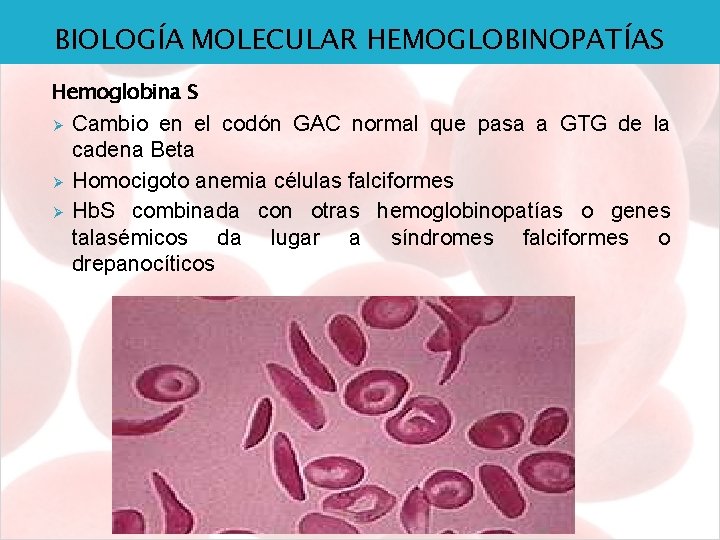
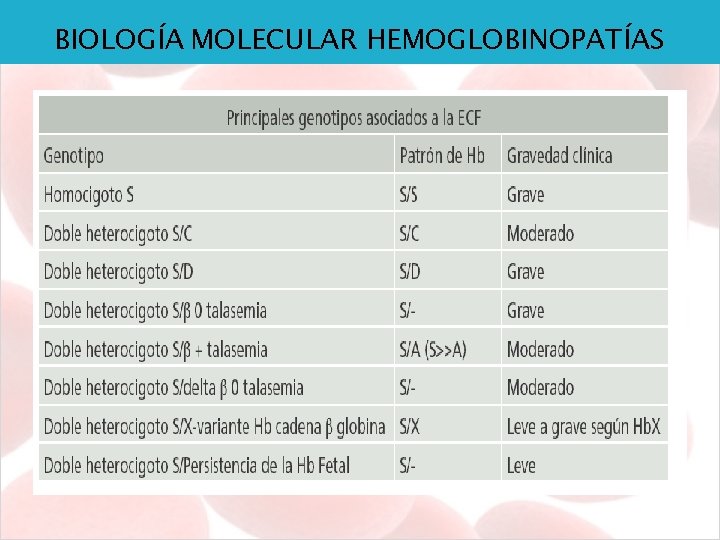
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Hemoglobina S Ø Ø Ø Cambio en el codón GAC normal que pasa a GTG de la cadena Beta Homocigoto anemia células falciformes Hb. S combinada con otras hemoglobinopatías o genes talasémicos da lugar a síndromes falciformes o drepanocíticos Glóbulo rojo en forma de hoz

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Anemia Falciforme o Drepanocítica. Ø Pauling, 1949 Ø Enfermedad hereditaria, autosómica recesiva Ø Raza negra Ø La anomalía se sitúa en la cadena beta, cuya glutamina es sustituida por valina Ø Primeros síntomas después de 3 meses debido al efecto protector de la Hb. F
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
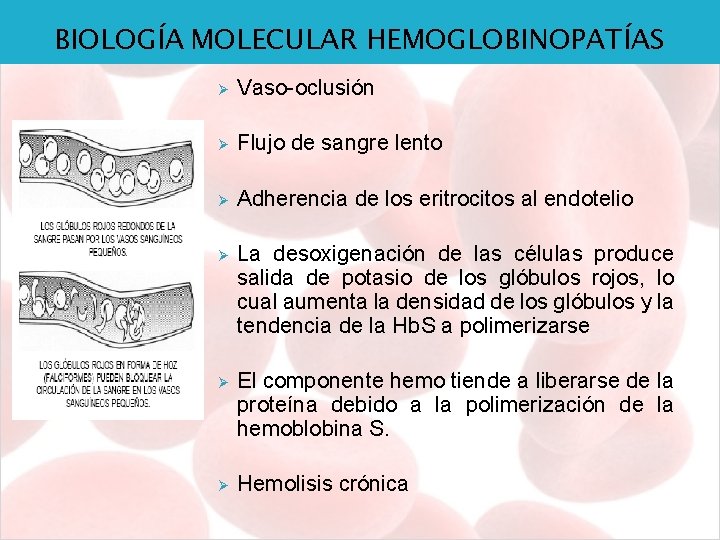
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Ø Vaso-oclusión Ø Flujo de sangre lento Ø Adherencia de los eritrocitos al endotelio Ø La desoxigenación de las células produce salida de potasio de los glóbulos rojos, lo cual aumenta la densidad de los glóbulos y la tendencia de la Hb. S a polimerizarse Ø El componente hemo tiende a liberarse de la proteína debido a la polimerización de la hemoblobina S. Ø Hemolisis crónica
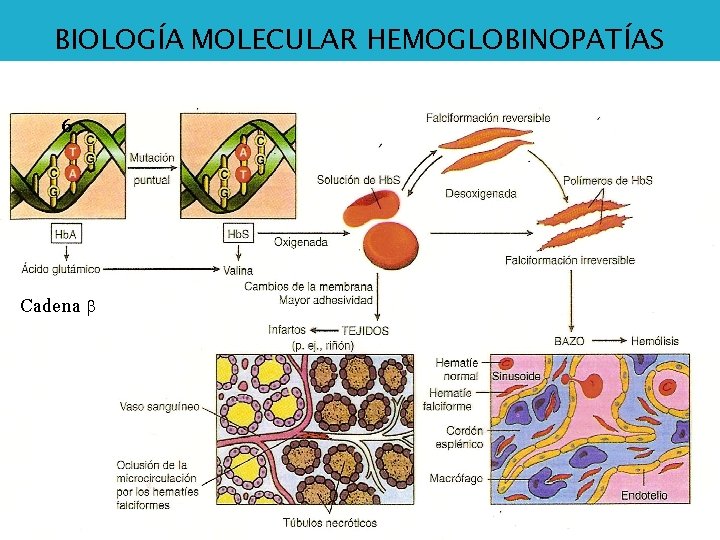
Anemia. MOLECULAR Falciforme, Drepanocítica, BIOLOGÍA HEMOGLOBINOPATÍAS en Forma de Hoz (sickle), o Hb. S 6 Cadena

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Ø Vaso-oclusión y hemolisis: ◦ Varia entre pacientes ◦ Dos modificadores principales Capacidad innata para producir Hb. F Coexistencia con alfa talasemias Ø Las técnicas de secuenciación masiva han identificado variantes genéticas en las que está modulada la expresión clínica de la ECF

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Hemoglobina C ØSe caracteriza por la sustitución del ácido glutámico de la cadena beta por lisina ØEl estado homocigoto (CC) se caracteriza por una ligera anemia hemolítica crónica con esplenomegalia; la vida media del eritrocito esta disminuida ØEl estado heterocigoto (AC) no produce trastorno alguno. ØSus síntomas incluyen un mayor riesgo de que se produzcan infecciones y un bazo agrandado

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Hemoglobina D Ø Mutación Ácido glutámico por glutamina ◦ D-los Ángeles = D-Punjab ◦ Mas de 7 diferentes Hb D de acuerdo a la posición de la mutación) Ø Frecuencia – localización: Anormalidad normalmente en India. Ø Signos Clínicos y biológicos : Heterocigota: o Asintomática, o Fracción Hb A: 65 – 70 % , Fracción Hb D: 30 – 35 % Homocigota: o Anemia muy ligera o Ausencia de fracción Hb A Fracción Hb D 100 %

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS II-Variantes de Hemoglobina Inestables ØLas hemoglobinopatías inestables obedecen a mutaciones en la zona de unión de globina-hemo que desestabilizan la molécula de Hb. ØSe facilita su desnaturalización y la formación de precipitados intraeritrocitarios. ØPatrón de herencia es autosómico dominante ØReducción de la vida media del eritrocito. ØAnemia hemolítica crónica de intensidad variable ØCrisis de agudización en procesos infecciosos febriles y/o tras la ingesta de medicamentos oxidantes. ØSe han descrito hasta 151 mutaciones responsables hemoglobinopatías inestables en los genes α 1, α 2 y β globinas ØLas mutaciones “de novo” son relativamente frecuentes. de

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS HBB c. 128 T>C clínica grave. HBB c. 295 G>A clínica leve
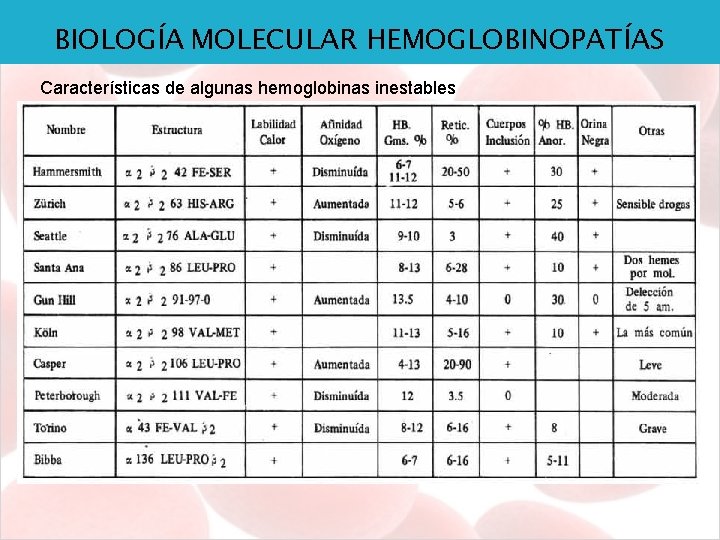
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Características de algunas hemoglobinas inestables
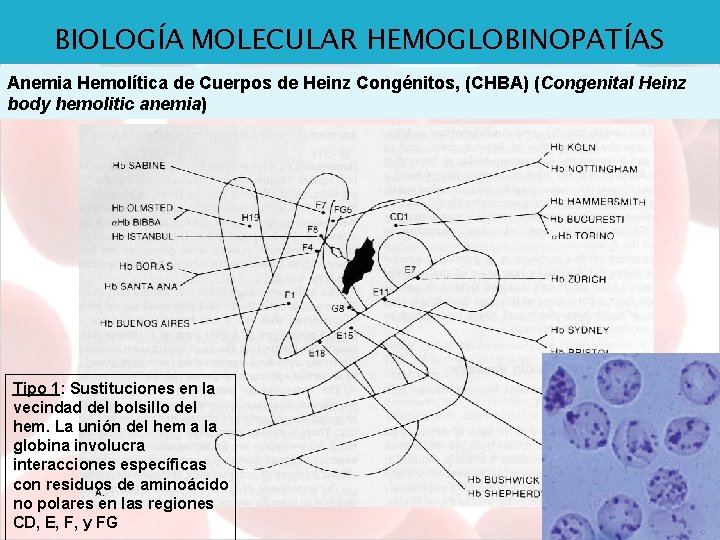
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Anemia Hemolítica de Cuerpos de Heinz Congénitos, (CHBA) (Congenital Heinz body hemolitic anemia) Tipo 1: Sustituciones en la vecindad del bolsillo del hem. La unión del hem a la globina involucra interacciones específicas con residuos de aminoácido no polares en las regiones CD, E, F, y FG
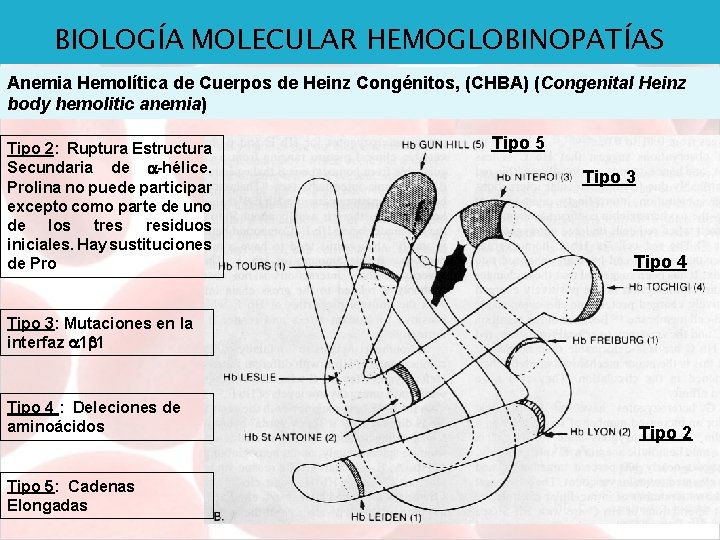
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Anemia Hemolítica de Cuerpos de Heinz Congénitos, (CHBA) (Congenital Heinz body hemolitic anemia) Tipo 2: Ruptura Estructura Secundaria de -hélice. Prolina no puede participar excepto como parte de uno de los tres residuos iniciales. Hay sustituciones de Pro Tipo 5 Tipo 3 Tipo 4 Tipo 3: Mutaciones en la interfaz 1 1 Tipo 4 : Deleciones de aminoácidos Tipo 5: Cadenas Elongadas Tipo 2

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS III- Variantes con afinidad al O 2 alterada ØSon debidas a mutaciones que afectan a regiones de la molécula relacionadas con los cambios conformacionales que se producen en el proceso de fijación reversible del oxígeno. ØHemoglobinas con alta afinidad por el oxígeno: o Más frecuentes o Cursan con una eritrocitosis como consecuencia de la hipoxia tisular (ejemplo la Hb Barcelona HBB c. 283 G>C) ØHemoglobinas de baja afinidad: o Disminución en el número de hematíes y de hemoglobina (falsa anemia), (ejemplo la Hb Vigo HBB c. 200 A>T)

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS IV-Hemoglobina M o metahemoblobina ØEl ion ferroso (Fe 2+) del grupo hemo se oxida al estado férrico (Fe 3+). Esto convierte la hemoglobina en metahemoglobina. ØCausa una disminución de la capacidad de liberar oxígeno a los tejidos (hipoxia) ØLa formación espontánea de metahemoglobina se reduce normalmente a través de la donación de electrones por la NADH metahemoglobinareductasa o el ácido ascórbico o los sistemas de enzimas glutatión ØLos sistemas enzimáticos de metahemoglobina a menos del 1%. protección, mantienen los niveles de Metahemoglobinemia congénita o. Autosomico recesivo o Debido a una deficiencia de la enzima NADH metahemoglobina reductasa Metahemoglobinemia adquirida. o. La exposición a drogas exógenas oxidantes y sus metabolitos (benzocaina, dapsona, nitratos) aceleran la velocidad de formación de metahemoglobina hasta mil veces, superando el sistema protector de enzimas.

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Estudio molecular hemoglobinopatías estructurales ØLa Hb. S, Hb. C, Hb. D y Hb. E se agrupan en el conjunto de hemoglobinopatías con alteración de carga superficial ØPresentan cambios aminoacídicos en la superficie de la molécula con carga eléctrica diferente a la normal. ØPueden detectarse mediante HPLC, electroforesis en geles o la electroforesis capilar. ØHomocigoto de la Hb. S, facil detectable ØDoble heterocigoto Hb. S/β 0: o. Gravedad similar al homocigoto S. o. Dificil diagnóstico (=patrón de Hb. S que el homocigoto S) ØRealizar siempre que sea posible el estudio familiar del paciente con el objetivo de separar los defectos genéticos y facilitar su identificación

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS ØPara identificar mutaciones puntuales de hemoglobinopatías estructurales: o. Secuenciación SANGER de las regiones promotora, exónicas e intrónicas flanqueantes del gen de la β globina o. Si se asocia con beta talasemia discriminaríamos la presencia de mutaciones puntuales responsables de β-talasemia pero no la de grandes deleciones o. Técnicas alelo específicas como ARMS, RFLP o RT-PCR. ØEn ausencia de estudio familiar, la interpretación de los resultados: o. Mediante ARMS, RFLP o RT-PCR posibilidad de falsos positivos para la homozigosis de la Hb. S : o. Hb. S se encuentre combinada con un alelo β afectado por una β-talasemia que englobe el codon 6 o. Gran deleción como en el caso de la δβ -talasemia o. Persistencia hereditaria de la Hb. F.

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Talasemias Ø Defecto en las cadenas alfa y/o beta. Ø Mas de 500 mutaciones responsables de talasemia Ø Mutaciones puntuales/deleciones de los genes de las globinas: Ø o Ausencia o disminución de la síntesis de las cadenas de globina o Desequilibrio en la síntesis de las cadenas Los síndromes graves: afectos 2 genes β, o bien 3 -4 de los genes α Efectos patológicos asociados: o Daño en los precursores eritroides o Eritropoyesis inefectiva o Daño en los eritrocitos maduros o Anemia hemolítica. o Microcitosis o Hipocromia Se dividen en: 1. Alfa talasemias 2. Beta talasemias

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
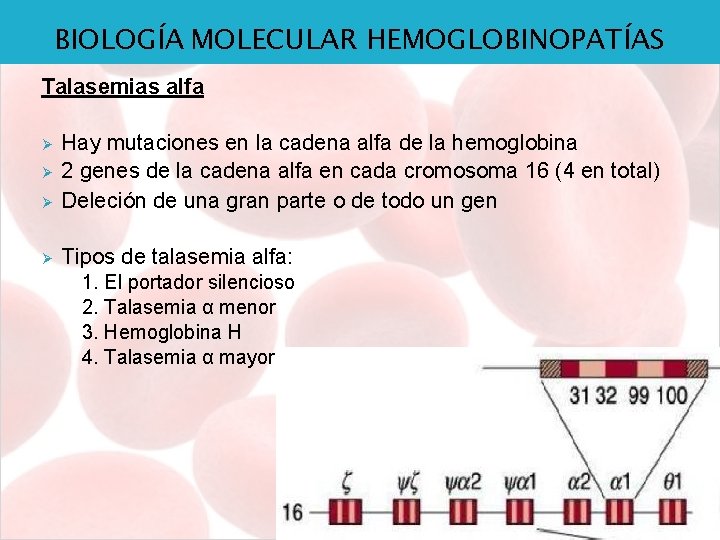
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Talasemias alfa Ø Hay mutaciones en la cadena alfa de la hemoglobina 2 genes de la cadena alfa en cada cromosoma 16 (4 en total) Deleción de una gran parte o de todo un gen Ø Tipos de talasemia alfa: Ø Ø 1. El portador silencioso 2. Talasemia α menor 3. Hemoglobina H 4. Talasemia α mayor
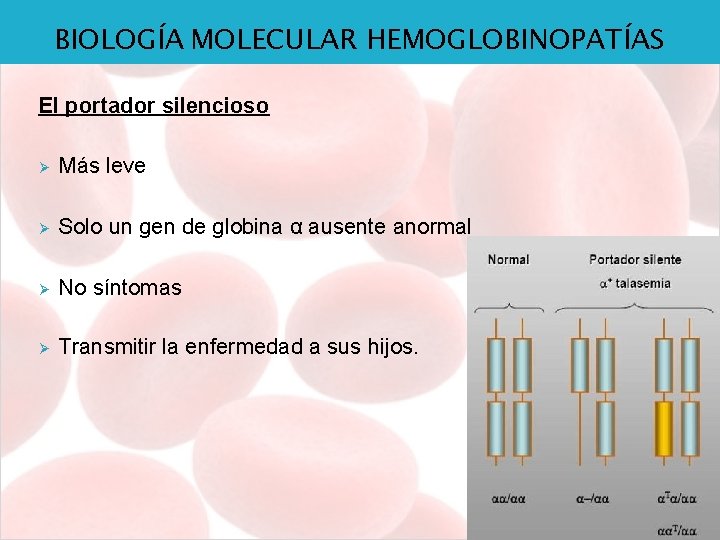
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS El portador silencioso Ø Más leve Ø Solo un gen de globina α ausente anormal Ø No síntomas Ø Transmitir la enfermedad a sus hijos.
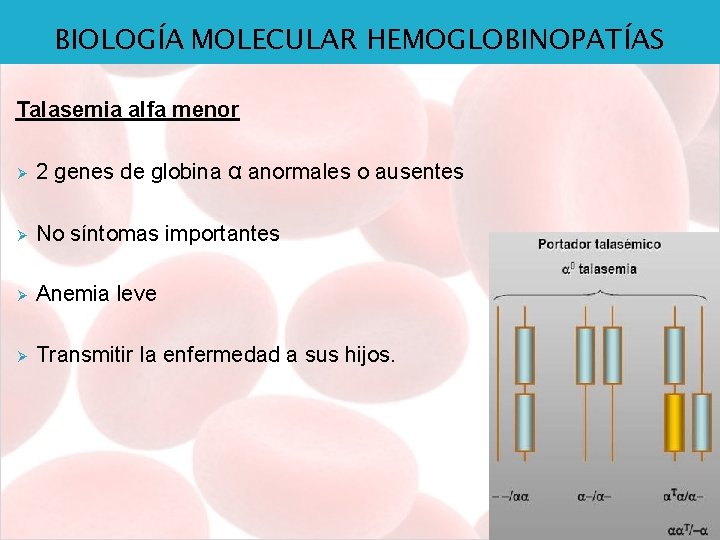
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Talasemia alfa menor Ø 2 genes de globina α anormales o ausentes Ø No síntomas importantes Ø Anemia leve Ø Transmitir la enfermedad a sus hijos.
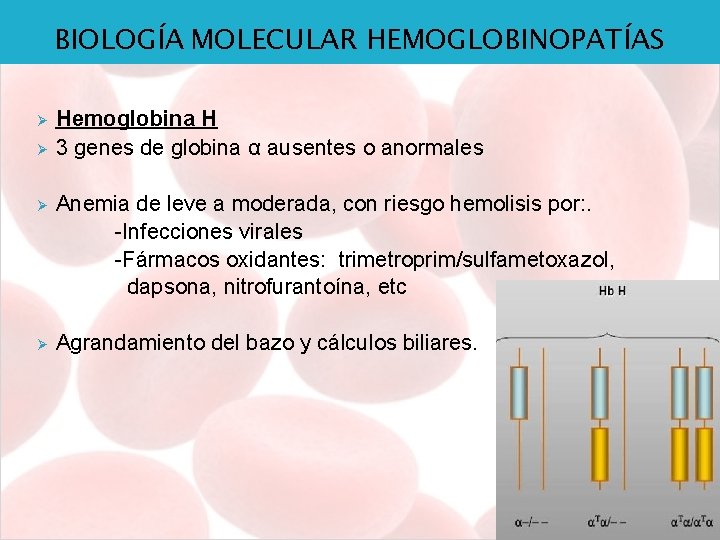
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Ø Ø Hemoglobina H 3 genes de globina α ausentes o anormales Ø Anemia de leve a moderada, con riesgo hemolisis por: . -Infecciones virales -Fármacos oxidantes: trimetroprim/sulfametoxazol, dapsona, nitrofurantoína, etc Ø Agrandamiento del bazo y cálculos biliares.
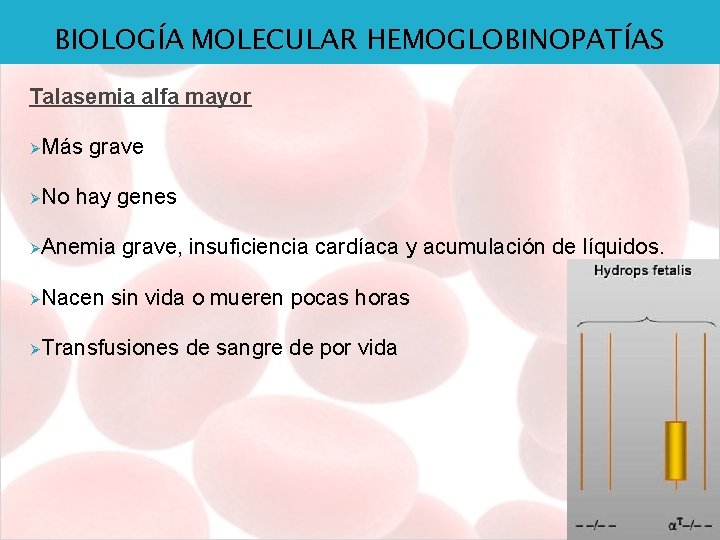
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Talasemia alfa mayor ØMás ØNo grave hay genes ØAnemia ØNacen grave, insuficiencia cardíaca y acumulación de líquidos. sin vida o mueren pocas horas ØTransfusiones de sangre de por vida

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS ØEl mecanismo molecular de la α-talasemia predominantemente por grandes delecciones: es Afectan a un solo gen α globina (α 1 o α 2), deleciones -3. 7 Kb y -4. 2 Kb, conocidas como mutaciones α+. o Ambos genes α globina (α 1 y α 2), mutaciones -MED; MEDII, -SEA; -FIL; -THAI; -20. 5, DUTCH I, conocidas como mutaciones α 0. o ØPara la identificación de grandes delecciones se usan técnicas alelo específicas: GAP-PCR, múltiple o sencilla, o. MLPA para cribado de grandes delecciones no conocidas. o

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS ØUna minoría se producen por mutaciones puntuales: o. Las que afectan al gen α 2 son más graves que las que afectan al gen α 1 y a las α 1 deleción, ya que el gen α 2 se expresa entre 2 -3 veces más que el gen α 1. Ø Las mutaciones α globina no delecionales pueden caracterizarse mediante: o. Secuenciación SANGER de las regiones promotora, exónicas e intrónicas flanqueantes de los genes α 1 y α 2 globina Mediante técnicas dirigidas concretas como RFLP. o a identificar mutaciones
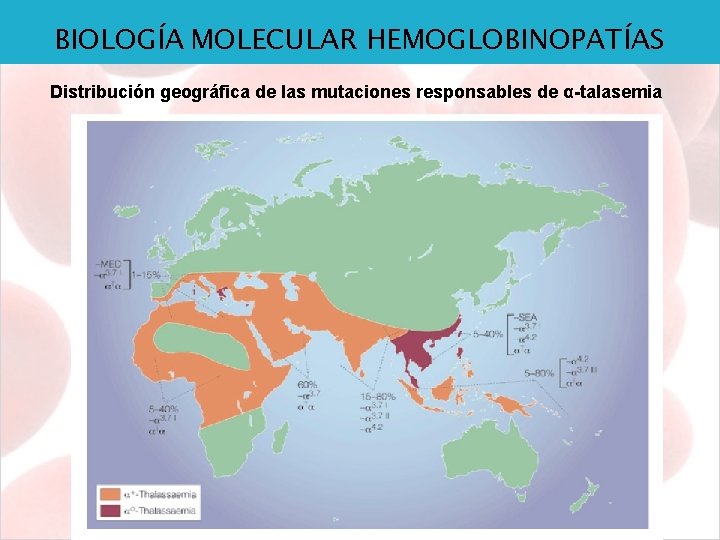
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Distribución geográfica de las mutaciones responsables de α-talasemia

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Talasemias beta ØMecanismo molecular a mutaciones puntuales: o. Sustituciones de una única base nitrogenada Deleciones o inserciones muy cortas que alteran la transcripción o la maduración del RNAm. o ØDentro de los síndromes β-talasémicos se encuentran asociaciones entre genes β-talasémicos y genes δβ-talasémicos, como la Hb Lepore. ØOcho mutaciones se consideraban responsables de más del 90 % de las β-talasemias de la región mediterránea. ØLos flujos inmigratorios han variado el mapa mutacional de la βtalasemia en España, incrementando su heterogeneidad molecular.
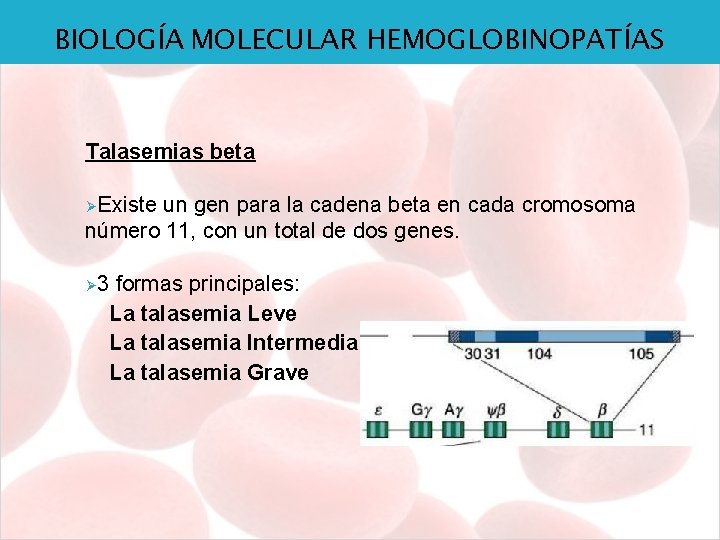
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Talasemias beta ØExiste un gen para la cadena beta en cada cromosoma número 11, con un total de dos genes. Ø 3 formas principales: La talasemia Leve La talasemia Intermedia La talasemia Grave

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS La talasemia Leve o minor Denominada rasgo talasémico Causada por una mutación en un gen de globina beta. La mayoría de las personas afectadas no presenta síntomas aunque algunas padecen anemia leve. Las personas afectadas pueden transmitir el gen anormal a sus descendientes.

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS La talasemia Intermedia Resultado de anomalías en ambos genes de globina beta. Son menos graves que las que causan la talasemia mayor. Los niños afectados padecen anemia de leve a moderada, presentan agrandamiento del bazo y anomalías en los huesos. Necesitan transfusiones complicaciones. de sangre para reducir las

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS La talasemia Grave o mayor Forma más grave Resultado de mutaciones graves en ambos genes de globina beta. También se denomina “anemia de Cooley”. La mayoría de los niños afectados parecen saludables al nacer. No obstante, durante el primer o el segundo año de vida se vuelven pálidos e irritables y pierden el apetito. Su crecimiento es lento y a menudo tienen ictericia (su piel y sus ojos adquieren un color amarillento).
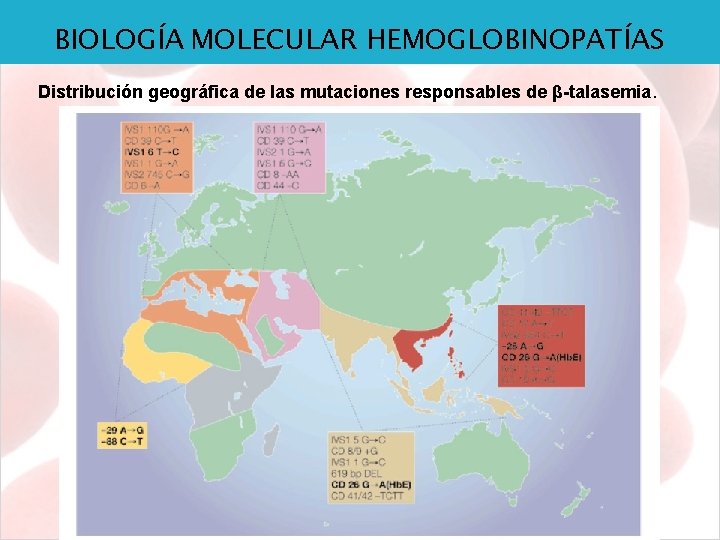
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Distribución geográfica de las mutaciones responsables de β-talasemia.

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Delta-Beta talasemia ØCausada por deleciones de los genes delta y beta con aumento de síntesis de cadenas gamma y aumento de Hb. F ØDescrita en muchos grupos étnicos, es muy frecuente en Grecia, Italia y España. ØHeterocigotos asintomáticos, con microcitosis leve y sin reducción de la Hb. A 2. ØHomocigotos tienen una presentación clínica leve. ØHereda conjuntamente con la beta-talasemia clásica (doble heterocigoto), los pacientes suelen presentar el fenotipo de talasemia intermedia. ØMuy relacionada con la persistencia hederitaria hemoglobina fetal

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS ØLa técnica de elección actual: o. Secuenciación SANGER de las regiones promotora, exónicas e intrónicas flanqueantes del gen de la β globina Se han dejado de usar técnicas dirigidas a identificar mutaciones concretas como ARMS-PCR o RFLP. o De utilizar técnicas alelo específicas, es importante conocer el origen étnico del paciente. o ØConsiderar grandes deleciones que afectan al gen o al cluster β globina: o -619 bp, δβ Spanish, HPFH-1, HPFH-2, HPFH-3, HPFH-7, Lepore. ØPara identificar grandes deleciones se usan técnicas alelo específicas: o. GAP-PCR, múltiple o sencilla, o. MLPA para cribado de grandes deleciones no conocidas.

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Persistencia hereditaria de hemoglobina fetal ØProducción de Hb F en el adulto que excede el nivel normal en ausencia de cualquier cambio hematológico mayor. ØExisten diferencias fenotípicas: o. Cantidad de hemoglobina F producida o. Relación de las cadenas Gγ / Aγ que contienen. ØEl análisis molecular de la PHHF ha demostrado: o. Casos con deleciones que afectan el extremo 3´ del cluster con remoción completa de los genes δ y β (deleción). o. Casos con el cluster de β globina está intacto (no deleción)

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Persistencia hereditaria de hemoglobina fetal tipo deleción ØSon la mayoría de los casos ØSe debe a la pérdida de cantidad variable de material genético que incluye generalmente los genes δ y β. ØGγ Aγ PHHF es muy similar a la Gγ Aγ δβ talasemia, aunque los heterocigotos tienen mayor nivel de Hb F ØHomozigotos tienen un cuadro hematológico y síntesis de globina similar a la talasemia β heterocigota (con 10% de Hb F) ØLa condición con deleción se puede dividir: 0 o. Gγ Aγ (δβ) -PHHF o. Hb Kenya-PHHF 0 o. Gγ Aγ (δβ) -talasemia 0 o. Gγ (Aγ δβ) - talasemia 0 o(ε Gγ Aγ δβ) -talasemia. ØEn cada grupo el cuadro clínico y hematológico es relativamente uniforme.

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Persistencia hereditaria de hemoglobina fetal tipo no deleción Muchas variantes en las que la mutación de una única base dentro o fuera del grupo de genes γ−δ−β origina el trastorno. o En estos casos la producción de cadena γ deriva casi completamente de uno de los dos genes γ. o El gen β sobre el cromosoma afecto está expresado en forma correcta. o Según la distribución de la Hb F en los hematíes: o PHHF: PHHF homogénea o pancelular con aumento uniforme de Hb F en todos los hematíes. o PHHF heterocelular, en la cual sólo una subpoblación de hematies contiene Hb F. o

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Hemoglobinopatías Talasémicas ØMutaciones de los genes de globina que, además de producir una disminución en la síntesis de cadenas globínicas, son responsables de alteraciones estructurales: o. Hb. E Hb Lepore o Hemoglobinopatías con alargamiento de la cadena de globina (Hb Constant Spring, Hb Tak) o Hemoglobinopatías con cadenas de globina muy inestables (Hb Showa-Yakushiji, Hb Houston, Hb Geneva, Hb Quong Sze, Hb Suan Dok, Hb Petah, Hb Lleida, Hb Clinic). o

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Hemoglobina E Ø Sustitución en la cadena de β-globina de ácido glutámico por lisina en la posición 26. Ø Defecto en la maduración del RNAm y disminución en la síntesis de cadenas de β-globina. Ø La segunda hemoglobina anómala más común después de la hemoglobina S Ø Expresividad clínica es superponible a la β-talasemia minor: los heterocigotos microcitosis y los homocigotos microcitosis y una ligera anemia. Ø Cuando la Hb E se asocia a un gen β- talasémico, la expresividad clínica es de una β-talasemia intermedia siendo la gravedad es muy variable Ø La Hb E se halla principalmente en la población del sudeste asiático (> 15% de incidencia de enfermedad homocigota).

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Hemoglobina Lepore ØFormación de un gen híbrido β, constituida por un fragmento δ y uno β. o. Cromosoma Lepore: gen β ha sido sustituido por el gen híbrido δβ o. Cromosoma anti-Lepore: gen híbrido βδ coexiste con los genes δ y β normales. ØEntrecruzamiento puede producirse en diferentes lugares, existen varios tipos de Hb Lepore (Boston, Baltimore y Hollandia). ØVariante más frecuente es la Hb Lepore Boston, incidencia elevada en determinadas áreas geográficas de Italia y centro de Europa. ØComportamiento clínico es superponible al de una β-talasemia: o. Heterocigoto: caracteristicas β-talasemia minor pero sin aumento de Hb. A 2 ni de la Hb. F. o. Homocigoto: características clínicas de una talasemia mayor.
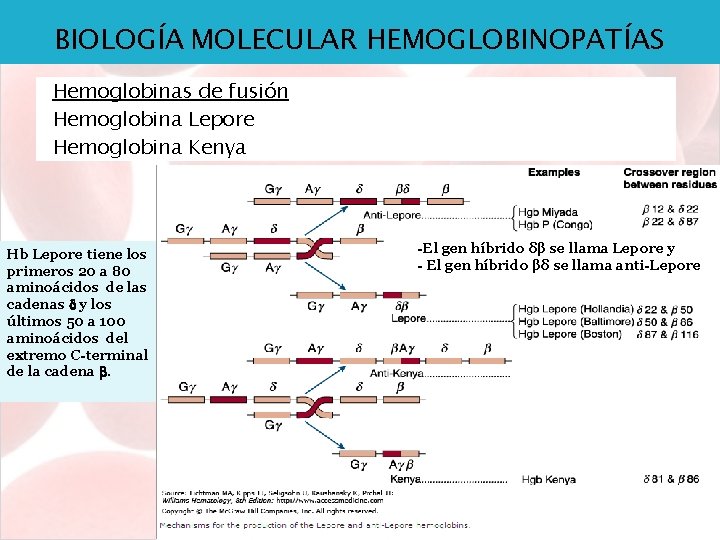
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Hemoglobinas de fusión Hemoglobina Lepore Hemoglobina Kenya Hb Lepore tiene los primeros 20 a 80 aminoácidos de las cadenas y los últimos 50 a 100 aminoácidos del extremo C-terminal de la cadena . -El gen híbrido δβ se llama Lepore y - El gen híbrido βδ se llama anti-Lepore
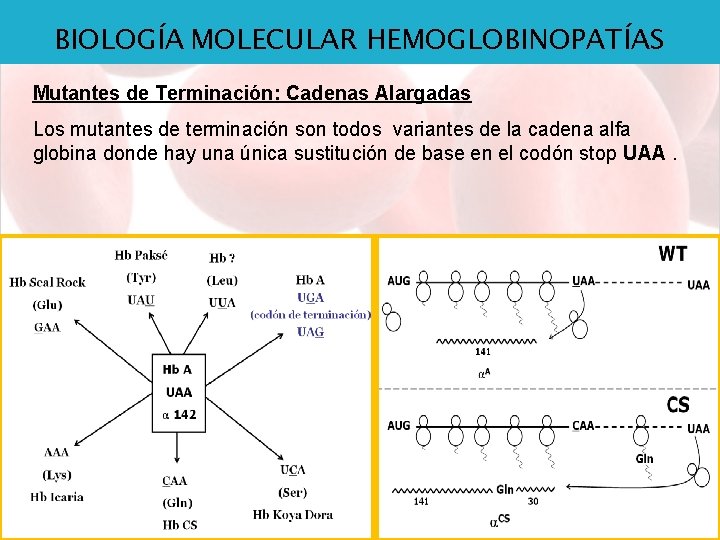
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Mutantes de Terminación: Cadenas Alargadas Los mutantes de terminación son todos variantes de la cadena alfa globina donde hay una única sustitución de base en el codón stop UAA.

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Variantes de cadena de Hb elongadas.

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS Cadenas de globinas truncadas Uno o más aminoácidos adyacentes se pierden, pero se conserva el resto de la cadena normal. Estas variantes involucran la deleción de 1 o más codones intactos, no afectando el marco de lectura de la proteína restante. Son ejemplos de deleciones : • Hb Freiburg (deleción de un aminoácido) • Hb Lyon (deleción de dos aminoácidos) • Hb Gun. Hill (deleción de cinco aminoácidos)

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS FIN
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
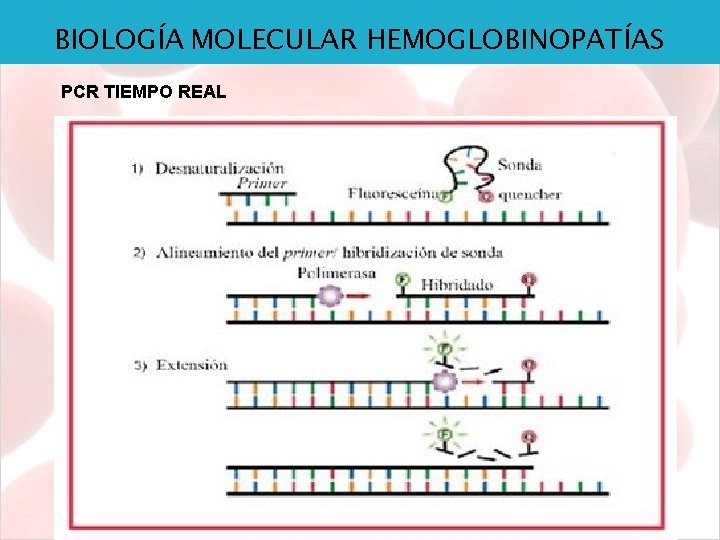
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS PCR TIEMPO REAL
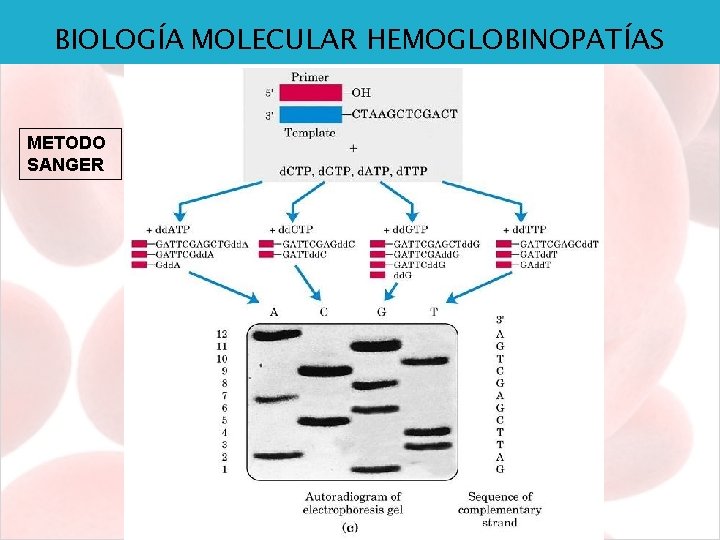
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS METODO SANGER
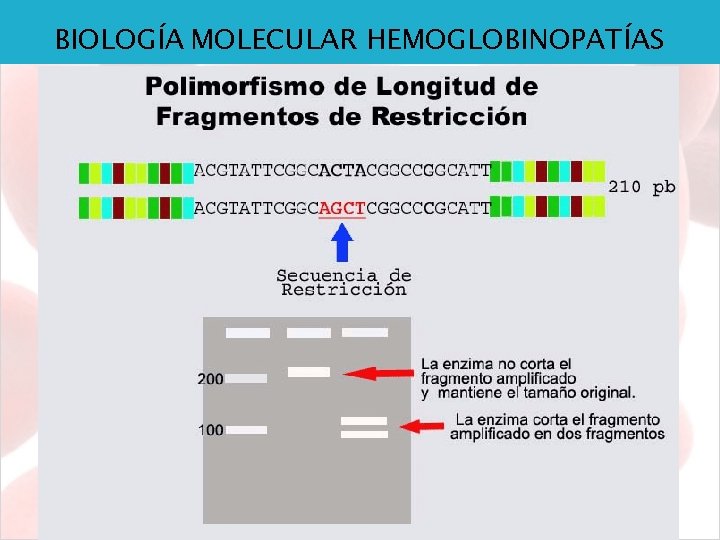
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS

BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS
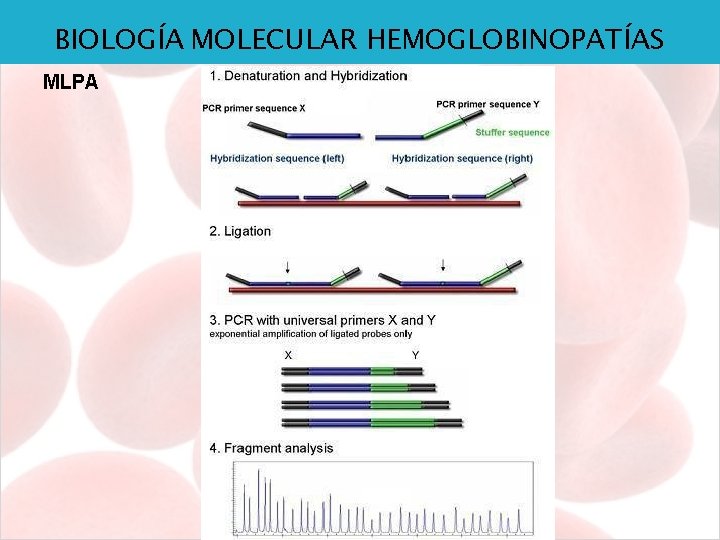
BIOLOGÍA MOLECULAR HEMOGLOBINOPATÍAS MLPA
- Slides: 68