Biokmiai Tumor Markerek Izotp Intzet Kft Immunoassay zletg
Biokémiai Tumor Markerek Izotóp Intézet Kft. Immunoassay üzletág

Definíció és osztályozás l A biokémiai tumor markerek olyan, a daganatsejtek által termelt és a testfolyadékokba kerülő anyagok, amelyek neminvazív módszerekkel mérhetőek. Mivel a tumor marker koncentráció korrelál az aktív daganattömeggel, a tumor markerek hasznosak a betegség lefolyásának nyomon követésére. 5 th International Conference on Human Tumor Markers, 1988. l Osztályozás: képződés/kimutatás helye (celluláris, extracelluláris), szerkezet (pl. peptid, glikoprotein), funkció (pl. hormon, enzim, receptor).

Klinikai alkalmazások - Szűrés Jelenleg nincs eléggé specifikus és érzékeny tumor marker, amely az általános lakosság szűrésére alkalmas lenne. Reálisabb megközelítések: High-risk populáció, magas regionális előfordulási arány, viszonylagos siker. Példák: l PSA + DRE 50 év feletti férfiakban (American Cancer Society ajánlás, 1992) l CA 125 + TVS herediter ovarium carcinoma betegek családtagjai körében (NIH konszenzus) l Kína: AFP – hepatocellular carcinoma screening, hepatitisz vagy májcirrózis előzménnyel rendelkező egyénekben.

Klinikai alkalmazások – Diagnózis (más módszerekkel együtt) l Diagnózis megerősítése l Ismeretlen primer tumor eredetének kiderítése, áttétes betegség esetén l Differenciál-diagnózis: azonos klinikai tünetek esetén a malignitás megállapítására (pl. Szabad/Totál PSA arány) vagy ismeretlen szövettan esetén az osztályozás céljából (pl. NSE tüdőrákban)

Klinikai alkalmazások – Prognózis Általában: Magas tumor marker szint – rossz prognózis Példák: l AFP, HCG és LDH a hererákban l CA 72. 4 a gyomorrákban (4 x nagyobb halálozási rizikót jelent) l NSE a SCLC esetén (minden 5 μg/L emelkedés a túlélési medián 10%-kos csökkenését jelenti)

Klinikai alkalmazások – Monitorozás 1. terápia 2. terápia Részleges válasz Sikeres 1. terápia Visszaesés Cut-off Remisszió Rezisztencia Sikeres 2. terápia

Tumor marker irányelvek/ajánlások l National Academy of Clinical Biochemistry (NACB): Laboratory Medicine Practice Guidelines (LMPG) www. aacc. org 1. Tumor Marker Quality Requirements – 2008 2. Use of Tumor Markers in Testicular, Prostate, Colorectal, Breast and Ovarian Cancers – 2009 3. Use of Tumor Markers in Liver, Bladder, Cervical and Gastric Cancers – 2010 l European Group of Tumor Markers (EGTM) www. egtm. eu 1. Anticancer Research 1999; 19: 2785 -2820 2. Int J Gynecol Oncol 2005; 15: 679 -91 Ovarian Cancer 3. Tumour Biology 2005; 26: 281 -93 Breast Cancer 4. Eur J Cancer 2007; 43: 1348 -60 Colorectal Cancer 5. Ann Oncol 2010; 21: 441 -7 Pancreatic Cancer
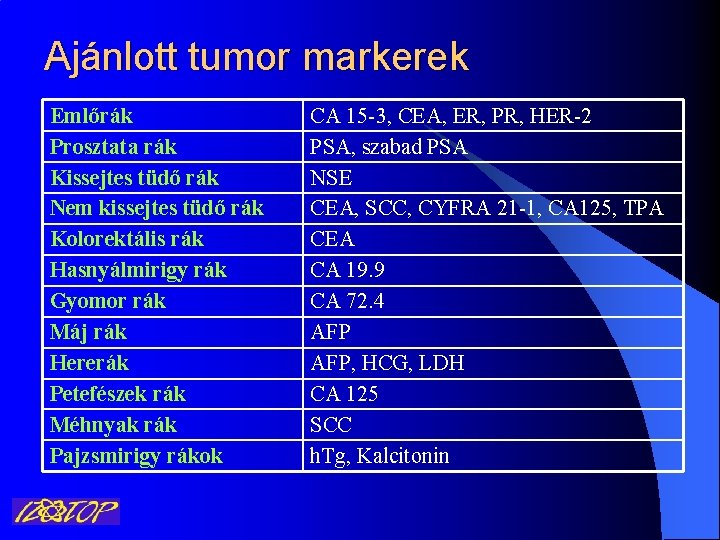
Ajánlott tumor markerek Emlőrák Prosztata rák Kissejtes tüdő rák Nem kissejtes tüdő rák Kolorektális rák Hasnyálmirigy rák Gyomor rák Máj rák Hererák Petefészek rák Méhnyak rák Pajzsmirigy rákok CA 15 -3, CEA, ER, PR, HER-2 PSA, szabad PSA NSE CEA, SCC, CYFRA 21 -1, CA 125, TPA CEA CA 19. 9 CA 72. 4 AFP, HCG, LDH CA 125 SCC h. Tg, Kalcitonin

Preanalitikai megfontolások 1. 2. 3. 4. Minta típusa: Általában plazma/szérum használható: termék leírás szerint! Minta stabilitása és tárolása: Alvadás után minél előbb szeparálni kell a szérumot/plazmát. Tárolás: 4°C-on 24 óráig, egyébként -20°C-on. Hosszú távon -70°C-on. Hőkezelést kerülni kell! Mintavétel időpontja: Élettani hatásokra, beavatkozások után emelkedhet a koncentráció. Pl. CA 125 menses alatt, PSA DRE, biopszia, transurethralis resectio után. Kóros folyamatok: gyulladások, fertőzések, máj és vese betegségek, tumor marker- termelő jóindulatú elváltozások. Pl. magas CEA a veseelégtelenségben, magas HCG postmenopauzában, magas CA 125 endometriózisban, magas PSA prosztatagyulladásban, magas CA 19. 9 hepatitisben.

Belső minőség-ellenőrzés (IQC) 1. 2. 3. 4. Reprodukálhatóság: Intra-assay < 5%, inter-assay CV < 10%. A mérés jóváhagyásához elfogadott IQC határok: definiálni kell, lehetőleg logikai kritériumok alapján. Pl. Westgard rules. IQC minták minősége: legalább egy független, szérum mátrix alapú kontroll szükséges. Nem a kit kontrollja! IQC minták koncentrációja: legalább egy negatív és egy alacsony pozitív kontroll kell, szélesebb koncentráció tartomány ellenőrzése szükség szerint.

Külső minőség-ellenőrzés (EQA) EQA minták követelményei: l Egyedi páciensmintából készült, nem antigénnel dúsított minták. l Szállítási stabilitás (szabad PSA és h. CG esetén probléma lehet) l Megfelelő koncentráció: munkatartomány átölelése, alkalomszerűen magas minta a hígítás ellenőrzésére, antigénmentes minta alapvonal ellenőrzésre. Értékelés: l Stabilitás: a célérték stabilitása ugyanazon szérum-pool többszöri szétosztásával l Valódiság: visszanyerés ellenőrzése a nemzetközi standarddal dúsított pool mérésével l Linearitás: ugyanazon pool különböző hígításai ugyanazon szérum-mátrix alappal Egyéb információ: különböző laboratóriumok összehasonlítása

Posztanalitikai megfontolások 1. Rövid klinikai információ az eredményt kérő orvostól: betegség eredete, kezelés fázisa, stb. 2. Referencia tartomány: megfelelő egészséges populáció alapján, beteg saját „alapvonala”, kezelés előtti értékek. 3. Mit jelent szignifikáns változás: analitikai és biológiai variabilitás ismerete. Általában +/- 25%. 4. Módszerváltás esetén ellenőrizni/kommunikálni kell a váltás eredményekre gyakorolt hatását. 5. A felezési/duplázási idő ismerete és közlése amikor releváns. Felezési idő: 50%-os csökkenéshez szükséges idő teljes tumor eltávolítás után.
- Slides: 12




















