Biokmia Wunderlich Lvius Ph D BME liviusmail bme

Biokémia Wunderlich Lívius Ph. D. BME livius@mail. bme. hu 2020

Alapkövetelmények - Középiskolai kémia: Általános és szerves kémia fontos Szervetlen kémia kevésbé fontos (csak a biológiailag releváns elemek, vegyületek) Kémiai technológia nem kell - Középiskolai biológia: Sejttan, szervtan, élettan, biokémia fontos Rendszertan, genetika kevésbé fontos Szupra-individuális szintek, etológia nem kell

Tematika -Gyorstalpaló kémia -Gyorstalpaló sejtbiológia -Leíró biokémia -Enzimológia -Bioenergetika -Szénhidrát anyagcsere -Lipid anyagcsere -Fehérje anyagcsere -Nukleinsav anyagcsere -Replikáció, transzkripció, transzláció -Táplálkozás, biotranszformáció és ami még belefér…

Aláírás követelmény: 2016. 10. 06. 2016. 10. 27. 2016. 11. 17. 3 db rövid írásbeli ZH A két legjobb számít Összesített átlag legyen legalább 50% Nincs javítási lehetőség!!! Vizsgakövetelmény: Az előadáson elhangzott tananyag

Ajánlott olvasmányok: Wunderlich, Szarka: A biokémia alapjai www. interkonyv. hu oktatas. ch. bme. hu oktatas konyvek biokemia Egeszsegugyi mernok biokemia Ádám et al. : Orvosi biokémia Csermely et al. : Bioorganikus kémia ? ? ? Mandl József: Biokémia Gergely et al. : Általános és bioszervetlen kémia …vagy bármely biokémia könyv viszonylag új verziója

Kémia gyorstalpaló
Az atom szerkezete
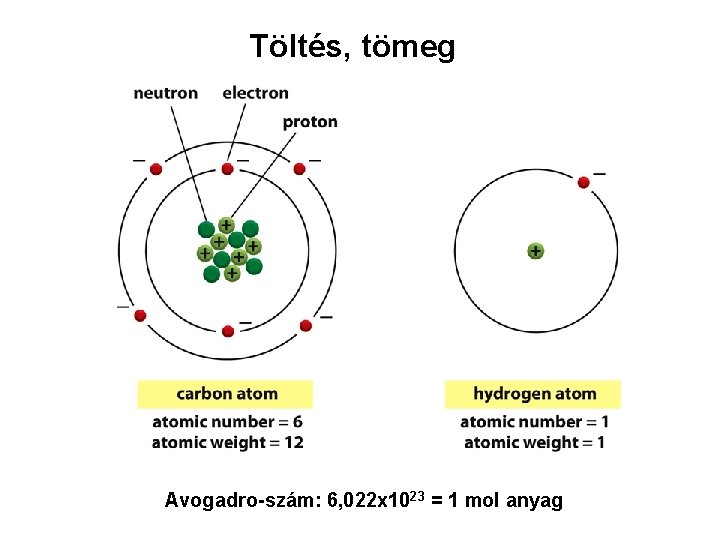
Töltés, tömeg Avogadro-szám: 6, 022 x 1023 = 1 mol anyag
Az atomok szerkezete 2 e- atompályánként

Elemek: Azonos protonszámú atomok anyaghalmaza Vegyületek: Különböző protonszámú atomok anyaghalmaza Izotópok: Azonos protonszámú, de különböző neutronszámú atomok
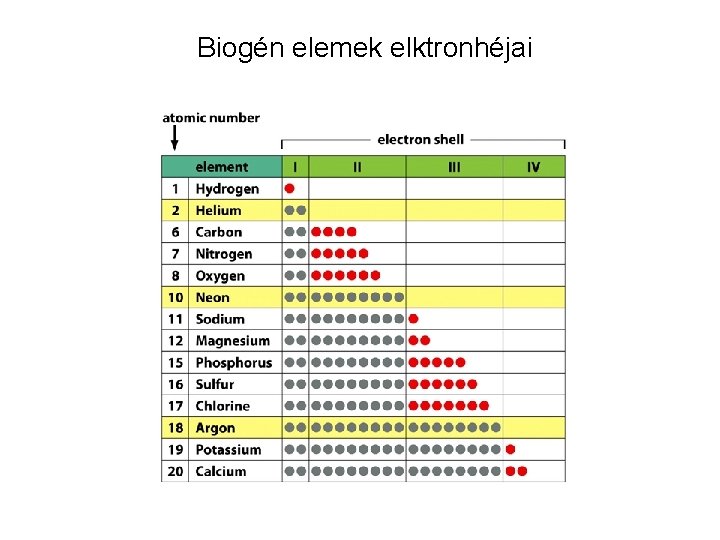
Biogén elemek elktronhéjai
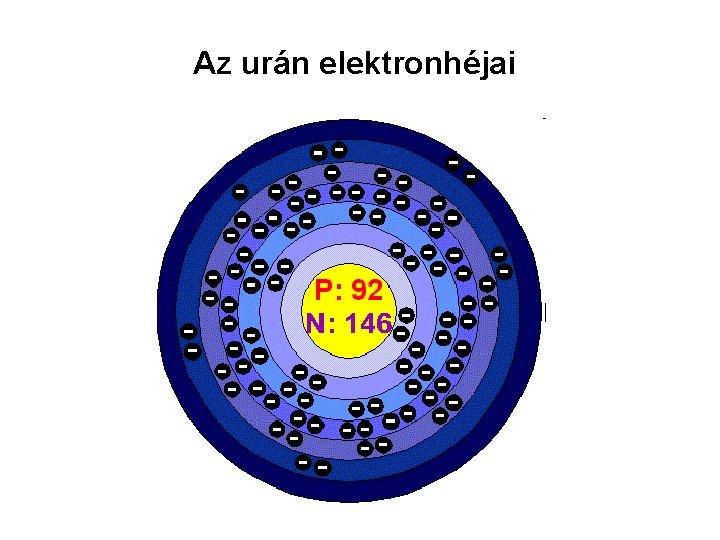
Az urán elektronhéjai
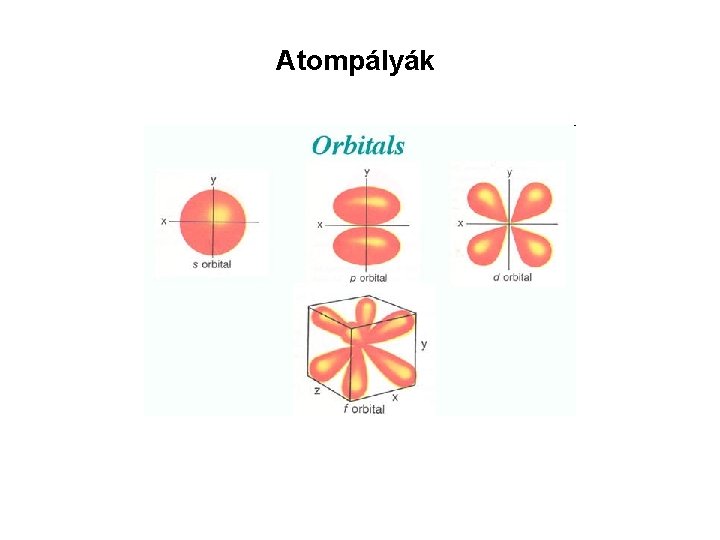
Atompályák
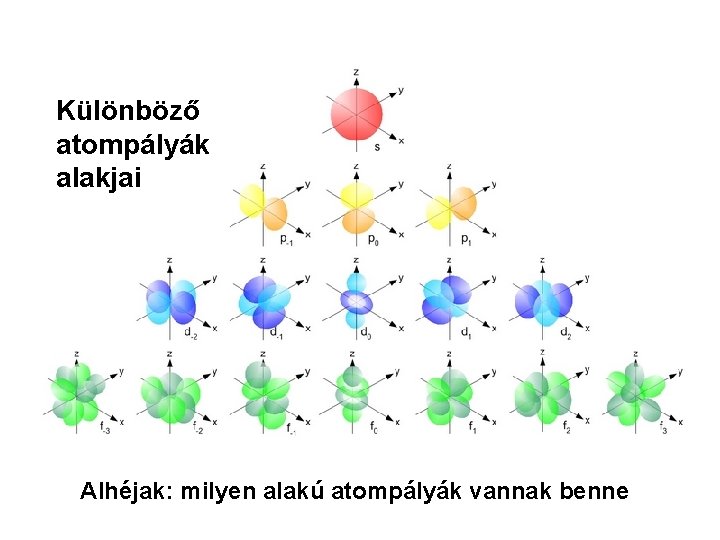
Különböző atompályák alakjai Alhéjak: milyen alakú atompályák vannak benne
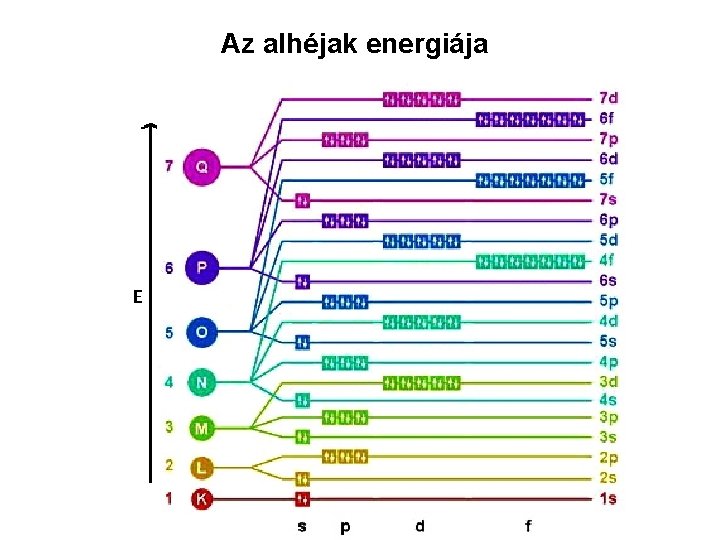
Az alhéjak energiája
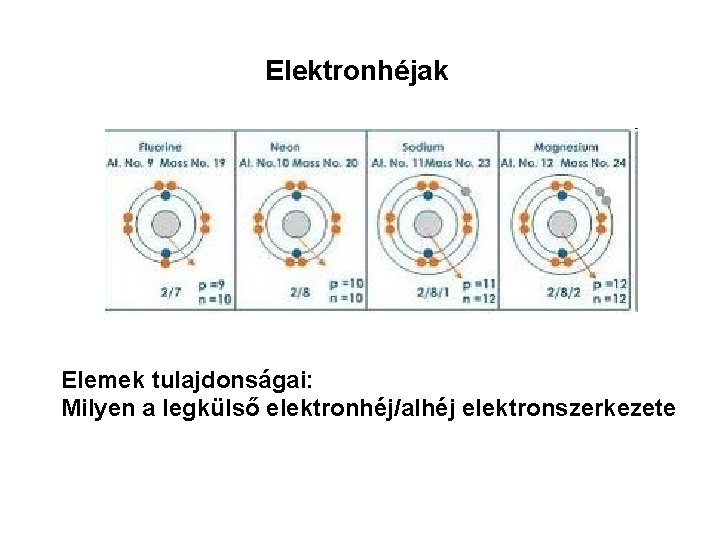
Elektronhéjak Elemek tulajdonságai: Milyen a legkülső elektronhéj/alhéj elektronszerkezete
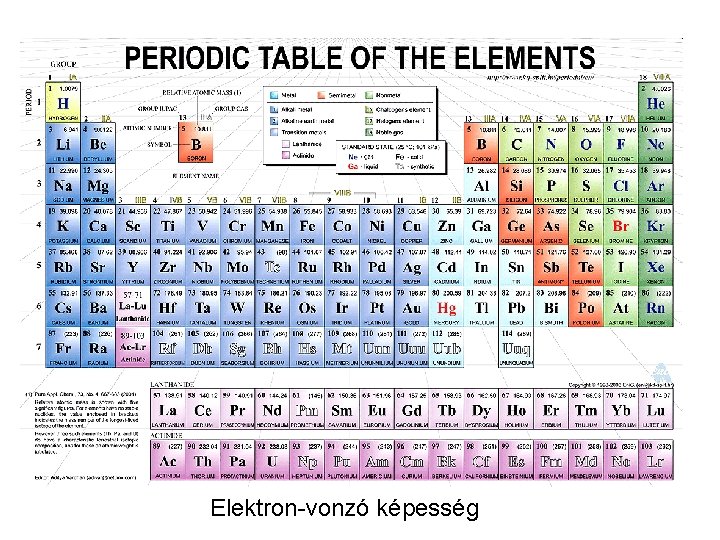
Elektron-vonzó képesség
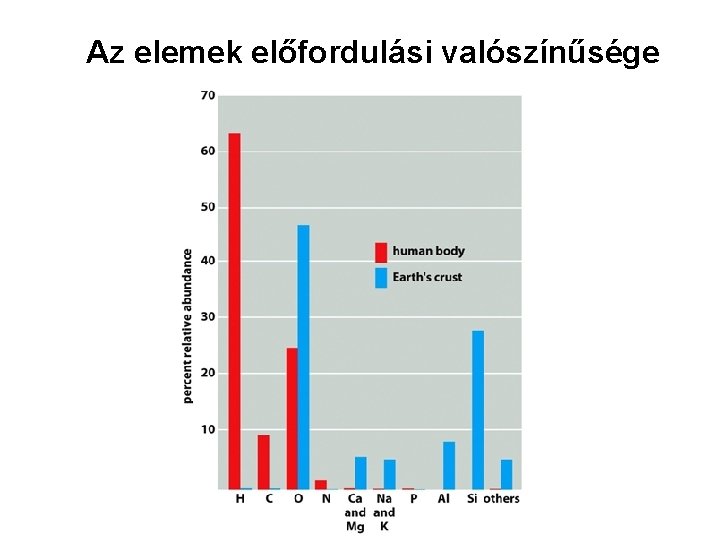
Az elemek előfordulási valószínűsége

A biológiailag fontos elemek Atomos állapotban: Csak a nemesgázok Elemi állapotban is csak kevés elem, többi vegyületben ? ? ?
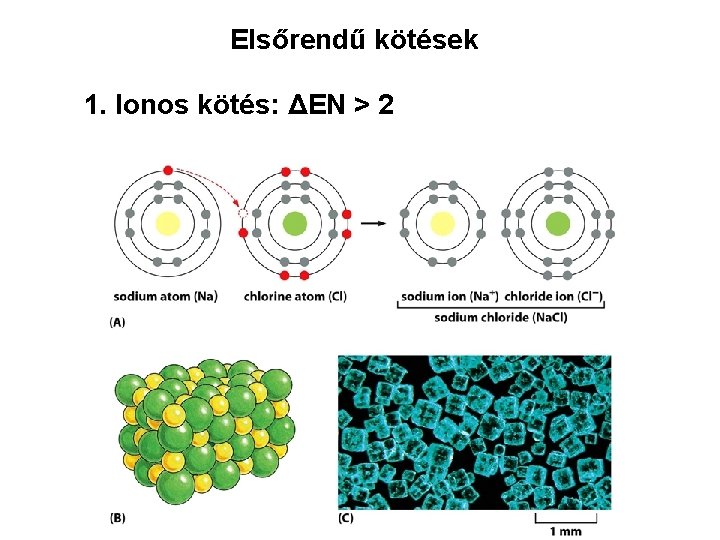
Elsőrendű kötések 1. Ionos kötés: ΔEN > 2
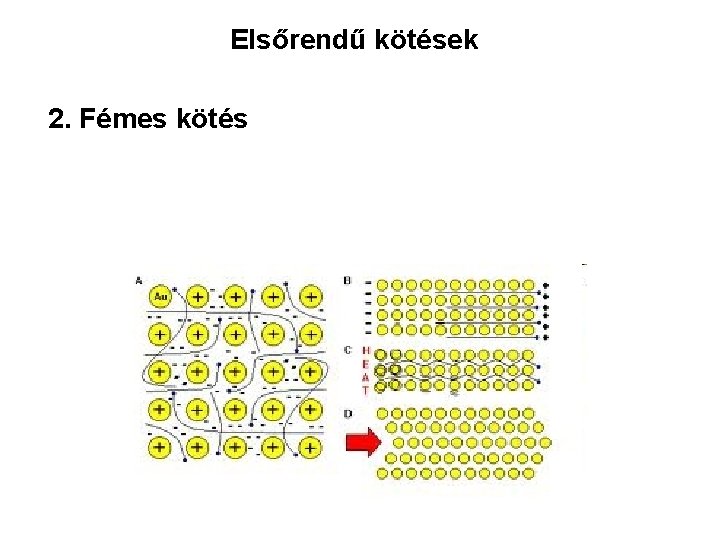
Elsőrendű kötések 2. Fémes kötés
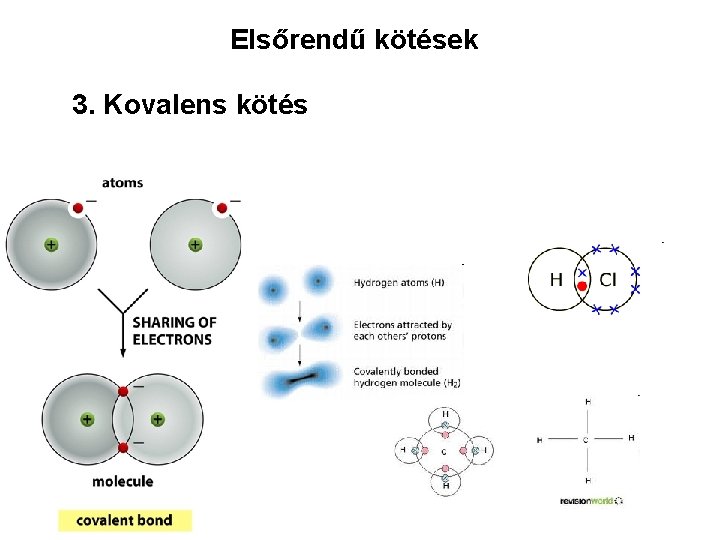
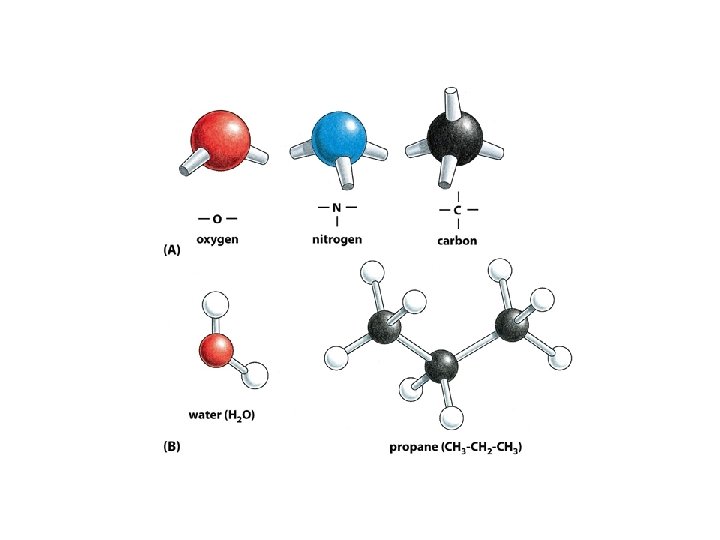
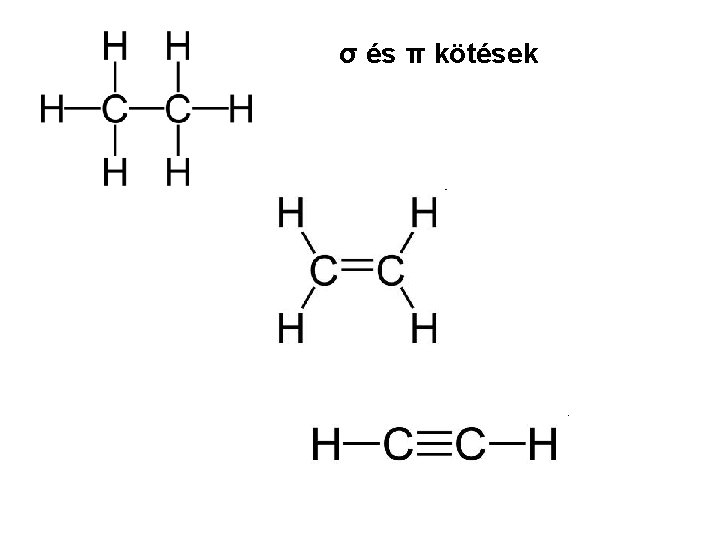
Elsőrendű kötések 3. Kovalens kötés
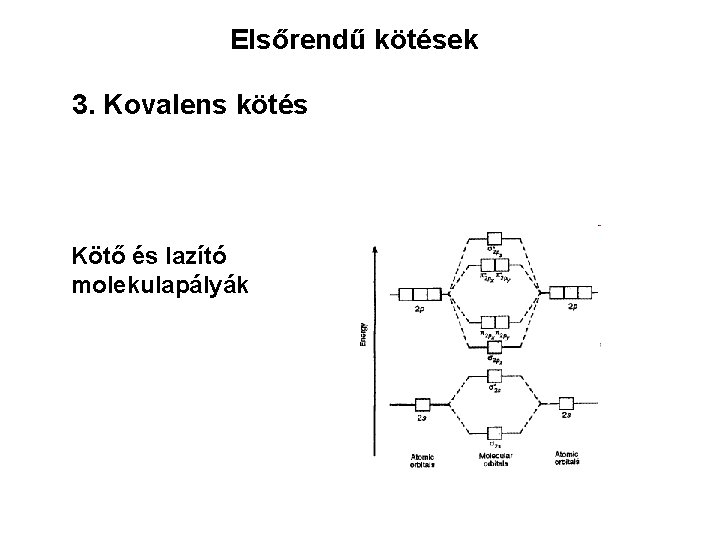
Elsőrendű kötések 3. Kovalens kötés Kötő és lazító molekulapályák
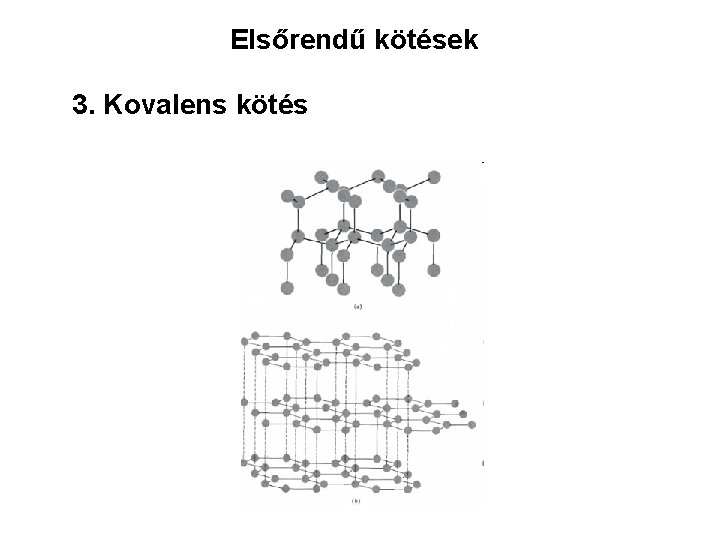
Elsőrendű kötések 3. Kovalens kötés
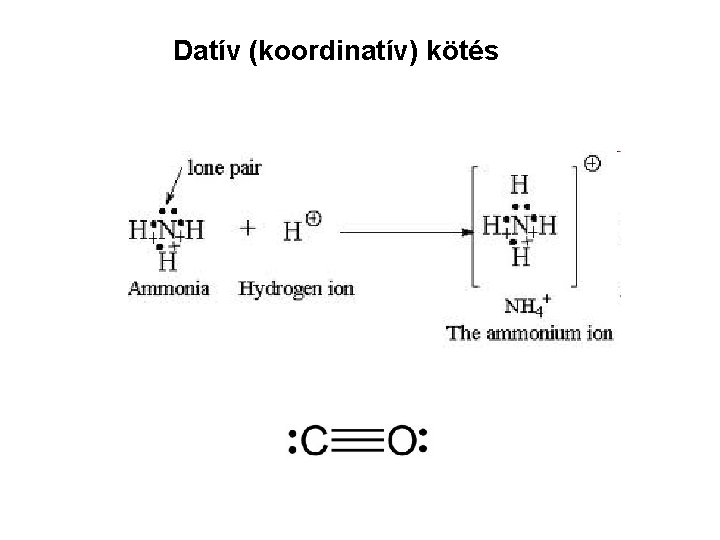
Datív (koordinatív) kötés
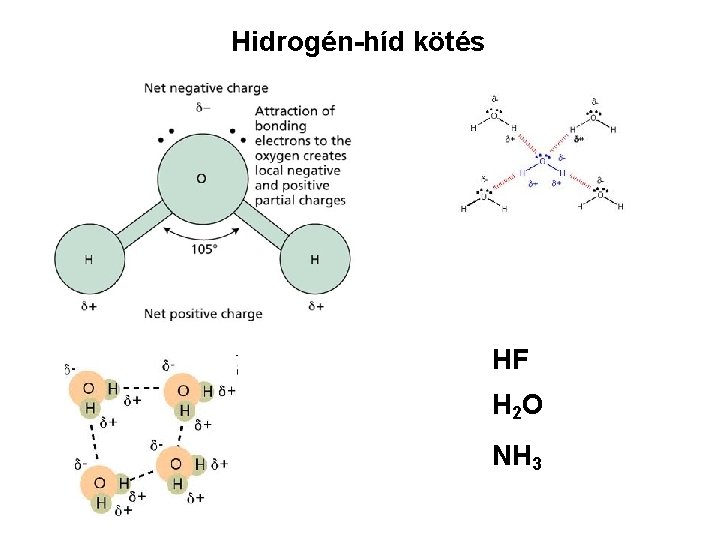
Hidrogén-híd kötés HF H 2 O NH 3
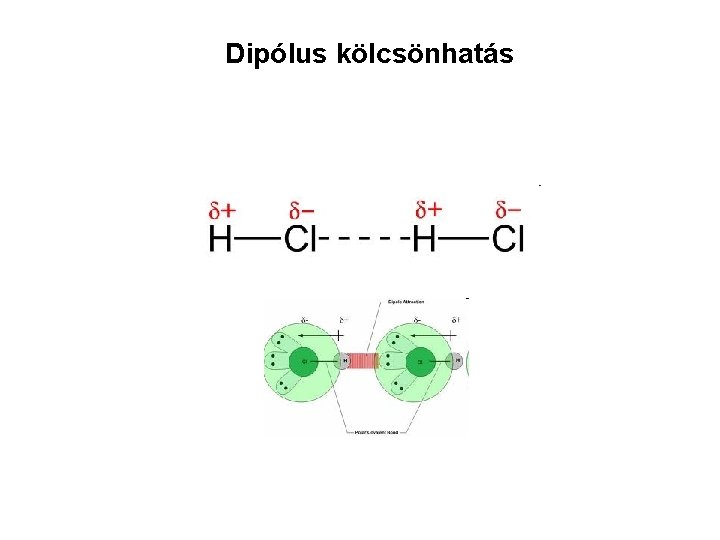
Dipólus kölcsönhatás
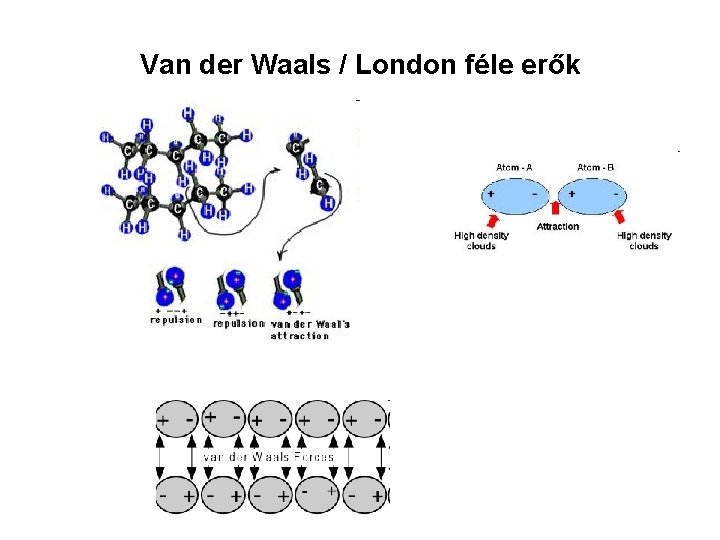
Van der Waals / London féle erők
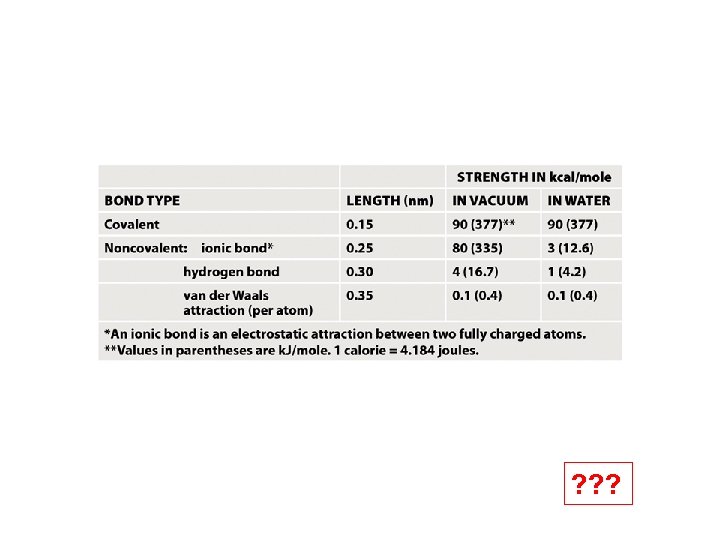
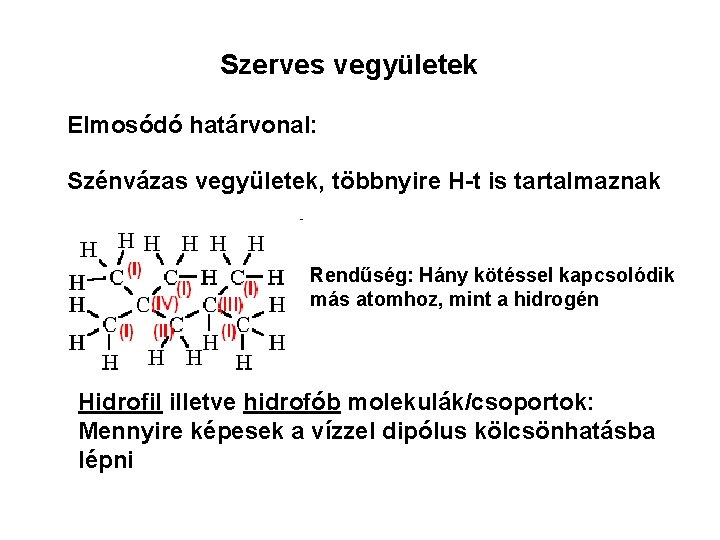
Szerves vegyületek Elmosódó határvonal: Szénvázas vegyületek, többnyire H-t is tartalmaznak Rendűség: Hány kötéssel kapcsolódik más atomhoz, mint a hidrogén Hidrofil illetve hidrofób molekulák/csoportok: Mennyire képesek a vízzel dipólus kölcsönhatásba lépni
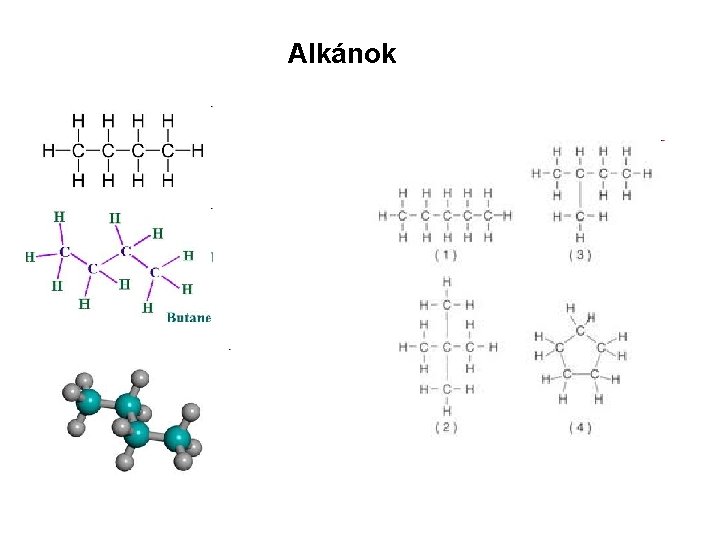
Alkánok
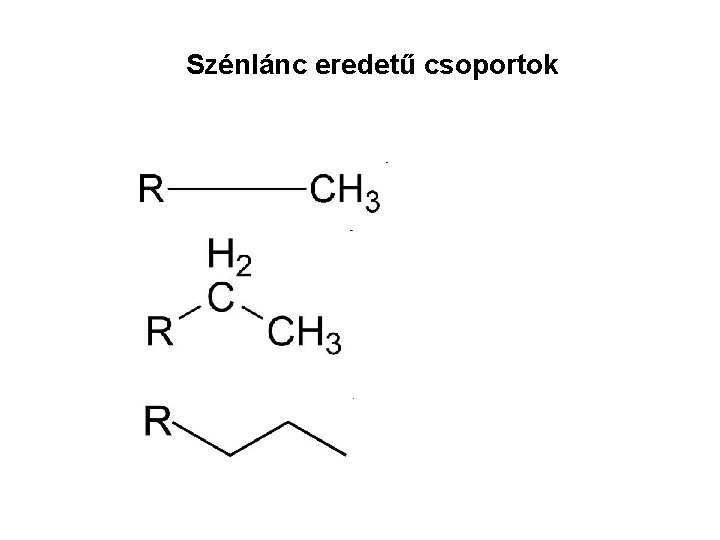
Szénlánc eredetű csoportok
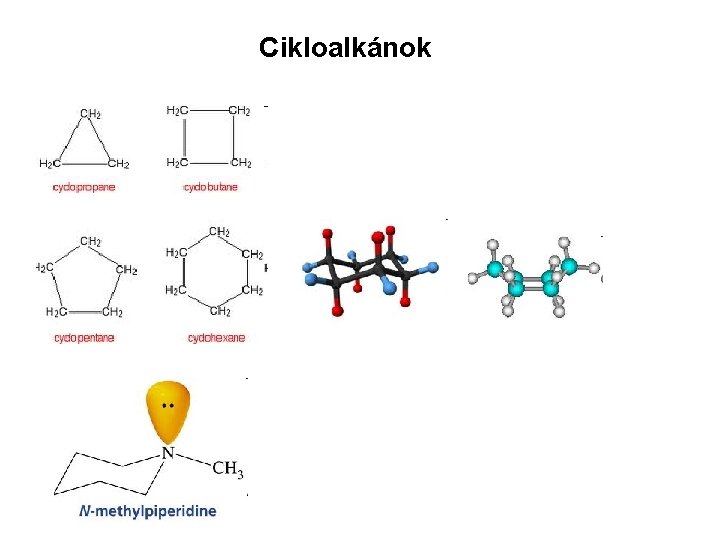
Cikloalkánok
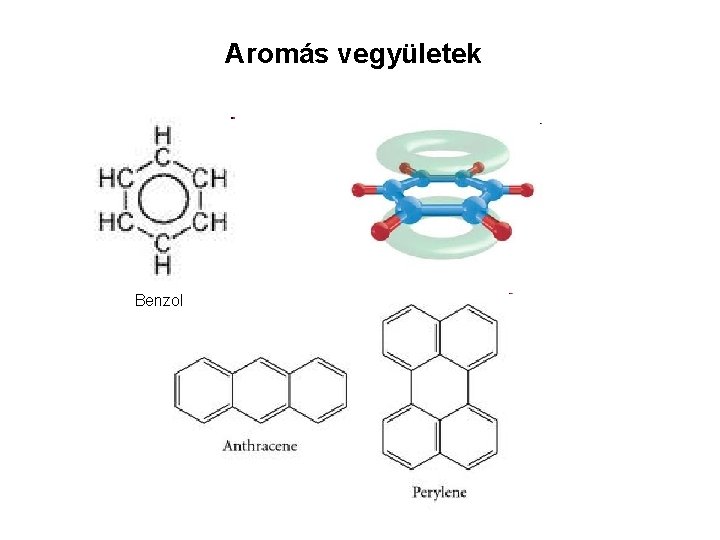
Aromás vegyületek Benzol
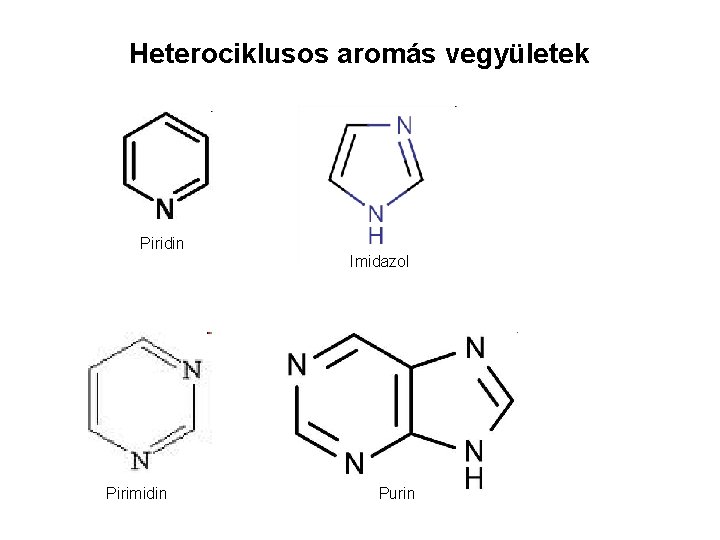
Heterociklusos aromás vegyületek Piridin Pirimidin Imidazol Purin
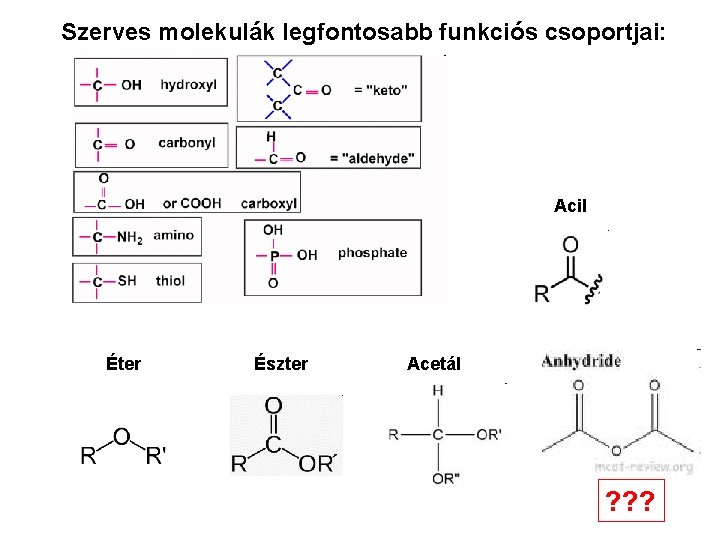
Szerves molekulák legfontosabb funkciós csoportjai: Acil Éter Észter Acetál ? ? ?
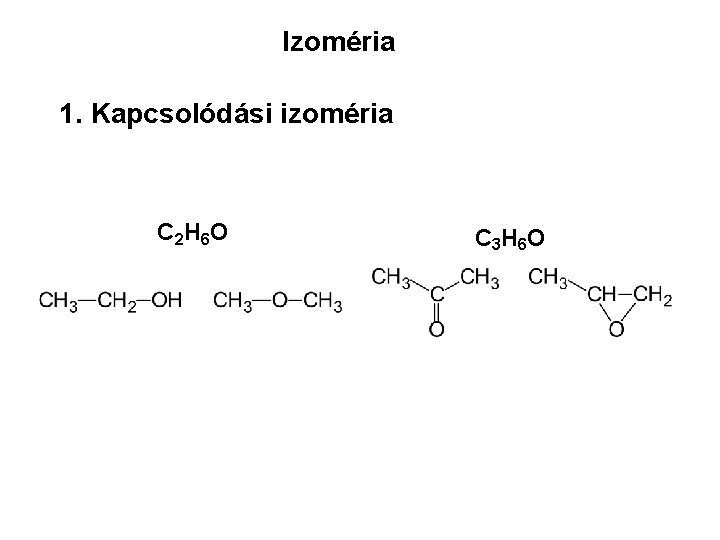
Izoméria 1. Kapcsolódási izoméria C 2 H 6 O C 3 H 6 O
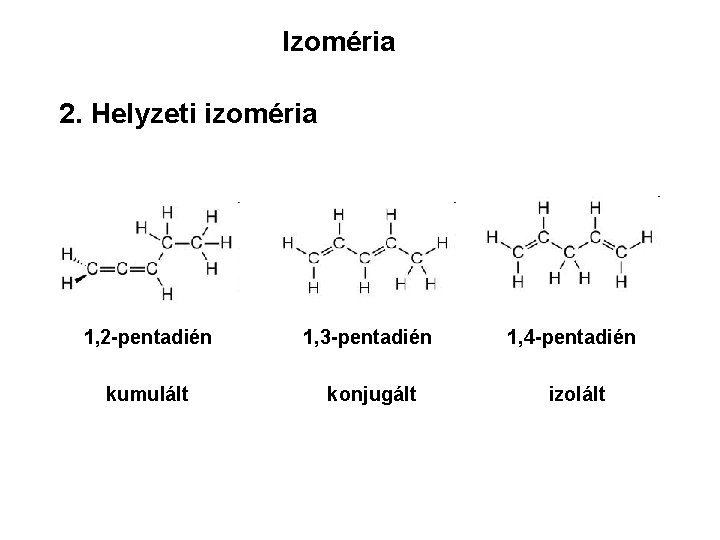
Izoméria 2. Helyzeti izoméria 1, 2 -pentadién 1, 3 -pentadién 1, 4 -pentadién kumulált konjugált izolált
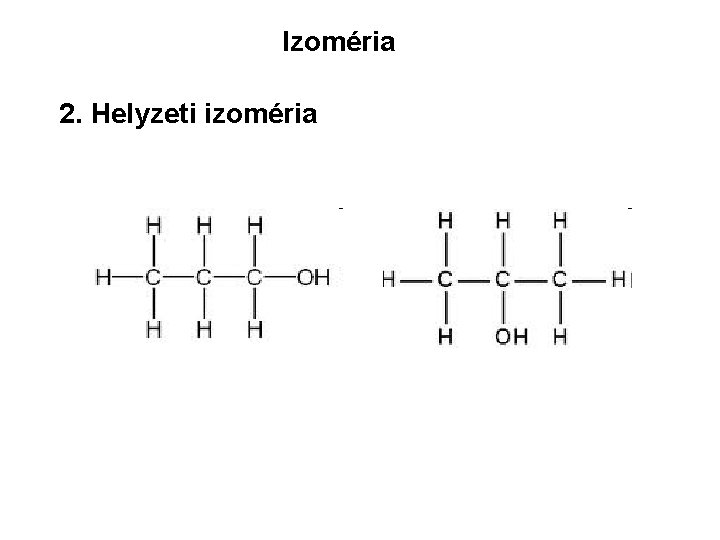
Izoméria 2. Helyzeti izoméria
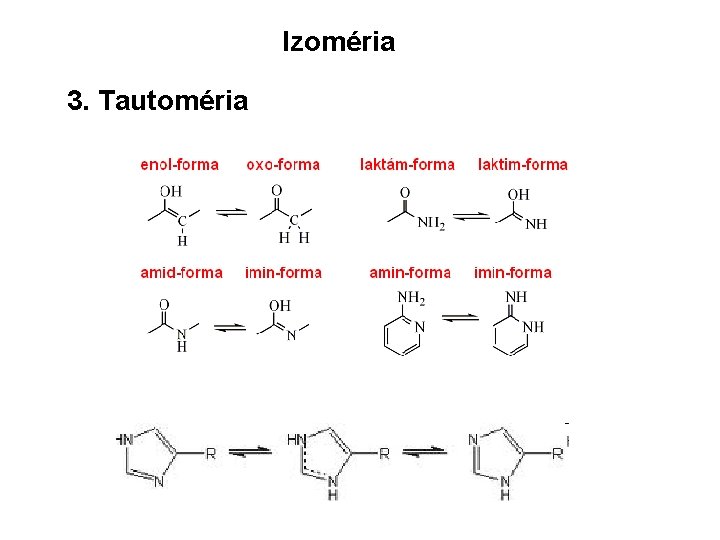
Izoméria 3. Tautoméria
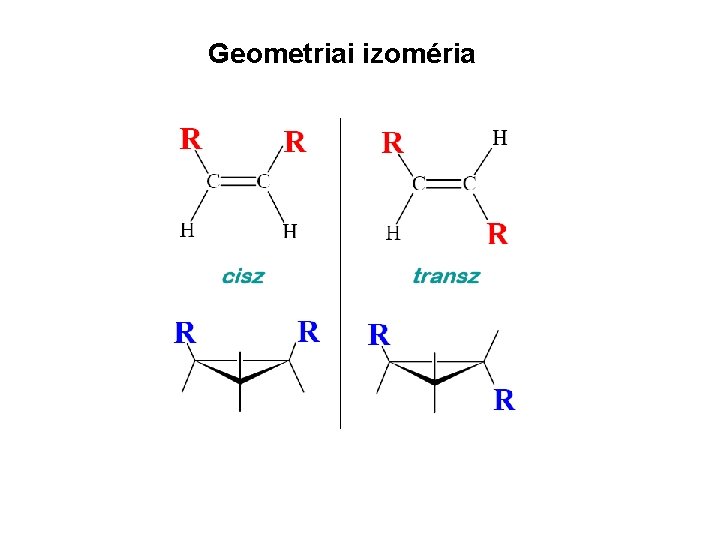
Geometriai izoméria
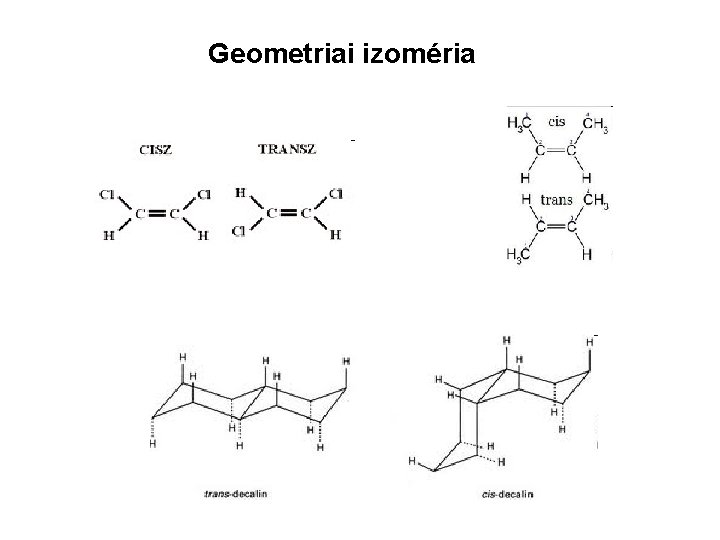
Geometriai izoméria
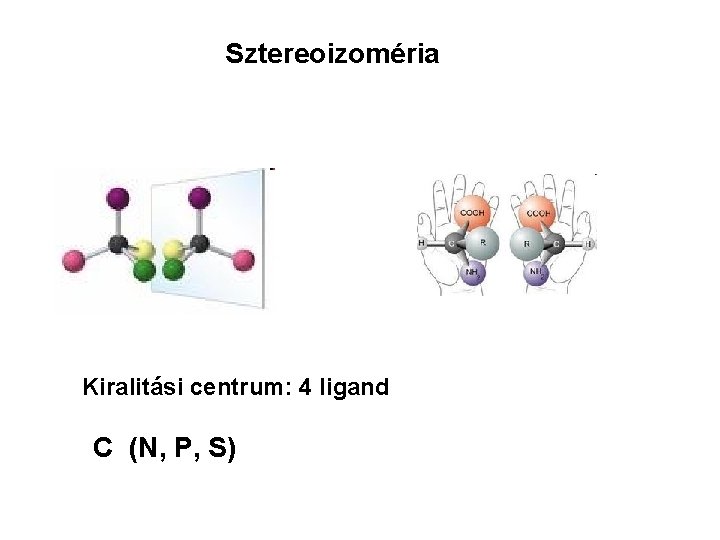
Sztereoizoméria Kiralitási centrum: 4 ligand C (N, P, S)
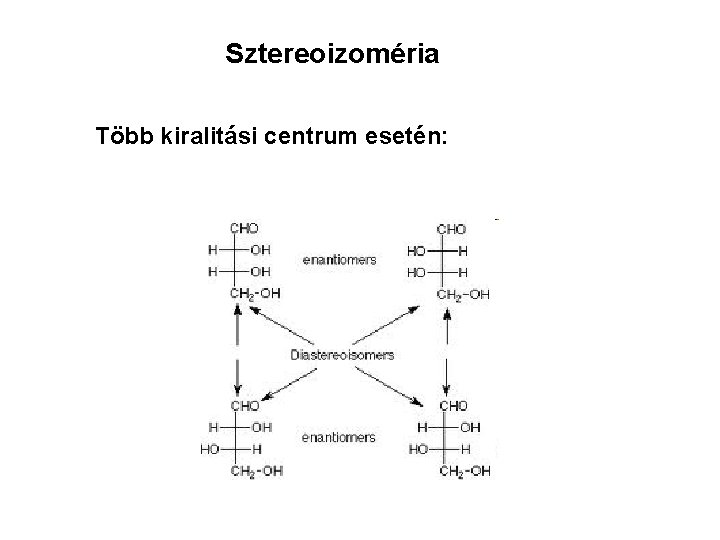
Sztereoizoméria Több kiralitási centrum esetén:
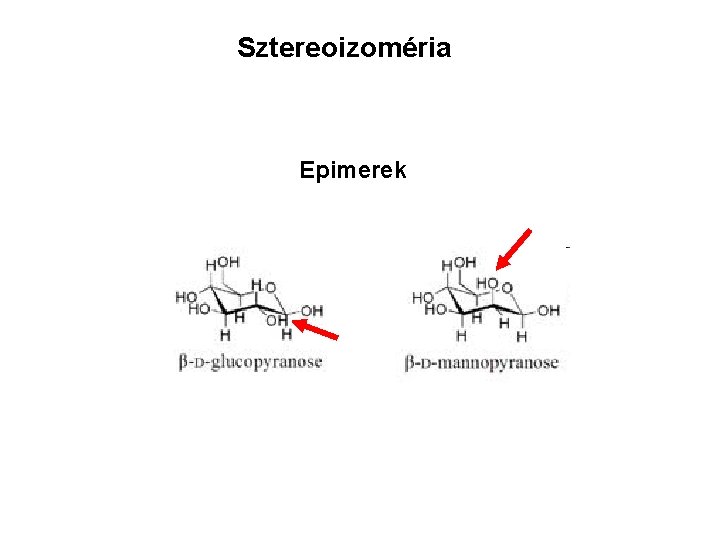
Sztereoizoméria Epimerek
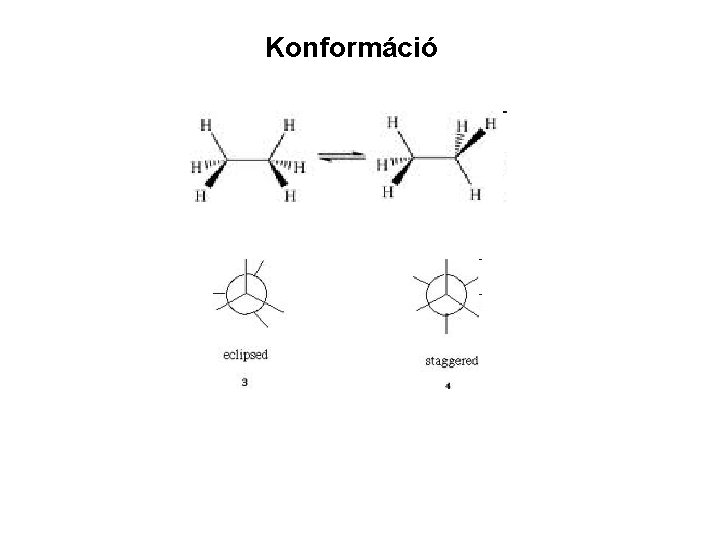
Konformáció
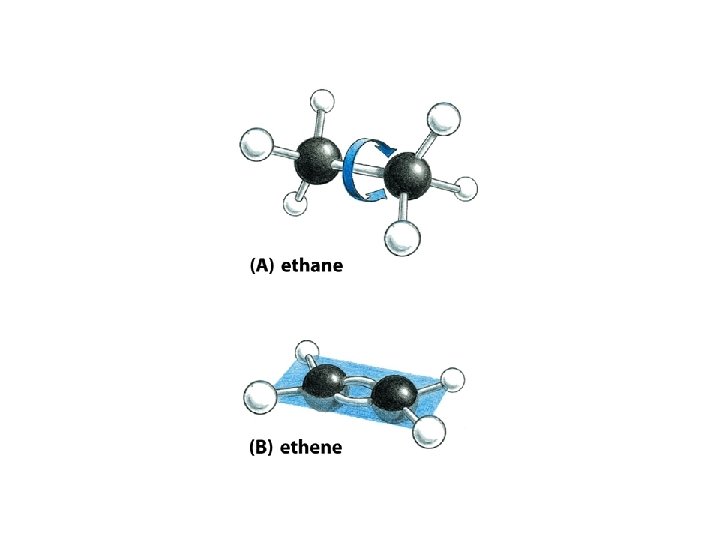
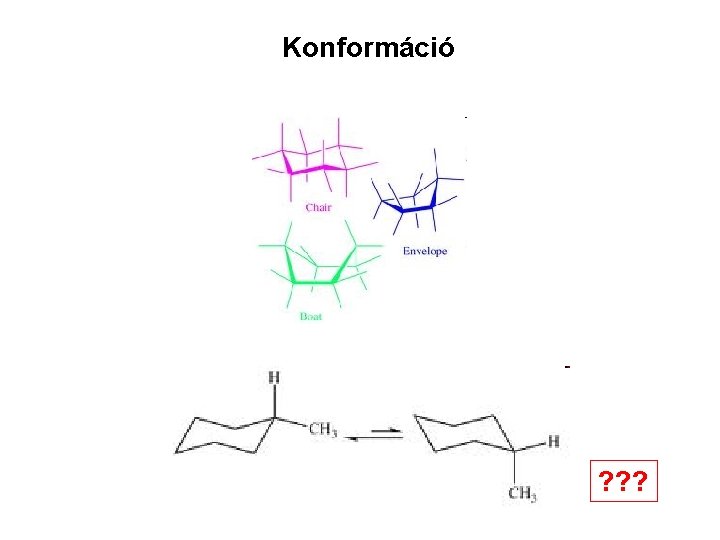
Konformáció ? ? ?

Kémiai reakciók - Az atomok/ionok/molekulák reagálni képesek egymással. - A funkciós csoportok jelenléte nagymértékben befolyásolja az adott molekula hajlandóságát egy adott típusú kémiai reakcióra. x·A + y·B n·C + m·D [C]n·[D]m K= [A]x·[B]y
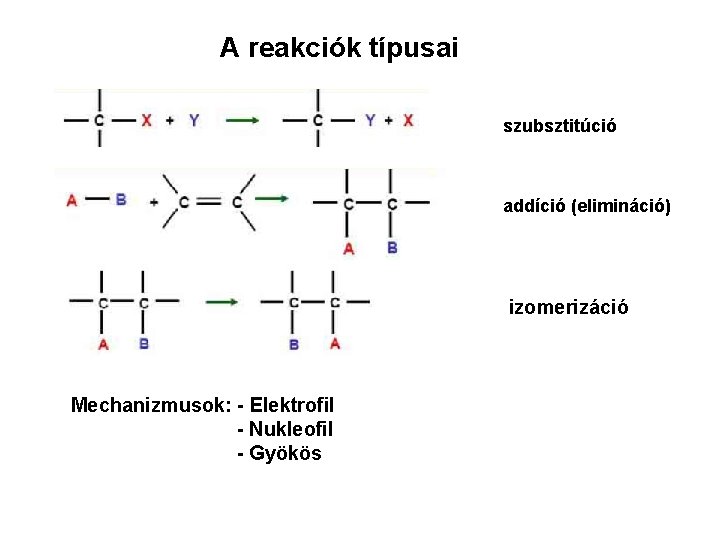
A reakciók típusai szubsztitúció addíció (elimináció) izomerizáció Mechanizmusok: - Elektrofil - Nukleofil - Gyökös

Sav-bázis reakciók: protonátmenet Redox reakciók: elektronátmenet Exergonikus reakciók: Maguktól végbemennek (ΔG: -) Endergonkus reakciók: Maguktól nem mennek végbe (ΔG: +)

Sav-bázis elméletek
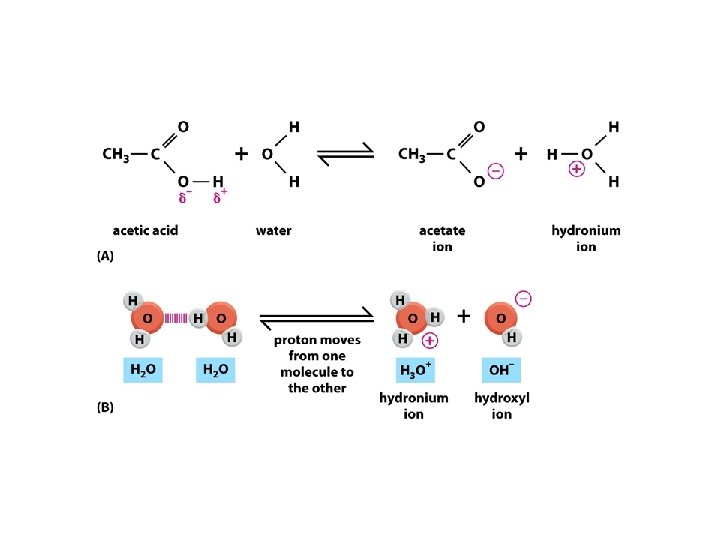
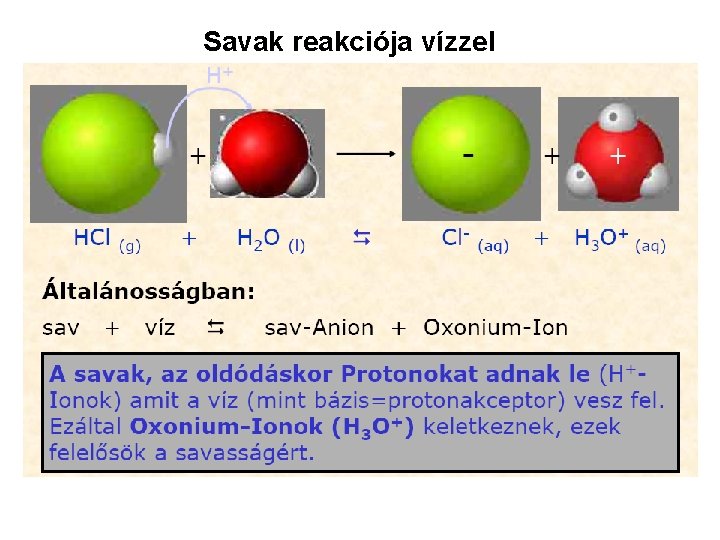
Savak reakciója vízzel
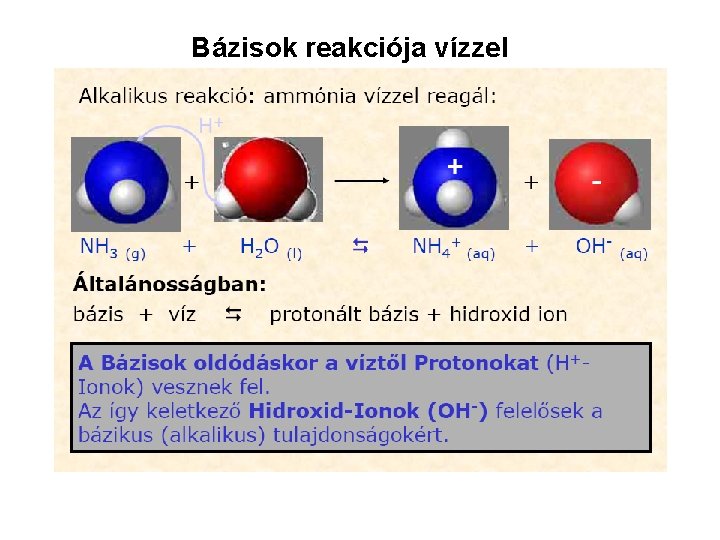
Bázisok reakciója vízzel
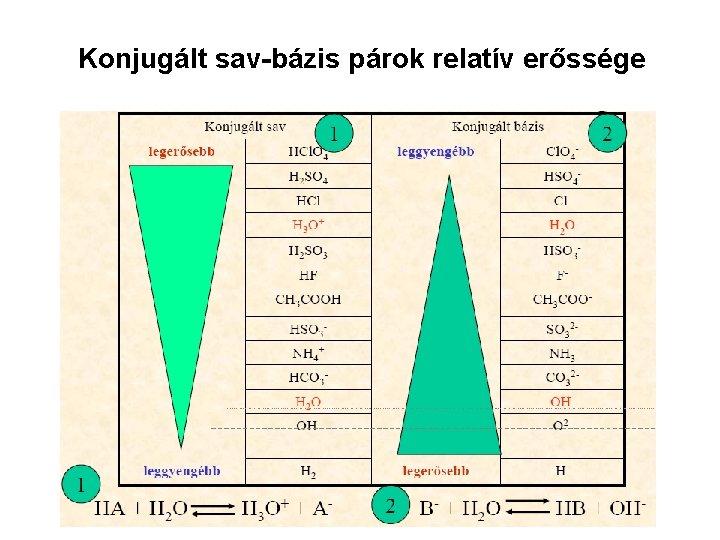
Konjugált sav-bázis párok relatív erőssége
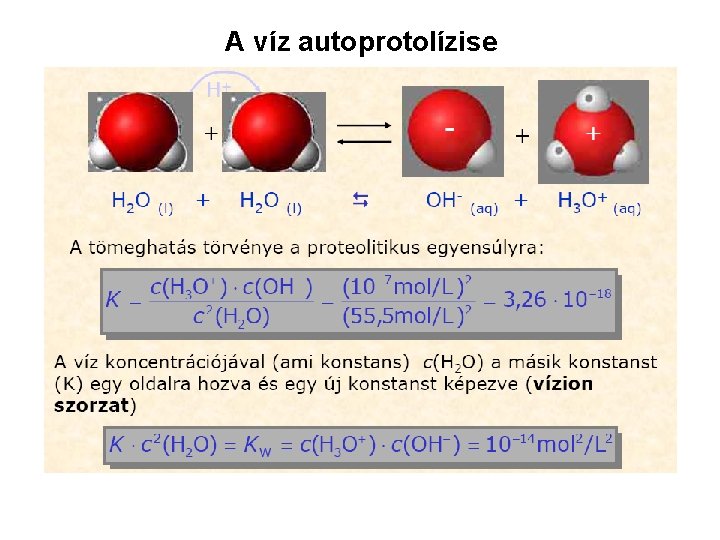
A víz autoprotolízise
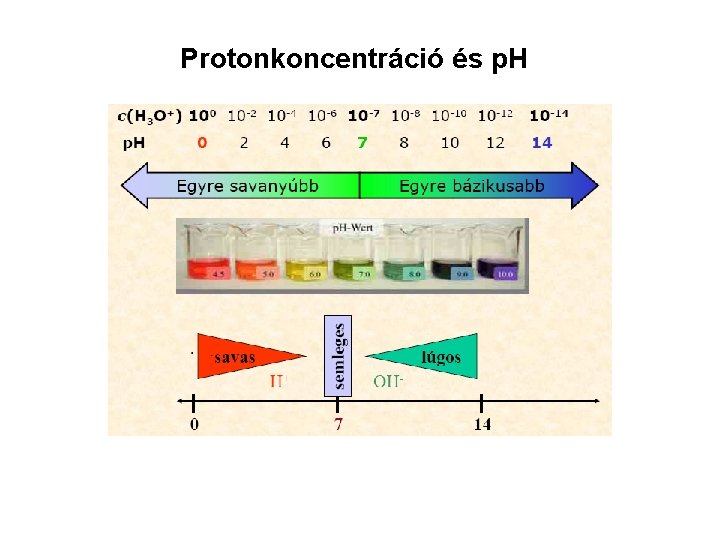
Protonkoncentráció és p. H

Egyensúlyi „állandó”

A víz disszociációja, a p. H fogalma Tömeghatás törvénye
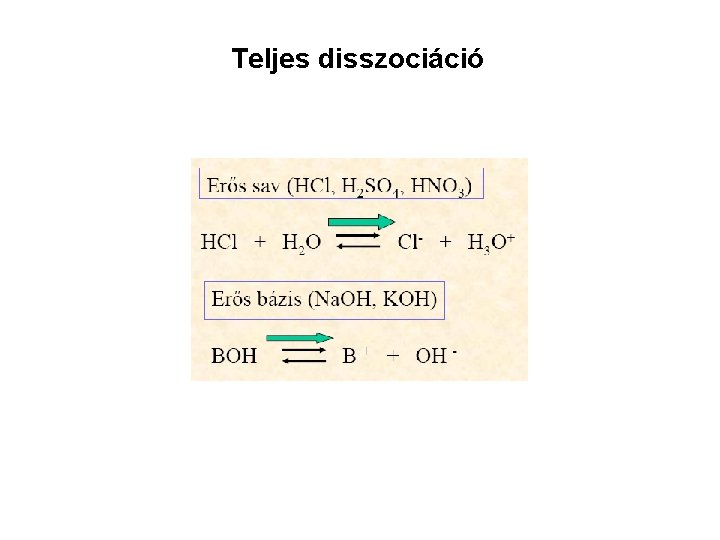
Teljes disszociáció

Gyenge savak p. H-ja
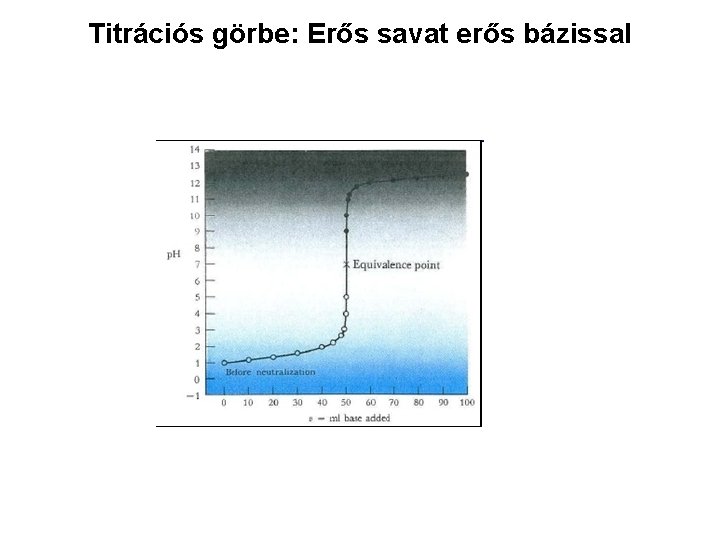
Titrációs görbe: Erős savat erős bázissal
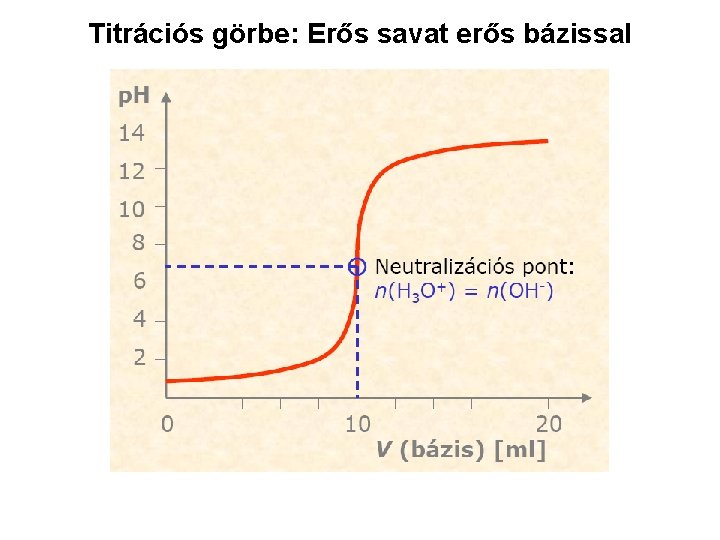
Titrációs görbe: Erős savat erős bázissal
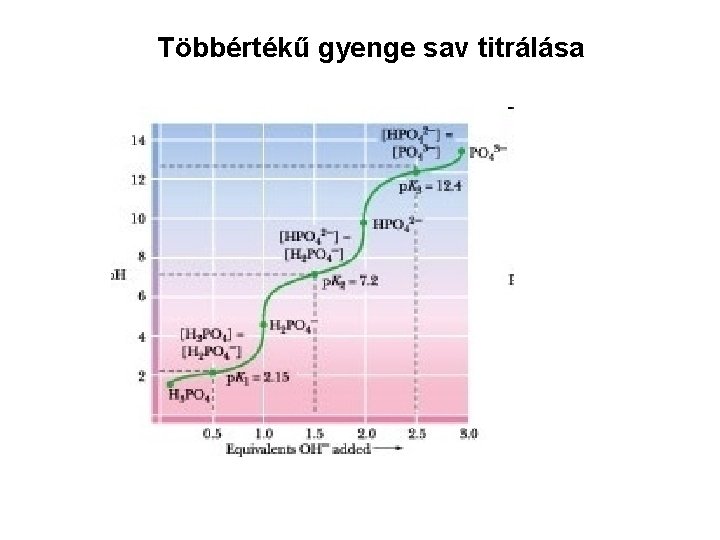
Többértékű gyenge sav titrálása
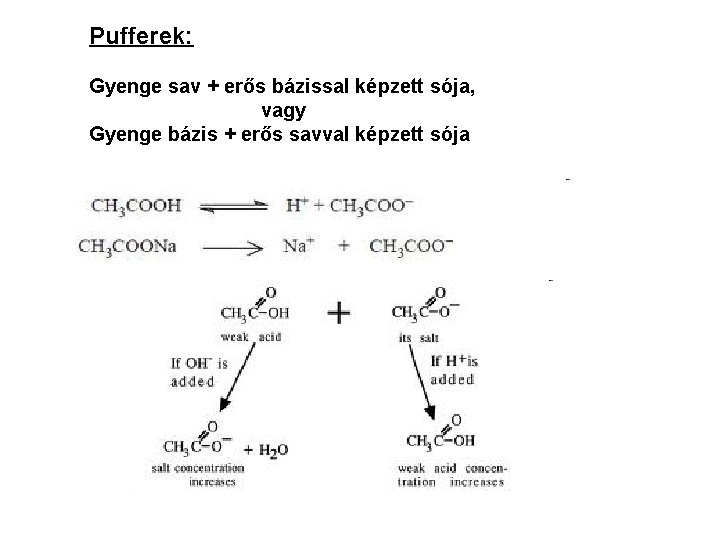
Pufferek: Gyenge sav + erős bázissal képzett sója, vagy Gyenge bázis + erős savval képzett sója

Pufferek p. H-jának kiszámolása

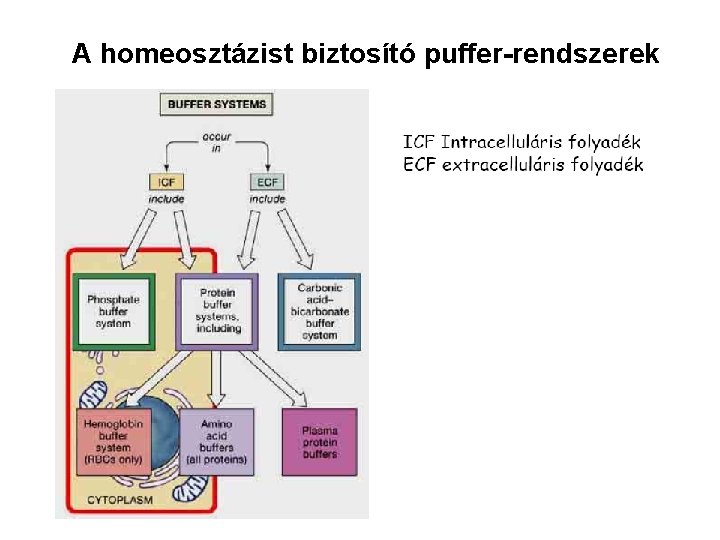
A homeosztázist biztosító puffer-rendszerek
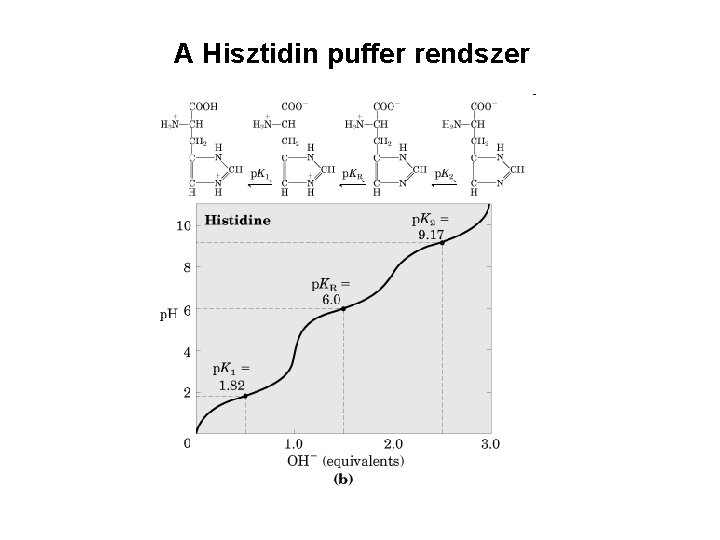
A Hisztidin puffer rendszer
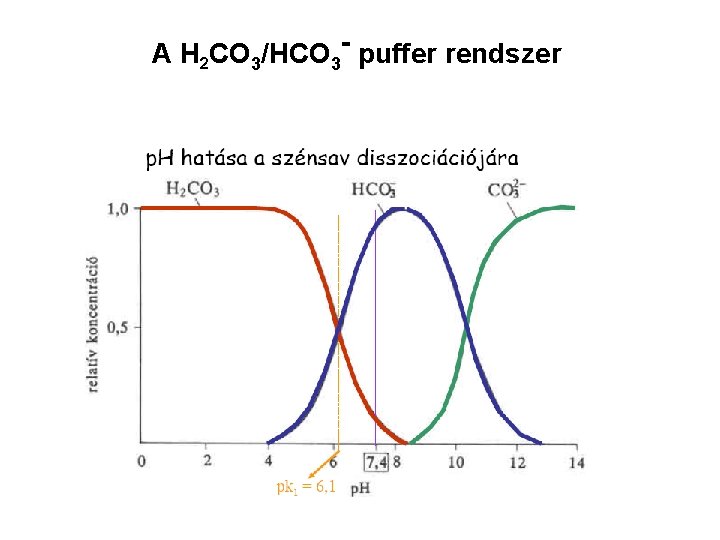
A H 2 CO 3/HCO 3 - puffer rendszer
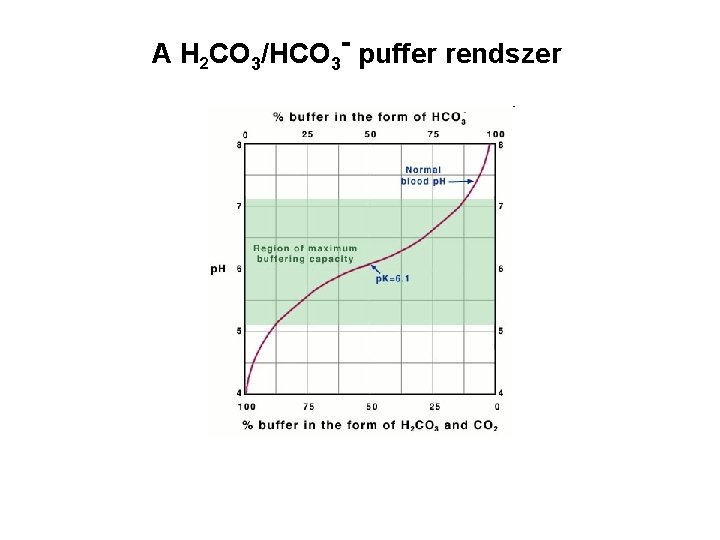
A H 2 CO 3/HCO 3 - puffer rendszer

Redox reakciók Elektronátmenttel, vagy oxidációs szám változással járó reakciók ? ? ?
- Slides: 75