Biofisicoqumica Introduccin a la Dinmica Molecular Dr Eduardo

Biofisicoquímica Introducción a la Dinámica Molecular Dr. Eduardo Prieto edprieto@quimica. unlp. edu. ar Dr. Ariel Alvarez aariel@iflysib. unlp. edu. ar INSTITUTO DE CIENCIAS DE LA SALUD UNIVERSIDAD NACIONAL ARTURO JAURETCHE Av. Lope de Vega 106, Florencio Varela – Buenos Aires – Argentina

¿Qué es la Dinámica Molecular Clásica? • Mecánica Clásica (Newtoniana) • Para cada átomo ƩF = M. a • Resolver las ecuaciones de movimiento para un sistema de N partículas que interactúan entre sí, a una dada temperatura y presión. • ¿Cómo interactúan? Las fuerzas se calculan a partir de potenciales de interacción.
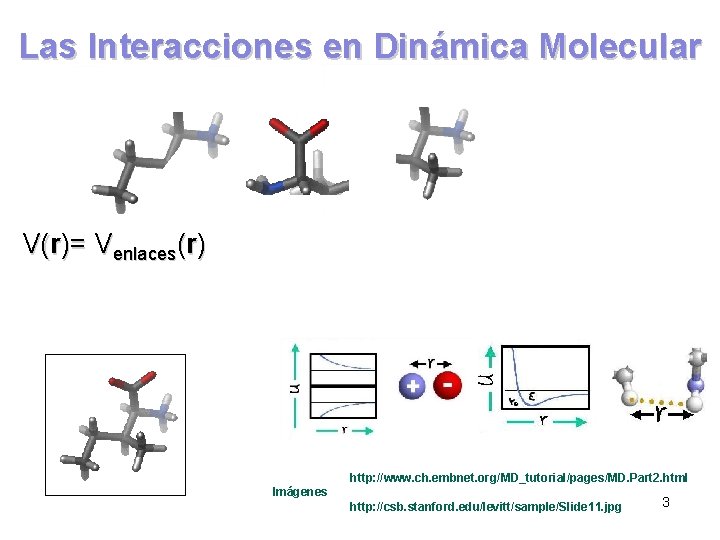
Las Interacciones en Dinámica Molecular V(r)= Venlaces(r) + Vángulos(r) + Vdihedros(r) + Vno-enlazantes(r) = VCoulomb(r) + VLJ(r) http: //www. ch. embnet. org/MD_tutorial/pages/MD. Part 2. html Imágenes http: //csb. stanford. edu/levitt/sample/Slide 11. jpg 3
Para describir las interacciones, además de los Potenciales, necesitamos información sobre las partículas que interactúan: • Carga • Masa • Parámetros de los Potenciales Campos de Fuerza

El Campo de Fuerzas Un campo de fuerzas usualmente consta de tres partes: • Un grupo de funciones (los potenciales). • Parámetros para esos potenciales, que, usualmente, dependen del tipo de átomo. • Un grupo definido de “bloques” (moléculas, monómeros, etc. – p. ej. aminoácidos). • Los campos de fuerza son “efectivos”.

La elección del Campo de Fuerzas La elección del campo de fuerzas es uno de los factores más importantes para realizar un estudio por DM • Un buen Campo de Fuerzas requiere de Años de Trabajo de Mucha gente. • ¡Todos los parámetros para todas las moléculas deben ser consistentes! • La primera pregunta es ¿Cuál campo de fuerzas tiene parámetros para todos los átomos del sistema? Cuando faltan parámetros: • Buscarlos en literatura. • Si no hay éxito, se deben construir (parametrización del campo de fuerzas).

Gráficamente…

¿Qué podemos estudiar por DM? • Propiedades de sólidos y líquidos TP. • Propiedades de pequeñas moléculas en solución.
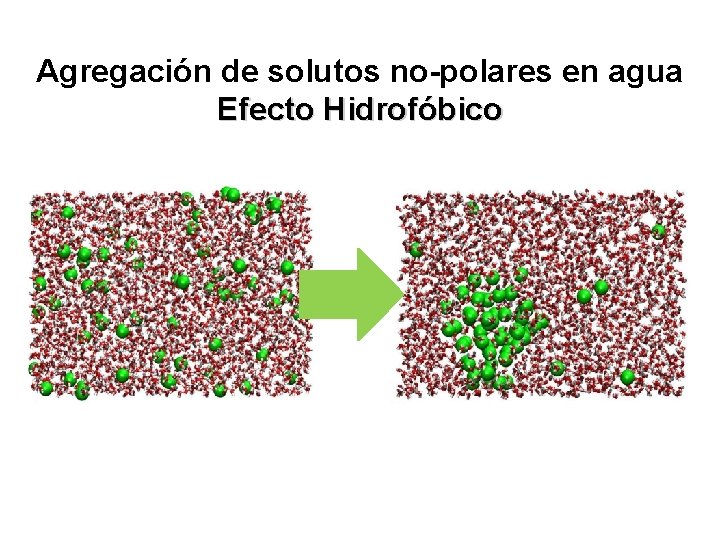
Agregación de solutos no-polares en agua Efecto Hidrofóbico
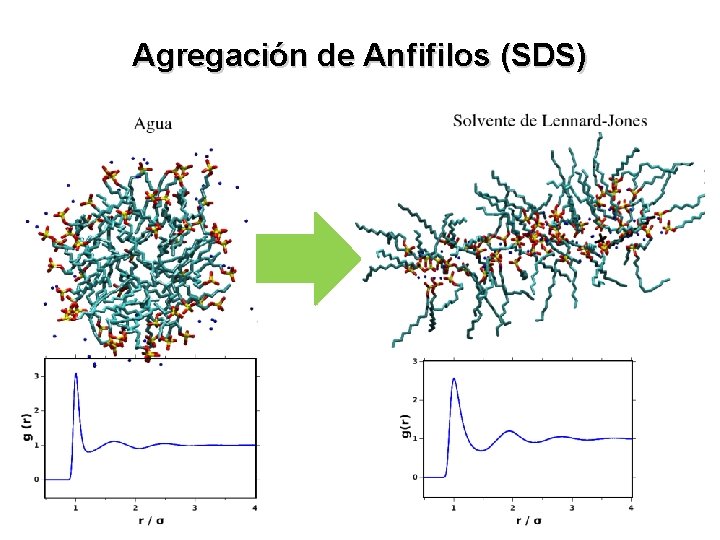
Agregación de Anfifilos (SDS)

¿Qué podemos estudiar por DM? • Propiedades de sólidos y líquidos TP. • Propiedades de pequeñas moléculas en solución. • Estabilidad de Biomacromoléculas, incluso en condiciones extremas, difíciles de alcanzar experimentalmente (Temperatura, presión, solventes). • Estudios cinéticos y búsqueda de mecanismos moleculares.
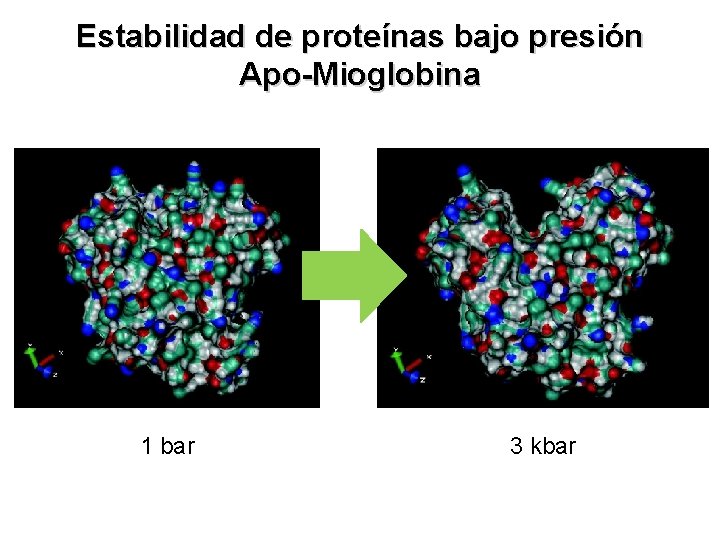
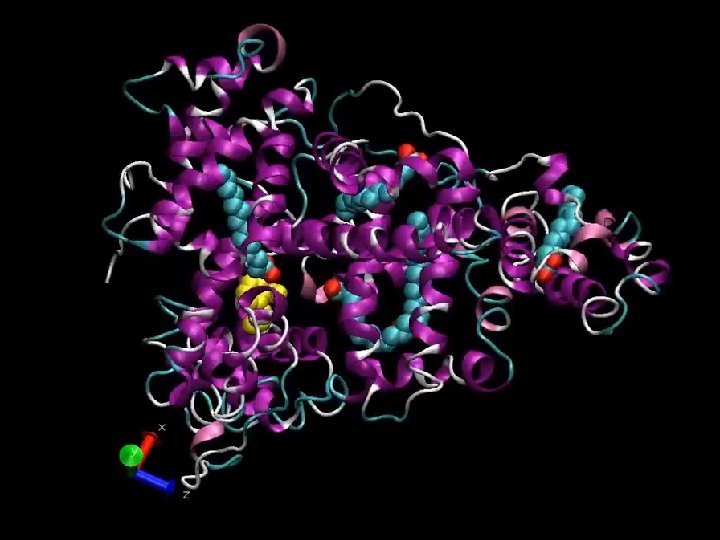
Estabilidad de proteínas bajo presión Apo-Mioglobina 1 bar 3 kbar

Práctico del Hielo • Esquema general – Parto de datos experimentales (ice. pdb) – Minimizo la energía (prueba “ 0” para el campo de fuerzas – modelo) – “Calentamos” a 100 K – Calentamos a 273 K – Calentamos a 320 K – Enfriamos a 273 K – Finalmente… ¡Analizamos!
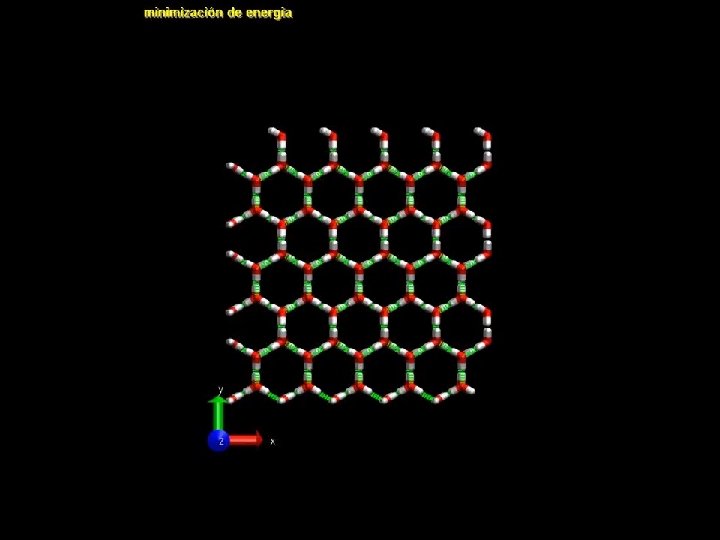
Ahora… la “Película”
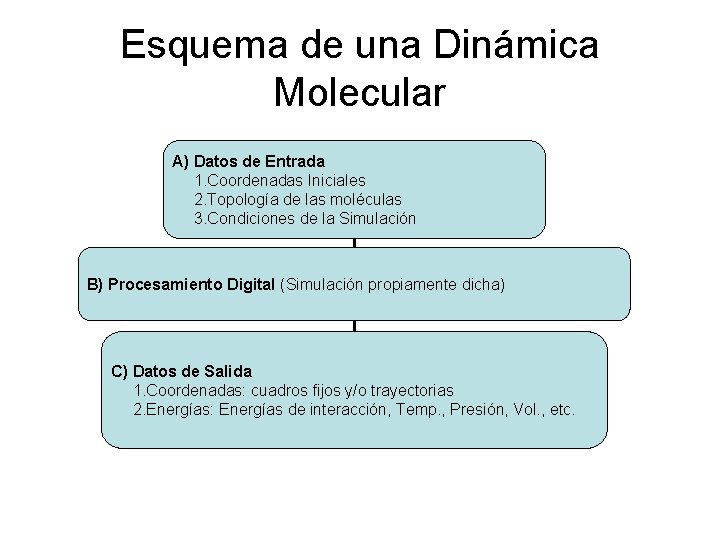
Esquema de una Dinámica Molecular A) Datos de Entrada 1. Coordenadas Iniciales 2. Topología de las moléculas 3. Condiciones de la Simulación B) Procesamiento Digital (Simulación propiamente dicha) C) Datos de Salida 1. Coordenadas: cuadros fijos y/o trayectorias 2. Energías: Energías de interacción, Temp. , Presión, Vol. , etc.
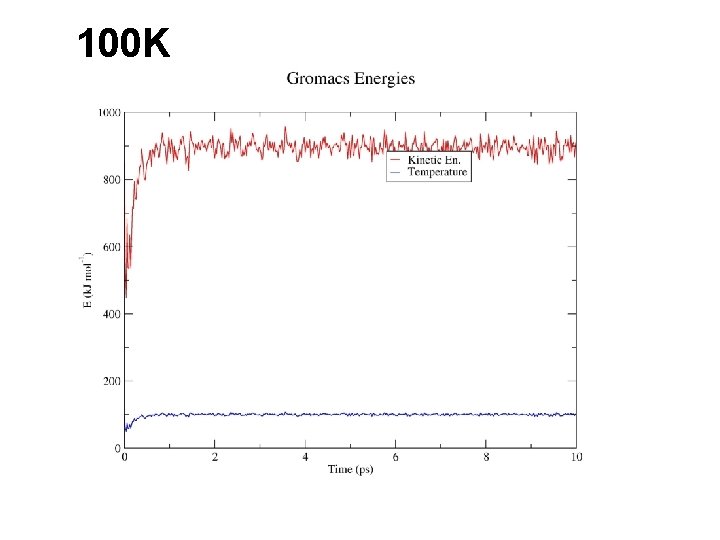
100 K
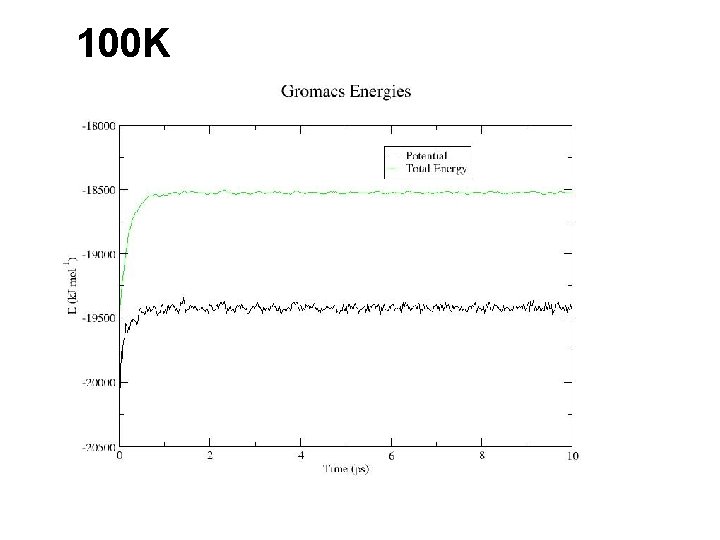
100 K
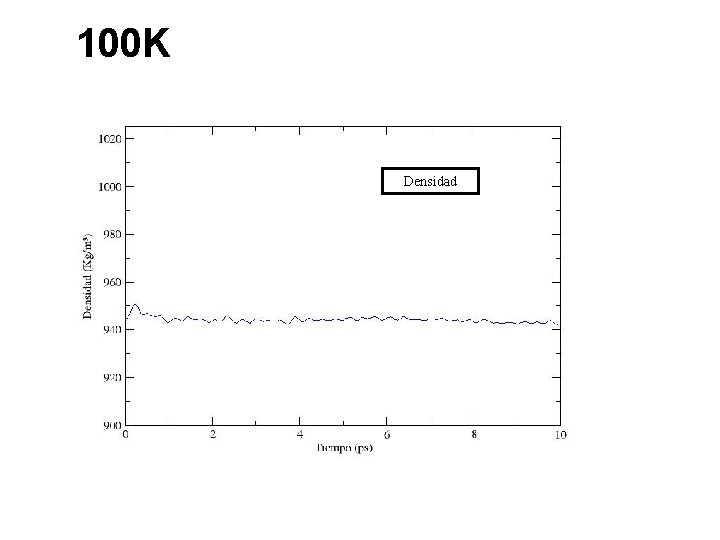
100 K Densidad
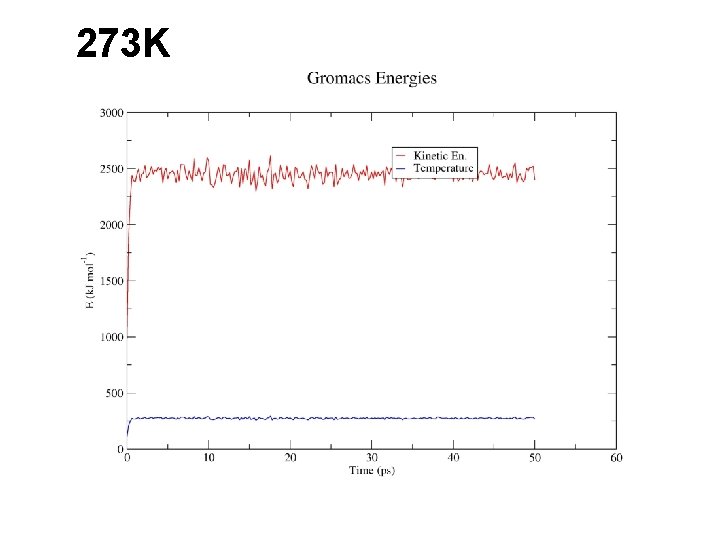
273 K
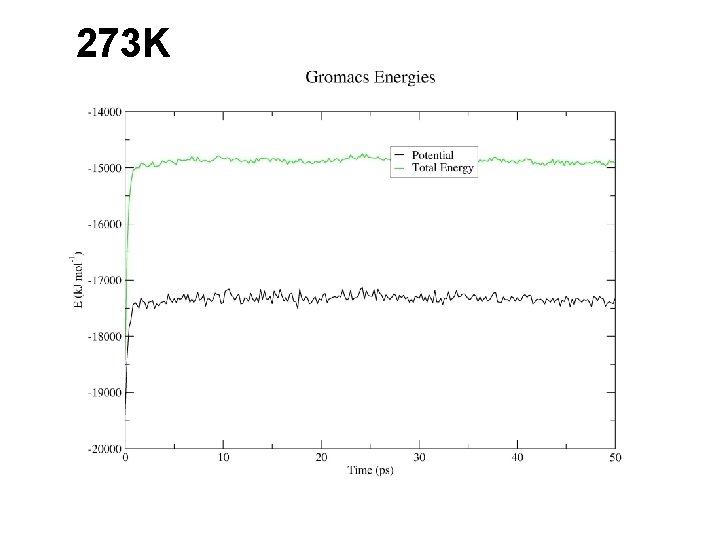
273 K
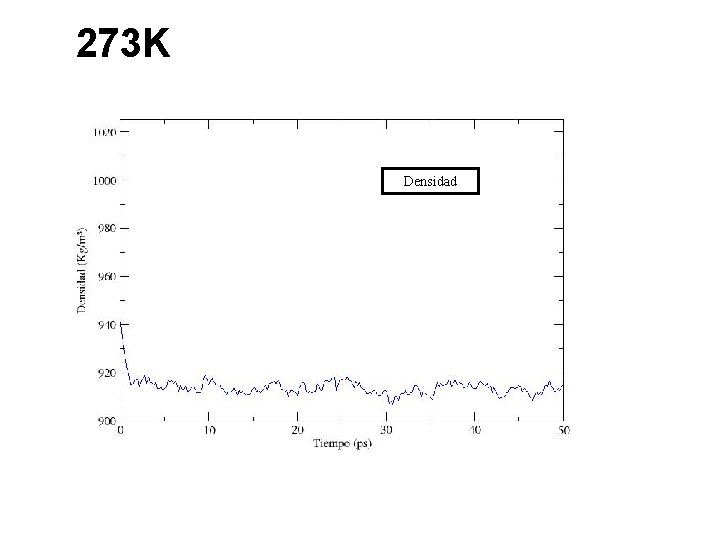
273 K Densidad
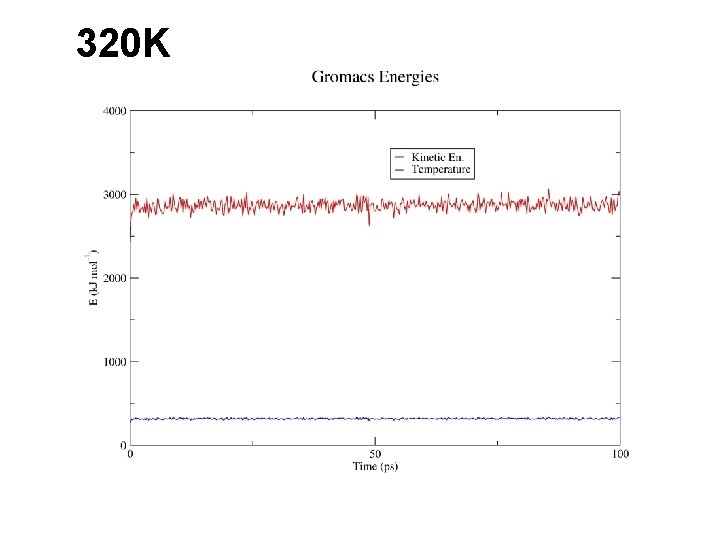
320 K
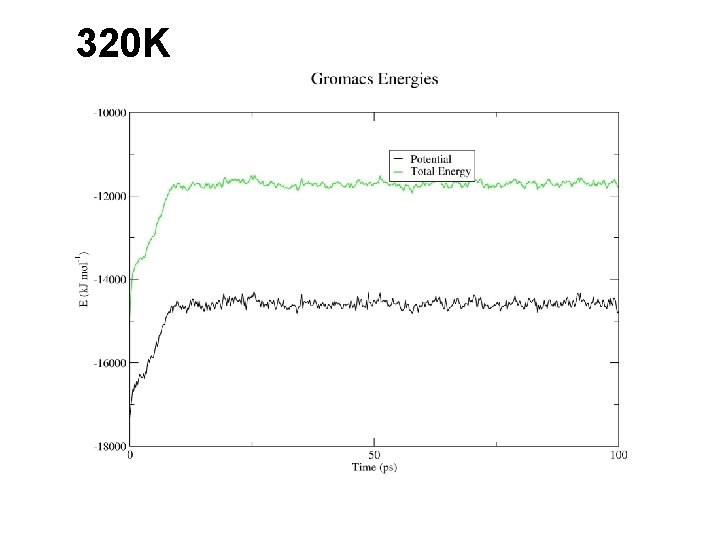
320 K
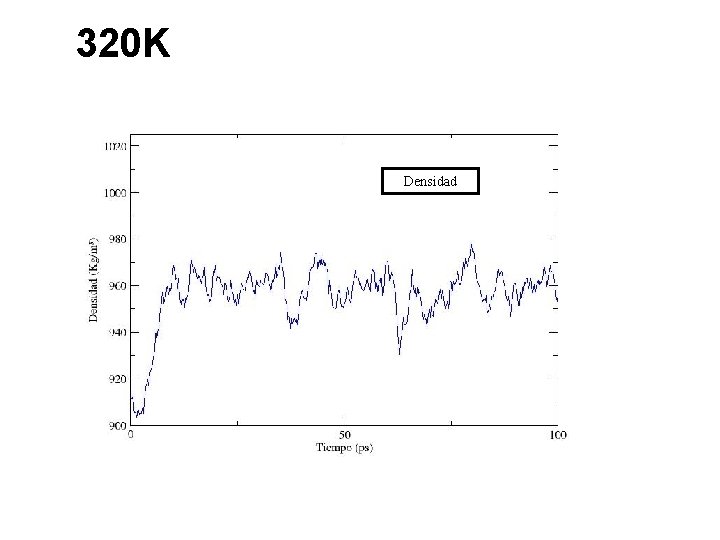
320 K Densidad
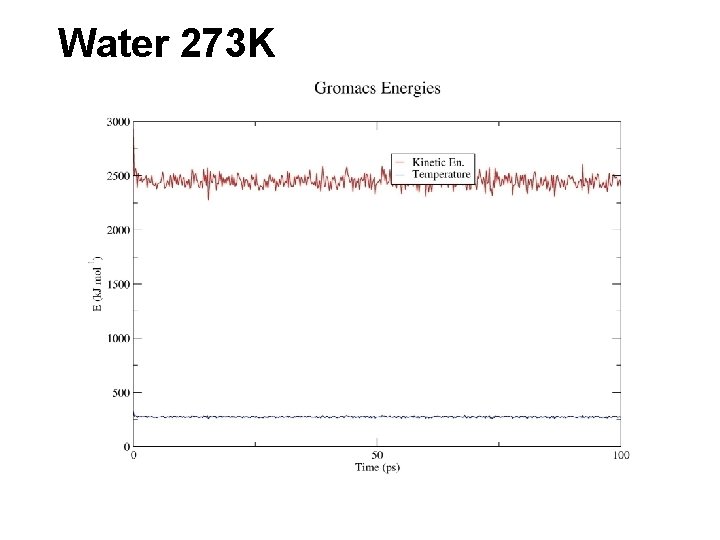
Water 273 K
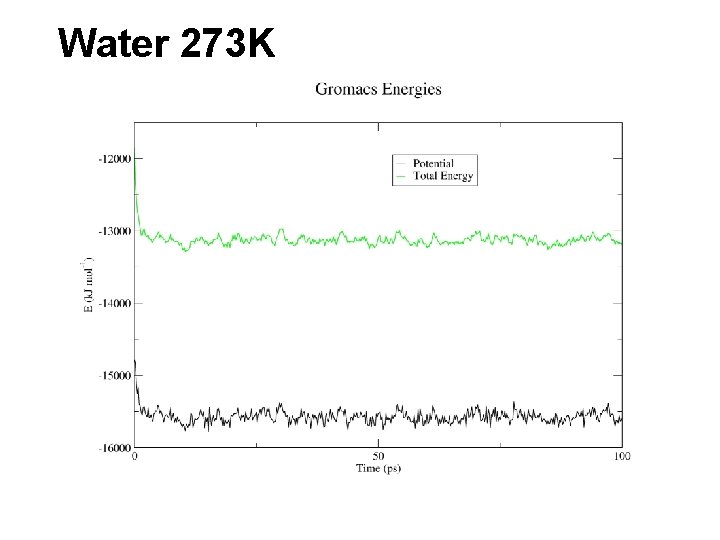
Water 273 K
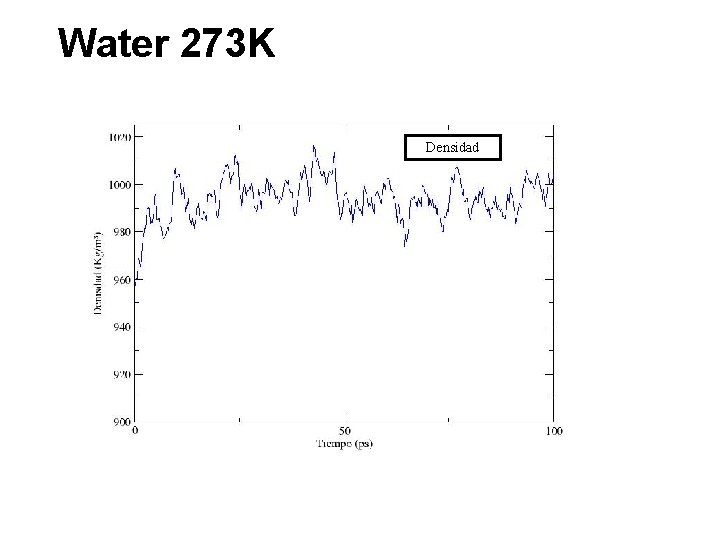
Water 273 K Densidad
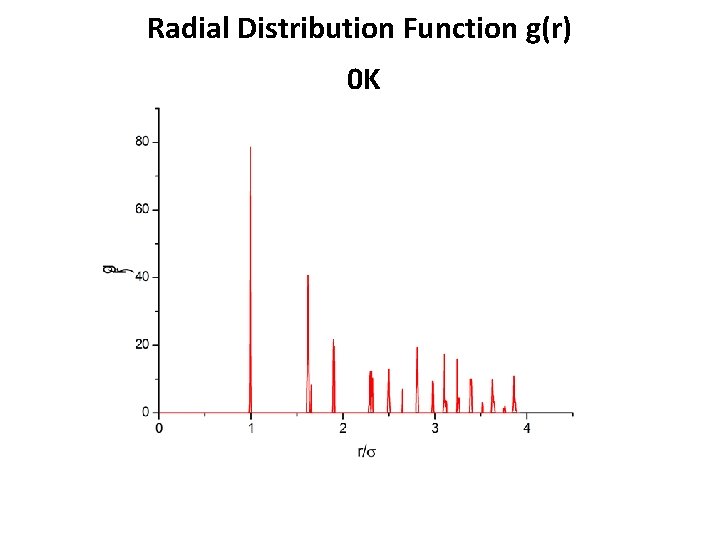
Radial Distribution Function g(r) 0 K
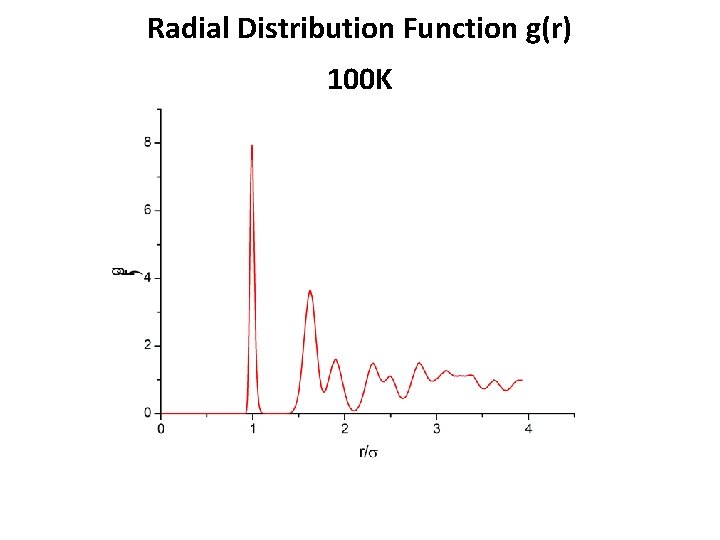
Radial Distribution Function g(r) 100 K
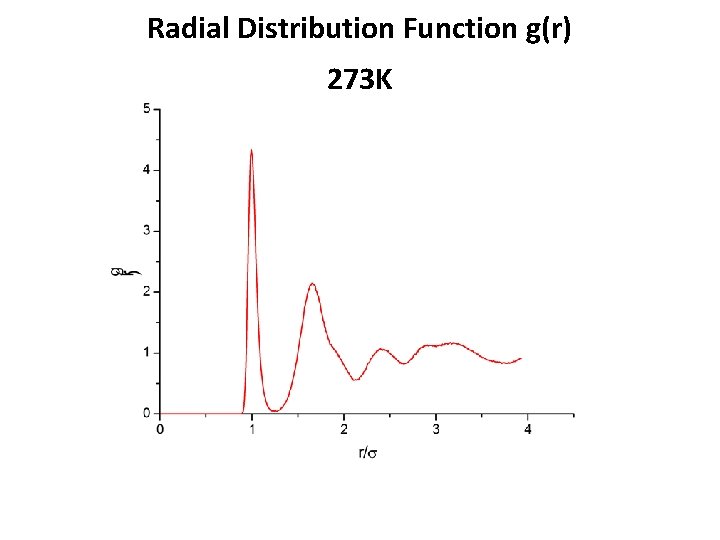
Radial Distribution Function g(r) 273 K
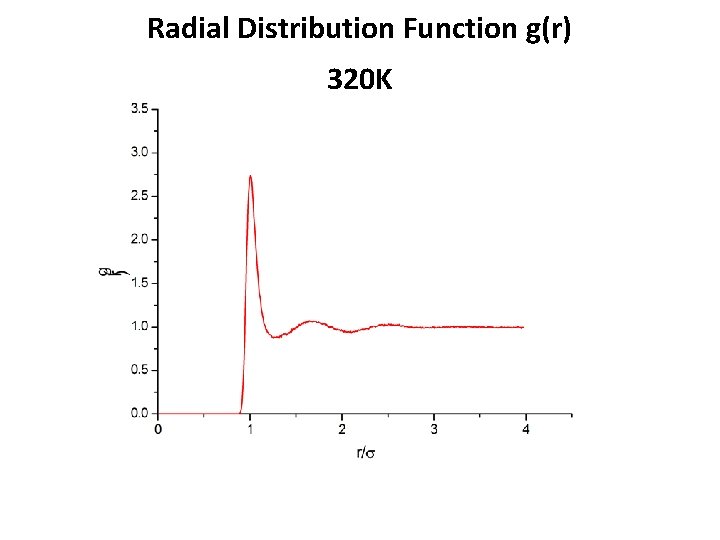
Radial Distribution Function g(r) 320 K
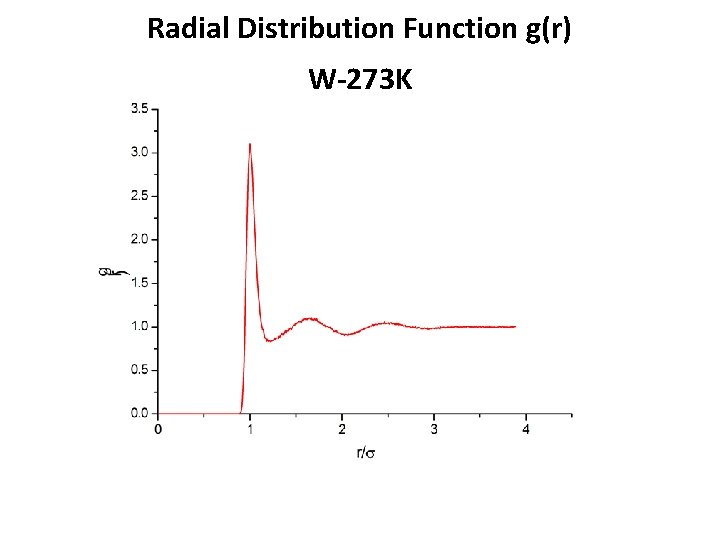
Radial Distribution Function g(r) W-273 K
- Slides: 33