BIOENERGTICA Para sobrevivir los humanos tenemos que consumir

BIOENERGÉTICA Para sobrevivir, los humanos tenemos que consumir alimentos, que es una forma ordenada de energía y convertirlo en calor, que es una forma desordenada de energía Stephen Hawking

“Los objetos vivientes están compuestos por moléculas inertes” Albert Lehninger

Necesidades esenciales de las células Constituyentes esenciales de la célula 1. Moléculas indispensables 2. Catalizadores que aceleren las reacciones= enzimas 3. Información para dirigir actividades =ADN ARN 4. Energía para impulsar actividades 5. La capacidad para obtener, utilizar y almacenar energía es de hecho una de las características mas evidentes de los seres vivos

Materia y Energía l Materia: todo lo que tiene masa, volumen y ocupa un lugar en el espacio l Energía: La capacidad de un sistema para realizar un trabajo l Clases de Energía: mecánica, eléctrica, potencial, química, calorífica lumínica etc.

• TERMODINÁMICA • Therme (Calor) – Dynamis (Energía) FORMA DE RELACIONAR LAS DIVERSAS FORMAS DE ENERGÍA Y EL MODO EN QUE ÉSTA AFECTA LA MATERIA. BIOENERGETICA l La bioenergética o termodinámica es: Capacidad de causar cambios específicos l El estudio de los cambios de energía que acompañan a las reacciones bioquímicas, o sea el estudio del uso y de las transformaciones energéticas en los sistemas vivos.

Seis tipos de cambios que necesitan energía 1. Trabajo de síntesis: cambios en los enlaces químicos: Biosíntesis 2. Trabajo Mecánico: en la localización y orientación de una célula o de su estructura subcelular: mov. Bacterias, células ciliadas sist. Respiratorio movimiento cromosomas 3. Trabajo de concentración: movimiento de moléculas a través de una membrana en contra de un gradiente de concentración, para acumular substancias 4. Trabajo Eléctrico: movimiento de iones a través de membrana en contra de gradiente electroquímico mitocondria, cloroplasto producción ATP; cels nerviosas 5. Calor: Aumento de temperatura cambios de temperatura 6. Bioluminiscencia: producción de luz
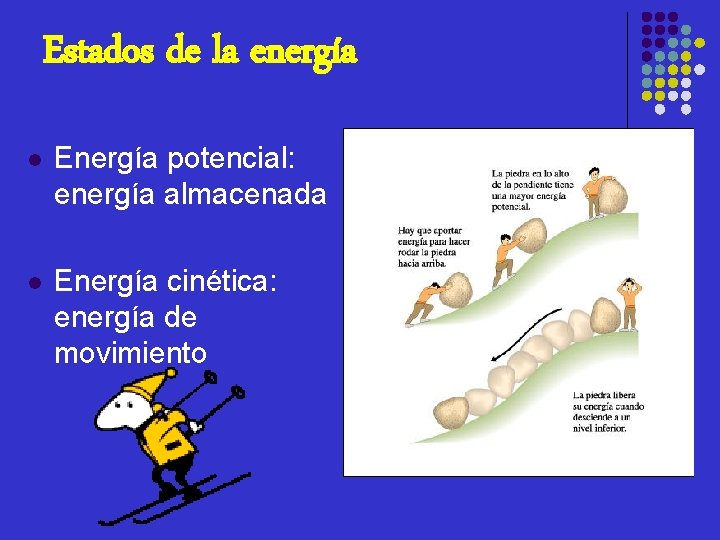
Estados de la energía l Energía potencial: energía almacenada l Energía cinética: energía de movimiento

TRANSFORMACIÓN DE LA ENERGIA l l l Potencial en cinética Eléctrica en mecánica Química en térmica Iónica en eléctrica: movimiento de iones a través de la membrana Radiante en química: formación de almidón a partir de CO 2 + H 2 O+ luz solar

El Universo l Se compone de dos partes: l Sistema: l La parte del universo bajo estudio l Espacio físico o porción de materia contenida dentro de un límite o frontera l Ej. una célula, una máquina l Entorno l Región fuera del límite o frontera l El sistema intercambia materia o energía con él

• EL SISTEMA ABIERTO n. El sistema abierto como organismo, es influenciado por el medio ambiente e influye sobre el, alcanzando un equilibrio dinámico en ese sentido. n La categoría más importante de los sistemas abiertos son los sistemas vivos. Existen diferencias entre los sistemas abiertos (como los sistemas biológicos y sociales, a saber, células, plantas, el hombre, la organización, la sociedad) y los sistemas cerrados (como los sistemas físicos, las máquinas, el reloj, el termóstato):

n El sistema abierto interactúa constantemente con el ambiente en forma dual, o sea, lo influencia y es influenciado. El sistema cerrado no interactúa. n El sistema abierto puede crecer, cambiar, adaptarse al ambiente y hasta reproducirse bajo ciertas condiciones ambientes. El sistema cerrado no. n Es propio del sistema abierto competir con otros sistemas, no así el sistema cerrado

• EN RESUMEN: • El sistema abierto es un conjunto de partes en interacción constituyendo un todo sinérgico, orientado hacia determinados propósitos y en permanente relación de interdependencia con el ambiente externo

La energía existe en diversas formas: luz, azúcar, movimiento de flagelo, electrón excitado, es de distribución universal Sistema: es una porción limitada de universo a evaluar Entorno: el resto del universo que lo rodea Sistemas abiertos o cerrados: si hay o no intercambio energía con entorno El intercambio de energía entre un sistema y entorno se produce de dos formas como calor que es la transferencia de energía de un lugar a otro poco útil en sistemas biológicos. Como trabajo: cualquier proceso que no involucre cambio de calor Caloría: Forma de cuantificar las variaciones de energía durante reacciones qq o procesos físicos

Termodinámica l Estudio de los cambios energéticos y el flujo de energía en un sistema l Las leyes de termodinámica no sólo gobiernan los cambios energéticos en una reacción, sino que proveen las herramientas que permiten predecir si la reacción será o no espontánea

Leyes de la Termodinámica l 1 ra. Ley Conservación de la energía: energía la energía no se crea ni se destruye, solo se transforma l 2 da. Ley Todos los sistemas tienden al equilibrio: equilibrio La inercia de todo sistema tiende a ir del orden al desorden Los eventos del universo proceden cuesta abajo para minimizar su contenido de energía libre l

Primera Ley de Termodinámica -LEY DE LA CONSERVACIÓN DE ENERGÍA -LA ENERGÍA DEL UNIVERSO ES CONSTANTE EL CALOR PUEDE SER ÚTIL PARA REALIZAR TRABAJO SOLO SI EXISTE UNA DIFERENCIA DE TEMPERATURA ENTRE EL SISTEMA Y EL AMBIENTE. NOSOSTROS SOMOS ISOTERMICOS INTERNAMENTE.
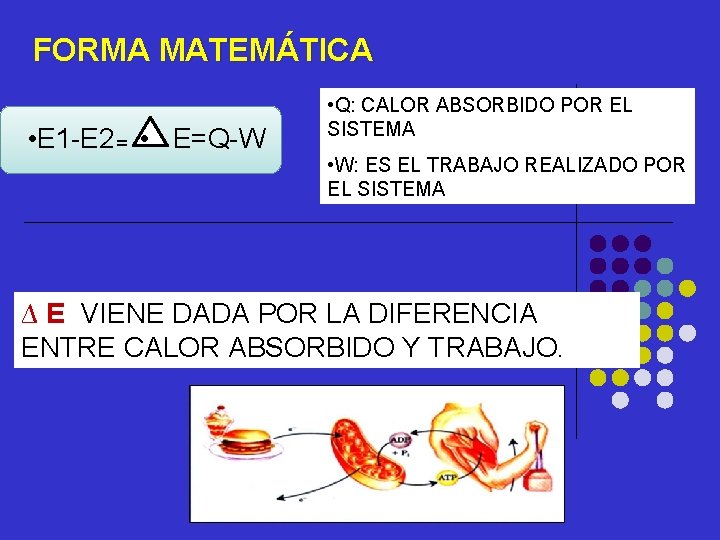
FORMA MATEMÁTICA • E 1 -E 2= • E=Q-W • Q: CALOR ABSORBIDO POR EL SISTEMA • W: ES EL TRABAJO REALIZADO POR EL SISTEMA ∆ E VIENE DADA POR LA DIFERENCIA ENTRE CALOR ABSORBIDO Y TRABAJO.

• MUERTE POR INANICIÓN, SE AGOTAN LAS RECERVAS DE ENERGÍA. • MUERTE POR OBOSIDAD ALMACENAMIENTO ELEVADO DE ENERGÍA

l Cuando se alcanza el contenido mínimo de energía en un sistema, se dice que el sistema está en equilibrio l En una reacción química los reactantes se convierten en productos, y viceversa. REACTANTES Glucógeno PRODUCTOS Glucosas libres

Equilibrio Químico l Las reacciones químicas también tienden al equilibrio, éste se establece cuando las velocidades de las reacciones directa e inversa son iguales A + B C + D Reacción directa Reacción inversa

Constante de equilibrio Keq l Es la razón que se establece entre la concentración de los reactivos y de los productos en el equilibrio Keq = K 1 / K 2 = [C][D] / [A][B] l Se calcula dividiendo la concentración de los productos entre la concentración de los reactivos: K eq [C] [D] [A] [B]

Valores de la Keq l Keq > 1 concentración de productos mayor que concentración de reactantes. La reacción favorecida es hacia la derecha (reacción directa) l Keq < 1 concentración de reactivos mayor que concentración de productos. La reacción favorecida es hacia la izquierda (reacción inversa) l Keq = 1 concentración de reactivos igual a concentración de productos

La bioenergética o termodinámica bioquímica es el estudio de los cambios de energía que acompañan a las reacciones bioquímicas, o sea el estudio del uso y de las transformaciones energéticas en los sistemas vivos.

Bioenergética l Describe la transferencia y utilización de la energía en los sistemas biológicos l Utiliza las ideas básicas de la termodinámica, particularmente el concepto de energía libre l Los cambios en la energía libre (∆G) permite cuantificar y predecir la factibilidad energética de una reacción química

Cualquier TRANSFORMACION se describe comparando las propiedades físicas o químicas, o ambas, de los estados inicial y final de un sistema, ésta requiere energía del medio, su descripción puede darse en función de:

ENERGIA INTERNA= INTERNA E (energía total de un sistema) ENTALPIA = H (contenido calórico del sistema, no ΔT) ENTROPIA= ENTROPIA S (grado de desorden del sistema) ENERGIA LIBRE = G (energía disponible) Su valor real es difícil o imposible de medir, por lo que se trata con CAMBIOS (Δ): estado inicial estado final (Ef - Ei ) En las funciones de estado Δ E, Δ H, Δ S y Δ G.

Espontaneidad termodinámica: puede o no producirse, pero no se producirá. Segunda Leydice de que Termodinámica La medida de espontaneidad es proporcionada por la segunda ley de la Termodinámica. “En cada cambio físico o químico, el universo siempre tiende hacia el mayor desorden o aleatoriedad o desorden” Entropía “S”: medida de la aleatoriedad o desorden de un sistema Energía Libre “G”: es la medida de la espontaneidad para un sistema. Su variación es medida de espontaneidad

ENERGÍA LIBRE (ΔG) : Es el cambio de energía disponible durante un proceso para efectuar trabajo. Josiah Willard Gibbs (1839 -1903) ΔH= ΔG + TΔS En condiciones de temperatura y presión constantes Entalpia= Energia Libre + Termp*Entropia
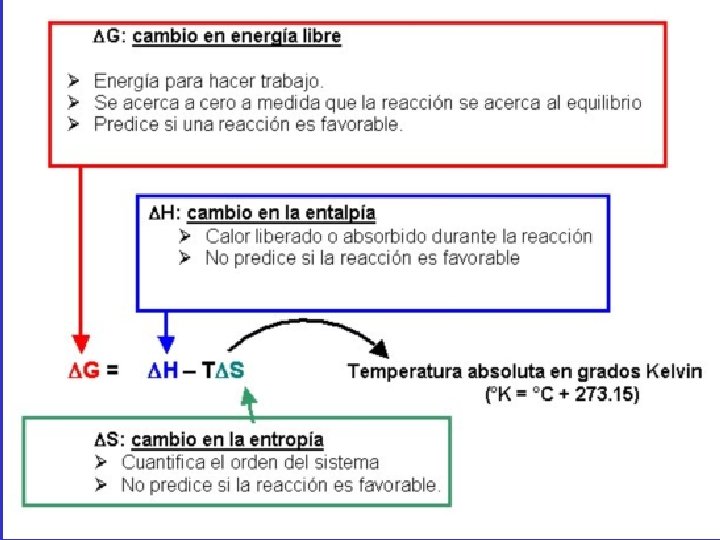

ENERGÍA LIBRE ESTÁNDAR (ΔGº’): Describe la diferencia de energía libre cuando un mol de cada reactante se convierte en un mol de producto a condiciones estándar: estándar A 25ºC, 1 Atm de presión, reactantes y productos a concentración de 1. 0 M y p. H 7

ENERGÍA LIBRE ESTÁNDAR (ΔGº’): ΔG se calcula a partir de la CONSTANTE DE EQUILIBRIO ó Keq que es la proporción predecible entre concentración de productos y concentración de reactantes. La Keq permite PREDECIR la dirección favorecida de una reacción mediante: Δ G°’ = - RT ln Keq Donde: R = constante de los gases (1. 9 cal/grado/mol) T = temperatura absoluta (298°Kelvin) ln Keq = logaritmo natural de la Keq

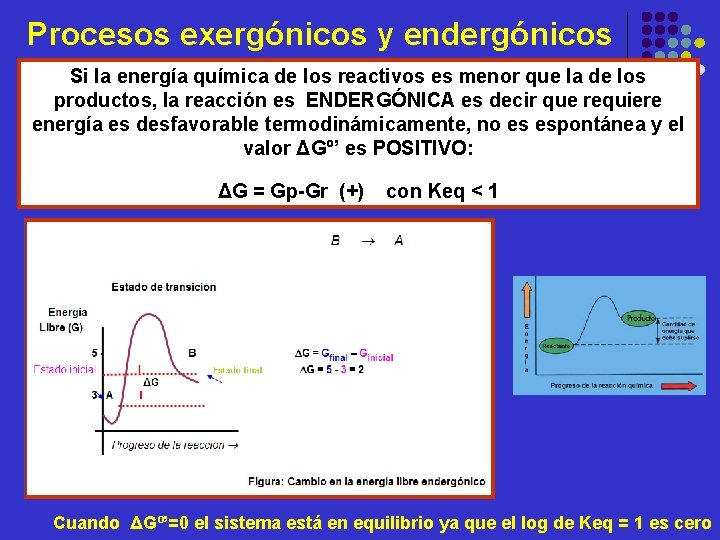
Procesos exergónicos y endergónicos Si la energía química de los reactivos es menor que la de los productos, la reacción es ENDERGÓNICA es decir que requiere energía es desfavorable termodinámicamente, no es espontánea y el valor ΔGº’ es POSITIVO: ΔG = Gp-Gr (+) con Keq < 1 Cuando ΔGº’=0 el sistema está en equilibrio ya que el log de Keq = 1 es cero
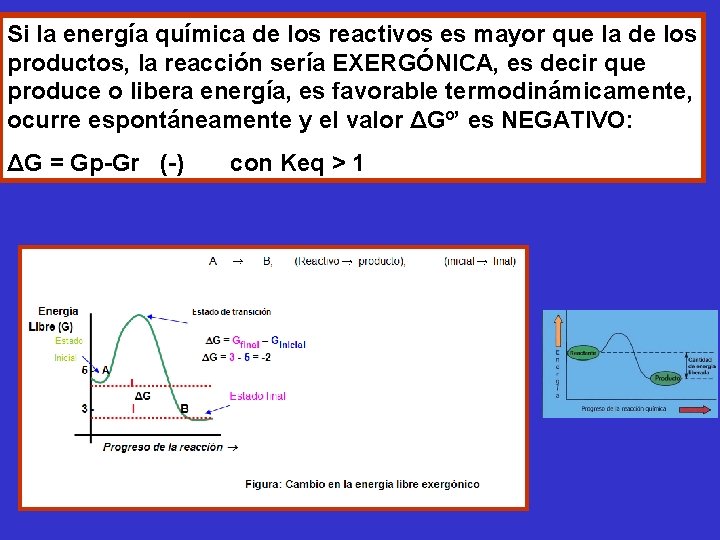
Si la energía química de los reactivos es mayor que la de los productos, la reacción sería EXERGÓNICA, es decir que produce o libera energía, es favorable termodinámicamente, ocurre espontáneamente y el valor ΔGº’ es NEGATIVO: ΔG = Gp-Gr (-) con Keq > 1

Proceso espontáneo y proceso que requiere energía

l Reacción exergónica l Reacción química que es cuesta abajo l Es espontánea l Libera energía al entorno l Su Keq es > 1 l Su DGº < 1 (negativa) l Reacciones de oxidación l Pérdida de electrones l Ganancia de Oxígeno l Pérdida de H l CATABOLISMO • Reacción endergónica • Reacción química que ocurre cuesta arriba • No es espontánea • Necesita energía para ocurrir • Su Keq es < 1 • Su DGº > 1 (positiva) • Reacciones de reducción • Ganancia de electrones • Pérdida de Oxígeno • Ganancia de H • ANABOLISMO

Los organismos vivos capturan energía de su ambiente porque no la pueden crear y la cambian a otras formas que puedan utilizar para hacer trabajo. Ej. Las células vegetales capturan la energía lumínica del sol a través del proceso de fotosíntesis y la convierten en energía química que es almacenada en los enlaces químicos de las moléculas orgánicas. Cuando la célula necesita esa energía o cuando un humano ingiere la planta como alimento, la energía química es liberada al romper los enlaces de las moléculas orgánicas. Esta energía es entonces utilizada para hacer distintos tipos de trabajo en las células.
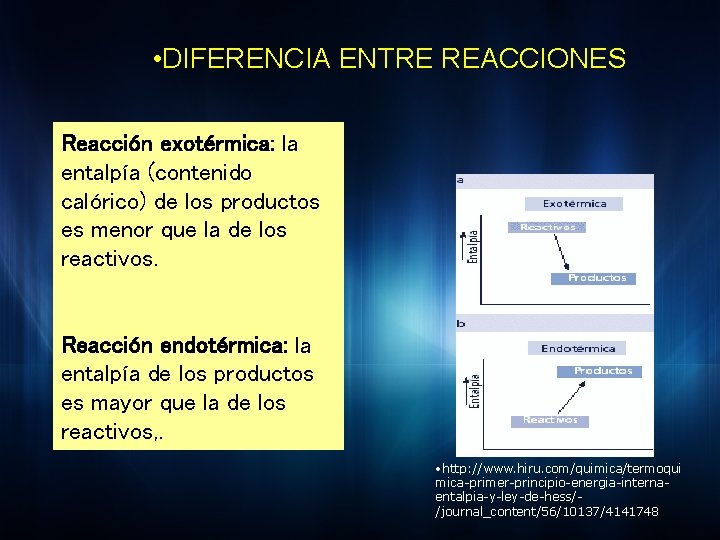
• DIFERENCIA ENTRE REACCIONES Reacción exotérmica: la entalpía (contenido calórico) de los productos es menor que la de los reactivos. Reacción endotérmica: la entalpía de los productos es mayor que la de los reactivos, . • http: //www. hiru. com/quimica/termoqui mica-primer-principio-energia-internaentalpia-y-ley-de-hess//journal_content/56/10137/4141748

Entropía / Aleatoriedad / Desorden Es una expresión cuantitativa de la aleatoriedad o desorden de un sistema cuando los productos de una reacción son menos complejos y mas desordenados que los reactivos se dice que la reacción transcurre con ganancia de entropía.
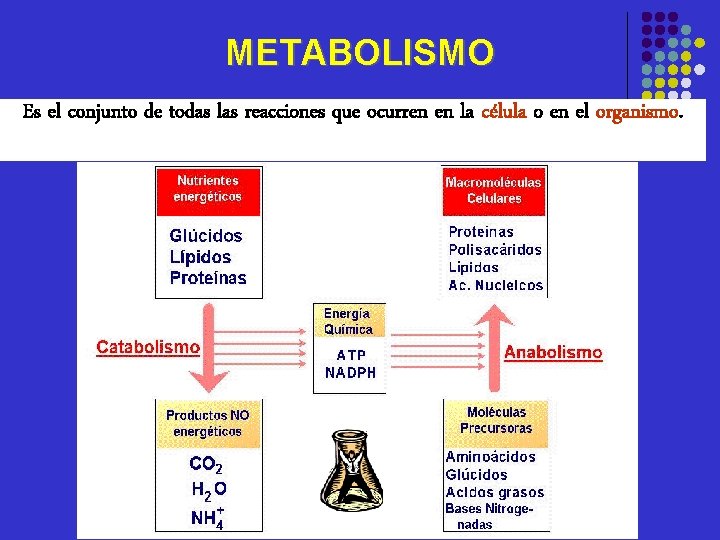
METABOLISMO Es el conjunto de todas las reacciones que ocurren en la célula o en el organismo.

Una ruta metabólica son un conjunto de reacciones secuenciales consecutivas que tienen como finalidad formar determinado producto, a cada uno de los intermediarios se le llama metabolito.

METABOLISMO l Conjunto de reacciones bioquímicas que ocurren en un organismo, incluyendo su coordinación, regulación y necesidades energéticas l El metabolismo es un proceso de transformación de energía donde el catabolismo proporciona la energía requerida para el anabolismo

ANABOLISMO l Ruta metabólica de biosíntesis o construcción macromoléculas (proteínas, DNA, etc. ) a partir de moléculas precursoras más pequeñas l Se dan los procesos de reducción y formación de los cofactores oxidados NAD+, NADP+ y FAD+ l Requiere de energía (procesos endergónicos) por lo que se consume ATP l Hay divergencia de rutas metabólicas

CATABOLISMO l Ruta metabólica de degradación de macromoléculas (grasas, carbohidratos y proteínas) en moléculas más simples l Se dan los procesos de oxidación y formación de los cofactores reducidos NADH, NADPH y FADH 2 l Se libera la energía química (procesos exergónicos) y se produce ATP a partir de ADP l Hay convergencia de rutas metabólicas
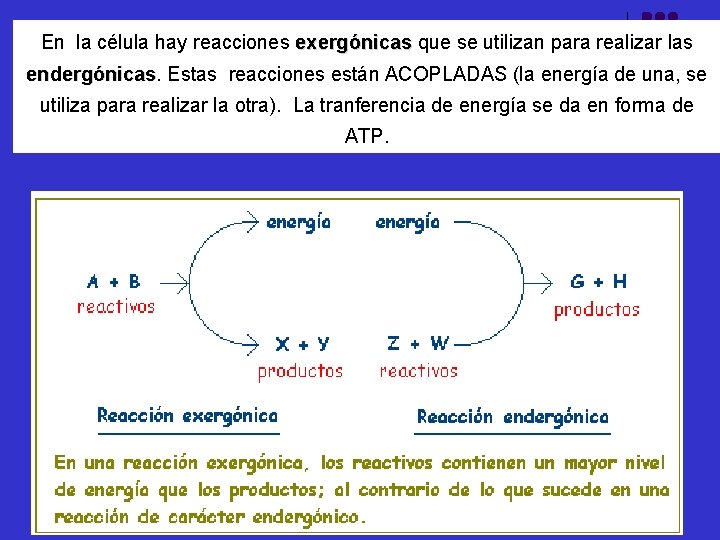
En la célula hay reacciones exergónicas que se utilizan para realizar las endergónicas Estas reacciones están ACOPLADAS (la energía de una, se utiliza para realizar la otra). La tranferencia de energía se da en forma de ATP.

Mecanismos para el intercambio de Energía en los Sistemas Vivos l l Transferencia del grupo fosforilo ATP-ADP Por transportadores de electrones (Reacciones Redox) Pares Redox: NADP+/NADPH, NAD+/NADH, FAD+/ FADH 2

La transferencia de energía se puede dar por reacciones acopladas que involucran ganancia o pérdida de electrones. Las reacciones que están acopladas y son de OXIDACIONREDUCCION se conocen como reacciones REDOX.
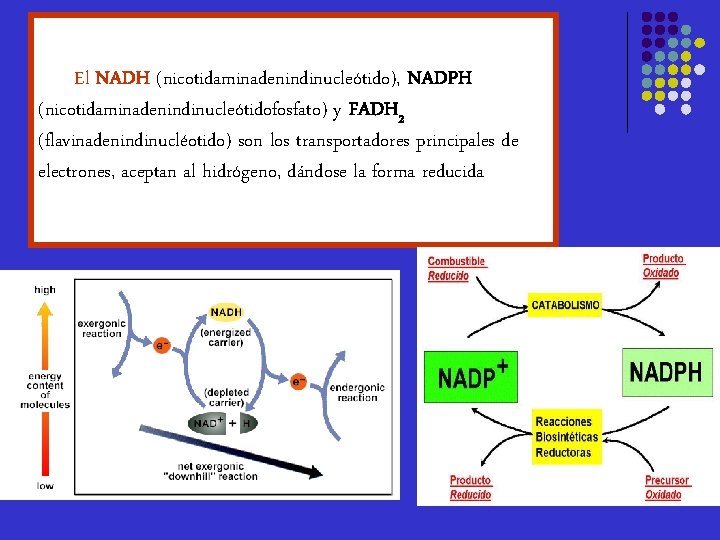
El NADH (nicotidaminadenindinucleótido), NADPH (nicotidaminadenindinucleótidofosfato) y FADH 2 (flavinadenindinucléotido) son los transportadores principales de electrones, aceptan al hidrógeno, dándose la forma reducida
Los transportadores de electrones que contienen un grupo HEM (porfirina-hierro), como los CITOCROMOS, transfieren electrones aislados entre los estados de valencia Fe+2 Fe+3. Las COENZIMAS son moléculas orgánicas no protéicas, esenciales para la actividad de varias enzimas. El COENZIMA A (Co A) , A se refiere a la acetilación, (acetil coenzima A), tiene un alto grado de transferencia de grupos acetilo

Aunque son muy diversas las biomoléculas que contienen energía almacenada en sus enlaces, es el ATP (Adenosín Trifosfato) la molécula que interviene en todas las transacciones de energía libre que se llevan a cabo en las células; por ello se la califica como "moneda universal de energía".
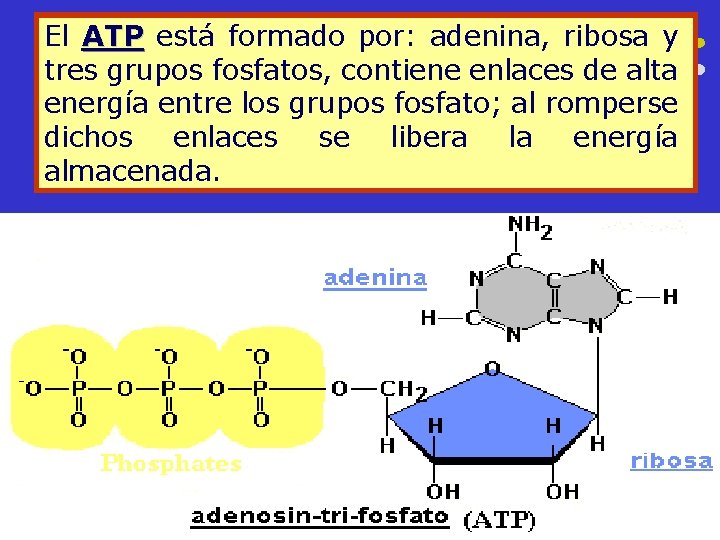
El ATP está formado por: adenina, ribosa y tres grupos fosfatos, contiene enlaces de alta energía entre los grupos fosfato; al romperse dichos enlaces se libera la energía almacenada.
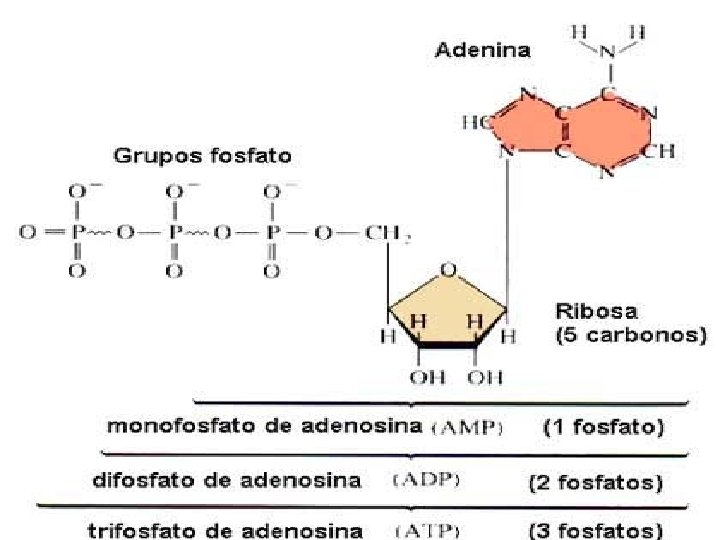

La FOSFORILACIÓN es una de las reacciones químicas más importantes en la célula. La hidrólisis del ATP : ATP + H 2 O ADP +Pi presenta una diferencia de energía libre estándar entre productos y reactantes de: 7. 3 kcal/mol Sólo en algunos casos se rompen los dos enlaces resultando AMP (Adenosin Monofosfato) quedando dos grupos de fosfato libre. ATP + H 2 O AMP + PPi
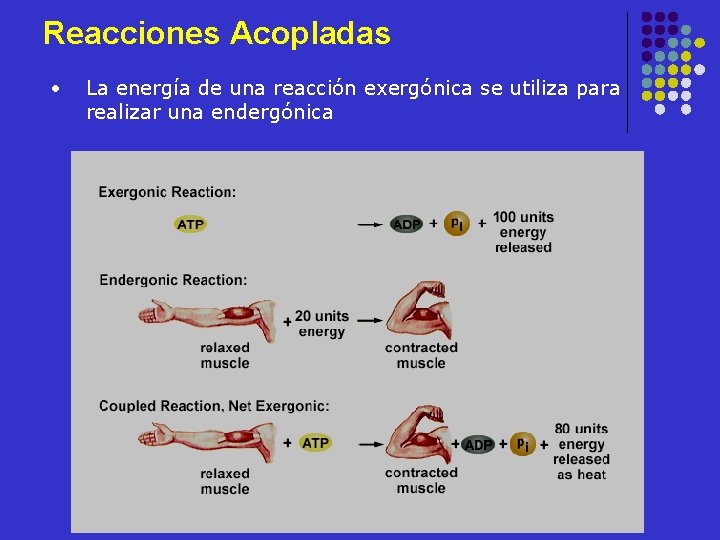
Reacciones Acopladas • La energía de una reacción exergónica se utiliza para realizar una endergónica

Reacciones Acopladas Ácido glutámico + NH 3 ------->Glutamina DGº' = +3. 4 kcal/mol El valor de DGº es positivo, indica que la reacción no es favorable, pero si esta reacción de aminación se acopla a otra que produzca un intermediario común fosforilado, la reacción sí será posible

Reacciones Acopladas Ácido glutámico + ATP ---> Fosfato de glutaminilo + ADP Fosfato de glutaminilo + NH 3 -----> Glutamina + Pi La reacción sumaria será entonces: Ácido glutámico + ATP + NH 3 -------> Glutamina + ADP + Pi DGº' = - 3. 9 kcal/mol

Mecanismos para el intercambio de Energia en los Sistemas Vivos l Transferencia del grupo fosforilo ATP-ADP Cada fosforilacion o desfosforilación intercambian 7. 3 Kcal/mol. l Reacciones Redox l Pares Redox: NADP+/NADPH, NAD+/NADH, FAD+/ FADH 2

Transferencia de Energía l La forma de intercambio energético en los organismos vivos es la molécula de ATP, el transportador universal de energía en las siguientes actividades celulares: l l Síntesis molecular Producción y eliminación de compuestos Flujo de información (núcleo~citoplasma) Movimiento de vesículas y bombeo iónico
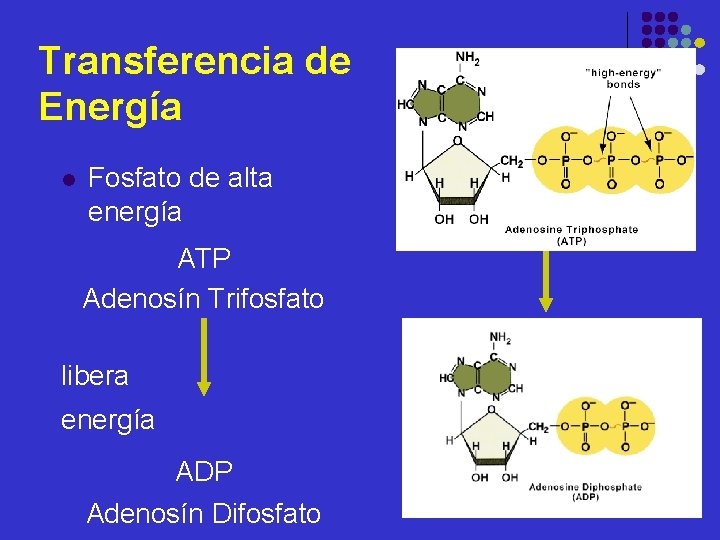
Transferencia de Energía l Fosfato de alta energía ATP Adenosín Trifosfato libera energía ADP Adenosín Difosfato
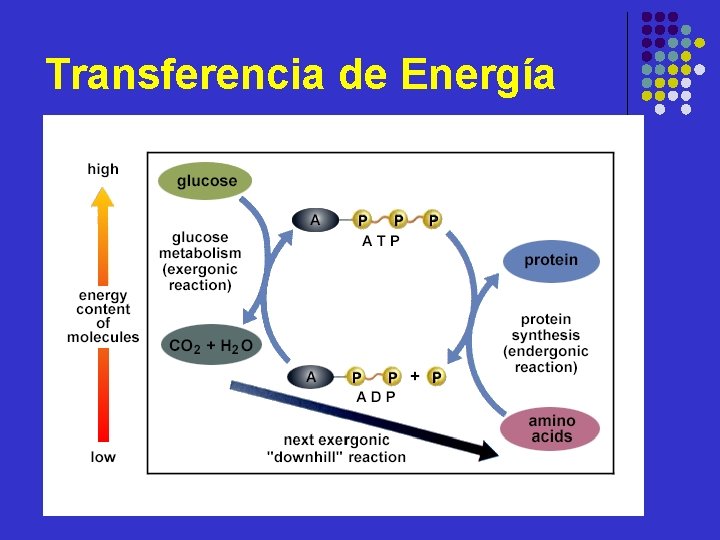
Transferencia de Energía

OTROS COMPUESTOS FOSFORILADOS DE ALTO CONTENIDO ENERGÉTICO l l l l Fosfoenol-piruvato Carbamil-fosfato Fosfocreatina ATP ( ----> ADP + Pi) ADP ( ----> AMP + Pi) AMP (-----> Adenosina + Pi) Glucosa-6 -fosfato Glicerol-1 -fosfato -14. 8 -12. 3 -10. 3 - 7. 3 - 3. 4 - 3. 3 - 2. 2

Reacciones de óxidoreducción l Son las reacciones que implican cambios en el estado electrónico de los reactantes. l Estos cambios se acompañan de ganancia o pérdida de electrones. Oxidación Fe° Fe 2+ Reducción

Reacciones de óxidoreducción l Procesos en los que hay transferencia de electrones y/o protones y son cruciales en el metabolismo celular, por dos razones: 1) Los seres vivos obtienen la mayoría de su energía libre a partir de la oxidación de ciertos compuestos bioquímicos como glúcidos, lípidos y aminoácidos 2) Muchos procesos biosintéticos implican la reducción de dobles enlaces

Reacciones de óxidoreducción l En ambos casos los electrones y protones deben poseer una considerable energía libre, esto ocurre en ciertos nucleótidos: los pares NAD+ /NADH + H+, NADP+/NADPH + H+ y FAD+/FADH 2

Reacciones de óxidoreducción l l Las formas reducidas de estos nucleótidos se originan mediante la oxidación de los combustibles celulares en el catabolismo. Serán utilizadas en: l l l reacciones de biosíntesis transferencia de energía en reacciones endergónicas Se reoxidan de nuevo, originando un ciclo de oxidación/reducción
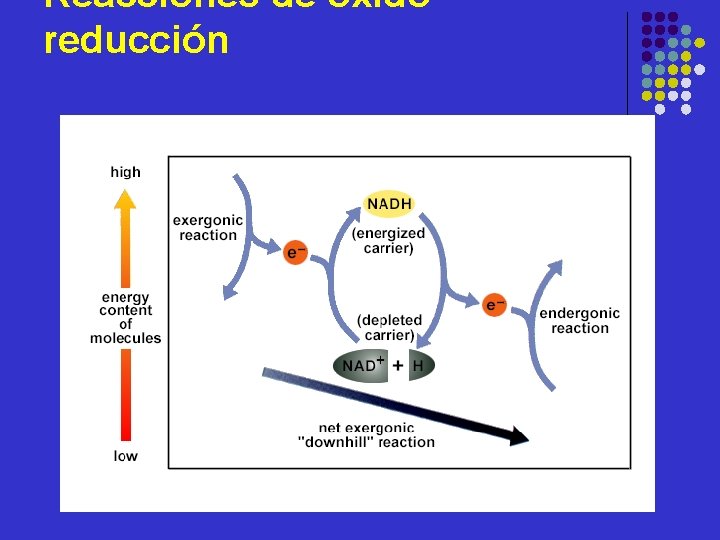
Reacciones de óxidoreducción
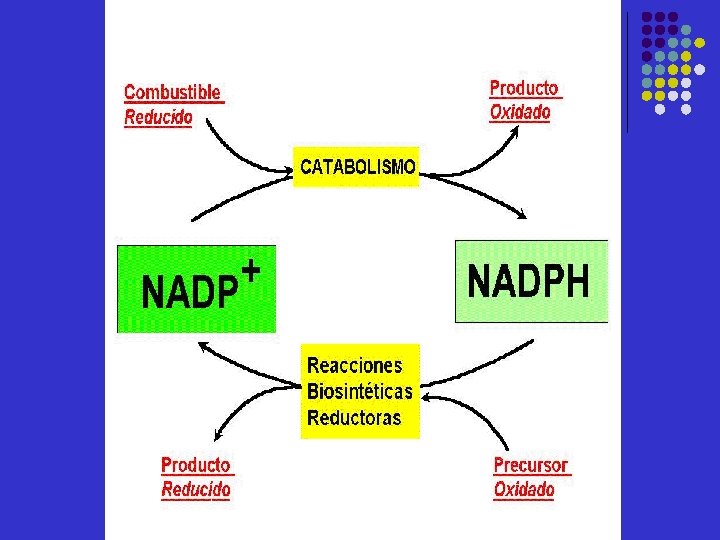

http: //perso. wanadoo. es/sancayetano 2000/biologia/apu/tema 3_1. htm http: //laguna. fmedic. unam. mx/~evazquez/0403/cambio%20 energia%20 libre%20 estandar. html
- Slides: 69